Изобретение относится к синтезу биологичеки активных химических соединений, в частности метафеноксибензиловых или р6 -циано-метафеноксибензиловых сложных зфиров 2галоидалкил (окси; тио-, сульфинил- или сульфонил) фенилалкановых кислот, проявляющих инсектицидную или кксодицидную активность.
Известны сложные эфиры фенилуксусной кислоты, например 3 -феноксибензил- об -изопропил-Фметоксифенилацетат,, 3 -феноксибензил- оС -изопропил- 3- меюксифенилацетат, 3 феноксибензил- ot -изопропил-4-хлорфенилацетат, 3 -феноксибензил-об-изопропил-Фметилфеннлацетат, 3-фенок 3 бензил-ой -изопропил-3-хлорфенилацетат к 3 -феноксибензил- ci-изопропил-4-фторофенилацетат 1. Многие из них являются зффективными средствами для борьбы с насекомыми и клещами.
Цель изобретения - метафеноксибензиловые эфиры 2-галоидалкил (окси-, тио-, . сульфинил- или сульфонил) фенилалкановых кислот формулы
RC1.
JgV-CH- СО- О- CH/ VOл XsJ
Г НгBS
где В СРзХ, У и Z находятся в мсти-или шра-положении по отношению к углеродному
RiCFgX
атому, к которому прикреплена группа сложного эфира алкановой кислоты;
X - О, S, SO или SOj; Y и Z - Н, С1, F, Вг. NO, СН или OCHj;
R - Н. F, С1, CHF2 или
R - этил, Н-пропил, изопропил, изопропе НИЛ или грег-бутил;
Н, СМ или
R4- Н, F, С1, СНз или ОСНд, либо их оптические изомеры при условии, что У и Z - водород; R - Н или F; X - О или S, R 2 - зтил, «-пропИл или изопропил, проявляющие инсектицидную и иксодицидную активность.
Метафеноксибензиловые сложные эфи{я 1 2-галоидалкил {окси-, то-, сульфишш- или сульфонил) фенилалкановых кислот формулы (1) получают реакцией -замещенного 2галоидалкил(окси-, тио-, сульфинил-. или сульфонил)фенилацетилгалоида формулы (П) предпочтительно хлорида, с метафеноксибензиловым спиртом формулы (111). Реакцию проводят в присутствии растворителя, такого как диэтиловый эфир, бензол или толуол, при 10-30 С в присутствии акцептора кислоты, в частности третичных органических аминов, триметилалшна, триэтиламина и пиридина;
сн- он
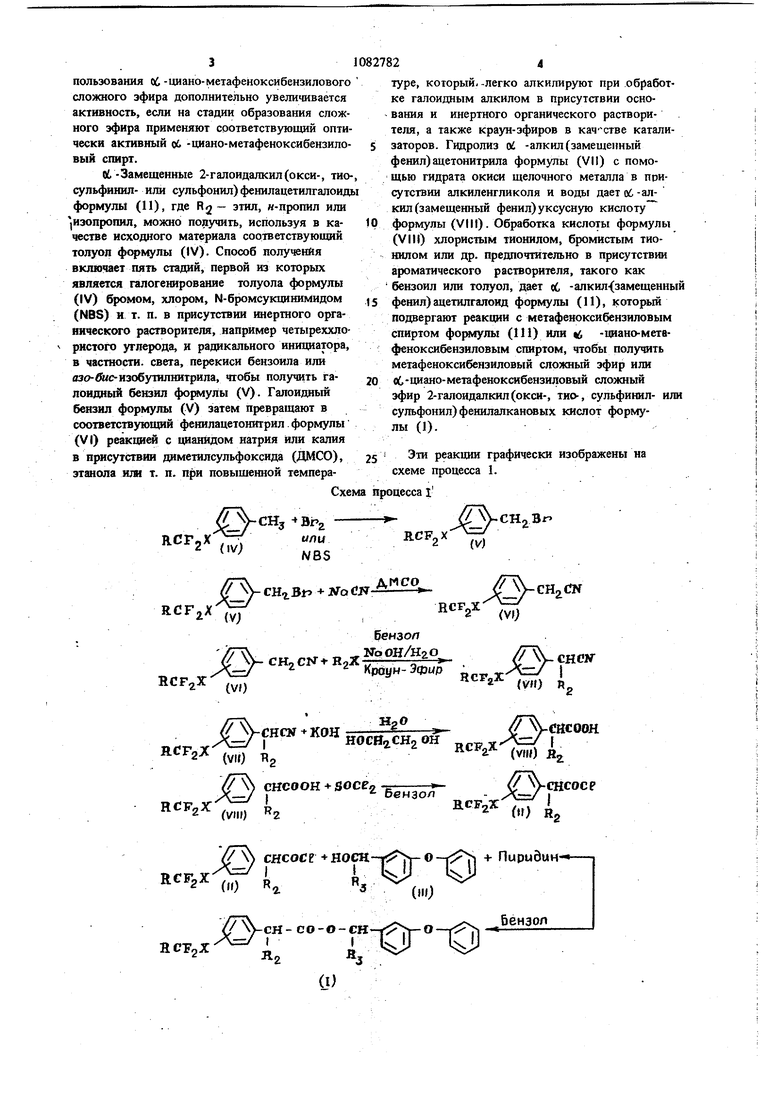
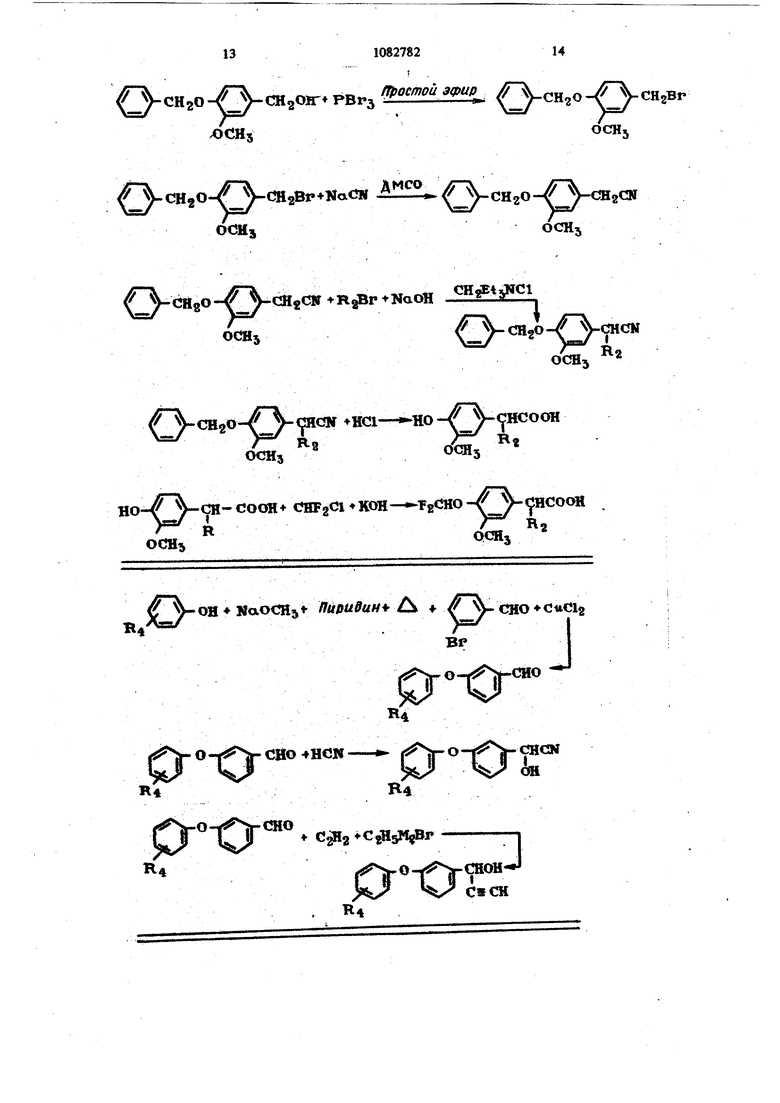
Акцег7гг ор кислоты где R, Сф - находится в мета- или в пораположении я углероду, к которому присоедин нена группа алкановой кислоты, X - О, S, S О или Rj - Н, F, С1, CHFg или Rj - этил, Ни-пропил, изопропил, изопро«| пенил или fjjer-бутил; RI - Н или CN; А - галоген, предпочтительно хлор. Соеданения формулы (1) могут &ггь получ чены в виде оптических изомеров. Например, iqw синтезе сложных эфиров формулы (1), где R - водород, а в Rjj имеется хиральный центр, получаются правовраща г , юшне и л овращаюшие изомерные пары. Кроме того, «6 -цианозамещение в Ri вносит дополнитель ный хиральиый центр, дающий дополнительные щ авовращающую и левовращающую пары. Если -изопропил-4-трифторометоксифенилуксусную кислоту. смеЩивают с 0,5-1,0 мольэкв. (-) -«С,.-фензтиламина в растворитеяе, таком как этанол или водный этанол, то осаждается соль (+) - кислоты. При подкислении эта соль освобождает кислоту, которая содержит свыше 85% (+)-изомера. Более высокого разделения оптических изомере можно достичь перекристаллизацией (-) -,6-фенэтиламиноврй соли или путем повторения процесса разделения оптических изомеров со свежим (-) -я -фенэтиламином. Метафеноксибецзиловые или об -ииано-метафеноксибензиловые сложные эфиры полностью разделенной (4-)-в&-изопропил-Фтрифторометоксифенилуксуснойкислоты вдвое инсектицидно зффеклсвнее, чем соответствующие сложные эфиры, получен.ные из рацемической кислоты. В случае ис3пользования об -циано-метафеноксибензилового сложного эфира дополнительно увеличивается активность, если на стадии образования сложного эфира применяют соответствующий оптически активный об -циано-метафеноксибензиловый спирт. Об -Замещенные 2-галоидалкил(окси-, тио сульфинил- или сульфонил) фенилацетилгалоид формулы (11), где Rj - этил, и-пропил или |Изопропил, можно , используя в качестве исходного материала соответствуюишй толуол формулы (IV). Способ получения включает пять стадий, первой из которых является галогенирование толуола формулы (IV) бромом, хлором, N-бромсукцииимидом (NBS) и т. п. в присутствии инертного органического растворителя, например четыреххлорнстого углерода, и радикального инициатора, в частности, света, перекиси бензоила или язо-бмс-изобутилнитрила, чтобы получить галоидный бензил фо{ялулы (V). Галоидный бензил формулы (V) затем превращают в соответствующий феиилацетошггрил формулы (VI) реакцией с цианидом натрия или калия в присутствии диметилсульфоксида (ДМСО), этанола или т. п. при повышенной темпера2туре, который, -легко алкилируют при обработке галоидным алкилом в присутствии основания и инертного органического растворителя, а также краун-эфиров в кач-стве катализаторов. Гидролиз oL -алкил (замещенный фенил)ацетонитрила формулы (VII) с помощью гидрата окиси щелочного металла в присутствии алкиленгликоля и воды дает об -алкил (замещенный фенил) уксусную кислоту формулы (VIII). Обработка кислоты формулы (VIII) хлористым тионилом, бромистым тиошшом или др. предпочтительно в присутствии ароматического растворителя, такого как бензоил или толуол, дает оС -алкил-(замещенный фенил)ацетилгалоид формулы (И), который подвергают реакции с метафеиоксибензиловым спиртом фортлуяы (111) или t -циано-метвфеноксибензиловым спиртом, чтобы получить метафеноксибензиловый сложный эфир или оС-гщано-метафеноксибензиловый сложный эфир 2-галоидалкил(окси-, тио-, сульфинил- или сульфонил) фешшалкансжых кислот формулы (1). Эти реакции графически изображены на схеме процесса 1.
иг л ys TV
( v-CHCN + кон- V у-СЙ
/ /Л-АЧ Я). чт л ттJy 1 f f
xAzz/ IHOCfJnCHo ОН „„,5 ...хлГГУ t
2 , W%
7 cttcoon + socey- « V-CHCOCP
-A-/ Iоензол- уЛ-/ I
(И) L,
Пиридин
бензол
В качестве альтернативы бромистому бенЗИ9У формулы (V), указанному в схеме процесса 1, где продукты ограничены замещеь нием в шрв-положение, можно хлорметилиро - вать соответствующий галоидалкил (окси- или тио) бензол формулы (IX). ис1тользуя смесь // л.. ,RCF2Y-f3 (H20)j HC где У - О или S Метафеноксйбензиловый и 06 -циан9-мета(Ьеноксибензиловый сложные эфиры ее . алкил-3 (4) тртфторометоксифенилуксусной кислоты можно также получить алкилированием метаили пара-метоксифенилацетонитрилапри использовании галоидного алкила в присутствии краун эфира и основания. При использовании в этой реакции метаметоксифенилацетонитрила получают t6 -алкил-З-метоксифенилацетонитрил, а при использовании пара-изомера - об -алкил-4-метоксифешшацетонитрил. Положение метоксигруппы в фенилацетонитриловом исходном материале определяют положение трифторометоксизаместителя в конечном продукте. (X.-Алкил-3 (4)-меток(Я1фенилацетош1трш1 превращают в ОС-алкил-3(4)-оксифенилацетоHHTjHui обработкой бромистым бором в присутствии растворителя, в частности хлористого метилеиа. Обработка полученного таким образом фенола трифосгеном и основанием в присутствии растворителя, например хлороформа, дает в результате хлортиосложный зфир 0-, метаядра-формальдегида или триоксана с хлористым цинком и безводным хлористым водородом, чтобы получить хлористый бензил формулы (X), который затем используют вместо бромистого бензила формулы (V) для завершения синтеза до соединения формулы (1) Clg .RCFgY CHgCl ИЛИ пара- (1 - ииаио- - 2- метилпропил) феиилмуравьиной кислоты. Этот сложный эфир превращают в ОС -адкил-3(4)-трифторометоксифенилацето нитрил с помощью щестифтористого молибдена. Соединение затем гидролизуют в соответствую- щую об -алкил-3(4)-трифторометоксифенилуксусную кислоту реакцией с зтилеигликолем в присутствии гидрата окиси щелочного металла и воды.: Обработка об - алкил-3 (4)-трифторометоксифенилуксусной кислоты хлористым тионилом в присутствии аро штического растворителя (бензол или толуол) дает хлорангидрид соответствующей кислоты, который подвергают реакции с метафеноксибензяловым или о -циано-метафеноксибензиловым спиртом, чтобы получить метанокшбеизиловый или оС -циано-метафеноксибензиловый сложный зфир об -алкил-3(4)-трифторометоксифенилуксусной кИслоТы. Эти реакции графически показаны на схеме процесса 11.
СН-С11 ВВгз CHjOКгНО




















| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Алкил-2-(4-фторметокси-4-фтортио)-фенилуксусная кислота в качестве промежуточного вещества для инсектицидов | 1978 |
|
SU1221220A1 |
| ПРОИЗВОДНЫЕ 2-ЗАМЕЩЕННОГО ФЕНИЛ-2-ОКСАЗАЛИНА ИЛИ 2-ЗАМЕЩЕННОГО ФЕНИЛ-2-ТИАЗОЛИНА И ИНСЕКТИЦИДНАЯ И/ИЛИ АКАРИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1990 |
|
RU2029766C1 |
| Производные бициклооксифенилмочевины,проявляющие пестицидную активность | 1983 |
|
SU1425190A1 |
| Инсектицидная композиция | 1986 |
|
SU1695820A3 |
| @ -Циано-3-феноксибензиловый эфир IR-цис-2,2-диметил-3-/1-бром-2-хлорпропен-1-ил/-циклопропанкарбоновой кислоты, проявляющий инсектицидную и акарицидную активность | 1990 |
|
SU1775397A1 |
| ПРОИЗВОДНЫЕ АМИДОТИОФОСФАТА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, НЕМАТОДАМИ ИЛИ КЛЕЩАМИ | 1994 |
|
RU2124018C1 |
| Фосфорные эфиры циангидринов,обладающие инсектоакарицидной активностью | 1982 |
|
SU1134563A1 |
| Инсектоакарицидонематоцидное средство | 1976 |
|
SU612608A3 |
| Инсектоакарицидное средство | 1976 |
|
SU610472A3 |
| Инсектоакарицидонематоцидная композиция | 1975 |
|
SU747399A3 |
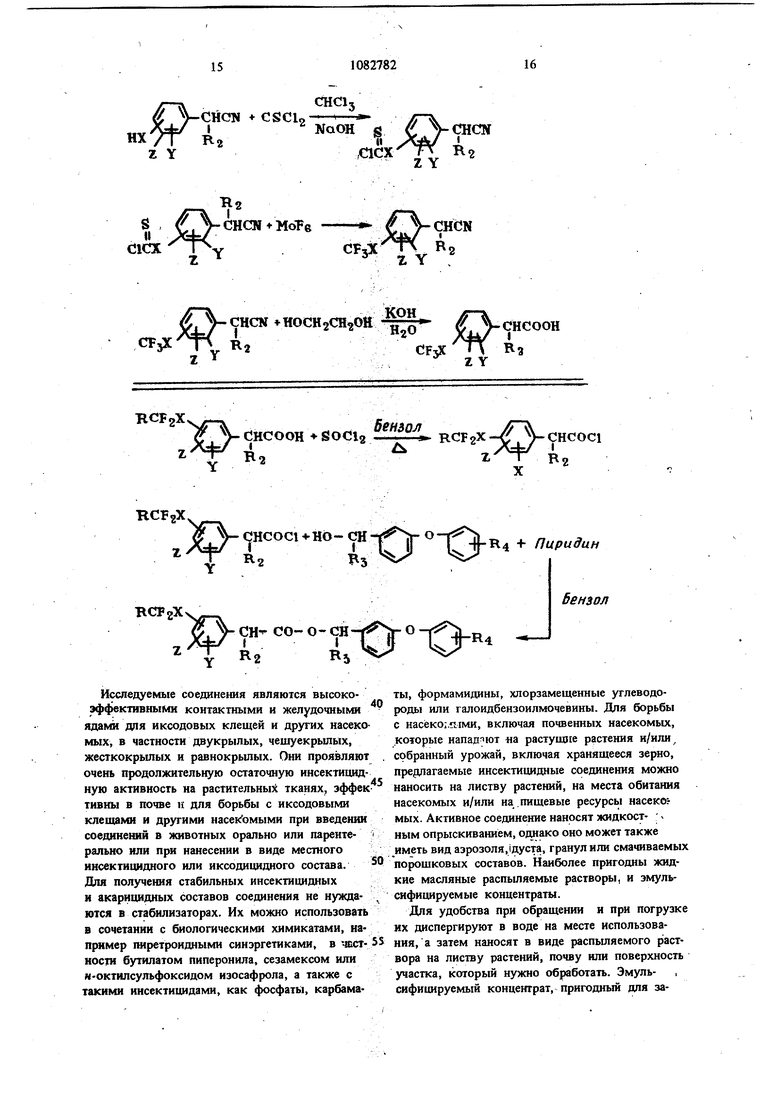
Метафеноксибензиловые или А -циано-метафеноксибензйловые сложные эфирЫ 2-галоидалкил(окси-, тио-, сульфинил или.сульфонил)фенилалкановых кислот общей формулы RpFjJC, - СО- о- . где RjCFj X- Y и Z находятся в метанли в пара-положении по отношению к углеродному атому, к которому прияреплена группа сложного эфира алкановой кислоты; X - О, S, SO или У и Z - по отдельности И, С1, F, Вг, NO, СН шш R - И, F, С1, CHFj или R - УОШ, н-пропил, изопропил, изопропьнил или трег-бутил;, R - Н, CN илн-С СН; R4 - И, F, С1, СН юш O€fl|. их оптические изомеры прт услов1т, что У -и Z - водород, RJ -| Н нли F;.X - О или S; : В 2 -пропил или изопропил, проявляю щие инсектшшдную и иксодщидную актнв(Л ; кость. Приоритет по признакам: 01.10.76 при X-S илих О; R - Н шга F; § R - этил, пропил или изопропкл; R - Н, ; CN или CyCHf RA - Н, F, Ct, СИ- или :OCHj. 11.07.77 при , SO или X Z и Y-H, ОТ, F, Br, NOj, ND ЭО , 01, F, CHF ШШ CFjj зтип, пропид, изопропил, трег-бутил или изопропе1аш; Rg-H. CN или -CsCK; H,F,C1, СН FO или OCHj.
ft r-CH-CO-O-CK CFjO R2
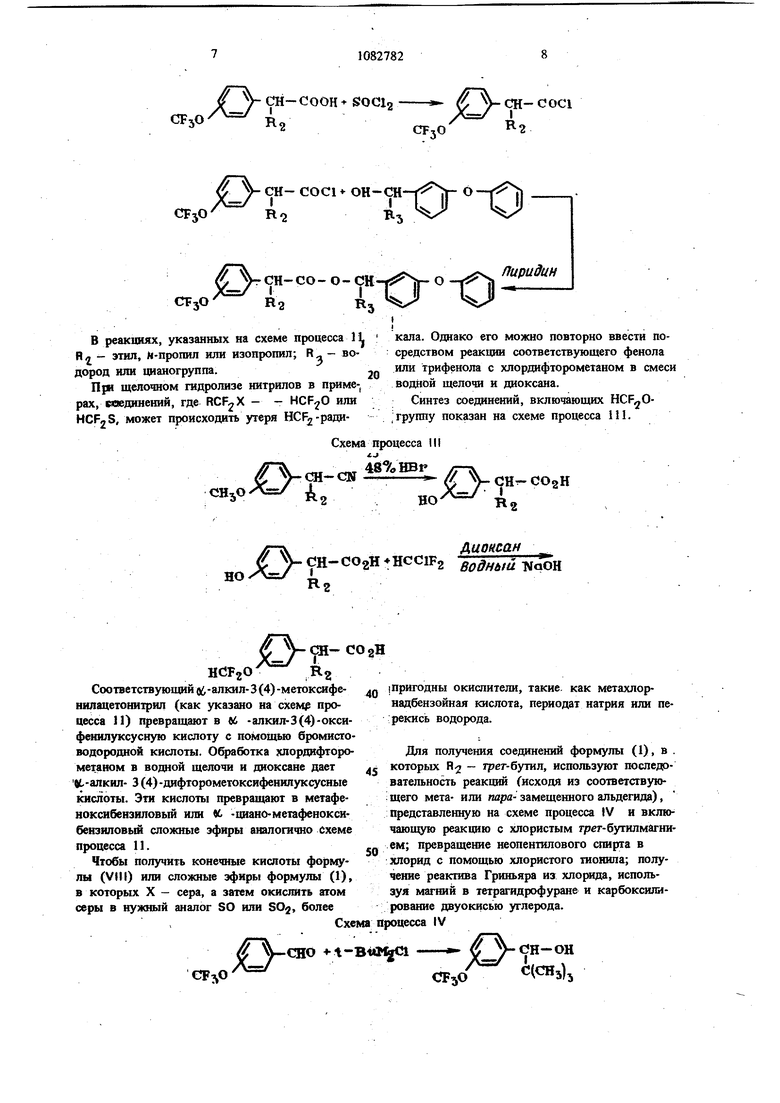
В реакциях, указанных на схеме процесса 1L кала. Однако его можно повторно ввести поЯл - этил, М-пропил или изопропил; R,, - во-средством реакции соответствующего фенола
дород или циаиогруппа.2п ™ трифепола с хлордифторометаном в смеси
При щелочном гидролизе нитрилов в приме-водной щелочи и диоксана. pax, соединений, где RCF2X - - илиСинтез соединений, включающих HCF,,jOHCF-S, может происходить утеря HCF2paди-, группу показан на схеме процесса 111.
Схема процесса III
.( - „ 48%HBi .iJT ЙусН-СОгН
СН О-Агг/ .. I
r vАиочсан
усн-согн-нсс№2 водшш тмоон
НО Лзг/
К2
Пиридин ij
СН-ОН С(СН5),
Ha схеме процесса IV показан в качестве примера синтез ж, тp eт-бy au 3(4)rpвфropo метоксифегашуксусной кислоты. 1Ьслоты можно преврапгть в соответствующие сложные эфиры по схеме процесса 1.
соединений формулы (1), в которых Я - изопрстешш, введение о -нзопррпениловрй группы можно осущесгайть, испо ьСхема процесса V
У13
« i-OH М
Х
СНз СНз
сн- со - о - снг-f o Iи J и
CFgO
с-он
СНз СНд
со - о - CM -YCNS-O -.х:5.
V. / II/ 111
/V
КдОСНз СНз
vS-сн-со - о-cHa-fi Iи
РдО
/ч
СНз %
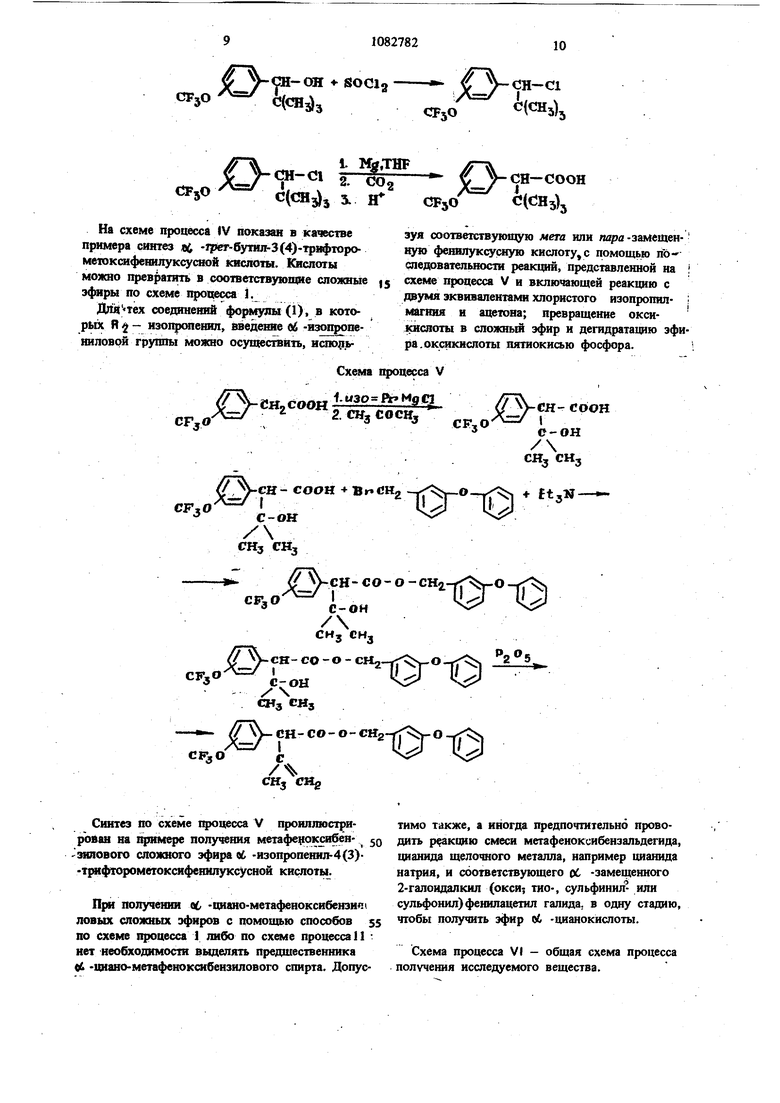
Синтез по схеме процесса V проиллюстрирован на щшмере полутення метафе11оксибён- 50 -зияового сложного эфира об -изопропешш-4(3)т{«фторомегокснфеннлуксусной кислоты.
П1Ж полученни об -циаио-метафенокси6еюи 11 ловых сложных эфнров с помощью способов 55 по схеме процесса 1 либо по схгале процесса 11 нет необходимости выделять предшественника «& цнано-метафеноксибеизилового спирта. Допусзуя соответствующую мета или пара -замещен«ую феНИЛукСУСНуЮ кислоту, с помощью ПО
спедовательности реакций, представленной на i осеме процесса V н включающей реакцию с двумя эквивалентами хлористого изопрошш- I магния и ацетона; превращение окснкислоты в сложный эфир и дегидратацию эфира, оксикислоты пятиокисью фосфора.1
У-СН- соон / е-он
СРдО/Л
СНз СНз
тимо также, а иногда предпочтительно проводить смеси метафеноксибенэальдегида, цианида щелочного металла, например цианида натрия, и соответствующего об -замец(енного 2-галоидалкил (окси; тио-, сульфинил или сульфошш)фенилацетш1 галида. в одну стадию, чтобы получить об -цианокислоты.
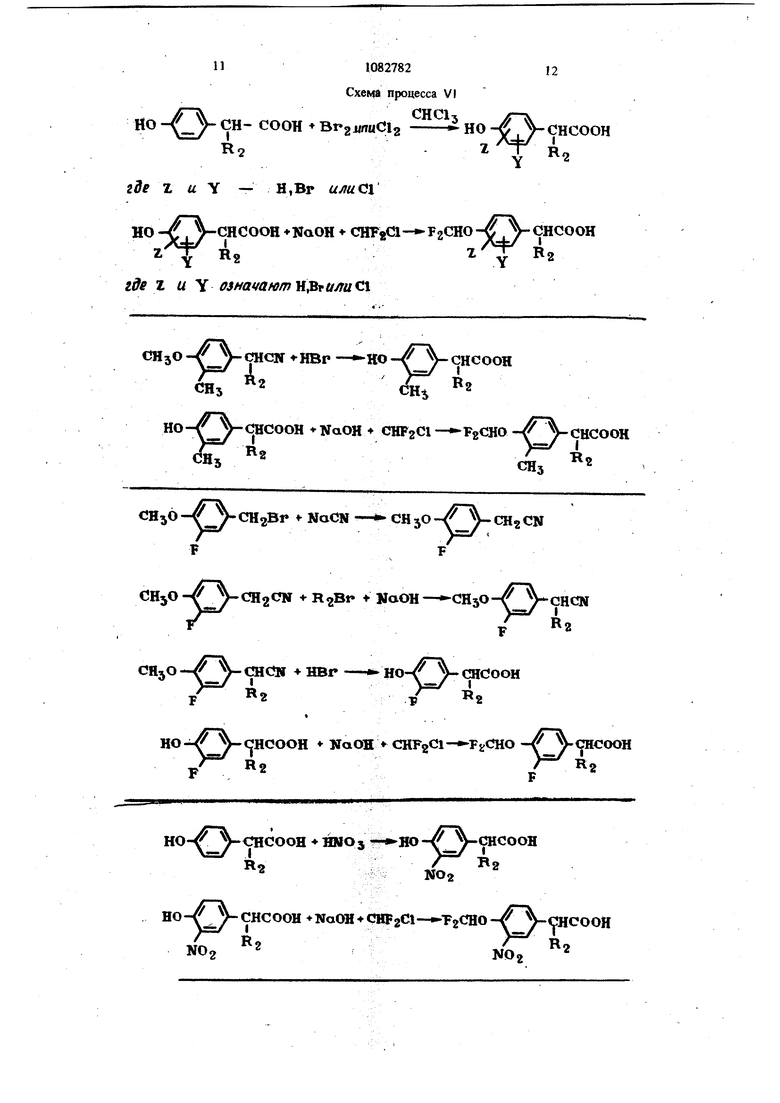
Схема процесса VI - общая схема процесса получения исследуемого вещества. НО где г и Y - Н,вр илис У СН- СООН Вг21|паС12 НО - . VcHCOOH R2X Схема процесса VI Y 2
но -г CHCOOH NaOH CHF2ei - FgCHO
«
HjO CH2B1 « NaCN CH 50 CH2 CN
CH2CN R2Bi llaOH
fA
CHjO- CHC N +НВГ HO
FR2 HO- CHCOOH NaOH CHF2C1CHCOOH«2 F5.CHO - VCHCOOH
V rWCOOH
/ B2
N02
// V
Ь CHCOOH NaOH + C HF2Cl-- -F2CHO - VCMCOOH
HONO.
л
N02 -CHgO-Oлен. VcHeO- CHgBj+NaOH OCHj -CHeC OC«5
VcH20- V- JHC N HCl--- HO-/ fHCOOM
оснз С Я-СООЯ CTOfgCl КОНROCHj
o4 V CHgOlT РВГз -CH,0-Q-CH2Br Л-СНгО- СЖ2С Г ОШ5 « З ОСИ, -Т2. f 2 Ъ
СЙО 4HCN (« 0-t -GHCN
-o
5
k U AH
H4
:
СНОМ
с СИ
CHClj
ft V-CHOTi + с SCI
Z Y
«CX T R2
CHCN носнгсн он «
m: Л2
JV CFjX
RCFgX
gOClg .1 . I j.
HCFjX
CHCOCH-H6
R2
R4 Пиридин
CH CO-O-CH R2RS
бензол
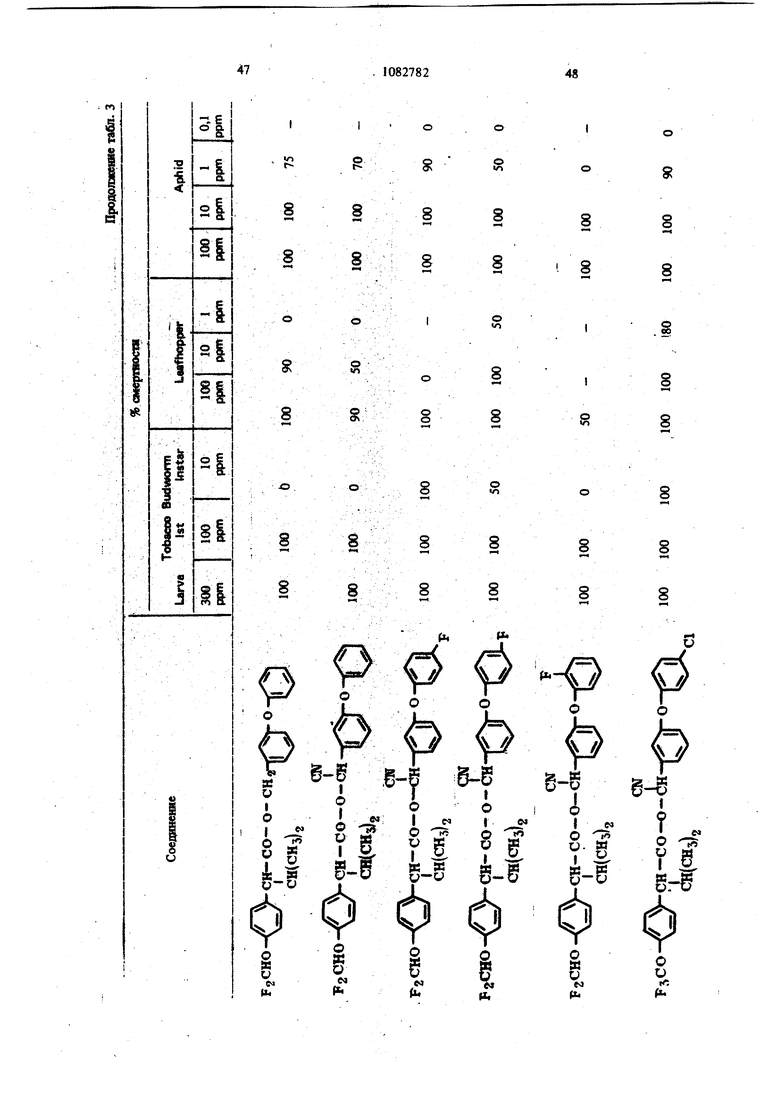
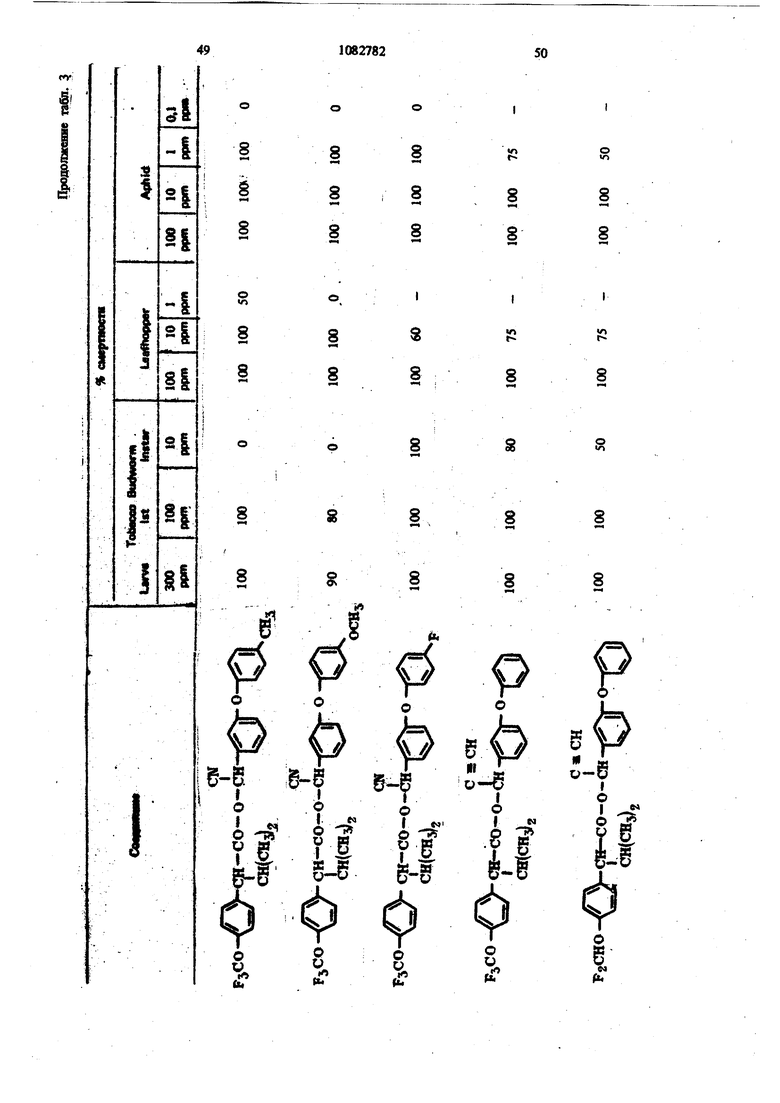
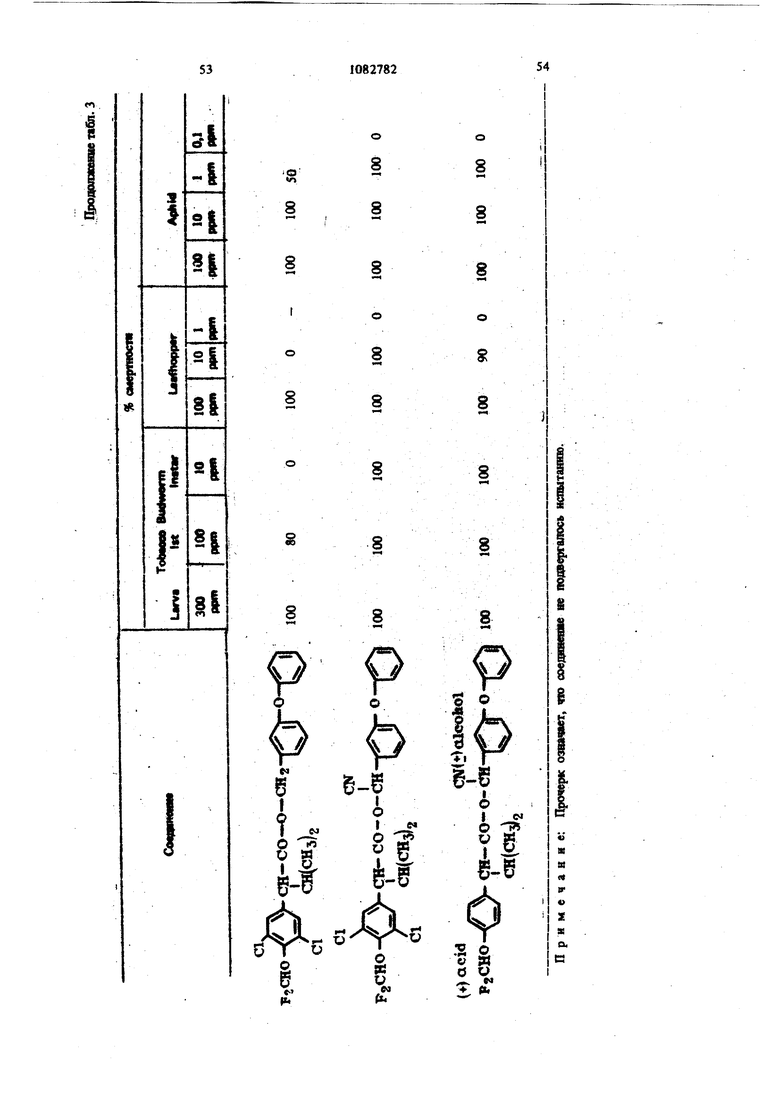
Исследуемые соединения являются высокоэффективными контактными и желудочными ядами для иксодовых клещей и других насекомых, в частности двукрылых, чешуекрылых, жесткокрылых и равнокрылых. Они проявляют очень продолжительную остаточную инсектицидную активность на расгательнь тканях, эффек тивны в почве н для борьбы с иксодовыми клещами и другими насекомыми при введении соедиие1д1Й в животных орально или парентерально или при нанесении в виде местного инсектицидного или иксодицидного состава. 0 Для получения стабильных инсектицидных и акарицидных составов соединения ие нуждаются в стабилизаторах. Их можно использовать в сочетании с биологическими химикатами, например пиретроидными синэргетиками, в част- 5S нести бутилатом пиперонила, сезамексом или м-октилсульфоксидом изосафрола, а также с такими инсектицидами, как фосфаты, карбаматы, формамидины, хлорзамещекные углеводороды или галоидбензоилмочевины. Для борьбы с насёког.шми, включая почвенных насекомых, которые нападают «а растущие растения и/или собранный урожай, включая хранящееся зерно, предлагаемые инсектицидные соединения можно наносить на листву растений, на места обитания насекомых и/или на.пищевые ресурсы насеко:мых. Активное соединение наносят жидкост- ным опрыскиванием, одаако оно может также иметь вид аэрозоля, I дуста, гранул или смачиваемы порощковых составов. Наиболее пригодны жидкие масляные распыляемые растворы, и эмульсифицируемые концентраты.
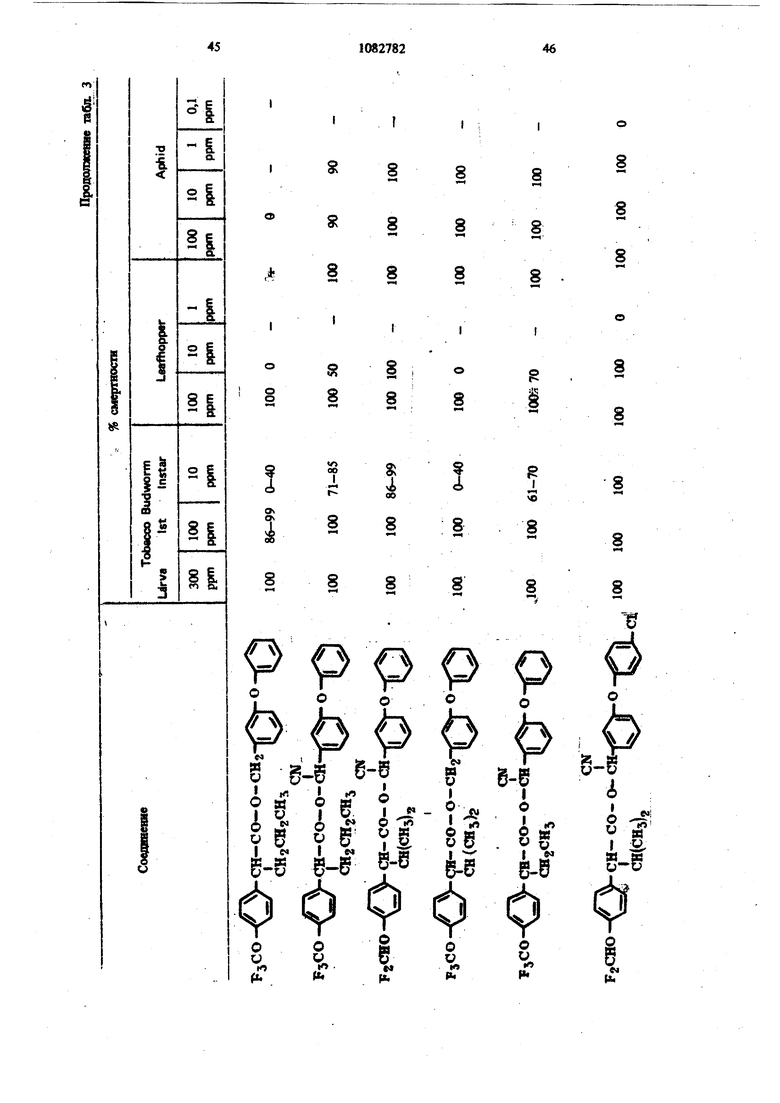
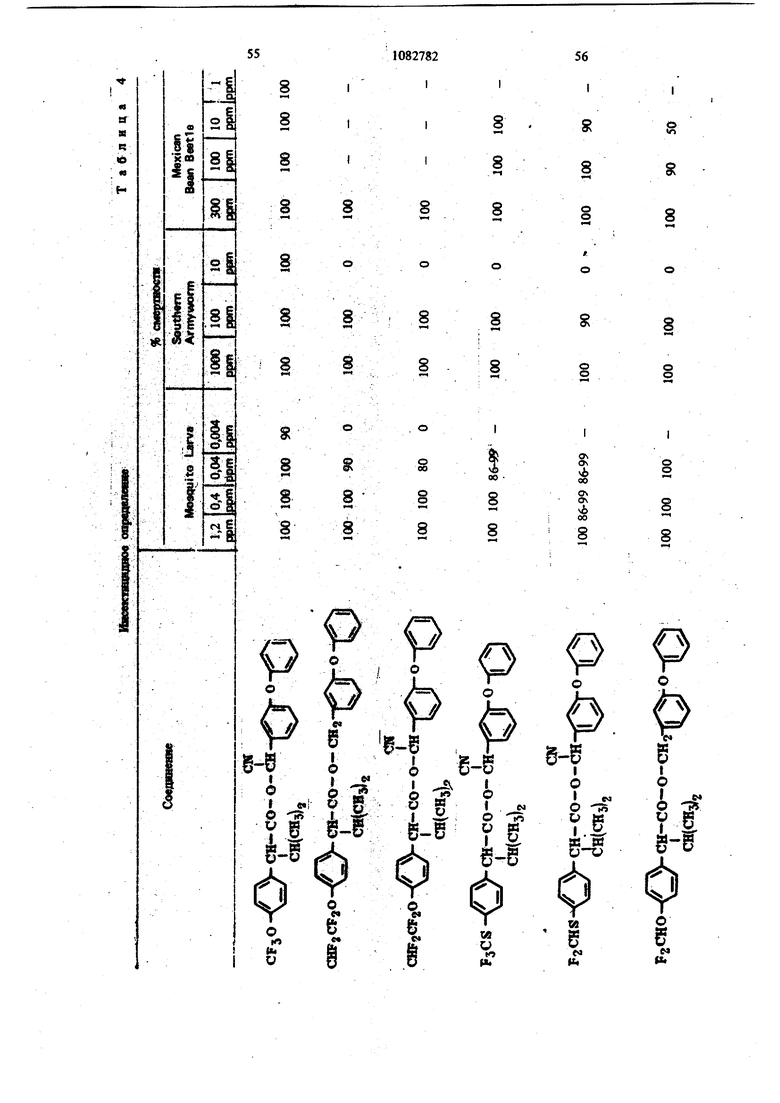
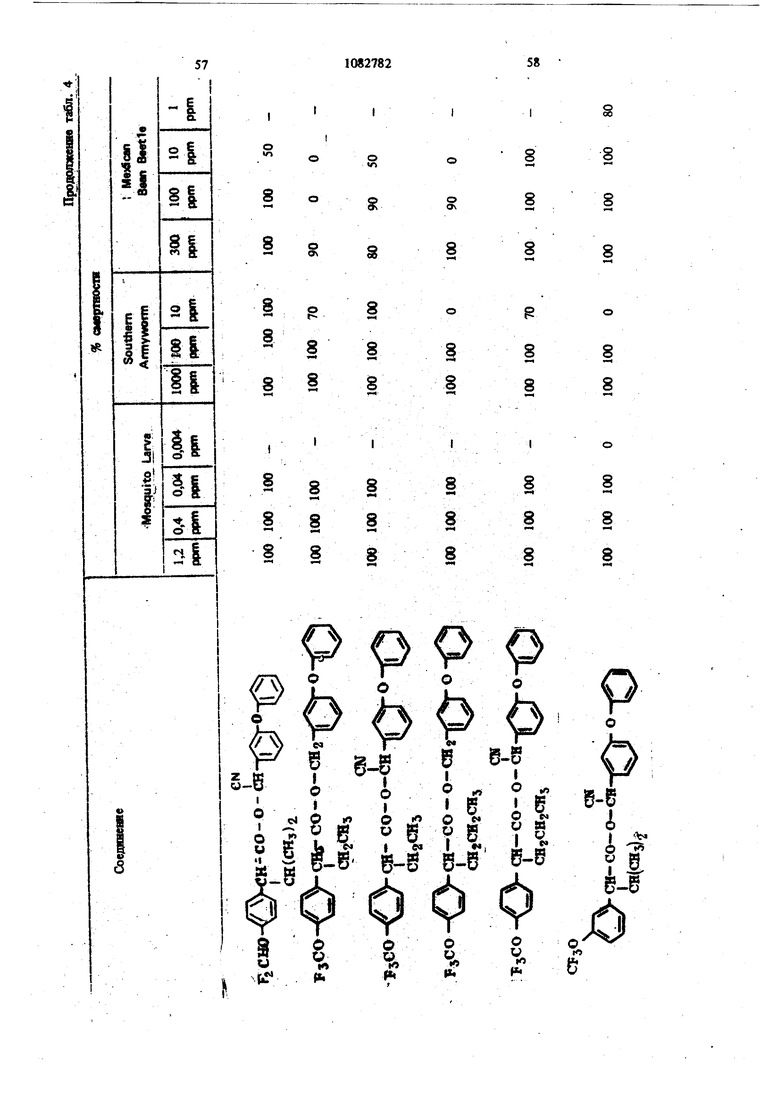
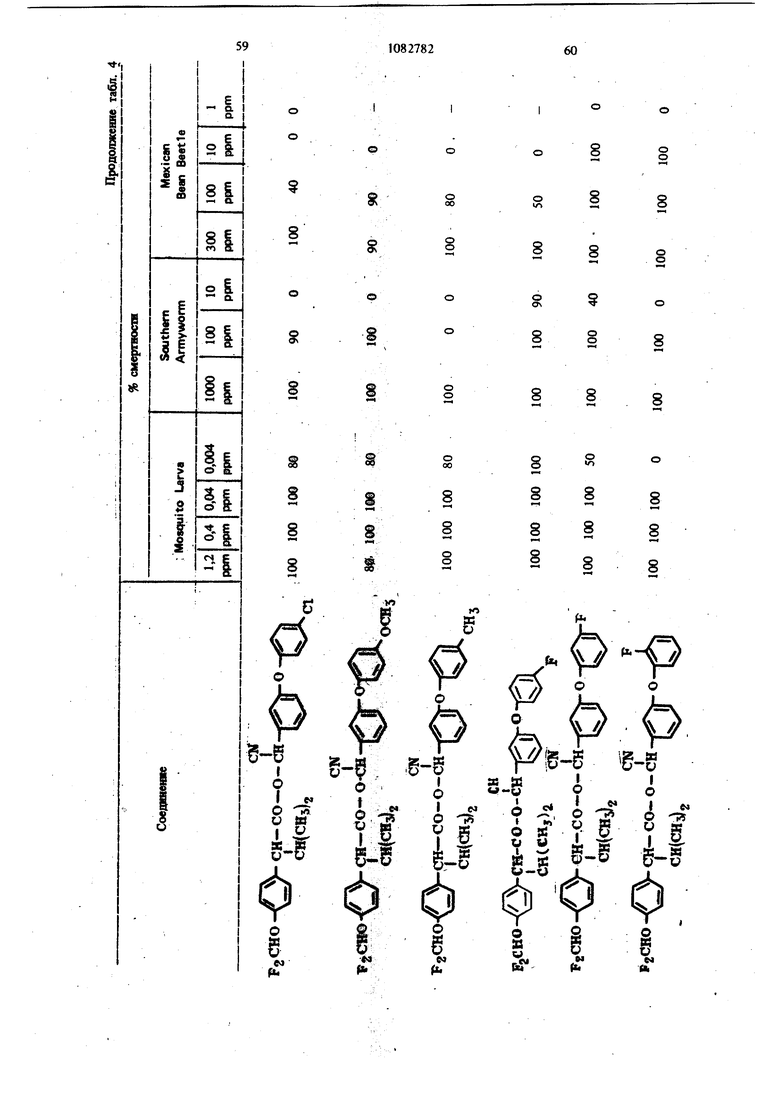
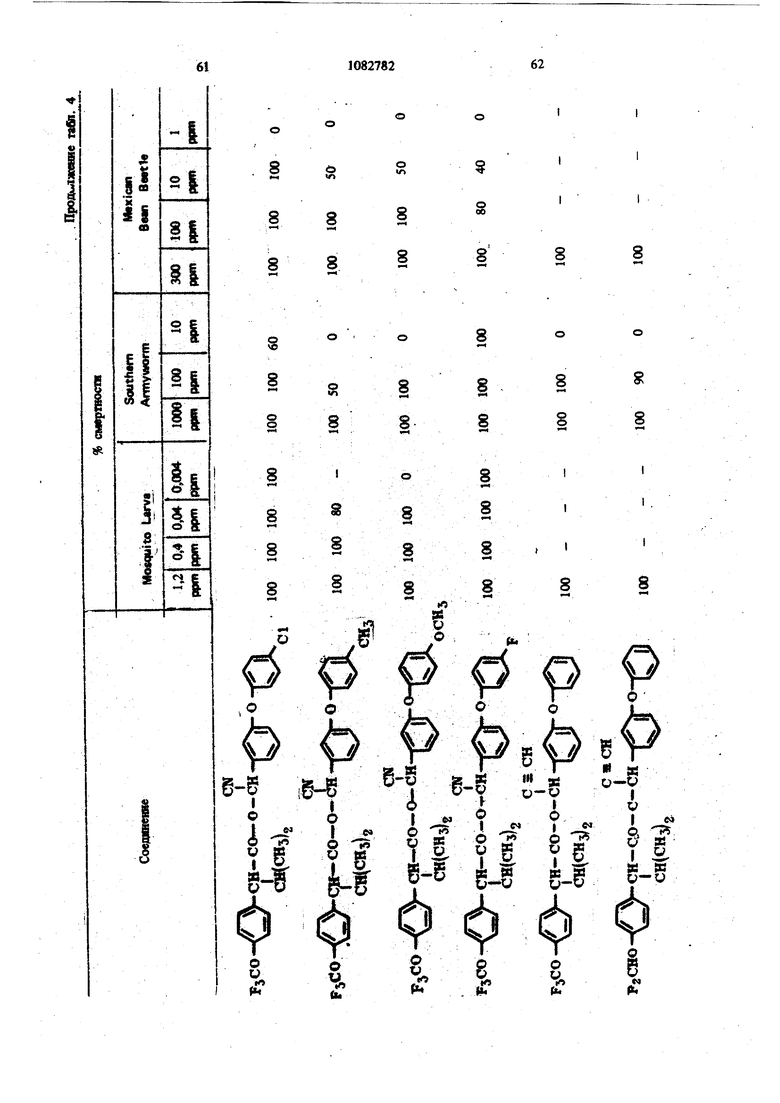
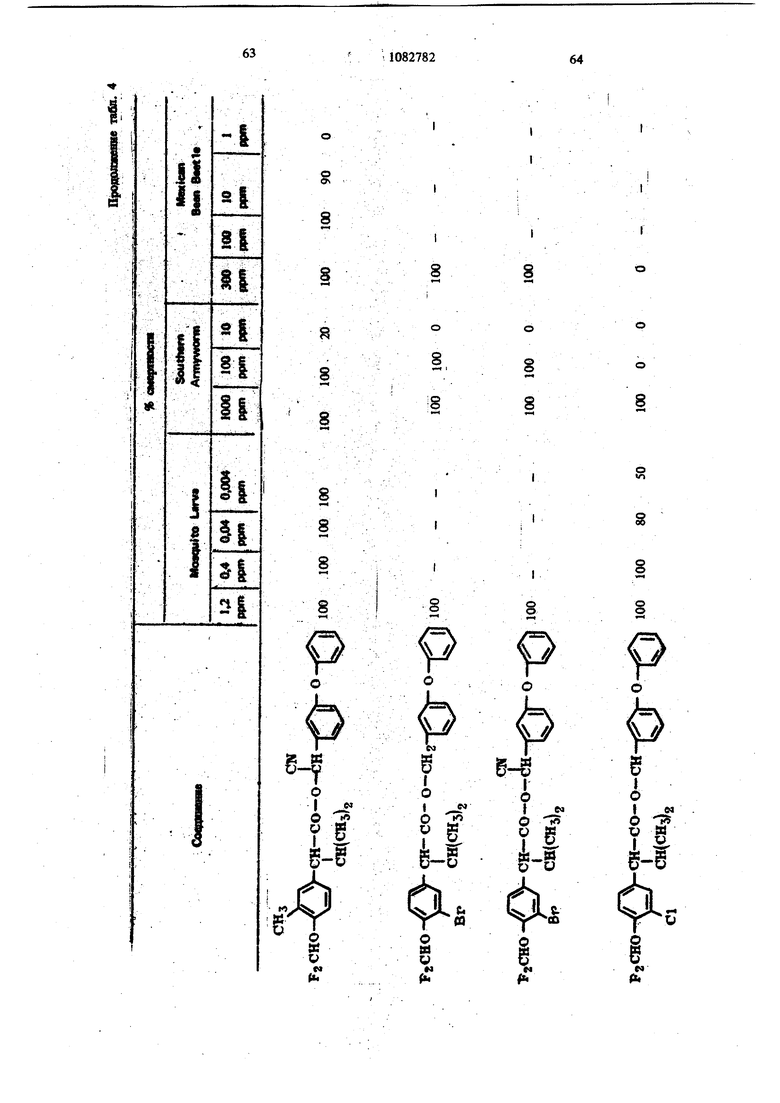
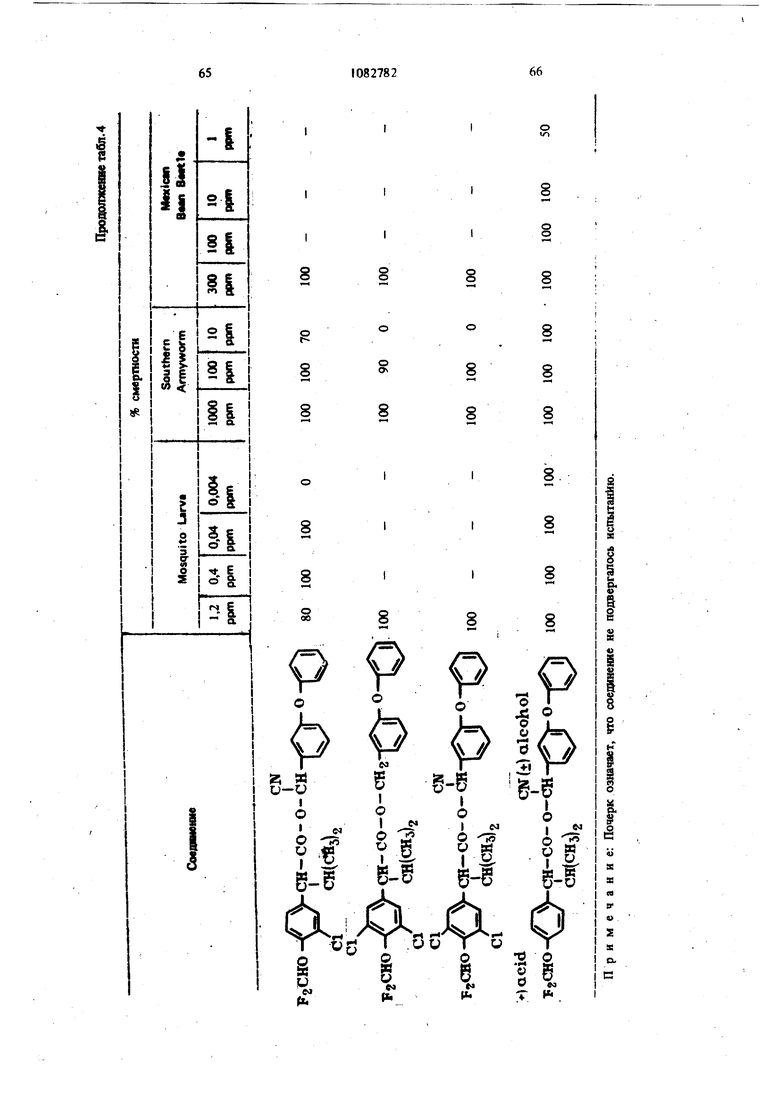
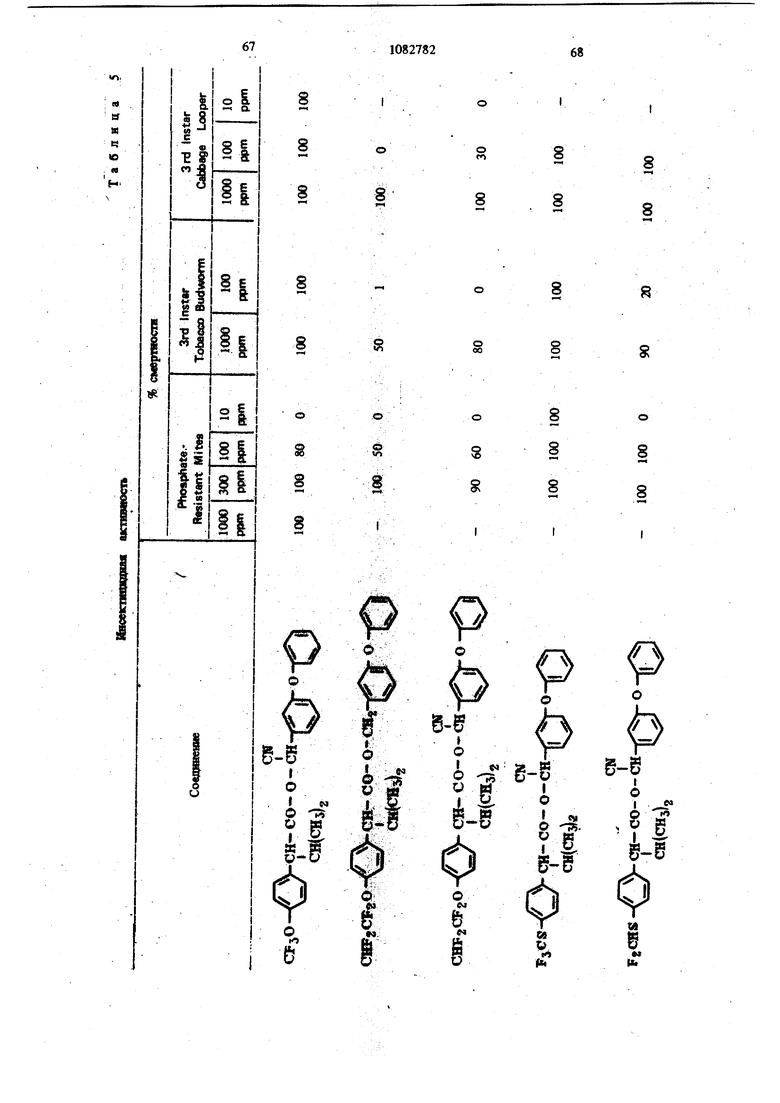
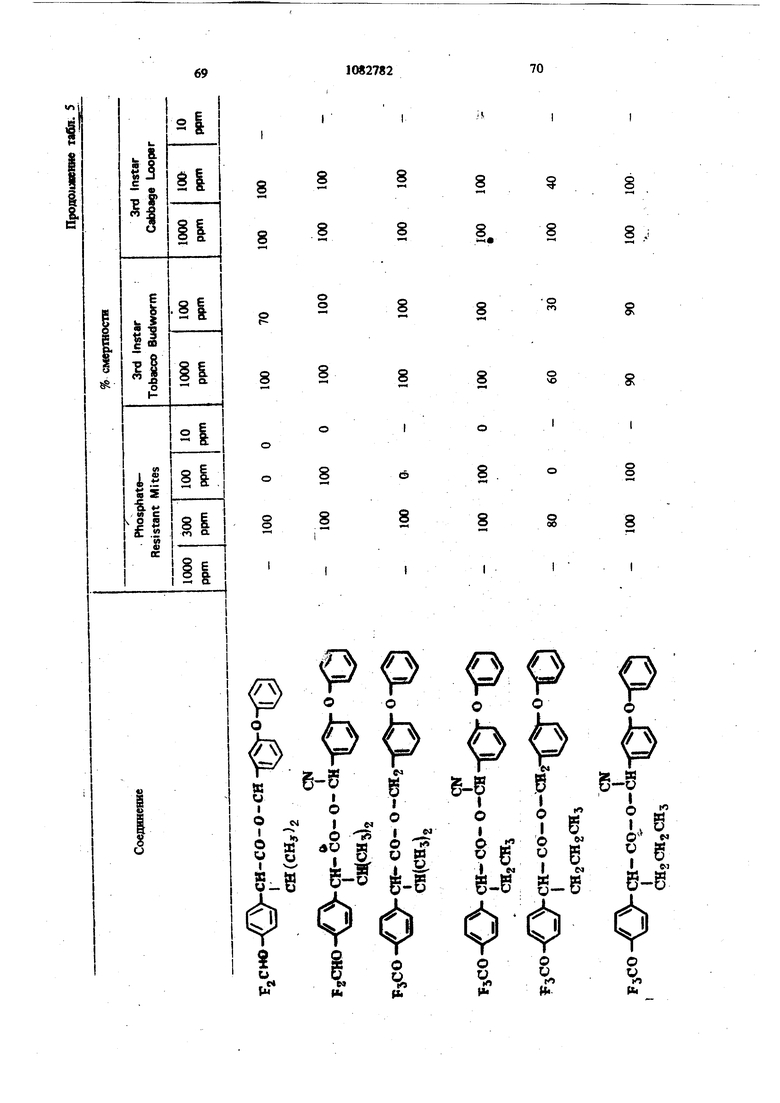
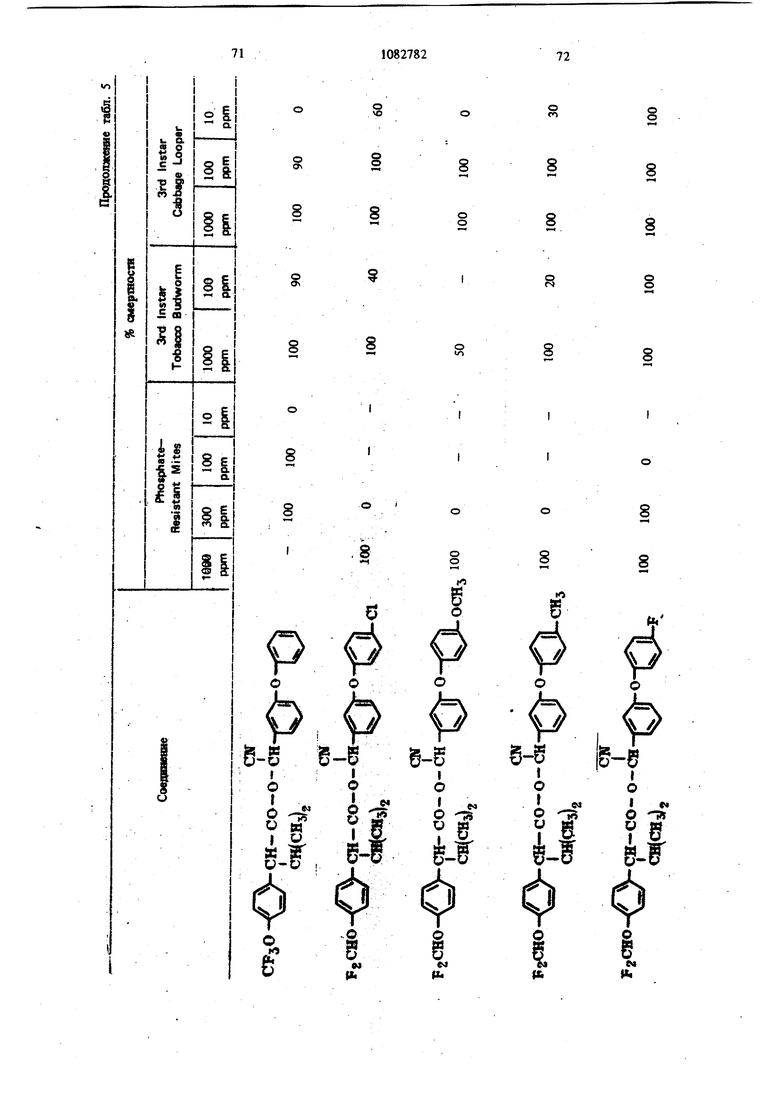
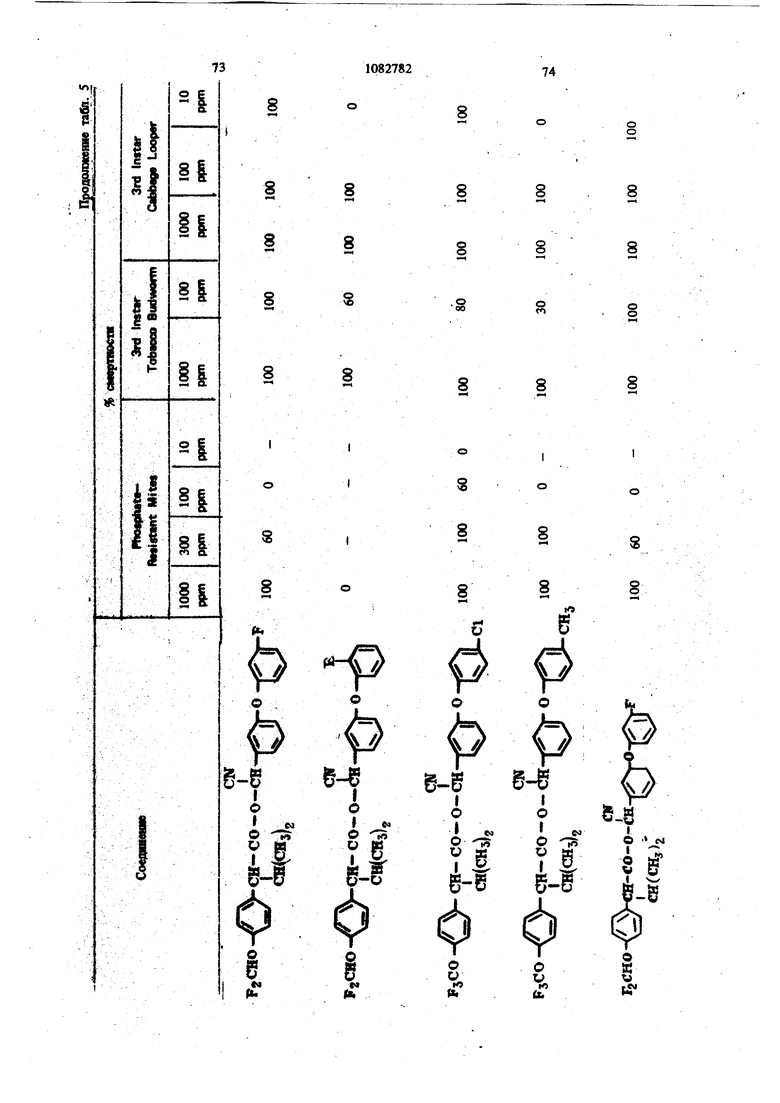
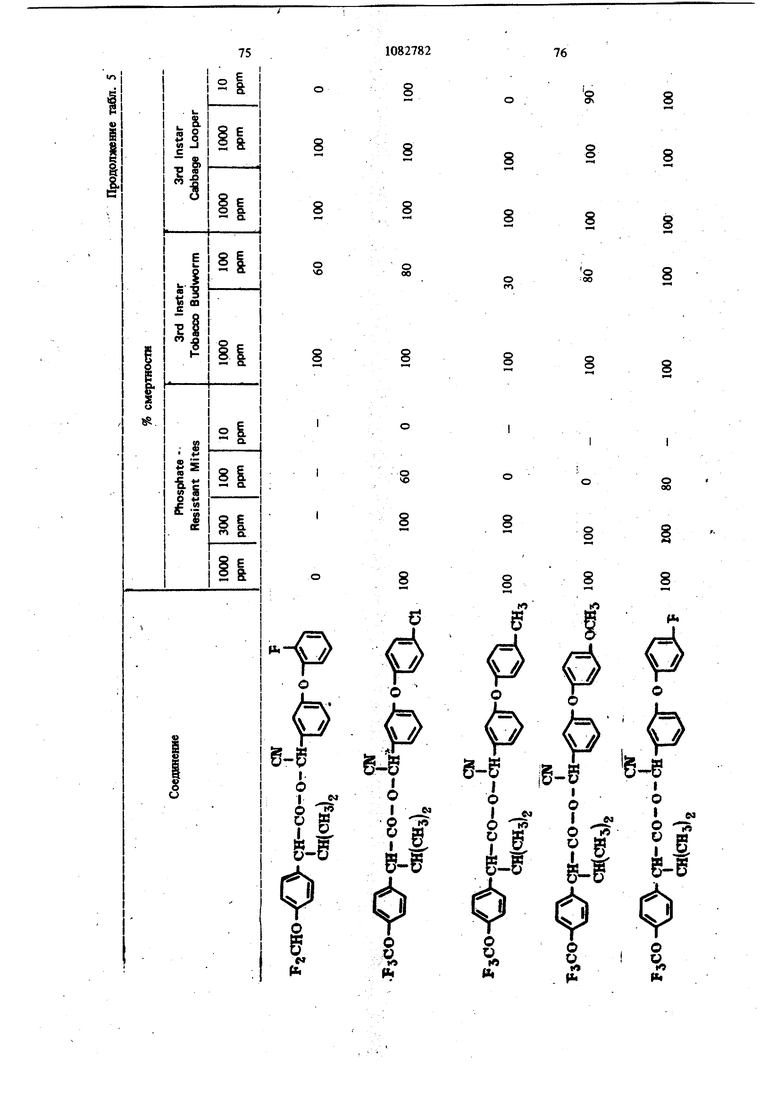
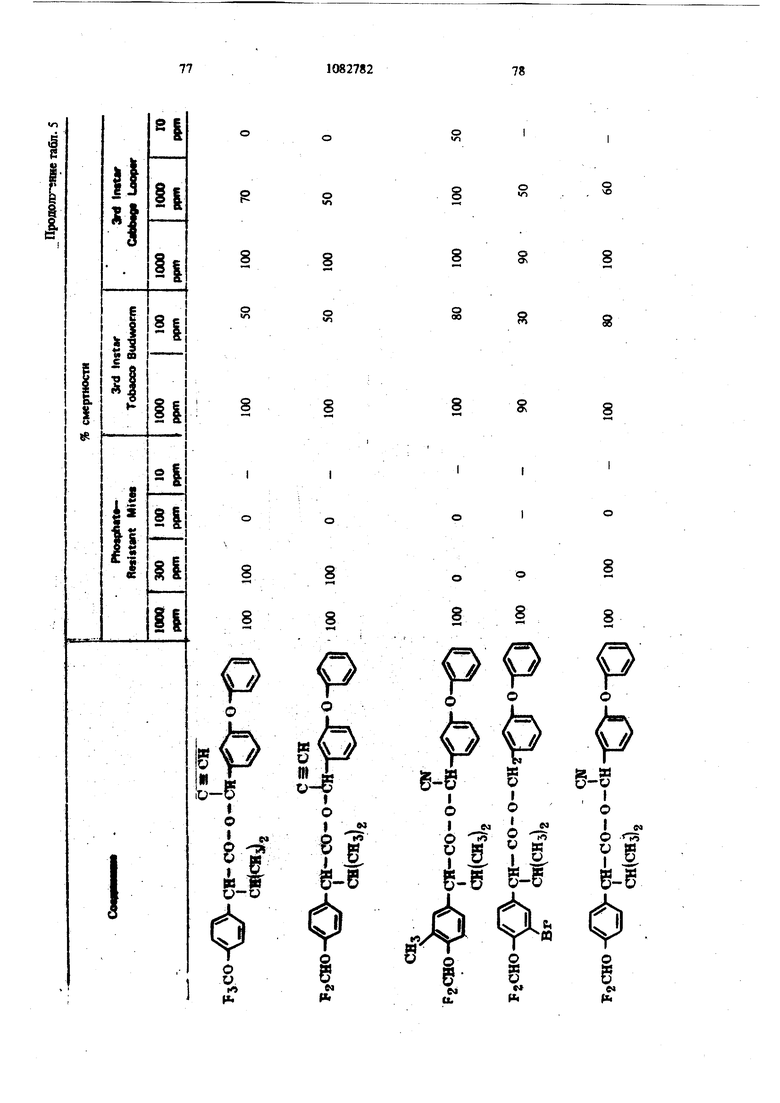
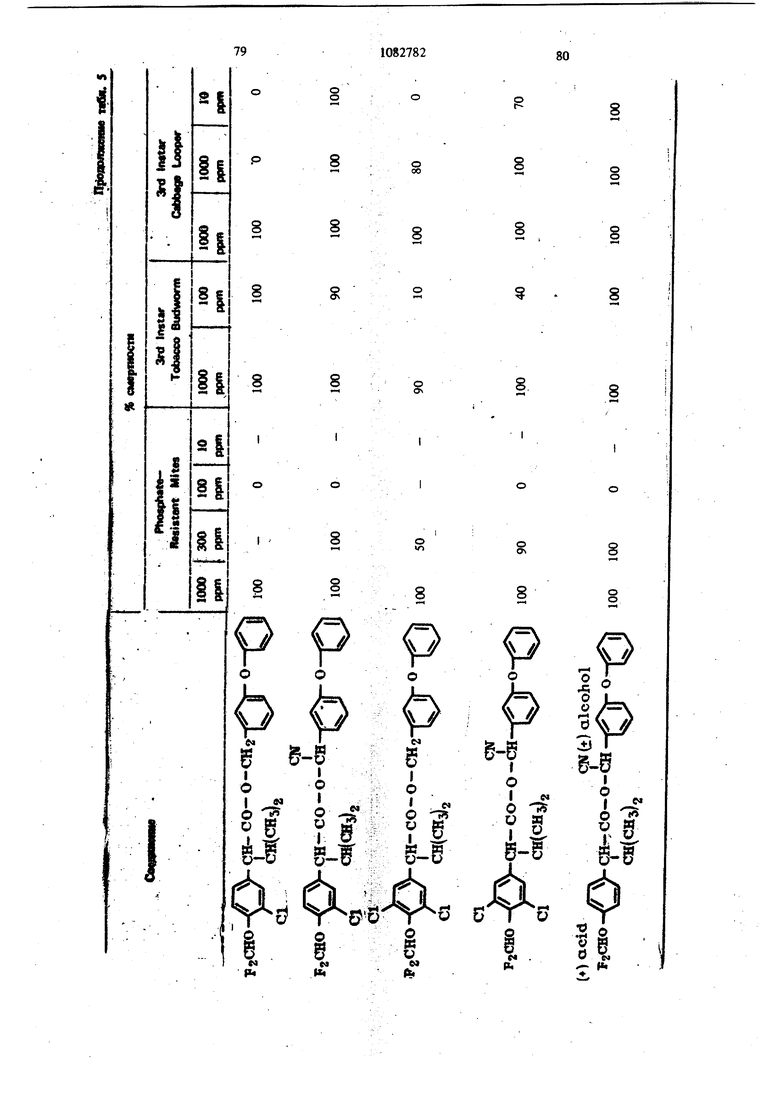
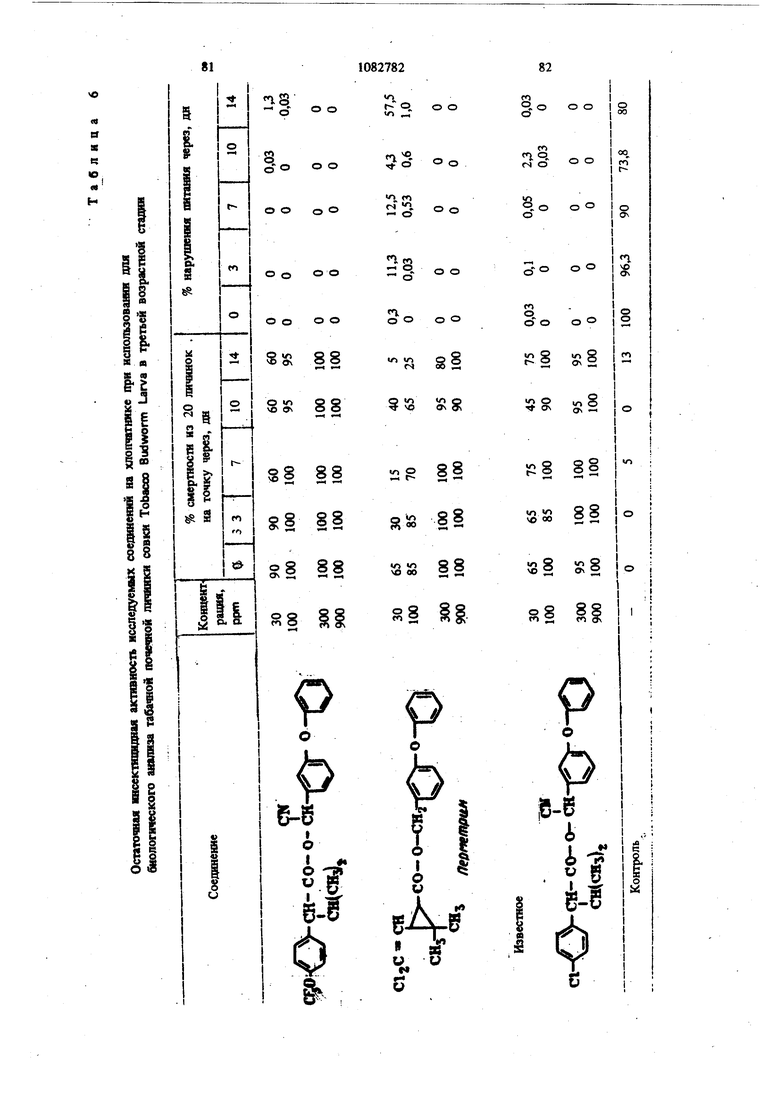
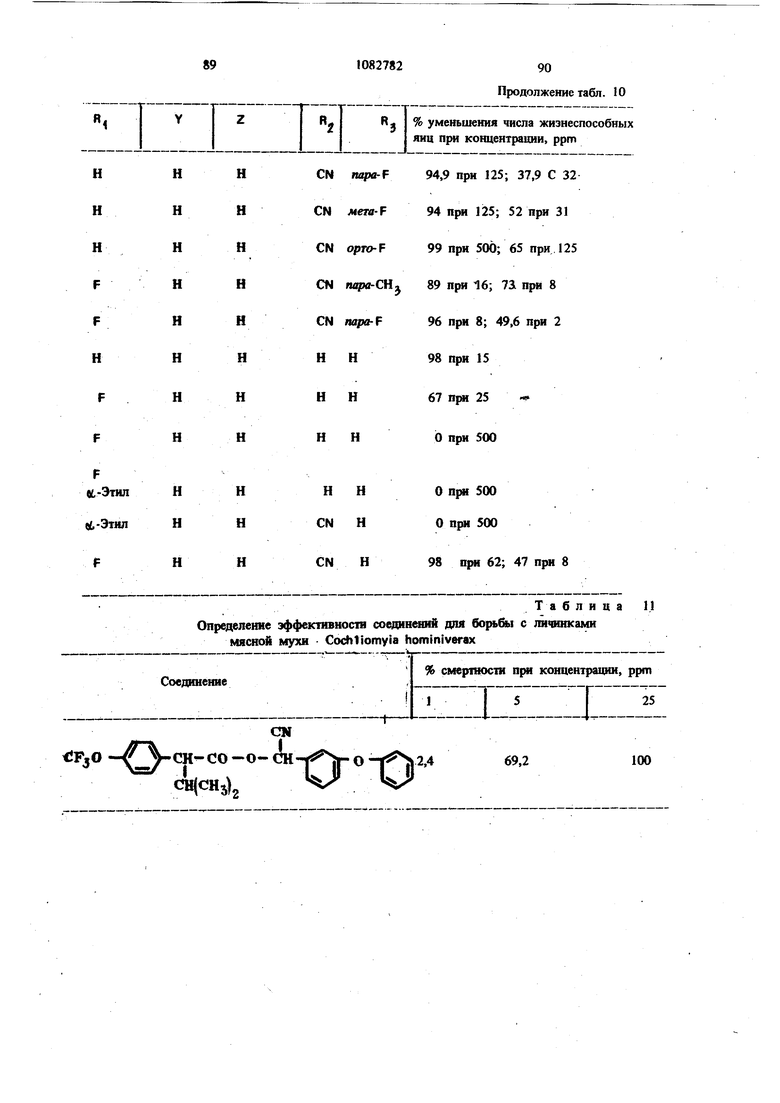
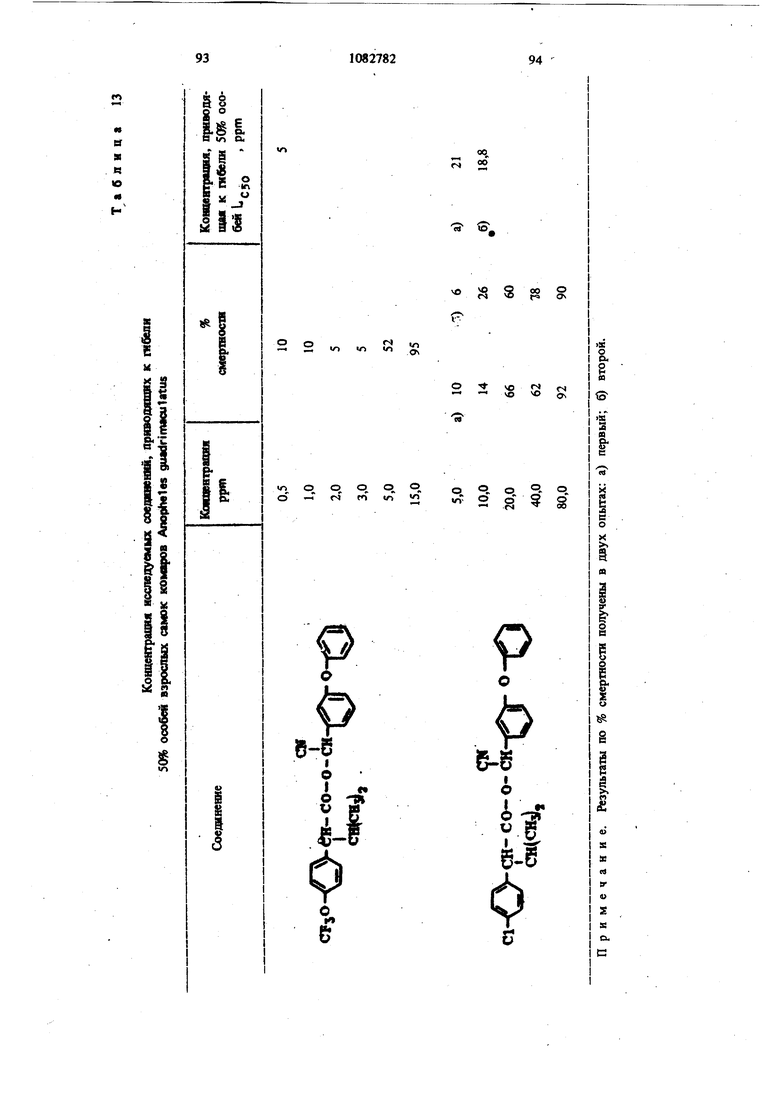
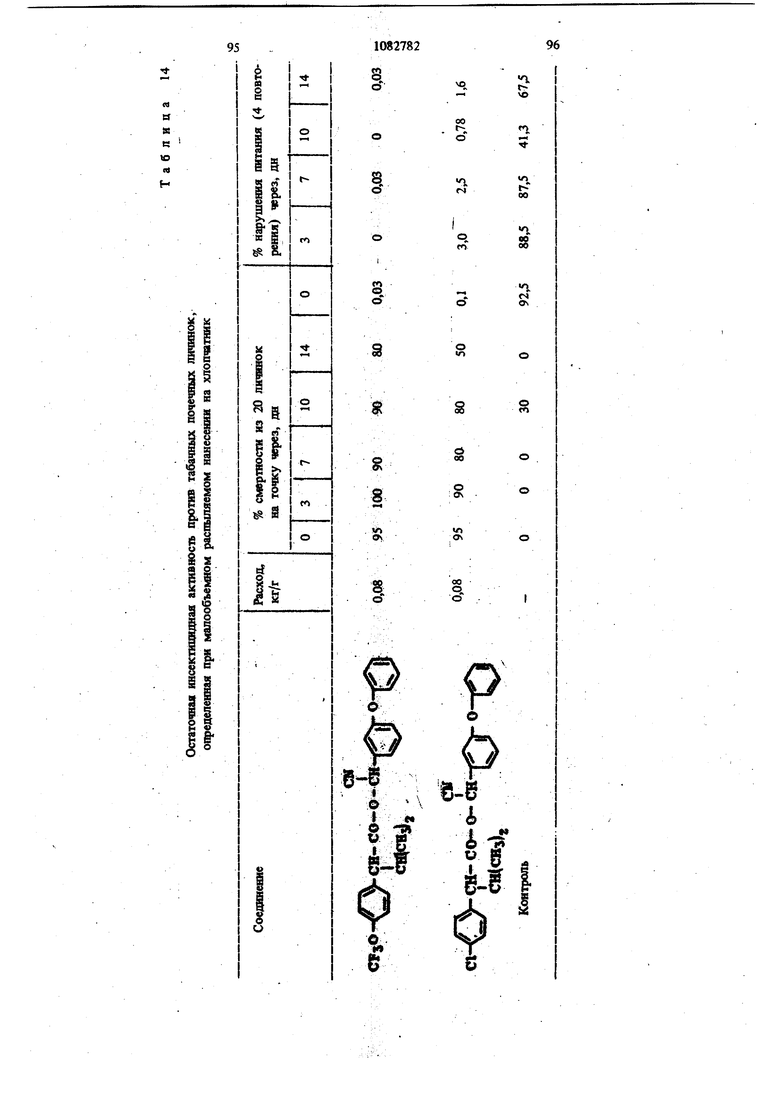
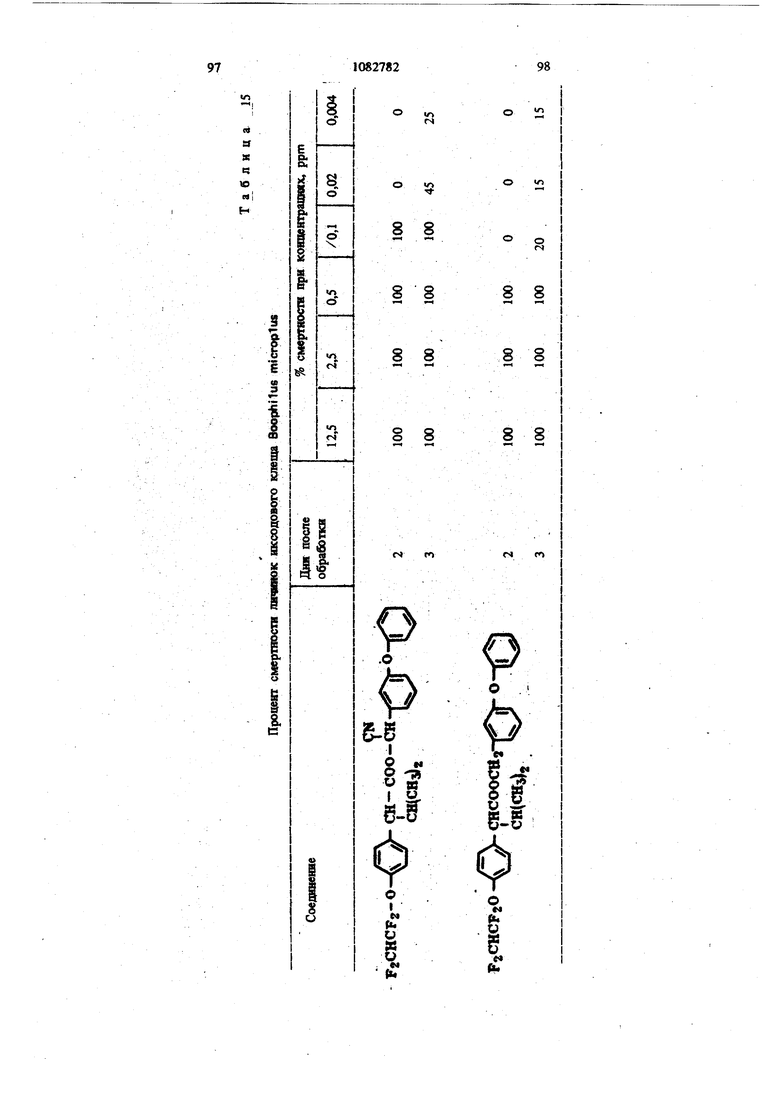
Для удобства при обращении и при погрузк их диспергируют в воде на месте использования, а затем наносят в виде распыляемого раствора на листву растений, почву или поверхность участка, который нужно обработать. Эмуль- , сифицируемый концентрат,-пригодный для защиты разнообразных культур, например хггебных злаков, капусты, тыквы, кукурузы, хлоп ка, табака, соевых бобов, декоративных расте ний и кустарников и т. п., может содержать, вес.%: активное вещество 20; эмульсификатор, используемый при приготовлении пиретроидны составов 4; поверхностно-активное вещество 4; органический растворитель (циклогексан) 25 и петролейный растворитель (минимальное ароматическое содержание 83 об.%) 47. Предлагаемые соединения при использовани их в качестве систематических инсектшщдиьк и иксодицидных средств для животных можно вводить в животное-хозяин либо орально, либо парентерально. При оральном введеиии его применяют в любой обычной форме, пред назначенной для орального введения (пилюля, капсула, таблетка или оральное, вливание). Активный агент можно также включить в пищу животному, такую как сбалансированное питание, содержащее 0,0001-0,1 вес.% (предпочтительно 0,001-0,05 вес.%) активного соединения. При необходимости систематическое инсектицидное и иксодицидное средства можн ввести в тело животного путем подкожной, внутримьплечной или внутрибрюшной инъекщш |С тем, чтобы оно распределилось по телу животного с током крови. Систематическое сред ство можно растворить или даспергировать в фармацевтически допустимом для введения носителе (вода, пропиленгликоль, растительное масло, глицеринформаль и т. п.). Систематические агенты обладают большим резервом безопасности и эффективности для защиты разнообразных животных, в частности домащнего скота и домашних животных (кру ный рогатый скот, овцы, лошади, собаки, коты и т.п.) от нападения блох, комаров, мух, клещей и т. п. В качестве инсектицидных и иксодицидных агентов наиболее эффективны следующие предлагаемые соединения: Метафеноксибензиловый сложный эфир изопрошш-Фтрифторометоксифеиилуксусной кислоты 5г -Циано-Метафеноксибензиловый сложный эфир оС -изопропил-4-трифторометоксифенилуксусной кислоты oi -Циано-Метафеноксибензиловый сложный эфир о -изопропил-3-трифторометоксифенилуксусной кислоты Ot -Циано-Метафеноксибензиловый сложный эфир Qt -изопропил-Фхлордифторометрксифенил уксусной кислоты «, -Метафеноксибензиловый сложный эфир ,(Х -изопропил-4(1,1,2,2-тетрафтороэтокси)фенит уксусной кислоты ОС -Циано-метафеноксибензиловый сложный эфир об -изопропил-4-пентафтороэтоксифеиилуксусной кислоты Метафеноксибензидо;вый сложный эфиро - этил- 3- трифторометоксифенилуксусной кислоты. У. -Циано-метафеноксибензиловый сложш эфир 06 -н-пропил-4-хлордифторометоксифешслуксусной кислоты et -Циано-метафеноксибензиловый сложный эфир об -1рег-бутш1-4-трифторометоксифенш1уксусной кислоты еС -Циано-матафеноксибензиловый сложный эфир 06 -изопропил-4-дифторометоксифенилуксусной кислоты est -Циано-метафеноксибензиловый сложный эфир()С, -изопропил-4-трифторометилтиофенилуксусной кислоты Метафеноксибензиловый сложный эфир ,ОС-этил-4-.трифторметилсильфинш1фёнилуксус- ной кислоты об -Циано-метафеноксибензиловый сложный эфир 06 -изопропил-З-дифторометилсульфонилфе нилуксусной кислоты ot -Циано-метафеноксибенэиловый сложный эфир об -этил-4-трифторометоксифенилуксусной КИСЛОТЬ oi -Циано-метафеноксибензиловый сложиый эфироО -изопропенил- 4- трифторометоксифенилуксусной кислоты Метафеноксибензиловый сложный зфир в6 изопропил- 3- бром- 4-дифторометоксифенилуксусной кислоты Qi -Циано-метафеноксибензиловый сложный зфир об -изопропил-З-хлор-4-дифторометоксифенилуксусной кислоты Метафеноксибензиловый сложный эфир (х;;-изопропил-4-хлор-4-дифторометоксифеш луксусной кислоты -Циано-метафеноксибензиловый сложный эфир OU -изопропил-З-бром-4-дифторометокгсифенилуксусной кислоты Метафеноксибензиловый сложный эфир 6t -п гопропил-3,5-дихлор-4-дифторометоксифенилуксусной кислоты с6 -Циано-метафеноксибеизиловый сложный эфир ОС -изопропил-3-ме1ИЛ-4-дафторометоксифенилуксусной кислоты ОС -Циано-метафеноксибензиловый сложный эфир ts6 -изопропил-З-фтор-4-дафторометоксифенилуксусной кислоты оС -Циано-метафеноксибензиловый сложный эфир оС-иэопрош1л-3-нитро-4-дифторометоксифенилуксусной кислоты ot-Циано-метафеноксибензиловый сложный эфир об -изопропил-З-метокси-4-дифторометоксифенилуксусной кислоты -Этинил-метафеноксибензиловый сложный зфир of- -изопропил-4-трнфторометоксифенилуксусной кислоты (+)-Oi -Циано-метафеноксибензиловый сложный эфир (4-)-()i-изопропил-4-дифторометоксифенилуксусной кислоты (t)-ot -изопропил-4-т{ |фторометоксифенилуксусной кислоты. Пример 1. метафеноксибен зилового эфира сб -изопропил-4-(1,1,2,2-тетрафторэтокот) фенилуксусной кислоты. К перемешиваемой смеси 6,81 г (0,0340 моль) метафеноксибензилового спирта, 3,0 мл (2,95 г, 0,0372 моль) безводного пиридина и 20 мл хлористого метилена добавляют в течение 20 мкн 20 мл раствора в хлори том метилене и 10,6 г (0,034 моль) 2-метш1-2- пара- (1,1,2,2-тетрафторэтокси) фгнил бутилхло{ШД8. Рвакщюнную смесь перемешивают при комнатной температуре 66 ч, а затем разбавляют 200 мл эфира. Эфирный раствор про мывают 200 мл 20%-ной соляной кислоты и 200 мл воды, высуишвают сульфатом натрия, отфильтровывают, а затем вьшартвают. . 16,24 г (100%). Этот продукт очищают на сухой силикагелевой колонке (116x5 см, элюент - 1:1 гексан-хлористый метилен), собирая пробы между 85 и 63 см (4ФОНТ растворителя 113 см). Получают 12,60 г (78%) прозрачного желтовато окрашенного масла. Вычислено,%: С 65,54; Н 5,08; F 15,95 C26H 4F404 Найдено,%: С 64,99; Н 4,96; F 19,10 Пример 2. Пол)гчениео6-циано-метафе нокетбензилового эфира oi -изопропил-4-(1,1,2 -тетрафтороэтокси) фенилуксусной кислоты. К перемешиваемой смеси 8,81 г (0,0333 моль) у, -цианЬ-метафеноксибензилового спирта, 3,0 мл (2,95 г, 0,0372 моль) безводного пиридина и 20 мл хлористого метилена добавляют в течение 20 мин 20 мл раствора 10,6 г (0,034 моль) 3-метил-2 яярв-(1,1,2,2-тетрафтор этокси) фенил бутиршхлорида в хлористом метилене. Реакционную смесь перемешивают при комнатной температуре 66 ч, а затем разбавляют 0 мл эфира, промывают 200 Мл 20%-ной (юляной кислоты и 200 мл воды, высушивают сульфатом натрия, отфильтровывают, а затем выпаривают до получения темнокрасного масла. Для того, чтобы удалить примесь метафеноксибензальдегида, масло подвергают реакиии с 0,5 г боргидрида натрия при температуре ледяной бани. Полученное масло очищают на силикагелевой безводной колонке (121х 5 см, элюент - 1:1 гексан-хлористый метилен), собирая пробы между 77 и 57 см (фронт растворителя 113 см). Получают 11,17 г (66%) прозрачного оран. жевого масла. Вычислено,%: С 64,67; Н 4,62; N 2,70; F 15,16 CnH.2,F4N04 220 Найдено,%: С 65,26; И 4,81; N 2,82; F 17,94 Пример 3. Получение оС -циано-метафеноксибензилового слохного эфира ci. -изопропил-4-трифторометоксифенилуксусной кислоты. Смесь (Х- -изопропил-4-трифторометоксифенилацетонитрила (2,0 г) и гидрата окиси калия (3,0 г в этилеигликоле (35 мл), а также воду (3 мл) нагревают при }40°С 8 ч. Раствор выливают в воду и экстрагируют эфиром (2x10 мл). Водный слой подкисляют разбавленной соляной кислотой и экстрагируют эфиром (3x10 мл), промывают водой (1x25 мл), высушивают и выпаривают до масла. Получают ОС -изопропил-4-трифторометоксифенилуксусную кислоту (1,23 г). ИК-спектр (чистый) 1700 см Раствор об -изопропил-4-трифторометоксифенилуксусной кислоты (1,2 г) и хлористого тионила (0,6 мл) в бензоле (5 мл) кипятят с обратным холодильником 4 ч. Выпариванием растворителя и избытка хлористого тионила получают хлористый об -изопропи:л-4-трифторометоксифенилацегил. Раствор хлористого об -изопропил-4-трифторометоксифенилаЦетила (4,58 ммоль) в эфире « (5 мл) добавляют к эфирному (20 мл) раствору об -циано-метафеноксибензилового спирта(4,58 ммоль) и пиридина (0,5 мл). Смесь перемешивают в течение ночи и отфильтровывают. Фильтрат после промывки выпаривают и остаточное масло очишают на силикагелевых пластинах 5x2 мм, используя в качестве элюента смесь 1:1 хлористого метилена и гексана. Зону с R - 0,55 экстрагируют простым эфиром и выпаривают, чтобы получить нужный сложный эфир (0,85 г). ИК-спектр (чистый) 1755 см . ЯМР (CDCC1);5 6,8-7,6 (т, 13 Н, ароматический Н); 6,31 и 6,28 (s, 1Н,-СН-Ar); 3,27(|, J 7 Гц, 1Н, -СН-СН(СНз)г); CN 2,0-2,6 (т lH,-CHCHj); 0,6-1,2 (четыре дублета, V 7 Гц, 6Н, изопропиловый СН); 19f химический сдвиг 58,8 S по отношению к Пример 4. Получение метафеноксибензилового сложного фира oL -изопропил-4-трИ фторометоксифенилуксусной кислоты. 1 К раствору метафеноксибензилового спирта (1,89 г) и пиридина (1 мл) в хлористом метилене (6 мл) добавляют раствор в хлористом метилене (7 мл) оС -изопропил-4-трифторометоксифенилацетил хлорида, полученного из соответствующей кислоты (2,46 г) аналогично при- с меру 3. После перемешивания реакционной смеси в течение ночи ее промьшают водой, разбавленным раствором соляной кислоты и разбавленным раствором гидрата окиси калия и выпаривают до оранжевого масла. Очисткой с помощью силикагелевой хромате графин получэтат нужный сложный эфир (2,76 г). ИК-спектр (чистый) 1738 . ЯМР (CDClj) 6,73-7,45 (m, 13Н); 5,03 (s ,2Н); 3,20 (OC,J 10,5 Гц,1Н); 2,26 (m, IH); 0,66 и 0,94 (два об, J 6,6 Гц, 6Н). Пример 5. Получение сложных эфиров оС-этил- ио -н-пропил-4-трифторометоксифенилуксусной кислоты. (1 -Этил-4-трифторометокснфенил)тссусную и ot -н-пропил-4-трифторометоксифенилуксусную кислоты превращают в сложные эфи{я 1 аналогн но примерам 3 и 4 соответственно (табл. 1). Пример 6. Получение об -циано-метафен оксибензнлового сложного эфира 2-изопрошш-4-трифторометилтиофенидуксусной кислоты. о(, -Изопропил-4-трифторометилтиофеннлацето нитрил (6,9 г, 0,0265 моль) и 50%-ный гидрат окиси натрия (25 г, 0,312 моль) смешиваю± в 53 мл 31131ленп1иколя и нагревают с умеренной флегмой 18 ч. Реакционную смесь выливают в ледяную воду и экстрагируют эфиром. Водну фазу подкисляют концентрированной НС1, затем повторно экстрагируют эфиром, экстракт промьшают водой и высушивают над сульфатом натрия. Выпаривание под вакуумом дает 2,05 г маслянистого продукта об -изопропид-4-трифторометилтиофенилуксусной кислоты. Чтобы синтезировать соответственно об -этил-4-трифторометилтиофенилуксусную иоС-и-прошш-4-трифторомегилтиоуксусную кислоты в качестве исходного материала используют ot - зтил- 4- трифторометилтиофенилацетонит|яш или ей-н-пропил-4-трифторометилтиофенилацетоиитрил. Используясь - изопропи л- 4-трифторометилтиоферилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде масла. Вьиислено,%: С 64,32; Н 4,57; F 11,74; N 2,79; S 6,60 Найдено,%: С 64,27; Н 4,62; F 11,68; N 2,68. S 6,43. Сравнимые результаты получают, используя л -этнл-Фтрифторометилтиофениизтссусную или и-«-прош1л-4-трифторометилтиофенилуксусную кислоты, чтобы синтезировать соответственно о(,-циано--метафеиоксибензиловый сложный эфир с -зтил-4-трифторометилтиофенш1уксусной кислоты и oL -циано-метафеноксибензиловый сложный эфир об -Н-пропил-4-трифторометилтиофенилуксусной кислоты. Пример 7. Получение метафеноксибензилового сложного эфира с -изопрош1Л-4-трифторометилтиофенилуксусной кислоты. ИспользуяоС -изопрош1л-4-трифторометилтиофенилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде масла. Пример 8. Получение ot -диано-метафеноксибензилового сложного эфира об -изопропил-4-дифторометилтиофенилуксусной кислоты. Гидрат окиси натрия (18,4 г, 0,46 моль) в 50 мл воды и с -изопропил-4-меркаптофенилуксусную кислоту (11 г, 0,05 моль) в 40 мл диоксана смшшвают и нагревают до 50С. Хлордифторометан (фреон-22) барботирзчот медленно под поверхность жидкости, вызывая непосредственное экзотермическое повышение температуры до 75 С. Добавление продолжают до тех пор, пока экзотермическое выделение тепла не начинает медпенно спадать (пртмерно 0,5 ч). Рзакционную смесь охлаждают до комнатной температуры и обрабатывают 100 мл ледяной воды. Водный слой экстрагируют 3X 200 мл эфира, затем подкисляют при 15-20 С концентрированной HCl. Полученное масло удаляют зфн{Я)ой экстракцией. Эфирный раствор промывают водой и насыщенньпм хлористым натрием перед высушиванием над сульфатом натртя и выпариванием в вакууме. Получают 10,2 г темно-коричневой смолы ot -изопро1Шл-4-дифторометил1Нофенилуксусной кислоты, которую используют без послед}гющей очистки. Аналснично получают об -изопрошш-З-хлор-Ф -дифторЮметилтиофаяшуксусную кислоту, используя оС -изопрош1л-3-хлор-4-ме1Исаптофенилуксусную кислоту. При использовании о -изопрош1Л-4-дифторомепштиофенилуксусясш кислоты аналогично примерам 3 и 4 получают продукт в виде масла. Высислено,%: С 66,79; Н 4,96; F 8,13; N 3,00; S 6,86. CzfeH FiNO S Найдено,%: С 66,59; Н 5,13; F 8,02; N 2,8; S 6,95. Пример 9. Получение метафеноксибензилового сложного эфира oi, -изопропил-4-ди- : фторометоксифенилуксусной кислоты. В перемешиваемую магнитной мешалкой при 8(гС смесь 10,00 г (0,0515 моль) об -изопропил-4-оксифенилуксусной кислоты, 65 мл диоксана, 19,08-г (0,464 моль) гидрата окиси натрия и 30 мл воды барботируют 47 г (0,532 моль) хлордифторометана в течение 4ч . Реакционную смесь выливают в 250 мл ледяной воды, промывают эфиром, подкисляют концентрированной соляной кислоты до рН 3, а затем экстрагируют 200 мл эфира. Эфирный раствор промьшают один раз 100 мл воды, высушивают сульфатом натрия, фильтруют, Ъ затем выпаривают, получая белую пасту. Добавляют смесь гексана и хлористого метилена и полученную смесь отфильтровывают, чтобы удалить твердое вещество - исходный материал Фнлырат выпаривают. Получают 5,41 г прозрачного коричневого масла ot -изопропил-4-дифторометоксифенилук сусной кислоты чистотой не менее 85%. ЯМР (СОССЦ-о 5-пиридин) S 7,43, (оС, J 8,2 Гц, 2Н); 7,08 (об, J 8,2 Гц, 2Н) ; 6,57 (t, J 74,3 Гц, Ш); 3,63 (S, примесь); 3,25 (d, J 10 Гц, 1Н); 2,37 (т, Ш); 1,19 (d, J 6,5 Гц, ЗН); 0,78 (d. J 6,5 Гц, ЗН); 13,82 (s, Ш). Аналогично получают об-этил-4-дифторометок(жфеннлуксусн)пю и в6 я-пропил-Фдафторометокетфеннлуксусную кислоты, применяя е6-эяш-4-окснфеннлуксусную или oL- -н-прошл4-оксифенилуксусную кислоту соответственно. Используя оС-изопропил-4-дифторомётокс№ фенилуксусную кислоту, аналогично примерам 3 и 4, получают нродук± в виде бледно-желтог . масла. Вычислено.%: С 70,41; Н 5,67; F 8,91 Cj H24FjO4 Найдено,: С 73,36; Н 5,96; F 10,56 Сравнимые результаты получают, используя вй-этил-4-дифторометоксифенилуксусную ишс о, претил-4-дифторометоксифенилуксусную кислоту, чтобы синтезировать метафенокеибенэиловый сложный эфир oi -этил-4-дифторометоксифенилуксусной или -и-пропил-Фдифтора метоксифенилуксусной кислоты соответственно Пример 10. Получение -циано-метафеноксибензилового сложного эфира 6i -изопропил-Фдифторометоксифенилуксусной кислоты. Используя об -изопропил-4-дифторометоксифенилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде масла. ЯМР (CDCC1,) S 0,88 (четыре дублета, J 6 Гц, 6Н, СН,); 2,30 (т, 1Н,-СН-СН(СН,)); 3,24 (et, J 10,1 Гц, Ш, -СН-СН (СН.),); 6,33 (два синглета, Ш, -CHCN); 6,45 (t, J 74 Гц, Ш, СН,0-); 7,16 (т,ВН ароматический Н). Вычнслено,%: С 69,17; Н 5,13; F 8,42; N 3,10 CigH2, Найдено,: С 69,41; Н 5,20; F 10,25; N 3,70 Срав1шмые результатьг получают, используя ti -зтил-4-днфторометоксифенилуксусную или ot -к-пропил-4-дифторометоксифенилуксусную кислоту, чтобы синтезировать с -циане-метафе нокосбензиловый сложный эфир об -этил-4-дифторометоксифенилуксусной кислоты и об -циано-метафеноксибензиловый сложный эфир ei -«-11р011Ил-4-дифтороме1оксифенилуксусн6й кислоты соответственно. Пример 11. Получение метафеноксибензилового сложного эфира об -изопропил-4трифторометилсульфинилфенилуксусной кислоты Смесь 10,0 г метафеноксибензилового сложного эфира oi -изопропил-4-трифторометилтиофенилуксусной кислоты и 4,1 г метахлорнадбензойной кислоты (85%) нагревают в 100 мл хлористого метилена в течение нескольких часов, а затем отфильтровывают. Сконцентрированный остаток очищают из силикагелевой сухой колонке (2:1 хлористый метиле| -гекЬан). Получают продукт в виде бледно-желтого масла. Аналогично получают метафеноксибензиловый сложный эфир об -этил-4-трнфторометилсульфишлфенилуксусной кислоты и метафеноксибензиловый сложный эфир об -н-пропил-4-трифторометилсульфинилфенилуксусной кислоты, используя метафеноксибензиловый сложный эфир -этил-4-трифторометиптиофенилуксусной кислоты или метафеноксибензиловый сложный эфир 6i -к-пропил-4-трифторометилтиофенилуксусной кислоты соответственно. Пример 12. Получение о4 -циано-мета. фёноксибензилового сложного эфира об -этил-3-дифторометилсупьфонилфенилуксусной кислоты. Смесь 10,0 г об -циано-метафеноксибензилового сложного эфира об -этнл-3-дифторометилтиофенилуксусной кислоты и 9,0 г метахлорнадбензойной кислоты (85%) кипятят с обрат- / ным холодильником в 100 мл дихлорэтана в течение ночи. Смесь после фильтрования и концентрирования очищают хроматографически на сухой колонке силикагеля (2:1) хлористый метилен-гексан). Получают продукт в виде желтого масла. Аналогично получают об -циано-метафеноксибензиловый сложный эфир у, -изопропил-4-трифторометилсульфонилфеиилуксусной кислоты и oi -циано-метафеноксибензиловый сложный эфир oi -н-пропил-4-трифторометилсульфонш1фенилуксусной кислоты, используя ot -циано метафеноксибензиловый сложный эфир об -изопрОпил-4-трифторометилтиофенилуксусной кислоты или d -циано-метафеноксибензиловый сложный эфир об -н-пропил-4-трифторометилтиофенилуксусной кислоты соответственно. Пример 12. Получение метафеноксибензилового сложного эфира 4-трифторометоксИОб-изопропешшфенилуксусной кислоты. К раствору ларй-трифторометоксифенилуксусной кислоты (22 г, 0,1 моль), полученной щелочным гидролизом в эфире (50 мл) добавляют при температуре ледяной бани раствор хлористого изопрошшмагния (0,2 моль) 25 в эфире. Реакционную смесь перемешивают в течение 2 ч при комнатной температуре, к ней добавляют безводный ацетон (5,8 г, 0,1 моль) кипятят с обратным холодильником в течение 5 ч, охлаждают, осторожно подкисляют водной серной кислотой и экстрагируют эфиром. Смешанные органические слои экстрагируют 10%-ным раствором карбоната натрия. Щелочно слой подкисляют соляной кислотой и экстраги руют эфиром. Эфирный экстракт высушивают (NartSO) и выпаривают. Получают Фтртфторо метокси- /,/3-диметилатропиновую кислоту. К раствору 4-трифторометокси-/3 ,-диметилатропиновой кислоты (13,9 г, 0,05 моль) и триэтиламнна (6,1 г, 0,06 моль) в ацетоне (100 мл) доба вляют метафеноксибензилбромид (13,2 г, 0,05 моль) при температуре ледяной бани, после чего смесь кипятят с обратным холодильником 4 ч. Смесь выливают в холодную разбавленную соляную кислоту и экстрагируют эфиром. Эфирный слой промьшают 10%-ной соляной кислотой и водой, высуши1вают (NagSO Л и выпаривают, получая эфир оксикислоты, который обезвоживают ® золе при в течение 18 ч. Фильтрованием и удалением растворителя получают неочищенный сложньш эфир. Очистка материала хроматографией на сухой иолоике сшшкагеля (50:50 хлористый метилен - гексан в качеств растворителя) дает продукт в виде бледно-жаь тои смолы. Пример 13. Получениеоб-циано-метафеноксибензилового сложного эфира оС -JpcT бутил-4-трифторометоксифенилуксусной кислоты. Хлористый неопентил превращают в реактив Гриньяра Н подвергают последующей карбонизации углекислым газом по способу Вайнштейна и Морзе. Получают 2-7рйГ-бутил-4-трифторометоксифетилуксусную ютслоту в виде белого твердого вещества. Пример 14. Получение метафеиоксибензнлового сложного эфира об -изопропил-Збром-4-дафторометоксифешшуксусной кислоты Смесь ОС -изопрошш-4 оксифенилуксусной кислоты (20 г, 103 моль) в хлороформе (250 мл) охлаждают до О С и., д.обавляют бром (16,5 г, 0,103 моль) в хпорофо1 е (15 мл) в течение 30 warn. Реакционный раствор перемешявш т при О С 30 мин, а затем оставляют нагреваться до комватнсж температуры. Рвство{Штель вьшарившрт, а остаток перекрисгаллиэотывают из ал&зя гексан-бензоя. Получают монобромпроизводвое Об -язопрс 101Л-4-окскф ашуксусиой кислоты (22,1 г) ст.пл. ПЗ-пЛ. 2 Oi - Изопропил- 3- бром- 4- оксифенилуксусную кислоту (18,0 г) превращают в соответствующую дифторометоксикислоту. об -Изопропил- 3- бром- 4- дифторометоксифенилуксусную кислоту получают в виде воскообразного твердо-, го вещества (4,7 г) путем отделения непрореагировавщего исходного материала с помощью хроматографии на силикагеле (элюент 3,5%-ный метанол в хлороформе). Используя 0 -изопропил-З-бром-4-дифторометоксифенилуксусную кислоту, аналогично примерам 3 и 4, получают продукт в виде бледногжелтой смолы. ЯМР (СОССЦ) S 6,8-7,7 (т, 12Н, , ароматический Н); 6,45 (t, J 7,4 Гц, 1Н, OCHf); 5,10 (bs, IH, СН); 3,18 d, J 9 Гц, Ш, СН - СН(СНз)2); 1,0 и 0,71 (2d. J 6 Гц, 6Н, изопропиловый СН). Пример 15. Получение об -циано-метафеноксибензилового сложного эфира в6 -таопропил-3-бром-4-дифторометоксифенш1уксусной кислоты. Используя об - Изопропил-3-бром-4-дифторометоксифенилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде желтой смолы. ЯМР (CDCCl,) 6,9-7,7 (m, 12Н, ароматический Н); 6,50 (t, J 74 Гц, Ш, ОСНР); 6,33 и 6,36 (2 S, Ш, CH-CN); 3,25 (oi, СН-СН(СН)); 0,6-1,1 (4d, 6Н, изопропиловый СН). Пример 16. Получениеоб-циано-мета- феноксибензилового сложного эфира об -изопропил- 3- хлор- 4- дифторометоксифенилуксуснсШ кислоты. Смесь оС -изопропил-4-оксифенилуксусной кислоты (30 г, 0,154 моль) в хлороформе (600 мл) охлаждают до температуры , медленно барботируют газообразный хлор (12,0 г, 0,169 моль) и отгоняют растворитель Получают лС -изопропш1-3-хлор-4-оксифе-1 нилуксусную кислоту перекристаллизацией из смеси бензол-гексан. Т. пл. 125-128 С. Используя aJ -изопропил-З-хлор-4-оксифениЯ уксусную кислоту, аналогично примерам 9, 3 и 4 получают продукт в ввде смолы. ЯМР (CDCC1)5 6,8-7,5 (m, 12Н, ароматический); 6,50 (t, J 74 Гц, Ш, OCHF); 6,33 и 6,30 (2s, IH, -CH-CN); 3,25 (d. J 10 Гц, Ш, СН-СН(СН)2). Вычислено,%: С 64,26; Н 4,56; N 2,88; С1 7,30; F 7,82 С2бН22С1Р2 NO4. Найдено,%: С 64,27; Н 4,70; N 2,94; С1 7,20; F 7,78. Пример 17. Получение метафеиокси бензилового сложного эфира об -Изопропил-3-хлор-4-д11фторометоксифенилуксусной кислоты. Используя об -изопропил-З-хлор-Фоксифёнилу сусную кислоту, аналогично примерам 9, 3 и 4 получают продукт в виде желтого масла. ЯМР (CDCC1.2)8 6,8-7,6 (m, 12Н, ароматический If); 6,47 ( t, J 74 Гц, OCHF), 5,07 (bs, 2H, CH). Вычислено,%: С 65,16; Н 5,03; Cl 7,69; F 8,24 Ci H ClfyO Найдено,%: С 65,46;. Н 5,05; Cl 7,73; Пример 18. ПолучениеоС-даано-метафеиоксибензилового сложного эфира об -изопропил-З-бром-4-дИфторометоксифенилуксусной, кислоты. Смесь оС-изопропШ1-4-оксифейилуксусной кислоты (30 г, 0,155 моль) в хлороформе (SCO мл) ошьно охлаждают в бане лед-соль. Газообразный хлор (примерно 30-35 г) барботируют 1ФИ 0-5°С 90 мин. Раствор перемешивают при О-5С 1 ч и оставляют нагревать ся до комнатной температуры. Выпаривают растворттель. Получают et -изопропил-3,5-дихлор-4-оксифенилуксусную кислоту в виде белого твердо го вещества (29,8 г) перекристаллизацией из гексана. Т. пл. 152-154°С. i Используя полученный OL -изопропил-3,5дахлор-4-оксифенилуксусную кислоту, аналогично примеру 9 получают оС -изопропил-3,5Д1ИОЮр-4-дифторометоксифенилуксусную кислоту а виде масла с содержанием 15 моль% исходного материала. Исполз я с6-изопропил-3,5-дйхлор-4-дифт{ р меток«яйфе1шлуксусную кислоту, аналогично пртмёрам 3 и 4 получают продукт в виде желтой смолы. ЯМР(СОСС1а)8 6,9-7,7 (т, 1Ш, ароматячесК1Й Н); 6,67 (t, J « 74 Гц, Ш. OCHg) 6,33 Н 6,40 (28, Н, CH-CN); 3,23 (оС , J - 10 Гц, Ш, СН-СН(СНз)2) 0,6-4,1 (4с, 6Н, изопрошшовьш СНЛ. Выадслено,%: С 60,01; Н 4,07; N 2,69. NO Найде1Ю %: С 59,78; Н 4,30; N 2,31. П р и м е р 19. Получение метафеяоксибеизршового сложного эфира об -изопропил-3,3 -дихлор-4-дифторометоксифенилуксусной кислоты. Используя ot -изопропил-3,5-дихлор-4-дифторокютоксифенилуксушую кислоту, аналогично примерам 3 и 4 получают продукт в виде смолы. Вычиспено,%: С 60,61; Н 4,48; С1 14,32; F 7,67; Найдено,%: С 60,50; Н 4,60; С1 14,13; F 7,52 Пример 20. Получение sL -циано-метафеноксибензилового сложного эфира об -изопропил-З-метил-4-дифторометоксифенилуксусной кисл-эты. З-Метил-4-метоксифенилацетонитрил преравщают в uL -изопропил-З-метил-4-дифторометоксифенилуксусную кислоту. Продукт загрязнен ot -изопрогшл- 3- мегил-4- оксифенилуксусной кислотой. Конечный сложный эфир очищают хроматографически. Сложный эфир имеет вид вязкого масла. ЯМР (CDClj) 6,8-7,6 (m, 12Н, ароматический Н); 6,45 (t, J 74 Гц, Ш, OCHF); 6,48 и 6,53 (2s, Ш, CH-CN); 2,25 (s, ЗН, СН). Вычислено,%; С 69,66; Н 5,41; N 3,01 Найдено,%: С 70,05; Н 5,86; N 2,83 Пример 21. Получение об -циано-метафеноксибензилового сложного эфира оС -изопропил-3-фтор-4-дифторометоксифенилуксуснойкислоты. Исходя из об -изопрогшл-З-фтор-4-дифторометоксифенилуксусной кислоты аналогично примерам 3 и 4 получают целевой сложный эфир в виде :келтого масла.. ЯМР (CDCClj) 6,8-7,5 (m, 12Н, ароматический Н); 6,63 (t, J 74 Гц, 1Н, OCHF4), 6,33 и 6,37 (2s, Ш, CH-CN). Вычислено,%: С 66,52; Н 4,72; N 2,98 Найдено,%: С 66,27; Н 4,87; N 2,99 Пример 22. Получение ОС -циано-метафеноксибензилового сложного эфира об -изопропил-З-нитро-4-дифторометоксифенилуксусной кислоты. Используя ОС -изопропил-З-нитро-4-оксифенилуксусную кислоту, аналогично примеру 9 получают oi -изопропил-З-нитро-4-дифторометоксифенилуксусную кислоту в виде неочищенного материала, содержащего непрореагировавший исходный материал. Однако в результате трехкратного повторения реакоди с фреоном -22 получают продукт в виде мелких бежевых твердых частиц (гек-. сан), т. пл. 88-90 С. Используя Сб -изопропил-З-нитро-4-дйфторометоксифенилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде желтого масла. Вычислено,: С 62,90; Н 4,47; N 5,64 Найдено,%: С 62,51; Н 4,77; N 5,58. Пример 23. Получение ей -1щано-метафеноксибензилового сложного эфира оС, -изопропил-3- метокси-4-дифторометоксифенилуксусной кислоты. Используя об -изопропил-3-метоксИ-4-дйфто ромеюксифенилуксусную кислоту, аналогично примерам 3 и 4 получают продукт в виде смолы. Пример 24. Получение замещенных ( -циано-метафеноксибензиловых сложных эфиров фтороалкоксифеннлуксусных кислот. Исходя либо из об -изопропил-4-дифторомет оксифешшуксусной кислоты, либо из с6 -изопро пил-4-трифторометоксифенилуксусной кислоты цианогидрина соответственного замещенного аль гида аналогично примерам 3 и 4 получают сложные эфиры, представленные в табл. 2. Пример 25. Получение М -этинилмет феноксибензилового сложного зфнра об -изопропил- 4- тряфторюметоксифенилуксусной кислоты.. Ацетилен сушат тремя ловушками: сухим : льдом-ацетоном, концентрированной серной ки лотой и хлористым кальцием, а затем барботи руют под давлением 0,35 атм в безводный тетрапщрофуран (100 мл) в течение 10 мин. БрОАгастый этилмагний (0,14 моль) добавляют по каплям в течение 2 ч с такой скоростью, чтобы шьвделение этана было медленным и устойчивым. Затем ацетилен барботируют в те чение 15 мин. К реакздн добавляют метафене оксибензахгьдегид (27,7 г, 0,14 моль) в тетрапщрофуране (25 мл) при 15-20 С. Реакционной смеси дают нагреться до комнатной тем пературы и ее перемешивают в течение ночи Комплекс разлагают насьпценным растовром хлористого аммония. Продукт экстрагируютэфиром, промывают водой и высущивают (). Выпариванием растворителей с последующей вакуумной перегонкой с помощью аппарата Кугельгона получают нужный ( -этинилметафеноксибензиловый спирт (21,5 г). Используя указанный спирт н oi -изопрошш 4-трифторометоксяфенилуксусную кислоту, аналогично примерам 3 и 4, пол)1ают продукт в виде желтой смолы. Спектр ЯМР показывает характерный алкиниловый протон в виде мультиплета при о 2,52 и бензиловые протрны при 8 6,35. Вычнслено,%: С 69,22; Н 4,95 Найдено.%: С 68,17; Н 4,11 Аналогично получают згтн г т фбнокаябензнловый сложный эфир вС -изопропш1-4-дифторометоксифенилуксусной кислоты, использ спирт н в6 -изопрошш-4-дифторомет . оксифешшуксусную кислоту. Вычислено,: С 71,99; Н 5,37 C2iH24F204 Найдено,%: С Н 5,53 П р и 1ЙГе р 26. Получение (4)-в6-1шаномеим оксибензилового сложного эфира (f)- ct-изопропил-4-дифторометоксифенилуксусной кислоты. Теплый раствор (60°С) (-)-2-фениламина (4,96 г) в водном этаноле (60% этанола, 20 мл) добавляют к теплому раствору (60 С) рацемической кислоты (20 г) в водном этаноле (60% этанола, 50 мп) при перемешивании магнитной мешалкой. Так как раствору дают медленно остыть до комнатной температуры, происходит осаждение соли в виде белого кристаллического твердого вещества. Смесь оставляют стоять в течение ночи и твердые вещества собирают фильтрованием, промывают : водным этанолом (JO мл) и высущивают (9,5 г). Т. пл. 184-188 с. Вьщеленная кислота, полученная из указанной соли имеет вращение ot J. +37,1° (CHCIj, С 1,439 г/100 мл). Две последующие кристаллизации указанной соли из водного этанола (60% этанола) дают белые иглы с т. пл. 185-187с, причем вьщеленная нз них oi - изопропил-4-дифторометоксифенилуксусная кислота имеет вращение О + 40,4° (CHClj, С 1,353 г/100 мл). Выделенную (+)-кислоту превращают в сложный эфир аналогично примерам 3 н 4. ЯМР (CDCCli,) S 6,8-7,5 (m, 13Н, ароматический Н); 6,43 (t, J 74 Гц, 1Н, OCHFj); 6,30 и 6,23, (23, Ш, CH-CN); 3,27 (o.,J Ш Гц, Ш, СН-СН(СН)). I Пример 27. Получение (+)-(з6-Циано1 метафеноксибензилового сложного эфира (+) и (-) - 0 -изопропнл- 4- трифторометоксифенилуксусной кислоты. Смесь рацемической кислоты (26,2 г) и (-)-в6-фенэтиламина (12,1 г) в водном этаноле (60% этанол, 2 л) нагревают до растворения на паровой бане и оставляют медленно остывать до комнатной температуры. Соль собирают фильтрованием и высушивают (16,9 г). Т. пл. 189-193 С. Соль дважды перекристаллизовывают из водного этанола (60% этанол, 1 л и 600 мл соответственно). Т. пл. 194-19бс (8,0 г). (+)-ОС-изопропнл-4-трифторометоксифенш1уксусн)то кислоту получают путем нейтрализации соли разбавленной соляной кислотой с последующей экстракцией эфиром и выпариванием растворителя, ot 1: + 35,5(СНС1я), С 6,0 г/100 мл). Используя (+) - ot -изопропил-4-трифторометоксифенилуксусную кислоту, аналогично примерам 3 и 5 получают продукт в виде бледножелтого масла: ctj5) 6,1(СНСЦ, С 5 г/100 мл). Пример 28. Инсектицидная активность. Инсектицидную активность предлагаемых соединений проверяли на следующих видах насекомых: гусеница почек табака Heliotlus viresce (Фабр1цнус); западная картофельная вд кадка Empoasca abrupta (Делонг) и тля бобовую Aphis fabac (Скополи). Табачная почечная гусеница (Tobacco Bud- worm) Heliotlus virescens (Фабрициус). Перв возрастная стадия. Хлопковый росток с двумя распустившими ся листками опустили на 3 с при перемешива нии в раствор (35% водь и 65% ацетона), содержащий 3(Ю; 100 или 30 ррт исследуемого соединения. Каждый лист поместили в чашку с тампоном и перед закрыванием чашки крышкой добавили кусок марли, зараженный 50-100 только что выведенными личинками. Через 3 дн. при ЗО F и относительней влажности 50%. При исследовании чашки отметили смерть только что вылупившихся литанок. Полученные результаты приведены в табл. 3. Тля бобовая (Bean. Aphid) Aphis fabac (Скадюли).. Пять сантиметровых волокнистых горшочков, каждый из которых содержал росток настурции высотой 2 дюйма и был заражен за 2 дн до этого 100-150 тлями, поместили на вращающийся стол, поворачивающийся со скоростью 4 об/мин и опрыскали раствором (35% воды w 65% ацетона), содержащим 100; 10; 1,0 и 0,1 ррт исследуемого соединения, в течение 2 об, .используя распылитель Devibiss Atomizez и давление воздуха 20 фун тов/даойм примерно в 15 см от растений. Оп{Я 1скиваемый раствор направили таким образом, чтобы полностью покрыть тлей растения. Опрысканные растения поместили на соот ветсгаующне стороны белых эмалированных подаосов. Смертность оценивали через один день при 70 F относительной влажности 50%. Результаты приведены в табл. 3. Западная картофельная цикадка Empoasea abrupta (Делонг). Росток лимской фасоли с распустившимися первичными листьями 3-4 дюймов погрузили в раствор (35% воды и 65% ацетона), содержащий 100; 10 или 1 ррт исследуемого соединен;. Погруженные растения поместили в лытяжной шкаф, чтобы высушить, а затем отрезали 2,5 см кончика одного листа и поме тили в 4-дюймовую чашку Петри с влажной филь ровальжй бумагой на дне. 3-10 нимф во ВТОрой стадии превращения положили в чашку Пет{«, затем чашку закрывали. Смертность . оценивали после вьщерживания подготовленны тают образом чашек в течение 2 дн при 80® F и относительной влажности 50%. Полученные результаты приведены в табл.3. В опытах использовали в качестве стандарта или контроля перметрин. Пример 29. Инсектицидная активность. Предлагаемые соединения активны также по отношению к личинкам комара, а также к божьей коровке Epilachna varivestis и южным походным червям. Малярийный комар Anopheles quadrimaen- latus (С эй) 1 мл раствора (35% воды и 65% . ацетсца), содержащего 300 ррт исследуемого соединения, отмерили пипеткой в 400 мл химический стакан, содержащий 250 мл деионизованной воды, и перемешивали Пипеткой, получив концентрацию 1,2 ррт. Равные части этого раствора развели до концентраций 0,4; 0,04 и 0,004 ррт. Кольцо из воскованной бумаги шириной 0,6 см вставили внутрь химического стакана, чтобы оно плавало на поверхности исследуемого раствора и не давало яйцам всплыть по менисковой кривизне и высохнуть на краях стакана. Ложку в виде сетки использовали для сбора и переноса примерно 100 яиц (в возрасте 0-24 ч) в химический стакан. Через 2 дн при 80 F и относительной влажности 50% наблюдали инкубацию. Зарегистрированный процент смертности представлен в табл. 4. Божья коровка Ephilachha varivestis (М)ш Саженцы лимской фасоли (2, в горшочке) с первичными листьями длиной 7,5-Ю см погрузили в исследуемый раствор концентрацией 300; 100; 10 или 1 ррт и поместили в вытяжной шкаф для сушюс. Один лист отдели-. ли от растения и поместили в 10 см чашку Петри, содержащую влажную фильтровальную бумагу на дне и 10 личинок в последней возрастной стадии (13 дн от вылупления). На следующий день после обработки другой лист отделили от растения и дали на съедение личинкам после удаления остатков предьщущего листа. Через 2 дн после обработки третий лист дают личинкам на съедение, как правило, больше листьев; не требуется. Четвертый лист используют на третий день после обработки в том случае, :если личинки не кончили есть. Чашки выдерживали до тех пор, пока не вылупились взрослые особи (как правило, через 9 дн после начала обработки). После завершения превращения каждую чашку исследовали на наличие мертвых личинок, куколок или взрослых особей, уродливы.х куколок или взрослых особей; промежуточных форм личинка-куколка или промежуточных форм куколкавзрослая особь; или какие-либо отклонения от нормальной личинки, превращения или вылупления куколки или взрослых особей. Полученные результаты представлены в табл. 4. Южный походный червь Spodoptera eridama (Крамер). Саженцы лимской фасоли с двумя распуще ными первичными листьями длиной 7,5-10 см погрузили на 3 с при перемешивании в обрабатывающие растворы, а затем поместили в вытяжной щкаф для сушки. Листья после высь1хаиия срезали. Каждый срезанный лист поместили в 10 см чашку Петри, содержащую кусочек влажной фильтровальной бумаги и 10 личинок южного походного червья в третьей возрастной стадии длиной примерно 1 см Чащки Петри закрыли и хранили 2 дв при 80 F и 50%-ной относительной влажности. Процент смертности определили через 2 дн Полученные результаты представлены в табл. 4. Пример 30. Инсектицидаая активност Клещик паутинный двупятнистый Tetranych usticae (Кох). Саженцы лимской фасоли с тремя первичны ми листьями длиной 7,5-10 см заразили 100 взрослыми фосфаторезистентными клещами на один лист за 4 ч до начала опыта для того, чтобы допустить кладку яиц до обработ ки. Зараженные растения погрузили на 3 с при перемешивании в раствор с концантрадией 1000; 300; 100 или 10 ррт, а затем помес тили в вытяжной шкаф для сушки. Через 2 д при 80 F оценивали смертность взрослых клещей на одном листе под стереомикроскопом с увеличением в 10 раз. Другой лист оставили на растении еще в течение 5 дн, а затем исследовали при увеличении в 10 раз, чтобы оценить гибель яиц и вновь выведенIH.IX нимф, получая при этом меру овициднос тя (токсичности для яиц) и остаточного действия соответственно. Результаты опытов П{Я1ведещд в табл. 5. . Табачная почечная гусеница, совка Hel iotlus, virescens (Фабрициус). Третья возрастная стадия. Три хлопковых ростка с только что распустившимися семядолями погрузили в раствор с концентрацией 1000 или 100 ррт и поместили в вытяжной шкаф для сушки. Посл сушки каждую семядолю разрезали пополам и вместе с 10 лиственными срезами поместили в 28 г пластиковую медицинскую банку, содержащую 1,25 см зубной тампон, насыщенный водой, после чего добавили одну личинку почечной сусеницы в третьей возрастной . Банку закрыли и выдерживали в течение 3 ди при 80 F и относительной влажности 50%, после чего подсчитывали процент смертнести. Результаты опытов сведены в табл. 5. Совка ни Trichoplusia ni (Юбиер). Третья возрастная стадия. Листья хлопкового растения погрузили в раствор, содержащий 1000, 100 или JO ррт исследуемого соединения, перемешивали в течение 3 с и высушивали в вытяжном шкафу. После сушки лист поместили в 9,0 см чашку Петри с влажной фильтровальной бумагой на дне. Добавили десять личинок в третьей возрастной стадии и чаШки закрыли. Процент смертности подстатывали через 3 дн при 80 F (26,7С) и относительной влажности 50+10%. Полученные результаты сведены в табл. 5. Пример 31. Почвенная инсектицидная активность. Южная одиннадцатиточечная блошка Diabrov, tica undecimpunetate howardi (Барбер). 10 мг соединения разбавили до 10 мл аце- . тоном, чтобы приготовить исходный раствор А. 2 мл этого раствора затем разбавили до 10 мл ацетоном, чтобы получить раствор В. Примерио 0,7 г талька (Ругах ABB) поместили в 28 г цшрокогорлую банку и к тальку добавили 1,25 мл раствора. 1,25 мл раствора А - 56 кг/га. 1,25 мл раствора Б - 11,2 кг/а. Исследуемый раствор смешивали с тальком, чтобы равномерно смочить его перед сушкой и в воздуцрюй сушилке в течение 10-15 мин. 25 мл влажной стерильной горшечной почвы и приблизительно 0,6 г просяных зерен (пища для личинок) затем добавили в банки, содержащие исследуемое соединение. Банки закрыли и содержимое их перемешали на вибрационной мешалке. В каждую банку поместили по 10 личинок южной одиннадцатиточечной блошки, возраст которых составляет 6-8 дн. Банки плотно закрыли и хранили при ВСРр (26,7°С), относительной влажности 50% и постоянном освещении. Процент смертности подсчитывали через 6 дн. В зтом опыте о( -цианб-метафеноксибензиловый сложный эфир об -изопрошш-4-трифторометоксифенилуксусной кислоты обеспечил 100%-ную смертность южной оданнадцатиточечной блошки при расходе 56 кг/га и 70%-ную смертность при расходе 11,2 кг/га. Пример, 32. Остаточная инсектицидная активность, полученная при обработке листьев хлопчатника. Молодые растения хлопчатника на менее чем с двумя листьями, выращенные в 10 см пластиковых горошках, погрузили при перемешивании на 3 с в раствор (65% ацетона и 35% воды), содержащий 30; 100; 300 или 900 ррт. активного ингредиеита. После высушив ия листьев срезали по два листа от каждого растения и поместили в чашки Петри (90 х 10 мм) на влажную фильтровальную бумагу (9 см ватман № 1). Пять 35 табачных почечных личинок в третьей возрастной стадии поместили на каждый лист и чашки Петри закрыли. Зараженные чашки затем храни ли при постоянном освещении, 80°F и относительной влажности 50%. Подсчет личинок производили через 72 ч. Остальные растения поместили при условиях высокоинтенсивного освещения в теплицу, приспосрбсленную для обеспечения 14 св. ч/дн. Образцы листьев были подвергнуты испытанию с табачными почечными личинками в третьей .возрастной стадии через 3J 7; 10 и 14 дн пребывания в теплице. Результаты приведены в табл. 6. Пример 33. Иксодицидная активность (против иксодовых клешей). Личинка однохозяинного иксодового клеща Boophilus microplus, который может оставаться на единственном хозяине на протяжении трех своих стадий жизни (личинки, нимфы и взрослого). Использовали раствор (10%. ацетона и 90% воды), содержащий 0,025; 0,1; 0,5; 2,5 или 12,5 ррт исследуемого соединения, 20 личиною заключили в пипетку, закрытую на одном кон це пористым материалом. Раствор, содержащий исследуемое соединение, втягивали через пипет ку с вакуумньй с шлангом, посредством чего имитировалась опрыскивающая система. Клещей выдерживали 48 ч при комнатной температуре и определяли процент смертности. Опыты повторяли при концентрации исследуемого соединения 0,1; 0,25; 0,005 или 0,001; 0,1; 0,01; 0,001; 0,0001 или 0,00001; и 100 ррт. Результаты опытов приведены в табл. 7. В табл. 8 приведена иксодицидная активность соединения с различными радикалами при указанной концентрации. Пример 34. Эффективность предлагаемых соединеш1Й борьбы с взрослыми иксодовыми клещами Boophilus microplus определяли также в следующих опытах, в которь1Х применяли растворы, содержащие 125; 52,6; 31,2, 15,6 или 7,3 ррт исследуемого соединения. Взрослых налитых кровью самок клещей по грузили в исследуемый раствор на 3 с, помест ли в отдельные контейнеры и выдерживали 48 ч при 80 F и относительной влажности 50% В конце периода вьщержки, клещей осматривали и подсчитывали количество отложенных яиц. Яйца затем оставили для инкубации и коиечные результаты выразили в процентном уменьшении числа жизнеспособных яиц. Налиты кровью самок, которые не отложили яйца, .ч}1тали мертвыми. 82 Полученные результаты приведены в табл. 9 и 10. Пример 35. Эффективность предлагаемых соединений для борьбы с личинками мясной мухи Cah Ноту I а hominivorux являющейся Вредным насекомым для домашнего скота. Личинки Cochliomyia hominivorux получили в пищу смесь измельченного мяса (8,0 г), крови (7,0 мл), (2,1 мл) и раствора (0,9 мл) содержащего 1,5 или 25 ррт исследуемого соединения. Провели два опыта по 20 личинок на каждое значение дозы. Личинками давали питаться досыта на составленной среде в течение 24 ч, после чего определяли число мертвых личинок для каждого состава в каждом повторном опыте. Полученные результаты представлены в табл. 11. Пример 36, Определение концентрации исследуемых соединений, приводящих к гибели 50% особей табачной почечной личинки совки Heliotlus virescans на хлопчатнике. Молодые росткн хлопчатника с не менее чем двумя распустившимися листьями, росшие в 10 см пластиковых горшках, погружали при перемешивании на 3 ев раствор (65% ацетона и 35% воды), содержащий 1,1; 2,8; 7,5; 20; 60 или 150 ррт активного ингредиента. После сушки срезали по два листа с каждого растения и поместили в чашки Петри (90x10 мм) на влажную фильтровальную бумагу (9 см ватман № 1). Пять табачных почечных личинок в третьей возрастной стадии поместили на каждый лист и чашки Петри закрыли. Зараженные чашки хранили при непрерывном освещении, 80р (26,7°С) и относительной влажности 50%. Подсчет личинок производили через 72 ч. Каждый процесс повторили четыре раза; Полученные результаты сведены в табл. 12. Как видао из табл. 12 предлагаемые соединения 2-5 раз эффективнее для борьбы с табачными почечными личинками, чем известные соединения 1, испытанные в данном опыте, Пример 37. Определение концентра- ций исследуемых соединений, приводящих к гибели 50% особей взросль х комаров. Anopheles quatrimaculatus (Сзй). Для аэрозольного нанесения инсектицидные растворы переносили пипеткой (0,15 мл) в верхнюю часть сопла и просасьшали через распылтельное сопло. Еаспыле1шые капли переиосились потоком воздуха (4 мили/ч) к находящимся в садке комарам (25 взрослых самок на один садок) при жсспозиции 4-5 с. 3710 Затем комаров усьтпяли (3-4с) углекислым газом и переносили в садки. Садки с обработанными комарами хранили при 85 + 1 и относительной влажности 46 .t 2%. Процент смертности подсчитывали через 24 ч. Полученные результаты приведены в табл. 1 Как видно из Табл. 13 предлагаемые соеданения в 4 раза эффективнее для .борьбь с . взрослыми комарами Anopheles guatripi aculatu чем известное fj. Пример 38. Остаточная инсектицидная активность, определенная прк малообъемных нанесениях исследуемых соединений. Исследуемые соединения диспергировали в смесях 65% ацетона я 35% воды в Достат01Чных количествах, чтобы получить 0,08 кг/га соединения в 19,3 л ъода. Ростки хлопчатшиса затем поместили в камеру для опрыскивания и опрыскивали с помощью ншодвижного верхнего распылителя прк прохождении рост ков под ним. После высыхания срезали по два листа с каждого из двух растений и Поместили в чаипсу Пет|т (90 х 10 мм) на влажную фильт ровальную бумагу (9 см ватман № 1). Пять табачных гючечных личинок совки Heliothis virescens В третьей возрастной стадии поместили накаждый лист и чашки Петри закрыли. Зараженные чашки храншш при непрерывном освещении и относительной влажности 50%. - - - . -,Подсчет лнчинок производили через 72 ч. Остальные растения поместили при условиях высокоинтенсивного освещения в теплицу. Образцы листьев подвергали биологическому испытанию с табачными почечными личинками в третьей возрастной стадии через 3; 7; 10 и 14 дн. Получйшые результаты п| шедены в табл.14 Ц р и м е р 39. Иксодицидная активность. : Аналогачно примеру 33 определяли иксодицидную активность предлагаемых соединений при концентрациях 12,5; 2,5; 0,5; 0,1,0,02 или 0,004 ррт. Полученные результаты сведены в табл. 15. .. Пример 40. Эффективность предлагаемых соединений для борьбы со взрослыми мнргохозяинными клещами Rhipicephalus sanqu i nens (R. S.) и Dermacentor ver rabi1 is (D.V.) собак определяли, иоюльзуя исследуемое вещество по примеру 33 с концентрацией 100, 10 илн 1 ррт. Взрослых налитых кровью самок клещей погрузили в исследуемые растворы на 3 с, поместили в отдельные контейнеры и выдержюали в течение 48 ч. при и отноштельной влажности 50%. В конце периода выдерживакия клещей осматривали и подсчитывали количество отложенных яиц. Палитых кровью са2мок, которые не отложили яиц, считают м твыми. Полученные результаты приведены в табл.16. Пример 41. Взрослая кошачья блоха Ctenopephalites fel is in vitro. 10 взрослых кошачьих блох вида Ctenocep- halites fetis опрыскивали в течшие 30 с раствором (ацетои/вода), содержащим 100, 50, 10 или 1 ррт исследуемого соединения, а затем выдерживали в 48 ч ря комнатной температуре и относнтельной влажности 80%; Через 24 ч и 48 ч блох осматривали и подсчитывали смертность. noj emoiie результаты представлены в табл. 17. Опыт повторили при коицентрацюс HccnejdyeМого соединения 80; 40; 20; 10; 5 или 2,5 ррт. Р ез гльтаты представляют собой средние зиачения двух повторных опытов при каждой . концентрации и пртшедены в табл. 18. Пример 42. Иксодииндную активность предлагаемых соеданший определялн анадогично примеру 40 прт концентрации 1,0; 0,1; 0,01 или 0,001% активного ингредиента. Процент смертности подсчитывали через 24 ч и 48 ч аосле обработки. Полученные результаты приведены в Ta&i.l9 (чреярие значения двух опытов). прям е р 43. Эффективиость пpeдлaгaejv ; т - ...-.-. jii ..«.-мых соединений для борьбы с «росами Musca antumnalis. Однодневные дичинки мух питались кора . вьим навоз «, обработанным раствором, содержащим 0,13; 0,25 илн 0,50 ррт исследуемо to соединения. О результатах (дят по двум опьггам, ис- ; пользуя при этом по 10 личинок на каждую концентрацию. Ацетоновый раствор соответствующего количества исследуемого соединення добавили к 1 кг свежего коровьего навоза и смешивали в течение I мин электрической мешалкой. «авоз, используемый для контрольных опытов, обрабатьшали аналогично, но добавляли только ацетон. Образцы навоза разделяли в 4 бумажных стакана. (Для каждого значения концентрации и для контрольных опытов). Два стакана заразили однодневными личинками мух. Стаканы выдерживали в течение 7 ди при 80 и относнтельной влажности 50%. Затем стаканы осматривали на наличие куколок. Куколки подсчитали, взвесили и прмеспши в пластиковые про&фки, где они вылупились и погибли. Полученные результаты приведены в табл. 20 (средние значения двух опытов).
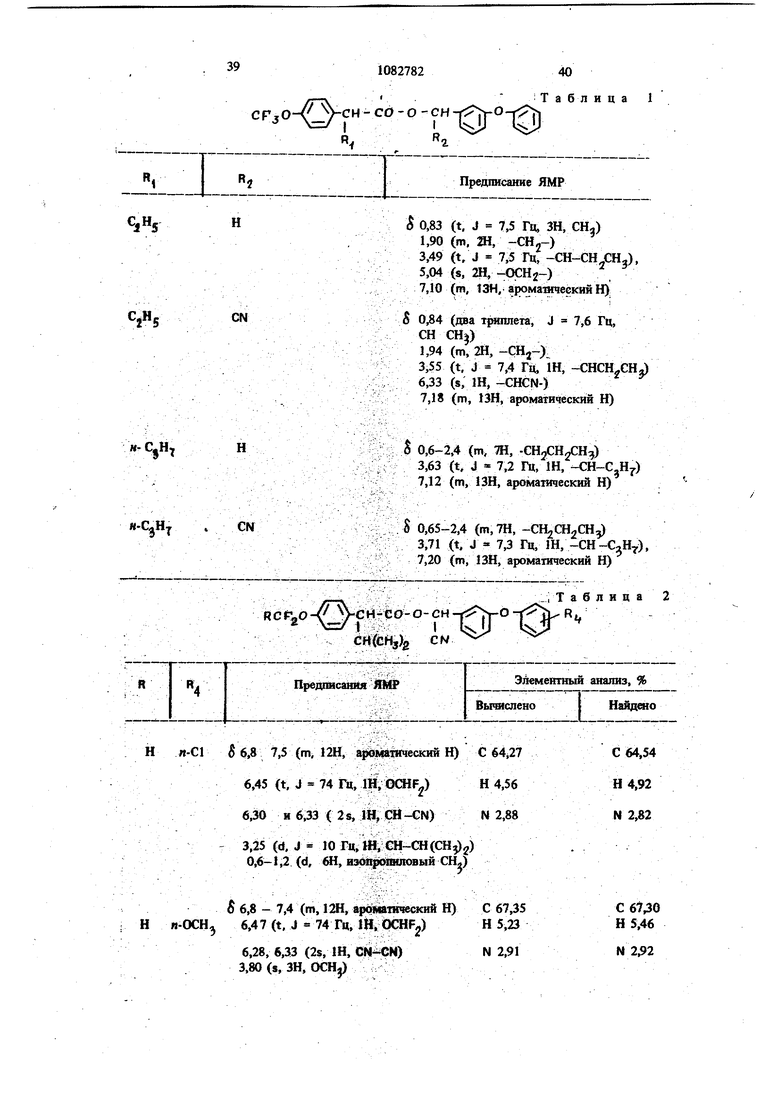
39
СО-О СНRC
rj
S«5
Н
CjHj
CN
«- С|Н,
Н
«СзНт
Ш
1082782
40 Т a б л и ц а
Предписание ЯМР
5 0,83(t. J 7,5 Гц, ЗН, СН-)
1,90(го, Ж, -СН,-)
3,49(t, J 7,5 Гц, -СН-СН СНа),
5,04(s, 2Н, -ОСНг-)
7,10(т, t3H,-аромалпеекийН)
.,.,- - -- , .
S 034 (два т| тлета, J 7,6 Гц, СН СН)
1,94 (т, 2Н, -CHj-X 3,55 (t. J 7,4 Гц, Ш, -СНСНХН 6,33 (S, Ш, -CHCN-) 7,18 (т, 13Н, ароматический Н)
$ 0,6-2,4 (т, 7Н, -CHjCHXH)
3,63 (t, J 7,2 Ти, Ш, -СН-е Ну) 7,12 (т, 13Н, ароматический Н)
S 0,65-2,4 (m,7H,
3,71 (t. J 7,3 Гц, IH, -CH-C HT), 7,20 (m, 13H, ароматический H)
/TV
RCft,04 )-CH-eo-0-CH
2-Л-/ ,,
Cf iCtis) СЫ
Предписания ffiifP
RJ
S 6,8 7,5 (m. 12Н, мвтичеосий Н) С
«-С1 6,45 (t, J 74 Гц, Ш, OCHF)Н 4,56
6,30 и 6,33 ( 2s, Ш, CH-CN)N 2,88
3,25 (d. J - 10 Гц, 1Н, СН-СН(СНз)2) 0,6-1,2 (d, Ш, иэопротшовый СН,.)
5 6,8 - 7,4 (т, 12Н, аро1Ш1теский Н) Н и-ОСН 6,47 (t, J 74 Гц, Ш. OCHF)
6,28, 6,33 (2s, Ш, CM-CM) 3,80 (s, ЗН, OCHj)
Элементный анализ, %
Найдто Вьршслено
С 64,54 Н4,92 N 2,82
С 6730 Н 5,46
N2,92
3,63 (8, ЗН, ОСН|)
Продолжение табл. 2
N 2,65
N 2,80
о
л
g
11
8
1
-ш
9
8
г
о
о г
п
8
8 8
8 8
8
f
i4
8
8
55
8 8
м
sf я
Is
R8
8
хш
О
м
§ 8
8
8
8
8
-.
I
i 8
8:
g
S
Г
8
8
2v
8 8
п
56
I
I
8
S
I
g
8
8
g
. «-I
8
8
о
8
о
t
о
8
s
8
ti
8
I 8
§
s
00
-H
§;
8 8
§
-i
8
8
s
8 8
f-ч
8
8 8
8 8 8
75
islj
Ill
li
8
8
8
о
Ю
8
2|
|i
8
fs II
111
76
I
g
8 8
8 8
8
8
-Ц
-
8
8 8
о oo
;g
о
(Л
8
8
8
о ю
g
8
8
8
8
8
о о
g-g
I
о
, §
e-f
e
fs.
8
i
I
8
ii
8
8
i|
в
8
8
S
it
8
8
8
R
8
8
О
о
8
8
8
§
8
8
S 8
8
о о
N
о
I
i -75
Y S g-f
2 I ::}S
о о
s
о о °
о о о о
о о о °
о о о о
2 8SI 88
я s я
&
2 S5 88
11
§8 88
,
i2
s
28 88
, is д -
о 8 88
Os s --I -
О Q fn О
S
о о
g
о о о
гл
о
го GI
о о
го tfs о
8
1о о о
00
о
О
п
о о
«
о о
m
о о о о
00 о о
si
ГО
ю
N
s;§
8
«л
° {
Tf
о «п
8 80
|§ 11
Jiic
SS3 88 jo
«8 S;8 1о
88
8 8
Й§
В-б
t
о
I «
о -2
w.g
it
1082782
,нср,о-0-сн-со-о-сн-г о-. сн(св4 А,
Н
н
н н
С1
н
н
CNН
С1
Таблица 8
100 при 100 75 при 100
1 V I «ж Т
Н
С1
С1
Н
Н
С1
С1
Н
Н
Н
Н
И
Ни
Н
Н
Н
Н
Н
Н Н
Н
«t-Этил FН
Н
C:N
см а
Н
Н
Н
Н
Н
CN Иксодицидаая активность против взрослого
Соединение
Продолжение табл. 8
смертности при концентрации, ррт
40 при 100
90 при 100
100 пен
100 1 0,04
100 « 100
1@0 та 190
Ш) ори 100
85 щя @,0@01
95 при 1; 70 нрт 0,1; 25 при 0,01
% смертности при концентрациях, ррт 125 I 62,5|з1,2 15,6 I 7,8 Т а б л и ц а 9 клеща Boophilus microplus
100100 99,4 98,887,2
0-t
Та блица 10
89
1082782
90 Продолжение табл. 10
I
о
s
I
s
«s
a
3
ro ON «2; 8 « 25 Й
Я Й 8R Й8 S 8 8
о e n§
S«n f t
8 88 R
S
§. 8 8 8 § I « к Я
o
dS
г. e
P
8-e i
if
i-f
|§ bi
П ID Oi
О
Ш
и
Ы
о о«
- ,Х / VI /1
V О О О С), О О - rf ГО Ш
00
5 2
® ;5 S § g
.X Du
ON
т VO
ГЧ ,sl
о
- S
tsо С) о о, о
X я
- 2 0-5 g
о
и
S
U
ш S X С4
sr
V
S
S Си
е
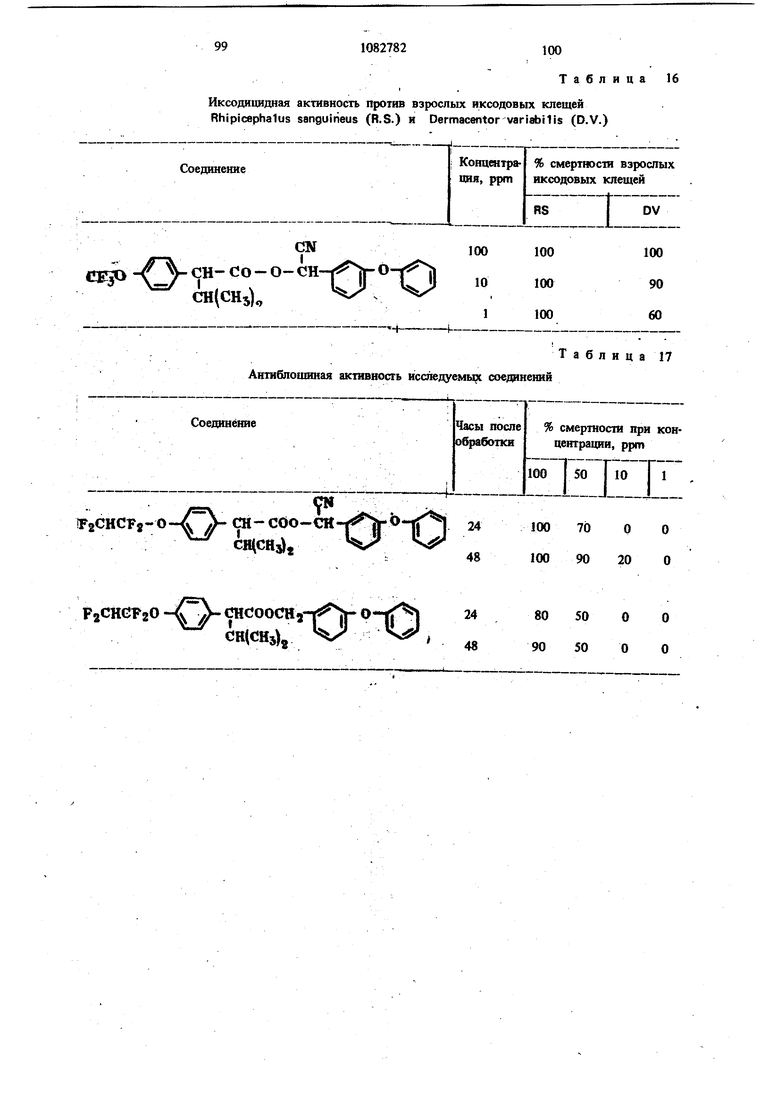
Иксодицидная активность против взрослых иксодовых клещей Rhipicephalus sanguitieus (R.S.) и Dermacentorvariabilis (D.V.)
Соединение
Таблица 16
Концентра% смертности взрослых иксодовых клещей ция, ppm
I
DV
RS
Антиблошиная активность исспедуемь соеданений
Таблица 17
а ч ю
N
н
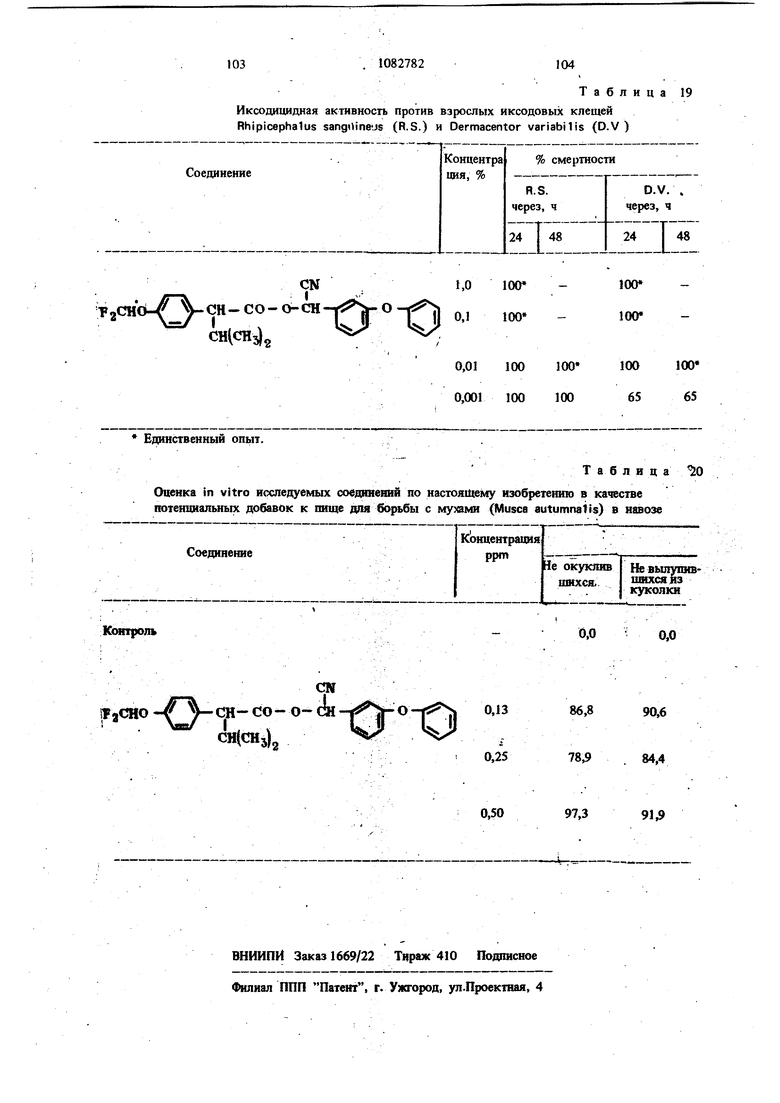
Иксодицидная активность против взрослых иксодовых клещей Rhipicephalus sangOine-JS (R.S.) и Dermacentor variabilis (D.V )
Соединение
: Контроль
Таблица 19
Концентрация ррт
Не окуюгав шихся..
0,0
0,0 Единственный опыт. Оценка in vitro исследуемых соеданений по настоя1Кему изобретению в качестве потенциальных добавок к пище для борьбы с мухами (Musca autumnatis) в навозе Т a 6 л и ц a 0
ifaCHo
86,8
90,6 78,9 84,4
0,50
97,3
91,9
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
Авторы
Даты
1984-03-30—Публикация
1978-10-12—Подача