Изобретение относится к органической химии, к новым химическим соединениям, а именно к замещенным фе- нилуксусным кислотам общей формулы
lf-CFj-X- O)-CH-СООН R
где R -CFj-X находится в пара-положении к углероду кислотной группы;
R; - i-pr,
R - Et, H-Pr,i-Pr
X - О, R - Н,
X - О, К - F,
X - S, R - F, в - i-Pr, используемых в качестве промежуточного вещества при получении инсектицидов ,
Известно производное замещенной фенилуксусной кислоты:
CN
сн-соо-ш
Рг
используемое в качестве инсектицида
Недостатком данного соединения является его невысокая инсектицидная активность (см. табл. 9).
Цель изобретения - нахождение новых производных фенилуксусной кислоты, используемых в качестве промежуточного вещестза для получения высокоактивных инсектицидов.
Поставленная цель.достигается новым химическим соединением 2-алкил- -2-(4-фторметокси-, 4-фтортио)-фенил уксусная кислота общей формулы
R-CF
-сн-соон
1,
где R находится в пара-положений к углероду кислотной группы;
X - О, R - Н, . X - О, R - F,
R - i-Pr, R - Et, H-Pr,i-Pr X - S, R - F, R - i-Pr,
вещества
в качестве промежуточного для инсектицидов,
Пример 1 . Получение о - изо- пропил-4-метоксифенш1-ацетонитрШ1а.
Раствор едкого натрия (50%, 300 мл) добавили к раствору п-меток сифенилацетонитрила (147 г, 1 моль) дициклогексш1-18-кроун-6 (18,63 г, 5 мол.%), 2-бромпропана (320 г, 2,6 моль) и бензола (300 мл). Смесь нагревали при 45 С в течение 4 дней Органическую фазу отделили, хорошо промыли водой (3x200 мл) и упарили до масла. Вакуумная перегонка дала
221220
продукт ( 1 75,6 г
2
81%)
10
,
-
15
.
25
40
45
50
с т.кип. 96100 С/О,15 мм рт.ст.; ЯМР (CDCI) показал, что в перегнанном веществе содержится 12,5 мол.% исходного нитрила.
Пример 2. Получение «,-из о- пропил-4-оксифенилацетонитрила.
51 г (0,2 моль) трехбромистого бора в 20 мл метиленхлорида добавили к раствору 37,8 г (0,2 моль) Л -изо- пропил-4-метоксифенилацетонитрила в 35 мл метиленхлорида при -40 С. Красному раствору дали нагреться до комнатной температуры и перемещивали 3 дня. Затем реакционную смесь вылили в лед, экстрагировали (3x100 мл), промыли водой (2x100 мл) и упарили до масла. Вакуумная перегородка масла дала 28,9 г (81%)об-изо- пропил-4-оксифенилацетонитрила с т.кип. 142-143 С/0,25 мм рт.ст.
Пример 3. Получение хлор- тио-0- п-(1-циан-2-метилпропил)-фе- нилового эфира муравьиной кислоты.
16,43 г (0,143 моль) тиофосгена в 50 мл хлороформа в течение 30 мин добавили к раствору ей-изопропил-4-ок- сифенилацетонитрила (25 г, 0,143 моль) в растворе едкого натрия (5%, 5,72 г, 30 0,143 моль-), применяя ледяную баню поддержания температуры ниже
Смесь перемещивали 15 мин и хлороформенный слой отделили, про- мьши водой и выпарили до желтого JJ масла (38,2 г). Продукт применяли в примере 4.
Пример 4 . Получение е -изо- пропил-4-трифторметоксифенш1ацетонит- рила.
38,2 г тиокарбоната, полученного по примеру 3, обработали гексафтори- дом молибдена (15,8 г) при . Густой реакционной массе дали нагреться до комнатной температуры и медленно нагрели до 160 С на масляной бане, Смесь охладили до комнатной температуры, затем вылили в воду и экстрагировали эфиром (4x50 мл), промыли водой (1x50 мл) и вьтарили до масла. Поеле вакуумной перегонки получили й-изопропш1-4-трифторметоксифенилаце- тонитрил с т.кип. 78-80°С/0,15 мм рт.ст.
Пример 5. Другой способ по- 55 лучения м -изопропил-4-трифторметокси- фенилацетонитрила.
А. Получение 4-трИфторметокси- бензилхлорида.
для 30°С.
3
355 мг триоксана, 340 мг хлорида цинка и 600 мг трифторметокс бензола нагревали при 73°С при одновременном пропускании через смесь газообразного хлористого водорода, Смесь охладили до комнатной температуры и разбавили эфиром. Органическую фазу промыли насыщенным растворо карбоната натрия и водой. После отгонки растворителей получили продукт в виде бесцветной жидкости (1,42 г). В. Ползгчение 4-трифторметоксифе- нилацетонитрила.
Указанное хлорное соединение пре- вратипи в соответствзгющ1й нитрил ана логично примеру 3 с выходом 93%.
С. Получение об-изопропил-4-три- фторметоксифенилацетонитрила.
Алкилирование 4-трифторметоксифе- нилацетонитрила вели аналогично при- меру 4 с выходом 90%.
Пример 6 . Получение об -изо- пропил-4-(трифторметокси)-фенилуксус ной кислоты.
Смесь 2,0 г ot-изопропил-4-три- фторметоксифенилацетонитрила, 3,0 г едкого калия в 36 мл этиленгликоля и 3 мл воды нагревали при в течение 8 ч. Этот раствор вылили в воду и экстрагировали эфиром (2x10 мл) Водиьй слой подкислили разбавленной НСЕ и экстрагировали эфиром (3x1 мл) промыли водой (1x25 мл), сушили сульфатом натрия, выпарили до масла (,23 г)..
ИК-спектр 1700 см ; ЯМР-спектр (СДСе,) Т 76-1377,5: 7,25 (АВ, 4Н, АрН); F3,15 (д., I 8 Гц, Ш, СН); 2,4 (м., Ш, ен(СИ,)2); So,62 и 1,08 (2 д., I 6 Гц, 6Н, СП,).
Пример 7. Получение об -изо- пропил-4-(трифторметокси)-фенилаце- тшпслорида.
Раствор 1,2 г of.-изопропил-4-три- фторметоксифенилуксусной кислоты и 0,6 мл тионилхлорида в 5 мл бензола кипятили с обратной перегонкой в течение 4 ч. После отгонки растворителя и избытка тионилхлорида получили хлорангидрид, который применяют для этерификации в примере 8.
П р и м е р 8. Получение об -циан- -м-феноксибензилизопропил-4-(трифтор- метокси)-фенилацетата.
Раствор 4,58 ммольог.-изопропил- -4-трифторметоксифеннлацетилхлорнДа в 5 мл эфира добавили к раствору в 20 мл 4,58 ммольа -циан-м-фенокси12204
бензилового спирта и 0,5 мл пиридина. Смесь перемешивали в течение ночи и фильтровали. Фильтрат и промывки упарили, оставшееся масло очистили на силикагелевых пластинках размером 5 X 2 мм, элкмрование вели смесью 1:I метиленхлорида и гексара. Эфиром экстрагировали полосу с Rf 0,55, выпарили и получили нужный эфир (0,85 г).
ИК (чистый) 1755 см ; ЯМР (CDCI,), S: 6,8-7,6 (м., 13Н, АгП); 6,31 и6,28 (с,, 1Н, рН-Аг), 3,27 (д.,1 7 Гц, 1Н,
CN
СН-СП(СН-)2; 2,0-2,6 (м., Ш, СП(СН ) 0,6-1,2 (4 д.), J 7 Гц, 6Н, изо- пропиловый СН); I9F химический сдвиг 58,85 относительно CFCI,.
Пример 9. Получение м-фенок- сибензил-с1-изопропил-4-трифторметок- сифенилацетата.
К раствору 1,89 г м-феноксибензи- лового спирта и 1 мл пиридина в 6 мп метиленхлорида добавили 7 мл раствора (/ -изопропил-4-трифторметоксифенил- ацетилхлорида, полученного из 2,46 г соответствующей кислоты как в.примере 10. После перемешивания реакционной смеси в течение ночи ее водой, разбавленной соляной кислотой, разбавлен1шм раствором едкого калия, водой и выпарили до оранжевого масла. Очистка хроматогра4мей на силикагеле дала 2,76 г нужного эфира.
ИК (чистый) 1738 см ; ЯМР(СВС1,), S: 6,73-7,45 (м., I3H); 5,03 (д., 2Н), 3,20 (д., а; 10,5 Гц, 1Н), 2,26 (м., 1Н), 0,66 и 0,94 (2д., 1 6,6 Гц, 6Н).
Пример 10. Получение а -этйи- Hot -пропи1-4-трифторметоксифеиипук- сусных кислот и их .эфиров.
Аналогично примерам 6 и 2-5, но заменив этипбром и 1-бромпропан на 2-бромпропан, получили ей-этил-4-Tjei- фторметоксифенилуксуснуто и об-пропил- -4-трифторметоксифенилуксусную кис- лоту.
Физические константы длял-про- пил-4-трифторметоксифеншгуксуснрй кислоты:
ЯМР-спектр Т 76-1169 ),S 12,12 (с., Ш){ 7,37 (д., 1 9,1 Гц, 2Н); 7,21 (д., I 9,1 Гц, 2Н); 3,49 (т., 1 7,0 Гц, 1Н); 1,98 (м., 2Н); 0,92 (т., I 7.5 Лч, ЗН); ИК-спектр 55234 (неразбавлето.): 3000 (st, кислот й||й ОН sbr); 1910 см (st.
кислотная С-0 линия); 1160-1270 (v.st., S-F полоса).
Физические константыot-изопропил- -4-трифторметилтиофенилуксусной кислоты:
ЯМР-спектр Т 76-1170 (СДС,),8 : 12,13 -(с., Ш); 7,33 (д., J 8,6 Гц, 2Н); 7,09 (д., 3 8,6 Гц, 2Н); 3,57 (т., J 7,0 Гц, Н); 0,64-2,40 (м., 7Н); ИК-спектр 55324 (чистая): 3000 CM (st, кислотная ОН полоса); 1710 (st, кислотная С-0 полоса); 1160-1280 (v.st., C-F полоса).
Пример 11. Получение сб-бром -4-трифторметилтиотолуола.
20,5 г (0,13 моль) брома в 20 мп четьфехзслористого углерода медленно добавили к раствору 29 г (0,15 моль) 4-трифторметилтиотолуола в 90 мп че- тыреххлористого углерода и кипятили с обратной перегонкой при освещении рутной лампой 275 Вт. По окончании добавления раствор кипятили с обратной перегонкой еще 1 ч. Больщую част растворителя отогнали при атмосферно давлении, остаток перегнали в вакуу ме. По газожидкостной хроматографии погон 15,5 г с т.кип. 64-77 С/0,6- 0,8 мм рт.ст., содержал 92% моно- бромсоединения.
Пример 12. Получение 4-три- фторметилтиофенилацетонитрила.
3,9 т (0,08 моль) цианида натрия добавили при к 40 мл диметил- сульфоксида в атмосфере азота. Тепло отводили, по каплям добавили 14,3 г (0,053 моль)о6-бром-4-трифторметил- тиотолуола с такой скоростью, чтобы температура не прёвьппала 75 с. Окрашенная в красный цвет реакционная. смесь нагревалась до 90-95 С в течение 45 мин, затем ее охладили до комнатной температуры и обработали 50-100 мл ледяной воды. Водную сус- . пензию экстрагировали несколькими порциями эфира, эти порции соединили промыпи водой и сушили сульфатом натрия. После отгонки в вакууме получили 9,7 г темно-красного масла 95%НОЙ чистоты по газожидкостной ХрО-
матографии.
Пример 13. Получение об-изo- пpoпил-4-тpифтopмeтилтиoфeншIaцeтo- нитрнла.. ,
13,5 мл 50%-ного едкого натрия по каплям в течение 30 мин добавили к суспензии 9,7 г (0,045 моль) 4-три фторметилтиофенилапетонитрипа, 9,5 г
(0,056 моль) 2-иодопропана и 0,61 г (0,0023 моль) 18-краун-6 в 13,5 мл бензола; температура поднялась до 43°С. После перемешивания при комнатной температуре в течение 2,5 ч проба на газожидкостной хроматогра- 1фии не показала остатков исходного нитрила. Реакционную смесь обработали добавлением ледяной воды, экстрагировали эфиром; экстракт промыпи 10%-ной НСЕ, водой и сушили сульфатом натрия. После отгонки в вакууме получили 10,2 г (86,8%) красно-коричневого масла.
Пример 14. Получение oi-изo- пpoпил-4-тpифтopмeтилтиoфeнилyкcyc- ной кислоты.
6,9 г (0,0265 моль)о -изопропил- -4-трифторметилтиофенилацетонитрила и 25 г (0,312 моль) 50%-ного едкого натрия соединили в 53 мл этиленгли- коля и кипятили .с осторожной обрат- ной перегонкой в течение 18 ч. Реакционную смесь вылили в ледяную воду и экстрагировали эфиром. Водную фазу подкислили концентрированной соляной кислотой, снова экстрагировали эфиром, промывку промыли водой и сушили сульфатом натрия. После отгонки в вакууме получили 2,05 г маслянистого продукта.
ИК-спектр 56113 (чистая): 1705 см кислота С-0; ЯМР-спёктр Т 77-1384 (СДСЕ,), S : 11,9 (с., 1Н); 7,0-7,6 . (м.,.4Н); 3,16 (д., I 11 Гц, 1Н); О 2,03-2,76 (м.. Ill)-; 0,63 и 1,03 (2д., I 6,5 Гц, бН).
Пример 15. Получение ее -циа- но-м-феноксибензил-о|1-изопропил-4-три фторметилтиофенилацетата.
Используя в качестве исходного соединения oi-изопропил-4-трифторметил- тиофенилуксусную кислоту, аналогично примерам 7 и 8, получают указанный в заготовке целевой продукт в виде масла.
Данные элементного анализа полученного продукта:
Вычислено, %: С 64,32; Н 4,57; F 11,74; N 2,89.
, ад,но,8.
Найдено, %: С 64,27; Н 4,62; F 11,66; N 2,68.
Пример 16. Получение«i-изо- пропил-4-оксифеНИЛуксусной кислоты.
Смесь 40,0 rot -изопропил-4 мет- оксифенилацетонитрила и 200 мл (48%) бромистоводородистой кислоты кипяти-
ли с обратной перегонкой при 126- 128°С 14 ч на масляной бане. Затем смесь разбавили водой и льдом, несколько раз экстрагировали эфиром, промыли водой и выпарили до твердого остатка. Этот остаток кипятили с 200 мл хлороформа, фильтровали и су- шили. Выход 23,8 г с т.пл. 172-174 С ИК (ньюджол) 3250-2900 (широкий, ОН) 1690 см- (С-О). -
Пример 17. Ползгчение об -изо- пропил-4-дифторметоксифенилуксусной кислоты.
Через перемешиваемую при 80 С смесь 10 Г; (0,0515 моль)сС-изопропил- -4-оксифенилуксусной кислоты, 65 мл диоксана, 19,08 г (18,56 г, 0,464 моль) едкого натрия и 30 мл воды в течение 4 ч барботировали 46 г (0,532 моль) хлордифторметана. Реакционную смесь вылили в 250 мл ледяной воды, смесь промыли эфиром, подкислили концентрированной соляной кислотой до рН 3, затем экстрагировали 200 мл эфира. Эфирный раствор один раз промыли 100 мл воды, сушили сульфатом натрия, фильтр овали и выпарили до белой пасты. Добавили смесь гексана и метиленхлорчда и полученную смесь фильтровали от исходных твер- дых частиц. Фильтрат выпарнлн и получили 5,41 г прозрачного коричневого масла.
ЯМР (, пиридин),8 : 7,43 (д., I 8,2 Гц, 2F); 7,08 (д., I 8,2 Гц, 2Н); 6,57 (т., J 74,3 Гц, 1Н); 3,63 (с., imp), 3,25 (д., 3 10 Гц, Ш); 2,37 (м., 1Н); 1,19 {д., I 6,5 Гц, ЗН); 0,78 (д., 3 6,5 Гц, ЗН); 13,82 (с,, 1Н).
Пример 18. Получение OU-циa- нo-м-фeнoкcибeнзил-oi.-изoпpoпил-4-ди- фторметоксифенилацетята.
Используя в качестве исходного соединения оС-изопропил-4-дифторметокси- фенилуксусную кислоту, синтезированную, как описано в примере 17, и применяя методики по примерам 7, 8, получили целевой сложноэфнрный продукт,
в виде маслообразного вещества.
I
ЯМР-спектр в дейтерохлороформе, 8: 0,88 м.д. (4д., 6Н, I 6 Гц, СН,); 2,30 м.д. (м., 1Н, -CH-ClUCHj)); 6,33 м.д. (2с., 1Н, -СНСй); 6,45 м.д. (т., I 7,4 Гц, 1Н, CHF 0-); 7,16 м.д. (м., 13Н, АгН).
Вычислено, %: С 69,17; Н 5,13; F 8,42; N 3,10.
s г 10
15 20 25 Q
0
5
5
0
5
Cj,H,,F,N04
Найдено, %: С 69,41; Н 5,20; F 10,25;N 3,70.
Пример 19. Получение м-(м- -фторфенокси) -бенз.ал ьдегида.
Натриевую соль 3-фторфенола по- .лучили смешением 15,13 г (0,135 моль) 3-фторфенола и .7,29 г (0,135 моль) метилата натрия в П5 мл пиридина.
Смесь нагревали до 110 С, за это время отогнали 34 мл пиридина-метанола. Смесь охладили до 80°С и добавили 25 г 0,135 моль м-бромбенз- апьде гида и 4,05 г (0,049 моль) хлорида меди (I). Реакционную смесь кипятили с обратной перегонкой в течение ночи. На следующий день большую часть пиридина отогнали, реакционную смесь охладили и разбавили 80 мл толусша. Твердые вещества отфильтровали, фильтрат промыли 20%- ной соляной кислотой, водой, 5%-ным едким натрием и водой, соответственно и упарили до темно-коричневого масла. Вакуумная перегонка дала продукт в виде пр озрачной жидкости в количестве 6,6 г с т.кип. 82-88 с/ /0,5 мм рт.ст.
Вычислено, %: С 72,22; Н 4,20; F 8,79.
C,,H,FO,.
Найдено, t: С 72,03; И 4,30; F 8,60.
П р и м е р . 20. Получение замещенных й -циан-м-феноксибензиловых эфиров фторалкоксифенилуксусных кислот .
Используя в качестве исходного соединения об-изопропил-4-дифторметок сифенилуксусной кислоты или oi-изопро- пил-4-трифторметоксифенилуксусной кислоты и циангидрин соответственно замещенного альдегида аналогично примерам 7 и 8 получили зфиры, представленные в табл. 1.
Пример 21. Исследование инсектицидной активности предлагаемых соединений с использованием тест-ин-; секТов (т.е. разновидностей насеко- них в качестве объектов для воздействия испытуеьа1х соединений) совкн Heliothis verosceus (Fabricius), ци- кадки картофельной Empoasca abrupta (Belong) и тли боОовой Aphis fabae (Scopoli).
При использовании в качестве тест- инсекта совки Heliothis veresceus (Fabricius), находящейся в первой
912
возрастной стадии,-методика проведения испытаний следующая:
Росток хлопчатника с двумя распустившимися и вполне оформившимися листами погружают на 3 с при перемешивании в тестируемый раствор (35% воды/65% ацетона), содержащий соответственно 300, 100 или 10 ч. на мпн испытуемого соединения. Далее каждый лист помещают в чашку с тампоном и перед тем, как накрыть чашку крышкой (колпаком), туда вносят кусочек марли, зараженный 50-100 вновь выведенными личинками совки. После вьщержи- вания в течение 3 дней при 80°Ф (26,7°С) и относительной влажности 50% Чашки внимательно исследуют и определяют число погйбпшх личинок.
При оценке инсектицидной активноети предлагаемых соединений, используя в качестве тест-инсекта бобовую тлю Aphis ГаЪае (Scopoli) методика тестирования следующая:
Каждый из 5-сантиметровых лубяных горшочков, содержащих по одному ростку настурции с двумя листами длиной 2 дюйма ( см), которые за 2 дня до этого заражены 100-150 бобовыми тлями, помещают на поворотньй стол, вращающийся вокруг вертикальной оси со скоростью 4 об/мин, и опрыскивают раствором (35% воды/65% ацетона), содержащим соответственно 100,10,1,0 и 0,1 ч на млн испытуемого соединения, в течение двух полных оборотов стола вокруг оси при помощи пульверизатора Де Вилбисса, работающего на сжатом воздухе под давлением 20 фунтов на квадратный дюйм (1,4 кг/см ) . Наконечник опрыскивателя держат при этом на расстоянии 15 см от растений и струю раствора направляют таким образом, чтобы обеспечить полное орошение растений и тлей. Опрысканные растения укладываю набок (горизонтально) на белые эмалированные подносы (лотки) и через день (температура 70 Ф (21,1 С), относительная влажность 50%) оценивают число и процент погибших тлей.
Дпя оценки инсектицидной активности предлагаемых соединений по отношению к картофельной цикадке Ега- poasca abrupta (Delong) используют следующую методику.
Ростки лимской фасоли с первичным листом длиной 3-4 дюйма (7,6-10.см) погружают в раствор (35% воды/65%
010
ацетона), содержащий соотпетственно 100, 10 или 1 ч. на млн соединения. Извлеченные из раствора ростки помещают в вентилируемый шкаф для просушки, затем от каждого ростка отрезают 2,5-сантиметровый кончик листа, и помещают его в чашку Петри с влажной фильтровальной бумагой на дне. Затем туда высаживают 3-10 нимф (личинок) во вторичной возрастной стадии и чашку накрывают крьшткой. Подсчет числа погибших личинок и вычисление процента смертности производят после выдерживания указанных чашек в течение 2 дней при (26,) и относительной влажности 50%.
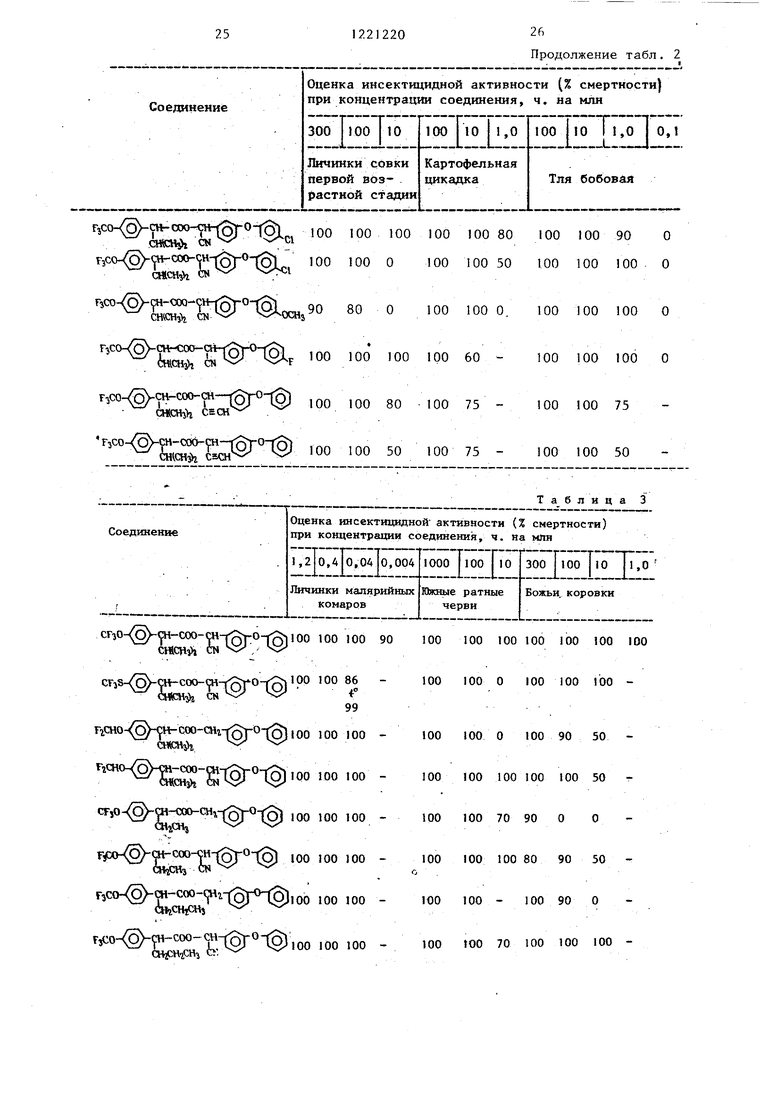
Полученные данные (с указанием процента смертности насекомых) представлены в табл. 2.
Пример 22. Исследование инсектицидной активности предлагаемых соединений с использованием в качестве тест-инсектов личинок комаров, божьих коровок и южных походных
(ратных) червей.
1
Методика испытаний инсектицидной активности предлагаемых- соединений по отношению к .личинкам малярийного комара Anopheles quadrimaculatus
(Say).
1 мл раствора (35% воды/65% ацетона), содержащего 300 ч. на млн испытуемого соединения, переносят пипеткой в химический стакан емкостью 400 мл с 250 мп дёионизованной воды. Содержимое стакана размешивают с помощью пипетки, получая концентрацию 1,2 ч на млн. Из этого раствора отбирают аликвоты в результате дальнейшего разбавления которых получают растворы, содержащие 0,4, 0,04 и 0,004 ч. на млн тестируемого соединения. В стакан с раствором помещают кольцо из вощеной (парафинированной) бумаги шириной 0,6 см так, чтобы оно плавало на поверхности раствора и удерживало яички малярийного комара от всплывания в пограничной со стенкой стакана зоне, где
раствор смачивает стенку стакана, образуя мениск определенной кривизны сил поверхностного натяжения, и где яички могли бы по мениску попадать на стенку стакана и погибать в
результате подсыхания. Затем, используя специальную ложечку-ситечко, зачерпывают примерно 100 комариных яичек (в возрасте от О до 24 ч) и пе
1Г1
реносят в стакан, где проводится тестирование , После выдерживания в течение 2 дней при (26,7°с и относительной влажности 50% подсчитывают число выпупливаний комаров из яиц помещенных в стакан с испытуемым раствором.
Методика оценки инсектицидной активности предлагаемых соединений по отношению к божьим коровкам Epilachn varivestis (Mulsaut),
Ростки лимской фасоли (по 2 на горшок) с первичными листами длиной 7, см погружают (окунают) в раствор, содержащий соответственно 300, 100, 10 или 1 ч. на млн испытуемого соединения, и затем переносят в вентлируемый шкаф для просушки. Затем с растения удаляют один лист и помещают его в 10-сантиметровую чашку Пет- ри, содержащую уложенный на дне увлажненный листок фильтровальной бумаги и 10 личинок божьей коровки в йоеледней возрастной стадии (53- дней от момента вьшупливания) . Через день после указанной обработки с растения удаляют другой лист и подкла- дывают его к личинкам ( после удаления из чашки того, что осталось от первоначального листа). Через два дн после этой обработки к личинкам под- кладьшают третий лист (обычно это последний лист, требуемый для завершения эксперимента). Четвертый лист используют на третий день после об- .работки, если еще не закончился период выкорма (т.е. личинки еще не кончили поедать подкладьгоаемые им листья). В этот период учет погибших личинок еще не производят. Чашки Петри с личинками выдерживают до появления взрослых божьих коровок.примерно через 9 дней после начала эксперимента (обработки). После завершения вьшупливания взрослых насекомых каждую чашку исследуют с целью определения числа погибших личинок, куколок или взрослых насекомых; деформированных (ненормальных) куколок или взрослых насекомых; промежуточных форм между личинкой и куколкой или куколкой и взрослой божьей коровкой; или любых других интерференции в сравнении с нормальной линькой, трансформацией и вылупливанием куколок или взрослых насекомых.
Методика оценки инсектицидной активности предлагаемых соединений
j
10
152025 30 35 5 сп 5
22012
по отношению к южным походным червям Spodoptera el-idania (Cramer).
Ростки лимской фасоли с двумя распустившимися первичными листами длиной 7,5-10 см погружают на 3 с при перемешивании в различные по концентрации испытуемых соединений растворы и затем переносят в вентилируемый шкаф для просушивания. Высохшие листы помещают в 10-сантиметровую чашку Петри, в которой находится кусок влажной фильтровальной бумаги и 10 личинок южного походного (ратного) червя Длиной приблизительно 1 см. Чашки Петри накрывают крышками и помещают в климатическую камеру, где выдерживают в течение 2 дней при 80°Ф (26,) и относительной влажности 50%. Число погибших личинок подсчитывают через 2 дня после начала эксперимента.
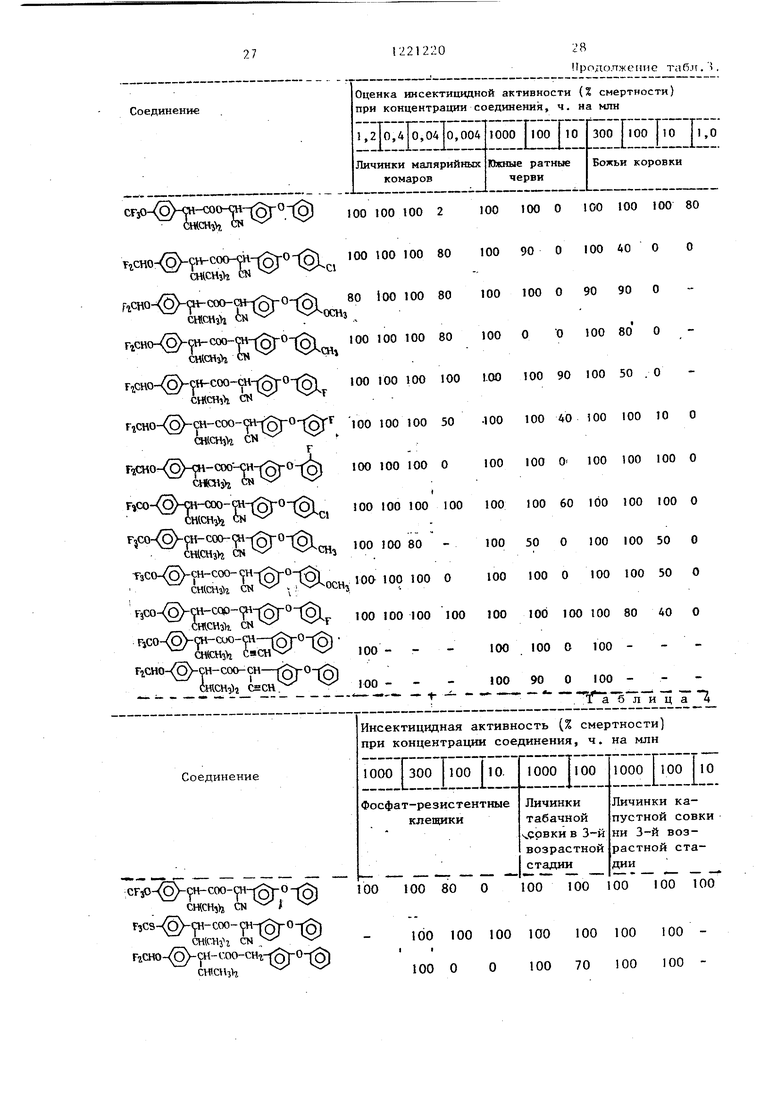
Полученные результаты (в пересчете на процент смертности насекомых) представлены в табл. 3.
Пример. 23. Исследование инсектицидной активности предлагаемых соединений против паутинного двупят- нистого клещика Tetranychus urticae (Koch).
Ростки лимской фасоли с тремя первичными листочками длиной 7,5-10 см заражают примерно 100 взрослыми устойчивыми к фосфатным инсектицидам (фосфат-резистентным) клещиками на каждый лист за 4 ч до испытаний, чтобы дать возможность насекоья 1м отложить яйца на новом месте. Зараженные растения погружают на 3 с в перемешиваемый раствор, содержапщй соответственно 1000, 300, 100 или 10 ч. на млн текстируемого соедйне- . ния, после чего переносят в вентилируемый шкаф для просушки. Затем обсохшие растения выдерживают 2 дня при 80 Ф (26,7 с) и производят оценку погибших взрослых клещиков на одном листе, используя для этой цели стереоскопический микроскоп с 10- ;кратным увеличением. Другой лист ос- i тавляют на растении еще на 5 дней и затем исследуют под микроскопом (при 10-кратном увеличении) с целью оценки числа умертвленных яичек и только что вылупившихся нимф, что -. позволяет определить овицидную и ос- таточную инсектицидную активность.
Методика оценки инсектицидной активности предлагаемых соединений про-(
13
тив личинок табачной совки Heliothis virescent (Fabricus), находящихся в третьей возрастной стадии.
Три ростка хлопчатника с только что pacпycтивши шcя семядолями погру- жают (окунают) в раствор, содержащий соответственно 1000 или 100 ч. на млн каждого из текстируемых соединений, после чего помещают в вентилируемый шкаф для просушки. Когда растения высохнут, каждую семядолю разрезают пополам и каждый из 100 лиственных срезов помещают в 28-граммовую пластмассовую медицинскую чашку, содержащую 1,25-сайтиметровый зубоврачебньй тампон (фитиль), пропитанный водой,-и вводят туда одну личинку совки в третьей возрастной стадии. Чашку закрывают крьш1кой и выдерживают 3 дня при (26,) .и относительной влажности 50%, после чего производят оценку процента смерности насекомых.
Методика оценки инсектицидной активности предпагаемых соединений про тив капустной совки ни Trichoplusia ni (НйЪпег).
Сформировавшийся на хлопчатнике лист погружают в раствор, содержащий соответственно 1000, 100 или 10 ч. на млн испытуемого соединения, перемешивают в течение 3с, затем удаляют и помещают в вентилируемую камеру для просушки. Когда лист подсохнет, его помещают в 9-сантиметро- вую чашку Петри с влажной фильтровальной бумагой на дне. Туда высаживают 10 личинок совки ни в третьей возрастной стадии, и чашку накрывают крышкой. Число погибших личинок под- считывают через 3 дня после выдержки при 80°Ф (26,7°с) и относительной влажности .
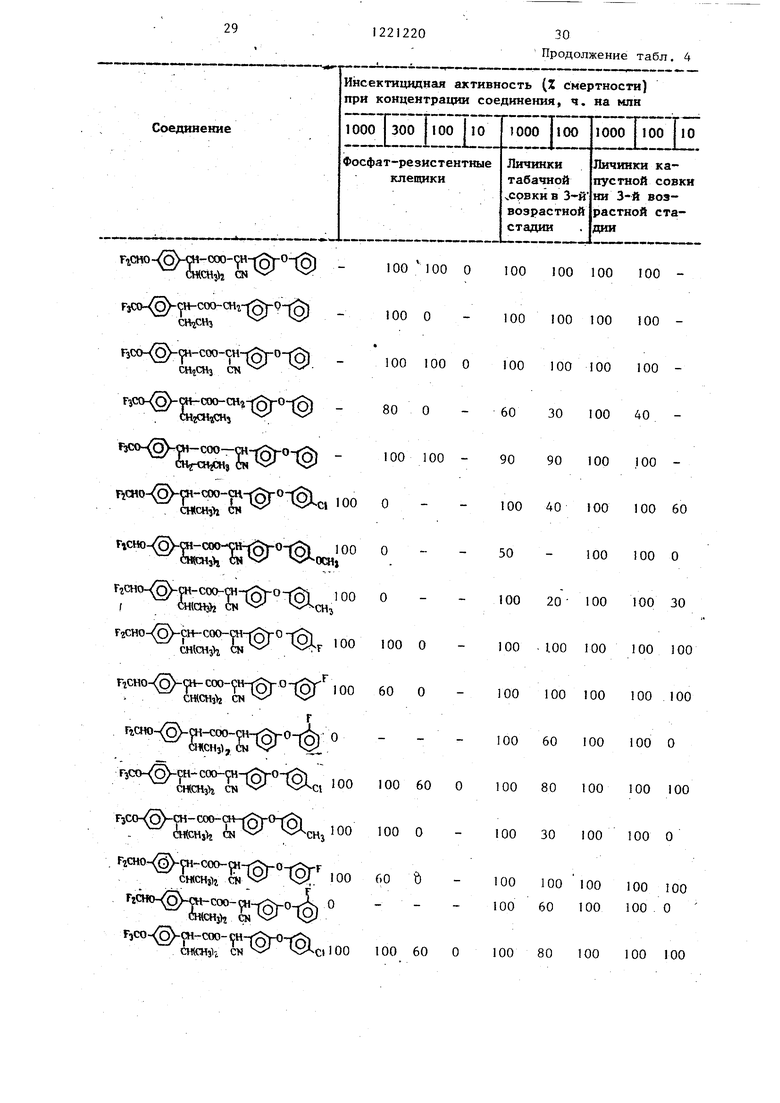
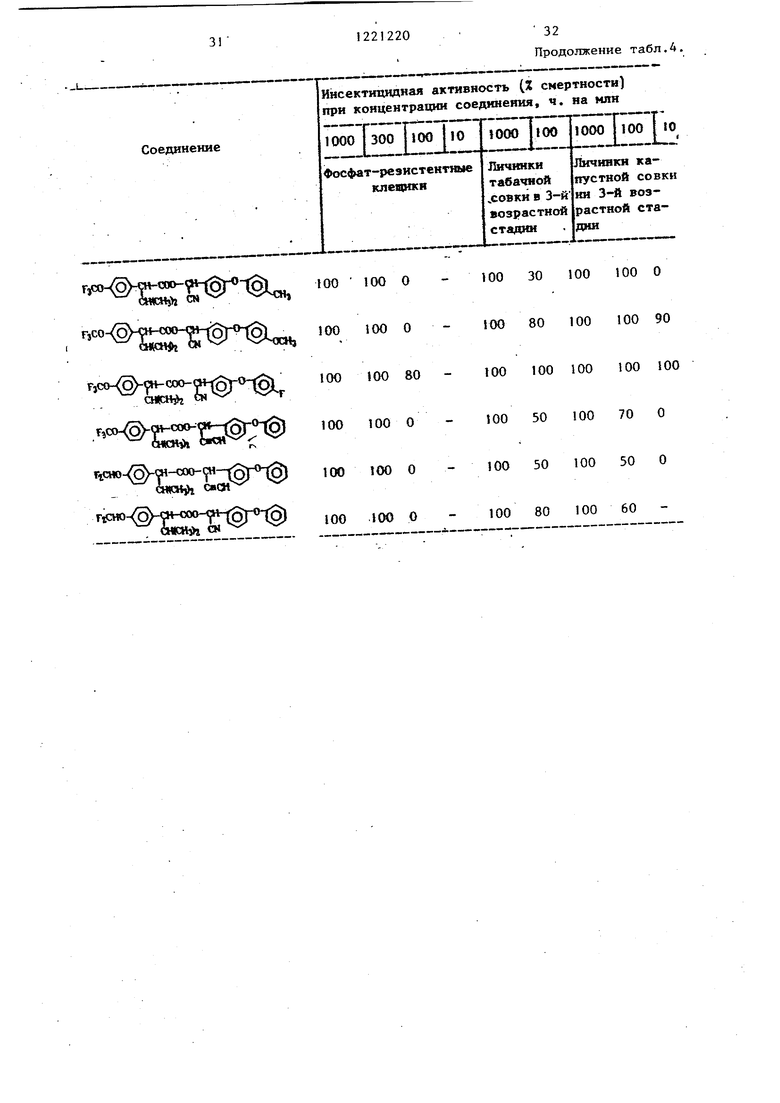
Полученные данные представлены в табл. 4.
Пример 24. Методика оценки почвенной инсектицидной активности предлагаемых соединений при внесении их в почву против личинок блошки длиноусой нжной Diabrotica undecimpunc- tata hovardi (ВагЪег).
10 мг тестируемого соединения разбавляют до 10 мл ацетоном для приготовления запасного раствора А ..Далее 2 мл этого раствора разбавляют до 10 мл ацетоном и получают таким образом раствор Б . Затем приблизително 0,7 г талька марки Ругах АВВ по22014
мещают в широкогорлую банку и прибавляют 1,25 мл выбранного раствора, чтобы концентрация тестируемого соединения соответствовала следующим значениям: 1,25 мл раствора А обеспечивает концентрацию 56 кг/га; l,25Nm раствора Б обеспечивает концентрацию 11,2 кг/га.
Выбранньм для проведения теста раствор смешивают с тальком, чтобы обеспечить его равномерное увлажне-; ние, и затем пропитанный раствором тальк подвергают высушиванию на воздушной сушилке (в струе воздуха) в течение 10-15 мин. В банки, содержащие тестируемые соединения, прибавляют 25 мл влажной стерилизованной почвы для горшочков и примерно 0,6 г просяной муки (корм для личинок). После этого банки закрывают крьш1ка- ми и содержимое тщательно перемешивают с помощью вибращюнного стенда- смесителя. В каждую банку вносят 10 личиной длинноусой блошки в возрасте 6-8 дней. Банки неплотно прикрывают крьшжами и вьщерживают в климатической камере при 80°Ф (26,7°С), относительной влажности 50% и постоянном освещении 6 дней. После этого подсчитывают число погибших личинок и вычисляют процент смертности .
При внесении 56 кг/га oi-циано-м- -феноксибензил сй-изопропил-4-три- фторметоксифенилацетата обеспечивается 100%-ное уничтожение личинок блошки длинноусой; применение указанного соединения в дозе 11,2 кг/га обеспечивает 70%-ную смертность насекомых.
Пример 23. Остаточная инсектицидная активность, получаемая при обработке листвы хлопчатника.
Молодые ростки хлопчатника, по крайней мере, с двумя сформировавшимися листами, растущие в 10-сантиметровых пластиковых горшочках, погружают (обычно одним листом за один раз) в раствор испытуемого соединения в смеси 65% ацетона и 35% воды и оставляют в нем при перемешивании 3 с. Концентрация каждого соединения |В указанных растворах составляла 80, 100, 300 или 900 ч. на млн активного ингредиента.
После того, как листы высохли, два листа от каждого из двух растений отщипывают и помещают в чашки
, . 122 Петри (90 X 10 мм) на выложенную на дно увлажненную фильтровальную бумагу (диаметром 9 см; марка бумаги Ватман № 1). На каждый лист высаживают пять личинок табачной совки j в третьей возрастной стаду.я. Чашки Петри с личинками совки накрывают крышками и помещают в климатическую камеру, где выдерживают в условиях постоянного освещения при 80 Ф ю (26,) и относительной влажности 50% 72 ч. После этого подсчитывают число выживших личинок.
Оставшиеся растения помещают в интенсивно освещаемую оранжерею 15 (теплицу) и регулируют режим освещения таким образом, чтобы растения в течение суток освещались 14ч (14-часовой световой день). Образцы
листьев исследуют на содержание ли- 20 чинок совки третьей возрастной стадии после 3,7,10 и 14 дней пребывания в оранжерее в указанных условия х.
Полученные результаты представлены в табл, 5 .25
Пример 26. Иксодицидная (ixodicidal) активность.Эффективное уничтожение личинок клещей показано в следующих тестах на личинках Boophilus microplus - зо one-host клеща, который может оставаться на одном хозяине в течение всех трех жизненных стадий, т.е. на стадиях личинки, нимфы и взрослого клеща. В этих тестах бьши использованы растворы в смеси 10% ацетона и 90% воды, содержащие соответственно 0,025, 0,1, 0,5, 2,5 или 12,5 ч. на млн тестируемого соединения. 20 личинок клеща вкладьгоают .в пипетку, дд один конец которой закрыт марлевой салфеткой, и затем через пипетку просасывают с помощью вакуумной магистрали раствор, содержащий тестируемое. соединение, имитируя таким образом 5 опрыскивающую систему. Затем клещей вьщерживают 48 ч при комнатной температуре и определяют процент смертности.
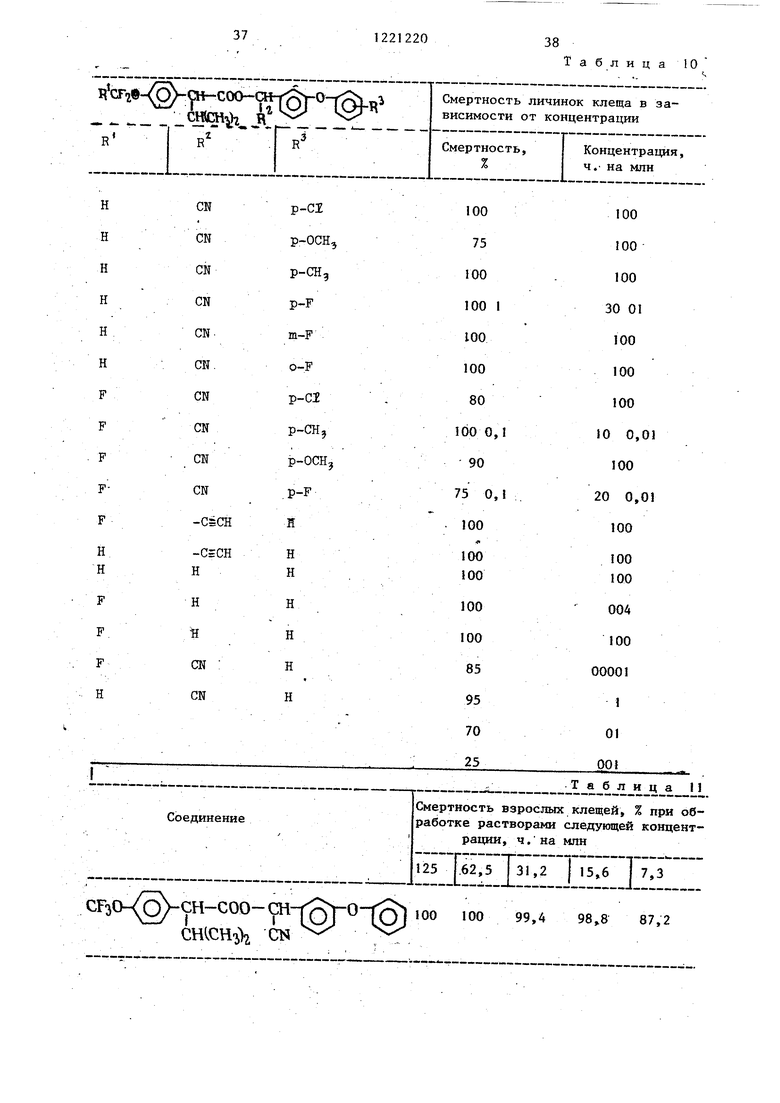
Полученные в зтой серии опытов .«j результаты представлены б табл. 6-10. :
Пример 27. Эффективность предлагаемзгк соединений в борьбе со / взрослыми клещами Boophilus micro- plus определяется в серии опытов, , где тестируемые соединения использу-, ; ются в виде растворов различной кой- центрации (аналогично примеру 26) в количествах, достаточных для при-
35
j ю
15
20
25
о д 5
j :
, ;
5
1220.16
готовления растворов,содержащих соответственно 125; 52,6; 31,2; 15,6 или 7,3 ч. испытуемого соединения на млн ч раствора.
Взрослых, насосавшихся крови самок клеща погружают в испытуемые растворы на 3 с, после чего извлекают и помещают в индивидуальные коробки, где выдерживают 48 ч при комнатной температуре (80 Ф 26,7°С) и относительной влажности 50%. По окончании периода выдержки коробки с клещами исследуют и подсчитывают число кладойг яиц (число отложенных яиц). Затем яйца оставляют до выпупливания личинок, а конечные, результаты выражают в виде процента уменьшения числа жизнеспособных яиц. Насосавшихся крови самок клеща, которые не отложили яйца, считают погибшими.
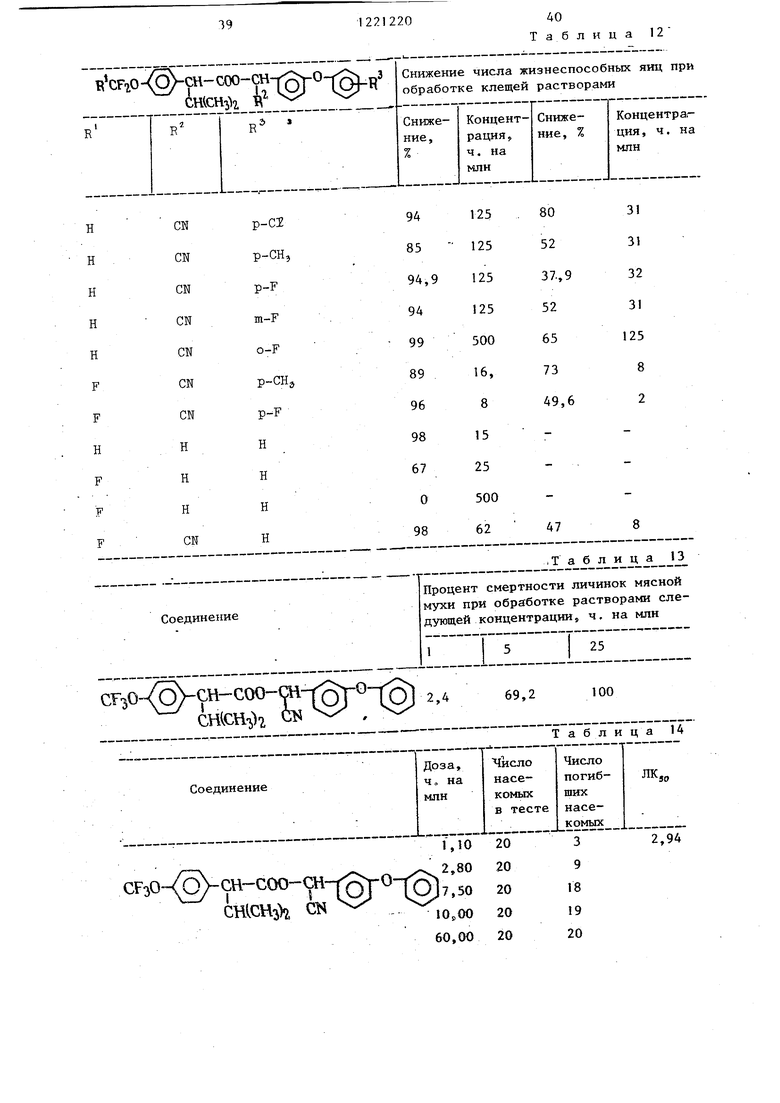
Полученные данные представлены в табл .11-12.
Пример 28. В следующей серии опытов показана эффективность предлагаемых соединений против личинок мясной мухи Cochliurayia homini- vorax, губительного для домашнего скота вредного насекомого. Тест .состоит в том, что личинки мясной мухи питаются смесью из 8,0 г говьяжьего фарша, 7,0 мл крови, 2,1 мл воды и 0,9 мл рецептуры, содержащей соответственно 1, 5 или 25 ч. на млн тестируемого соединения.
Для вычисления процента смертности мясных мух, обработанных указанным способом, используют результаты двух параллельных опытов, в каждом из которых обработке выбранной дозой подвергали 20 личинок мясной мухи. Личинки кормились указанной смесью без ограничения в течение 24 ч. По истечении этого периода подсчитывали число погибших личинок (для каждого опыта).
Полученные данные приведены в табл. 13.
П р и м е р 29. Определение ЛК тестируемых соединений против совки- листковертки на хлопчатнике.
. Молодые ростки хлопчатника, имеющие, по крайней мере, два распустившихся листа и растущие в 10-сантиметровых пластиковых горшочках, погружают (одним листом за один раз) в раствор тестируемого соединения в смеси 65% ацетона и 35% воды и оставляют там при перемешивании на. 3 с.
17
Концентрация каждого из тестируемых соединений в растворах 1,1, 2,8; 7, 20, 60 или 150 ч. на мпн активного ингредиента.
После просушки листьев два листа от каждого, из двух растений отрываю и помещают в чашки Петри (90 к 10мм на влажную фильтровальную бумагу (диаметром 9 см; сорт бумаги Ватман № 1). На каждый лист, находящи ся в чашках Петри, высаживают по пять личинок совки в третьей возрасной стадии, после чего чашки накрывают и помещают в климатическую камеру, где вьщерживают в ус
ловиях постоянного освещения при 80 Ф (26,7°С) и относительной влажности 50% 72 ч. После этого проводят подсчет живых и мертвых личинок. Каждую обработку повторяют 4 раза.
.Полученные данщле приведены в табл. 14, из которой видно, что предлагаемое соединение примерно в 2-5 раз эффективнее в борьбе против сов- ки-листковертки, чем известные.
Пример 30. Определение ЛК, тестируемых соединений против взрослых малярийных комаров Anopheles qua drimaculatus (Say).
Соединения, отобранные для указан ного опыта, растворяют в ацетоне до нужной концентрации. Для получения аэрозольной рецептуры приготовленные инсектицидные растворы вносят пипеткой (0,15 мл) в верхнюю часть распы- лительного сопла распьшителя-пульверизатора. Капельки раствора распыляются со скоростью 6,4 км/ч на комаров, находящихся в специальной сетчатой клетке (25 взрослых самок комара на клетку), в течение 4-5 с. Затем комаров анестезируют углекислым газом (в течение 3-4 с) и переносят в клетку для вьщержки. Клетки с обработанными комарами помещают в климатическую камеру, где вьщерживают при 8511 °Ф (29,5 с) и относительной влажности 4612%. Число погибших комаров подсчитьшают через 24 ч посл обработки.
Полученные результаты приведены в табл. 13, из которой видно, что предлагаемое соединение примерно в 4 раза эффективнее известного.
Пример 31. Остаточная ий- сектицидная активность, определенная для мапых объемов внесения тестируемых соединений.
Тестируемые соединения диспергируют в смеси 65% ацетона и 35% воды, взятой в количестве, достаточном для обеспечения дозы внесения 0,08 кг/га активного соединения в 5,1 галлона (19,3 л) воды. Затем ростки хлопчатника помещают в камеру для опрыскивания и опрыскивают из стационарного пульверизатора, работающего на сжатом воздухе, причем растения рас- лолагают чуть ниже сопла пульверизатора, чтобы капельки раствора попадали на растения .сверху. После того, как листья просохли, два листочка от каждого из двух растений удаляют, помещают в чашки Петри (90 х 10 мм) на влажную фильтровальную бумагу (диаметром 9 см; сорт бумаги Ватман № 1) и на каждый лист высаживают пять личинок совки, находящихся fB третьей возрастной стадии. Чашки Петри с содержимым накрывают крьшка- ми и помещают в климатическую камеру, где оставляют в условиях постоянного освещения при 80°Ф (26,7 С) .и относительной влажности 50% на 72 ч. После этого подсчитьша.ют погибшие и живые личинки.
Оставшиеся растения помещдаот в оцанжерею, где поддерживается режим освещения высокой интенсивности. Образцы листьев исследуют с использова нием личинок совки через 3,7,10 и 14 дней после опрыскивания.
Полученные данные приведены в табл.16.
Пример 32. Эффективность предлагаемых соединений в борьбе со взрослыми multi-host клещами Rhipi- cephalus sanguineus (R.S.) и Derma- centor variahilis (D.V.) на собаках определяется в следующих опытах, где тестируемое соединение используется в виде растворов, приготовленных аналогично примеру 26 имеющих концентрацию 100, 10 или 1 ч. на млн.
Взрослых, насосавшихся крови самок клеща «погружают в тестируемые растворы на 3 с и помещают затем в индивидуальные коробки, где выдерживают 48 ч при комнатной температуре ( 26,) и относительной влажности 50%. По окончании периода выдержки коробки с клещами исследуют и подсчитьгоают кладки яиц. Насосавшихся крови самок клеща, не отложивших яиц,, считают погибшими.
Полученные данные приведены в табл. 17.
Опыт повторяют, но для обработки используют растворы, содержащие соответственно 80, 40, 20, 10, 5 или 2,5 ч. на млн тестируемого соединения , Полученные данные являются сред- ними из двух опытов для,каждой концентрации (см. табл. 18),
Пример 33. Опыты ведут аналогично примеру 32, но используют взрослых самцов и самок multi-host клещей Rhipicephalus sanguines (R.S.) Dermacentor Yariabilis (D.V.). При этом используют количество соединения, достаточное для приготовления растворов, содержащих соответствеино 1,0, 0,1, 0,01 или 0,001% тестируемого соединения. Подсчет числа погиб ших клещей и вычисление процента смертности производят через 24 и 48 ч после обработки.
Полученные данные представлены в табл. 19.
Пример 34. Эффективность предлагаемых соединений против осенних мух Musca autiffiinalis определяется в опытах, где личинкам мух однодневного возраста кормились на коровьем навозе, содержащем соответственно Р,.13, 0,25 или 0,50 ч. иа млн тестируемого соединения.
Для вычисления процента смертности осенних мух, обработанных указанным способом, используют результаты двух опытов, в каждом из которых обработке выбранной дозой подвергали 10 личинок осенних мух указанного возраста. Вычисление процента смертности производят по результатам сравнения t конт22020
рольными опытами, где использовался навоз, не обработанным инсектицидом.
В каждом опь1те (при выбранном уровне дозировки тестируемого соединения раствор соответствующего количества тестируемого соединения в ацетоне прибавл5шт к 1 кг свежего коровьего навоза и перемешивают в течение 1 мин с помощью электрического миксера. Навоз, используемый в контрольных опытах, обрабатывают так же, но к нему прибавляют только ацетон. Образцы навоза разделяют на 4 части, каждую из KOTopEix помещают в бумажную чашку для суфле. Во все чашки высаживают однодневные личинки осенней мухи, после чего чашки вьщерживают в течение 7 дней при температуре около (26,7 с) и относительной влажности 50%. Затем содержимое чашек исследуют на наличие куколок, которых подсчи тьшают, взвешивают и помещают в пластиковые ампулы, где держат до вылуп- ливания и смерти. После того, как мухи погибли, их подсчитывают и определяют эффективность обработки (в процентах).
Полученные данные по оценке предлагаемых соединений в качестве кормовых добавок для борьбы с осенними мухами приведены в табл. 20 (средние дз-чные из двyk опытов) .
Инсектициды, полученные из производных фенилуксусной кислоты, проявляют более высокую инсектицидную активность, чем известные соединения аналогичной структуры.
Таблица 1
R CF OH O/ CH-COO-CH-Y-g О СН(СНзЪ CN
R Данные ЯМР
6,8, 7,5 (м., 12Н, АгН)
R p-Cf
p-OCHj
6,45 (т., Z 7,4 Гц, IH.OCHF)Н 4,56Н 4,92
6,30, 6,33, (2с., Ш, CH-CN)N 2,88N 2,82
3,25 (д., I 10. Гц, 1Н, СН-СН(СН,)2
0,6, 1,2 (д., 6Н, СН,)
6,8, 7,4 (м., 12Н, АгН)С 67,35С 67,30
6,47 (т., I 7,4Тц, 1Н OCHFj)Н 5,23.Н 5,46
I Вычислено
Вычислено I Найдено С 64,27 С 64,54
Таблица
















| название | год | авторы | номер документа |
|---|---|---|---|
| Мета-феноксибензиловые или @ -циано-мета-феноксибензиловые сложные эфиры 2-галоидалкил (окси-,тио-,сульфинил-или сульфонил) фенилалкановых кислот,проявляющие инсектицидную,иксодицидную активность | 1978 |
|
SU1082782A1 |
| Способ получения производных феноксибензил-2-(4-алкоксифенил)-2-метилпропилового эфира | 1983 |
|
SU1447275A3 |
| ПРОИЗВОДНЫЕ 2-ЗАМЕЩЕННОГО ФЕНИЛ-2-ОКСАЗАЛИНА ИЛИ 2-ЗАМЕЩЕННОГО ФЕНИЛ-2-ТИАЗОЛИНА И ИНСЕКТИЦИДНАЯ И/ИЛИ АКАРИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1990 |
|
RU2029766C1 |
| ПРОИЗВОДНЫЕ 1-АРИЛИМИДАЗОЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ИНСЕКТОАКАРИЦИДОНЕМАТОЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, КЛЕЩАМИ И НЕМАТОДАМИ | 1991 |
|
RU2072992C1 |
| Инсектоакарицидное средство | 1977 |
|
SU650480A3 |
| ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ И ПРОИЗВОДНЫЕ N-ФЕНИЛ-N'-(2,6-ДИФТОРБЕНЗОИЛ)-МОЧЕВИНЫ | 1987 |
|
RU2032343C1 |
| Производные бициклооксифенилмочевины,проявляющие пестицидную активность | 1983 |
|
SU1425190A1 |
| ПРОИЗВОДНЫЕ АРИЛПИРРОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2037485C1 |
| Инсектицидная и акарицидная композиция для применения в сельском хозяйстве и садоводстве | 1984 |
|
SU1817682A3 |
| Способ получения эфирохлорангидридов этилтиофосфоновой кислоты | 1984 |
|
SU1351515A3 |
2-Алкил-2-(4-фторметокси, 4-фтор- ,тио)-фенилуксусная кислота общей формулы , / R - CF i-X- O)-CH-COOH 1 где R CFjX находится в пара-положении к углероду кислотной группы; X - О; в - Н; -R - , X -О, R -F, , H-Pr, i-Pr-,/ X - S; , R - F, R - i-Pr, в качестве промежуточного вещества для инсектицидов. Приоритет по признака м 01. i0.76R F, X О,
100 100 100 100 70 100 100 90 90
ЮО 61 100 100 - 100 100 80
i 70
100 О 100 о
I
40
100 100 о
FiCHoX2 -CH-COOCH-|gj-0- ,QQ
crtcHjHCN
100 86 JOO 100 - 00 100 100
f 99
FjCO @-CH-COO-CH2 v-0-Yo)100
СН1СНз 1
T3CO-(g - fH-coo-c:H- 3rO-jgj ,QQ
CHjCH CN
0 100 0
i
40
61 too 70 ,- i 70
0 too 0
r
40
71 100 50 - -t
85
100 100 100
100 100 100
0
100 90 90
HFiCO-@-CH-COO-(pi-{g|-0- 100 CMCHj CN
100 100 100 100 0 100 too 100 0
°°
too 100 0 50
100 0 100 90 0 .100 too 75
100 0 90 50 0 100 100 70
100 too 100 0 - too too 90 0
too 50 100 100 50 100 100 50 0
100 100 0
( 100 100 100 100 100 80 100 100 90 о
F,co-/g -CT
СНКН CN F3CCh.O)- co&-CH-jgY-o-| 100 100 о 100 100 50 100 100 100 О
СЙСНэЧ CS -.
r3CO-(gHgj--coo-gb- o- gQ 80 о 100 100 0. 100 100 100 О
(O)
«ШзН СЯ
( 100 100 100 100 60 - 100 100 100 о
r,CO- g CHr-CCO-CH-{g)-0-(g) j g j j OfSCH jh ,(gr°-tO) 100 100 50 100 75 - 100 100 50
cr 0- COO-CH-r O-| 100 100 100 90 100 100 100 100 100 100 I DO CH№A CN , -CF 8- CH-COO-(|H-r Q| O-rQjlpO 100 86
fxKK- CN °
99
TlCHO- - H-COO-CHi-roJ-O-fQ IQO ,OQ ,00 ,QQ 100 0 100 90 50 - CWCHjIi V
flCHO-. ,QQ JQQ ,OQ ,QQ ,QQ ,QQ JQQ ,QQ Q
cFjO- - -ca -cH4- gj-o-j 100 100 loo - loo 100 70 90 о о CHjCHj F#X - -CH-COO-CH- gY-0- JQQ JQQ ,QQ ,QQ ,QQ JQQ gQ 90 50
СНчйСИз CN --
r3CO-(O;-CH-COO-(jHi-(Qj)-(C),QQ ,OQ ,OQ ,00 ,00 100 90 0
ClhCH CHj
r o- 9H-coo-cH-(gj-o- jQp
G.
100 100 0 100 100 100 100 too 70 100 100 100 Соединение
CF3p-@by-COCH:H-(gj-0-(o) ,00 ЮО ЮО 2 ЮО 100 о 100 100 100 80
100 100 100 80 100 90 О 100 40 О
TiCHO- - H-coo-CH-jgrO -(о1
CHlCHjH CN - r CHoXObjH-COO-CH- gt-O-gl 80 iOO 100 80 100 100 о 90 90 о снрнй та riCHo-(o)-Qft-coo-CH-YQj-o--r; lOO 100 юо 8о юо о о юо 80 о (
FiCHO- y-CH-COO-CH- Q-j-O-j 100 100 100 100 1.00 100 90 100 50 .0
сшснл сн . riCHO-(@)-CH-COO-CH-YQT-0- r r -,00 100 100 50 -100 100 40 100 100 10 О
СИ Г7рно- §Н;н-с о--сн-г о-г0
СИСНй ™ F CO- -CH-COO-W- Qj-0- Ql
ШСН CN
F,CO-(O -CH-COO-(JH- QrO-r3
адсНз 7 CN -/
100 100 100 о100100О 100100100о
f
100 too 100 10010010060100100100о
100 100 80 -10050о10010050О
T3CO-{O -CH-COO- JH-jgj-0- j 100 о 100 100 50 о
CHICH.T,) CN г . ,
FjC04;p)(OX 100 100 100 100 100 100 100 100 80 40 о
Cfflvn ll и
FjCO-)- jH-CUO-CH-() (ЖЩг СаСН 100 - 100 100 о 100 FiCHo- O)-CH-coo-cH-foT tO l
ШСНз)г СЭСН - 100 -coo-gH-f5r.
CFjOXO)
CN I ГзС8- сн- соо- JH-TOT Го1
CN
Ггсно- си- е.оо-снг- р} (С)
CHiai,h
Оценка инсектицидной активности (% смертности) при концентрации соединения, ч. на млн
1,2 0,4 0,04 0,004 1000 МОО МО
300 МОО JIO |l,0
Южные ратные черви
Божьи коровки
100 100 100 80 100 90 О 100 40 О
100 100 100 о100100О 100100100о
f
100 too 100 10010010060100100100о
100 100 80 -10050о10010050О
100 - 100 100 о 100 100 90 о 100 100 100 80 о 100 100 100 100 100
100 100 100 100 100 100 100 100 о о 100 70 100 100 FiCHO- -Oi-COO-IJH-jgj-O1ЛтлЛ1 12
ГзСО-(Н-соо-сНг- ОГ(О)
СНтрНэ
FjCO- -CH-COO-CH-rQY-O- Q j СНгСНз о
nco- -fb-cao-cHi-j-Qj-o-igj
100 100 о 100 100 100 100 100 о
100 100 100 100 100 100 О 100 100 100 100 80 О
60 30 100 40
100 100 - 90 90 100 100 100 40 100 100 60
50
100 100 О
100 20- 100 100 30
ГгсночОУ-сн-соо-сн-гоГО TrTl
,„.., ISfr 100 00 О - 100 .100 100 100 100
cHtoHjH
FiCHo- g - p-coo- fH-jgpo-jgj- ,QQ
CVttCH fZ - sx
/ s sngro-i ЕП:Т§Г°Т§ХС; .00
100 100 0
f.o Ъ
FiCHO- hCH-COO-OT-Y frO-ii 0 UCHjh S 5Г 10)
F5CO-(O -CH-COO- H-f
ШШэ1г CK
xCJlOO 100 60 0 100 80 100 100 100
60 0 - 100 100 100 100 100
100 60 100 100 0
100 60 0 100 80 100 100 100
0
Ъ
100 30 100 100 0
100 100 100 100 100 100 60 100 100 . 0
31
1221220
32
Продолжение табл.4,
)
ЙШЧ т
100 100 о
100 100 80
СНКИй
rtfWO-(4jH-4W-(fH- 3lrOTgj dwHih
100 100 о
100 30 100 100 о
100 80 100 100 90
too 100 100 100 100
100 50 100 70 О
100 50 100 50 О
100 1(Ю о - 100 80 100 60
Д-ЦЛ-ГМ-Т- -1Ш-Т |Г 11 L | - mjr, - -иТПИ 11- Г л -JJT-I- -ц -л |гЛ- - JJ Il l .ЛТЦ - т- ТИД-.
Соединение
сьо- О/-сн-соо-. -,
CN
Соединение
.0,1 I 0,025 I 0,005 0,001
Таблица 6
Процент смертности личинок клещей Boophilus microplus, обработанных раствором следующих концентраций, ч. на млн
12,5
2,5 I 0,5 j 0,1 j О,
025
100
100 100 100
Таблица 7
Процент смертности личинок клещей Boophilus microplus, обработанных раствором следующих концентраций, ч. на млн
(O)CH-GOO-CH-rQj-0 CHlCHoi T, CM
100
100
8080
Соединение
0,1 I 0,01 I 0,001 I 0,0001|о,00001
Fi€HC
;0 -сн--соо-сн- о- сн(Шз)г CN -
Соединение
Таблица 8
Процент смертности личинок клещей Boophilus microplus, обработанных раствором следующих концентраций, ч. на млн
100
100
100 50
Та б л в ц а 9
Процент емертвостн лячююк кпецей Boophilue mieroplus, обработанных раствором ковцеятрацих 100 ч. на млн
р2СНО-{О)- и соо-снгСШСНзЧFjCO- CH-COO-CHTrrQt-O
ГзСО- CH-COO-CH-r J-0
снгсн
соо- гШтСНз
100
100
too
100
CH-COO-GH-f
cmcH j) CN
Таблица 10
fQj 100 100 99,4 87,2
41
Данные, полученные в двух (1) и (2) различных опытах Сравнительные примеры
1221220
42
Продолжение табл J 4,
Т,а б л и ц а 16
0,08 95 0,03 00 О 90 003 90 О80 0,03
«ш)
CHKHj 4 СМ
Контроль-О 92,5 О 88,5 О 87,5 30 41,3 О 67,5
CpeAaidt % смертности яаршяок совки (расчет производился по 20 личинкам, подсчет погибяшх
лкчияок осуществлялся через 72 ч после инсектицидной обработкн) Средний И повреждения растешА в результате выедания оковек в листьях (по 4-м ларалпелъным опытам) Сравнителыв4е примеры
0,08 95 0,1 90 3,0 80 2.5 80 0,78 50 1,6
„. Т а б лиц а 18
Сифонаптерицвдная активность соединения
F2CHo--(o)--cH-a)o-cH--j
CHicH h с
I
Время после обработки.
Процент смертности взрослых кяецей при концентрации соединения, ч. на млнi
80
Uo Т 20 I 10 I 5 Т Т °
24
100 70
45
Единичное испытание
Таблица 17
.О
30
40
20
О
Составитель И. Ковалев Редактор К. Волощук Техред М.Ходанич
Заказ 2800Тираж 379Подписное
ВНИИГО Государственного комитета СССР
по делам изобретений и открытий. .
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
Таблица 19
Корректор И. Эрдейи
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ПРИБОР ДЛЯ ЗАПИСИ И ВОСПРОИЗВЕДЕНИЯ ЗВУКОВ | 1923 |
|
SU1974A1 |
Авторы
Даты
1986-03-30—Публикация
1978-10-16—Подача