где Ar имеет указанные значения, в среде инертного растворителя. Предлагаемые производные мочевины .могут быть получены при проведении реакции приблизительно эквимолярных количеств замещенных фенилизоцианата и 3-аминометилпиридина в присутствии инертного растворителя, например ацетонитрила, бензола, толуола или 1,2-диметоксиэтана (глима).. Исходные продукты для осуществления предлагаемого способа известны .или могут быть получены известными способами; Пример 1. Получение 1-.(3пиридилметил)-3-(4-нитрофенил)мочевины (1 ).. Раствор 415 г сырого п-нитрофенилизоцианата в 4,5 л толуола перемешивают при комнатной температуре. Смесь фильтруют и удаляют 35 г нерастворимых примесей. Содержимое раствора соответствует 380 г (2,32 моль) очищенного п-нитрофенилизоцианата. Раствор перемешивают в атмосфере сухого азота и по каплям добавляют 250 г (2,32 моль) 3-амин6метилпиридина. За счет экзотермичности реакции температура смеси повы шается до 40с. Образующуюся тонкую суспензию перемешивают до следующего дня и отфильтровывают в в.акууме. Про дукт промывают гексаном и сушат в .вакуумном шкафу при 60°С до следующе го дня. Получают 610,7 г (98 вес.%) продукта с т.пл. 220-221,5с. Продукт соответствует 1-( 3-пиридилметил -3-(4-нитрофенил) мочевине. Этот про дукт после перекристаллизации из 2-метоксиэтанола плавится с разложением при 223-225с. Пример 2. Получение 1-(3-пи ридилметил)-3-(4-цианофенил)мочевины Промежуточный фенил-N-(3-пирйдилметил)карбамат приготовляют следующим образом (2). Готовят раствор 21, (0,2 моль) 3-аминометилпиридина и 22,2 г (0,2. моль) триэтиламина в 150 мл безводного эфира. В течение 20 мин по каплям добавляют 31,4 г (0,2 моль) фенилового эфира хлормуравьиной кислоты в 100 мл сухого эфи ра. Образующуюся суспензию перемегиивают более 30 мин а затем отфильтро вывдют в вакууме для удаления- соляно триэтиламина. Из фильтрата после охлаждения выделяют 4,1 г требуемого карбамата, плавящегося при 88-90°С. Из второго фильтрата после выпаривания получают 25 г слегка загрязненного продукта, плавящегося при 75-85с, Солянокислый триэтиламин растворяют в воде и водный раст вор затем экстрагируют метилендихло.:ридом. При выпаривании осушенного ме тилендихлоридного экстракта получают Д1 г продукта, плавящегося при 82аВ С. Общий выход сырого фенил-N-(3-пиридилметил)карбамата составляет 40,1 г или 89 вес. % , Далее из карбамата гЮлучают мочевину. К раствору 10,9 г (0,05 моль) фенил-N-(3-пиридилметил)карбамата в 150 мл безводного этанола добавляют 5,7 г (0,05 моль) iv-аминобензонитрила. Смесь кипятят с обратным х длодильником 5 ч, охлаждают и выпаривают при пониженном давлении, получая темное масло. Это м.апло растворяют в эфире и образовавшийся раствор троекратно промывают порциями по 50 мл 5%-ного едкого натра. После высушивания эфирного раствора и испарения растворителя получают желтое масло, которое сушат в глубоком вакууме. При этом небольшое количество продукта сублимируется, а остаток кристаллизуется в колбе. Перекристаллизация из этилацетата прийодит к получению 5,2 г белых кристаллов, плавящихся при 184-187с. Полученный продукт с выходом 43 вес.% соответствует 1-(3-пиридилметил)-3-(4-цианофенил)мочевине. Пример 3. Получение 1-(3-пиридилметил)-3-(4-меркаптофенил) мочевины (4). А. Получение 4-меркаптофенилизоцианата. Реакционную смесь, состоящую из молярных количеств трет-бутилмеркаптана, едкого кали и ft-хлорнитробензола в 1,2л этанола, перемешивают в течение 4 дней при температуре от комнатной до 45°С и затем фильтруют. Фильтрат выливают в воду и. экстрагируют метилейдихлоридом, получают 161 г коричневого масла, что соответствует выходу сырого 4-(трет-бутилмеркапто)нитробензола 76 вес.%. К, суспензии 52,8 г (0,25 моль) 4-(трет-бутилмеркапто)нитробензола и 150 г х елезного порошка в 1 л воды добавл.яют 1 мл уксусной кислоты. Реакционную смесь перемешивают в течение 18 ч при 90°С и фильтруют. Как остаток, так и фильтрат несколько раз экстрагируют метилендихлоридом и объединенный осушенный экстракт концентрируют при пониженном давлении с получением 18,2 г коричневого масла. Выход 4-(трет-бутилмеркапто)анилина составляет 40 вес.%. К полученному маслу в 100 мл бенЭола по каплям добавляют затем 158 г 12,5%-ного бензольного раствора фосгена (0,2 моль) при охлаждении. Реакционную смесь перемешивают 1 ч при , затем до следующего дня при комнатной температуре и затем кипятят при перемешивании с обратным холодильником 7 ч. После выдерживания до следующего дня реакционную смесь фильтруют, а полученный фильтрат концентрируют при.пониженном давлении и подвергают вак.уумной разгонке. Собирают две фракции: первая фракция 2 г прод тов, перегоняющихся при 5б-61°С/ /0,85 мм рт.ст. и вторая 2 г продуктов, перегоняющихся при /0,45 мм рт.ст. Первая фракция является 4-меркаптофенилизоцианатом, а вторая фракция - 4-(трет-бутилмер капто)фенилизоцианатом. Б. Получение 1-(3-пиридилметил)-3-(4-меркаптофенил)мочевины. К 0,9 г (0,006 моль) 4-меркаптофенилизоцианата в 50 мл безводного бензола добавляют 0,65 г(0,006 моль 3-пиридилметиламина. В результате экзотермичности реакции температура повышается до 40С и образуется белый осадок. Реакционную смесь мгнове но нагревают с обратным холодильнико затем охлаждают до комнатной температуры и отфильтровывают с получение 1,2 г продукта, плавящегося при 155159°С. Выход полученной 1-(3-пиридил метил)-3-(4-меркаптофёнил)мочевины составляет 77,5вес.%. Пример 4. Получение 1-(3-пиридилметил)-3-(4-трет-бутилмеркаптофенил)мочевины (10). К 1 г (0,005 моль) 4-(трет-бутилмеркапто)фенилизоцианата (см.пример 3) в 50 мл безводного бензола добавляют 0,52 г (0,005 моль) 3-пиридилметиламина. Температура возрастает до и образуется осадок. Реакционную смесь очень короткое время кипятят с обратныг/1 холодильником, затем охлаждают и фильтруют. Получают 1,5 г (выход 98- вес.%) твердого вещества, плавящегося при 154-157,5с. Продукт является 1-(3-пиридилметил)-3-(4-трет-бутилмеркапто)фенилмочевиной. В таблице представлены физические константы и данные элементного анализа предлагаемых соединений.В приведенных данных элементного анализа величина в скобках соответствует теоретическому значению,рассчитанному по эмпирической формуле.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3-придилметил- (4"-замещенных фенил)=карбаматов | 1973 |
|
SU583745A3 |
| Способ получения производных @ -/моно-или дизамещенных /- @ -арилмочевин | 1981 |
|
SU1246891A3 |
| Способ получения производных @ -D-фенилтиоксилозидов | 1988 |
|
SU1567124A3 |
| Способ получения 3,4,5-триметоксибензонитрила | 1984 |
|
SU1452477A3 |
| ЗАМЕЩЕННЫЕ 3-ПИРИДИЛМЕТИЛАМИНЫ И ФОКУСИРОВАННАЯ БИБЛИОТЕКА | 2003 |
|
RU2228930C1 |
| Способ получения пиперазинилсодержащих производных мочевины или тиомочевины или их солей с соляной кислотой | 1984 |
|
SU1542415A3 |
| ИНГИБИТОРЫ FGFR4 | 2014 |
|
RU2715708C2 |
| СПОСОБ ПОЛУЧЕНИЕ АМИНОЭПОКСИДА ПУТЕМ НЕПРЕРЫВНОГО ПРОЦЕССА СИНТЕЗА IN SITU | 1997 |
|
RU2194045C2 |
| АЛКИЛЗАМЕЩЕННЫЕ ЦИКЛИЧЕСКИЕ АМИНЫ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ЛИГАНДОВ D3-ДОПАМИНА | 1997 |
|
RU2185372C2 |
| Способ получения десмедифама | 2023 |
|
RU2810479C1 |

223-225 CjjHj2N403 184-187
76-178 C Hi FjNjO
155-159 S
148-150 Cj HjgNjOS
140-143 С,, H.N.OS ia 17 о
130-133 С , N,jOS
136-137 С N.jOS
141-14 Cj HjiNgOS
154-157,,jOS
117-119Cj HjjN OS
142-143CjgHjjNjOj
157-159Cj H NgOg
168-170,
198-201q,
122-124 q H jN OjS.
221-223q H N O
20,8(20,6)
57,1(57,3)
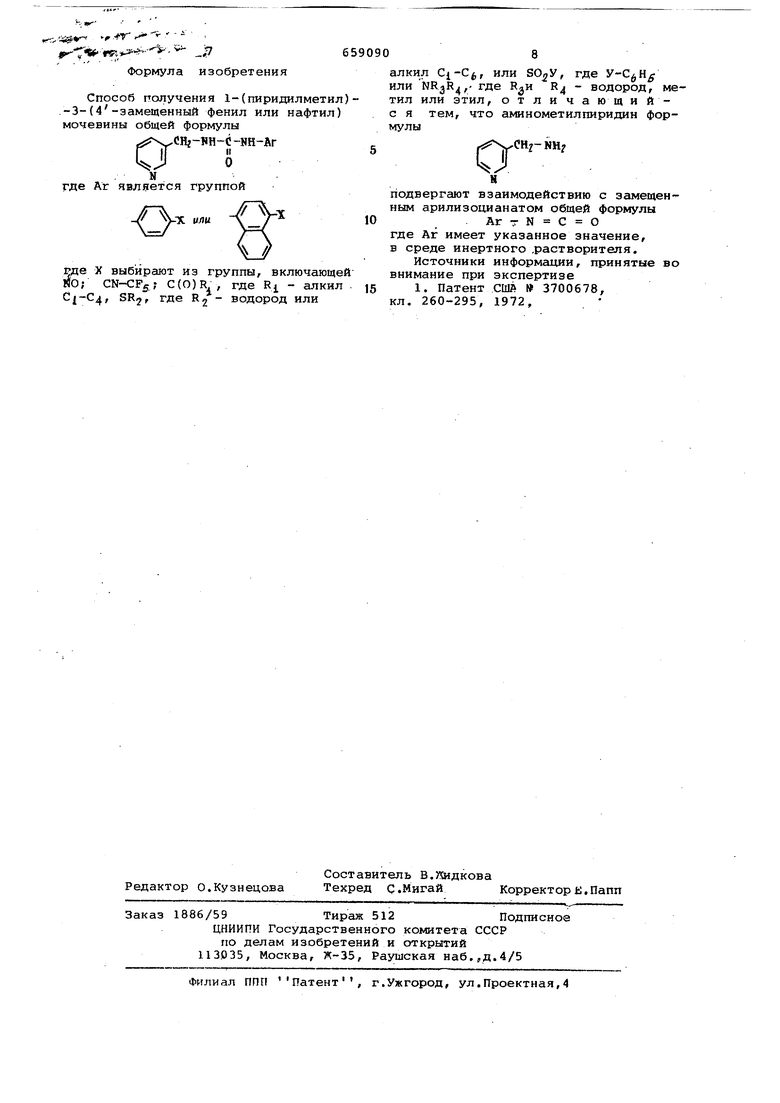
4,2(4,4) 21,9(22,2) 4,9(4,8) 66,4(66,7) 14,1(14,2) 4,0(4,1) 57,0(57,0) 16,0(16,2) 4,8(5,0) 59,9(60,2) 15,5(15,4) 5,6(5,5) 61,4(61,5) 14,6(14,6) 62,5(62,7) 5,8(6,0) 13,9(13,9) 6,4(6,4) 64,0(63,8) 13,5(13,3) 6,6(6,7) 64,8(64,7) 13,6(13,3) 6,5(6,7) 64,7(64,7) 13,5(13,3) 6,8(6,7) 64,5(64,7) 12,6(12,2) 7,2(7,3) 66,3(66,5) ,15,8(15,6) 5,4(5,6) 66,7(66,9) 14,7(14,8) 6,0(6,1) 67,2(67,8) 13,9(14,1) 6,4(6,4) 68,3(68,7) 11,3(11,4) 4,7(4,7) 62,2(62,2) 15,3(15,5) 6,0(6,1) 56,1(56,3) 17,1(17,4) 4,4(4,4) 63,4(63,4) ,..i .,r- ---; изобретения Формула Способ получения 1-(пиридилме .-3-(4-замещенный фенил или нафт мочевины общей формулы аСНг-SH-C-NH-Ar II о . N где Аг является группой где X выбирают из группы, включа НО; CN-CF. f C(O)R. , где R - ал , SRj, где 2 водород или 8 алкил , или , где или Д 3 4 водород, метил или этил, отличающийс я тем, что аминометилпиридин формулы .,снг-нн подвергают взаимодействию с замещенным арилизоцианатом общей формулы Аг т N С О где Аг имеет указанное значение, в среде инертного .растворителя. Источники информации, принятые во внимание при экспертизе 1. Патент сию 3700678, кл. 260-295, 1972,
Авторы
Даты
1979-04-25—Публикация
1976-12-02—Подача