Изобретение относится к способу получения 1,2-дихлорэтана, кото рый находит применение в качестве растворителя, а также исходного сыр для получения хлористого винила для получения полимерньк материалов. Известен способ получения 1,2-ди хлорэтана взаи1 1ОдейстБием этилена с хлористюл водородом и кислородом в присутствии псевдоожиженного слоя катализатора при повышенной те пературе 1. Однако, при этом происходит быстрое закоксовьюание ката лизатора вследствие наличия окислительной атмосферы. Прототипом изобретения является способ получения 1,2-дихлррэтана путем взаимодействия этилена, хлористого водорода и воздуха или моле кулярного кислорода в паровой фазе при температуре 230-355°С и давлени до 10 атм в присутствии неподвижног слоя катализатора - хлористой меди на носителе, при подаче исходных реагентов при соотношении близком к стехиометрическсму, их хорошо перемешивают и подают.на входе реак ционной зоны 2.Частицы используемого катализатора разбавляют инертньм разбавителем с тем, чтобы обеспечить равномерную томпературу по д.пине реакцтюнной зоны, облегчить ее регулирование, а такхе снизить до миним ма температуру так называемых горячих точек - точек пер.згрева зон катализатора. Горячие точки катал -:затора препятствуют норма.пьно№ протека1 ию проп.есса oKCiхлорирования и способствуггг образованию побочных продуктов oxHCJHsiiiiJi , При этом полу-геиную в процессе р-гт-аглп.онную массу подвергают разделению, Еыде.ляют жидкую фазу,содержащую 1,2-дихлорэтан, а нескопденсировавшиес.п газообразные проду сты .выбрасывают, в атмосферу. Недостатком известного способа является образование зон перегрева катализатора, наличие горггчих точек;, что делает процесс мало эффективньм. Целью изобретения является повышение эффективности процесса, Это достигается предлагаег. спо-™ собом получе 1ия 1 , 2-дшг-Лорэтана , состоящим в TOT.if что этилен подвергают взаимодейстЕию с хлористьм водородом и молекулярню.л кислородом в паровой фазе при температуре 230-355С и давлении 2-10 атм в присутствии неподвижного слоя катализатора - хло ристой меди носителе, с- последу1ощи выделением из реакционной массы жи;Дкой фазы, содержащей 1,2-дихлорэтану а органическую газообразную фазу рециркулируют в процесс, при этоН(. хлористый водород и молекулярный КУЮ ;7город подают порциями по всей реакцк ониой зоне, при поддержании молярног соотношения хлористого водорода к этилена (0,05-0,7); и :ислорода и этилена (0,02-0,12):. Отличительньоми признаками способа является проведение процесса при пойаче хлористого водорода и молекулярного кислорода порциями по всей реакционной зоне при поддержании молярного соотношения хлористого водорода и этилена (0,05-0,7) г и Кислорода и этилена (0,02-0,12):,, а газообразную фазу (после вьаделе-ния из реакционной массы жидкой фа-зы;) f рециркулируют в процесс. При этом при одинаковых скоростязс прохождения реагентов в результате реакции оксихлорирования с обычными катализаторами типа .Дикон в форме; неподвижного слоя в соответствии с данным процессом тем.пературн горячей точки значительно ниже и лег че регулируются, чем такие же тем- i пе атуры, достигаемые при работе с йеподвижн М слоем известньм способс ;, при получении дихлорэтана с бо льшой избирательностью. Значительное снижение температуры горячей точки и лучшая конверсия этилена объясняются тем фактом, что этилен, при достаточном избытке по сравнению со стех.иометрнчески необходимым к0личествог 1 функционирует в зоне реакции как эффективный поглотитель тепла (разбавитель и переносчик теп ла) , хотя сам этилен является реаги РУдащим в ейяес ТВ ом о Этилен, содержащийся в реакционной зоне в избытке, является эффектиБньгл поглотите лем теплаf что в качестве источника кислорода можно применять молекулярный кислород без разбавления инертными газами и добавлять хлористый водород в зону реакции по стадиям. Способ предусматривает процесс оксихлорирования с применением молекулярного кислорода. Хлористый водород можно добавлят по стадиям в зону реакции без образования горячих точек с чрезмерно высокий температурой в неподвижно слое. В процессе применяют постадий ное добавление хлористого водорода в зону реакции. Изобретение предусматривает такж рециркуляцию органической газообразной фазы, содержащей по крайней мере 55 об.% этилена. При таком оформлении процесса уменьшается опасность загрязнения атмосферы. Все реагенты, вводимые в зону еакции, должны быть относительно ИСТЬЕ.-Ш , Удобньм источником хлористого водоода является пиро/из дихлорэтана. ригоден хлористый водород более чем 98,8%-ный по объему. В качестве источника кислорода можно использовать любой промышленньзй процесс,- дающий относительно чистый молекулярный кислород, содержащий мало или не содержащий таких инертных газов, как азот, аргон и окись углерода. Такой кислород обычно получают при разных криогенных и э;гектролитических процессах и может быть более, чем 95%-ным по объему, Этиле) f применяе лый при оксихлорировании -.;ожно получать из таких обычных источников, как процессы крекинга иафты, газойля,.этана и т.п. с последую1-1ей очисткой получают 98,8%-ный по объему этилен. Циркулирующий поток f получаемый ; после обычного отде:ления продуктов реакции (дихлорэтан и вода) состоит в основном иэ непрореагнровавшего этилена и содержит очень небольшие количества побочнъ1ч продуктов реакции - хлористого эо:ила / и окисей углерода; общее количество этих побочных продуктов не более 30% по объему. Кроме того присутствует также дюглорэтан в количестве не более 5% по объему. С учетом 1соличества этилена, поступающего из циркулируЕощего удаляемого из зоны реакции потока, и количества свежего этиленаf в зону реакции практически поступает этилен более чем 70%ный по объему или прел,почтительно 78-90%-ный по объему. Количество посторонних в этилене можно поддерживать з указанных пределах при удалении части потока, удаляемого из зоны реакции, перед смешением его со свежим сырьем до введени5; его в зону реакции. Величина потока, yдaляe Ioгo в атмосферу, зависит непосредственно от концентрации инертнызс газов в свежем исходном прод тстео Катализатор, применяемый в процессвр является катализатором оксихлорирования типа Дикой, содержащюл хлорид меди в качестве активного ингредиента на носителе или подложке. Обычно активный ингредиент катализатора наносят на носитель в активной форме, т,е. в виде хлорида меди, или при желании источник меди наносят в форме, превращаемой в активный катализатор в условиях реакции оксихлорирования, например в виде смеси хлорида меди и хлорида меди (I), одного только хлорида меди (1) или Даже металлической, меди. В состав катализатора могут входить один или несколько щелочных металлов и их соли, щелочноземельные металлы и их соли, а также редкоземельные металлы и их соли, кото рые являются известными модификатор ми и стабилизаторами катализаторов оксихлорирования этого типа. Предпочтительными модификаторами и стаб лизаторами катализаторов оксихлорир вания являются хлориды щелочных металлов, особенно хлорид калия, хлориды в редкоземельных металлов, в частности хлориды церия и ди,цимия (дидимий представляет собой смесь, состоящую главным образом из лантана и неодимия и меньших количеств празеодимия и самария). К носителям катализатора от осят ся инертные материалы, обычно примен емые в процессах оксихлорирования в неподвижном слое катализатора, активным ингредиентом которого являетс хлорид меди. Пригодными носителями являются окись кремния, окись алкминия, фуллерова земля, пемза, инфузор ная земля и т.п. Особенно пригодны ввиду желательного действия их на активность катализатора такие матери лы, с большой площадью поверхности, как у-окись алюминия, алкмосиликат и окись кремния. Нанесенные на носитель композиции обычно содержат хлорид меди в пределах от 1 до 20% в пересчете на металл от общего веса металла и носителя. Модифицированные и стабилизированные композиции обнчно содержат модификатор и стабилизатор в количестве, от 0,1 до 30% от веса меди, присутствующей в композиции. Каталитическую композицию на НОСИ теле обычно приготовляют в форме гранул, кусков, частиц, таблеток, колец или шариков с размерами, пригодными для применения в виде неподвижного слоя. Обычно частицы катализ тора на носителе имеют такие размеры что проходят через сито с отверстиям 4,76 мм и задерживаются на сите с от верстиями 2,00 мм, однако, можно . применять и частицы других размеров. Катализатор на носителе размадают в зоне реакции обычным способом.Масс неподвижного слоя катализатора в зон реакции может состоять только из час тиц катализатора или частиц катализатора, тщательно смешанных с такими твердыми инертными разбавителями, как окись алюминия, окись кремния, карбид кр емния или графит. Такие твердые разбавители, имеющие меньшие размеры, чем размеры катализатора на носителе, обычно содержатся в количестве от 5 До 95% общего объема неподвижного слоя. Некоторое снижение температуры горячей точки достигается при поддержании меньшей концентрации катализатора в тек участках зоны реакции, в которых концентрация реагентов наибольшая. Таким образом, предпочтительно ис пользуют неподвижный слой катализатора, в котором концентрация катализатора постепенно увеличивается от входа реагентов в зону реакции, т.е. от той части этой зоны, в которую поступает значительная часть реагирующего этилена, до вьтхода продуктового потока из зоны реакции. Концентрация катализатора уменьшается в тех частях зоны реакции, где имеются значительные количества хлористого водорода и молекулярного кислорода, и температура относительно высокая. Такое изменение концентрации катализатора облегчается загрузкой в зону реакции слоями катализатора разной концентрации, .или увеличением концентрации содержания твердого разбавителя, или уменьшением концентрации акт1-шного катализатора, наносимого на носитель. При применении твердого разбавителя пригодна концентрация катализатора в пределах от 20 до 70% по объему в тех частях реакционной зоны, где концентрация реагентов наибольшая, и до более 90% . по объему, в частях зоны с наименьшей концентрацией реагентов. В тех случаях, когда содержание активного катализатора на носителе изменяется, пригодна концентрация катализатора от 1 до 10% по весу в тех частях зоны, где концентрация реагентов наибольшая, и до 15-20% по весу в частях зоны с наР1меньшей концентрацией реагентов. Хлористый водород и кислород добавляют к реакционной массе в нескольких точках по длине зоны реакции и во всей зоне реакции поддерживают в реакционной среде определенный малярный избыток этилена относительно других реагентов. В зоне реакции поддерживают такую температуру, при которой этилен преобразуется в дихлорэтан с большим выходом. Обычно используют однотрубчатый реактор с рубашкой и теплообменникам, в который загружают катализатор в виде неподвижного слоя. Весь или почти весь этилен поступает на входном конце реактора, а хлористый водород и молекулярный кислород (и остальной этилен, когда он неполностью подаете я на входе в реактор) водят во многих точках реакционной зоны, чтобы поддерживать молярные отношения реагентов в зоне реакции на указанных выше уровнях. Для веения процесса можно применять ного трубчатых реакторов, располоенных параллельно, снабженных рубаипоми и зaгpyжae tыx так, как описано выше. При предпочтительном осуществлении изобретения зону реак И.НИ разделяют на две или более посл довательные ceKUPiH примерно одинако вых размеров, например, применяют один трубчатый реактор или нескольк трубчатых реакторов, установлеинык параллельно. Предпочтительно испэл 1зуют три такие секции, В этом случа весь или почти весь этилен вводят взоне реакции через входной конец первой секциир а хлористый водород и молекулярный кислород добавляют У:ВХОДНЬК концов ПврВОЙ И ОДНОЙ или нескольких последующих секций таким образом, что молярное отношение хлористого водорода к этилену и молекулярного кислорода к этилену ггоддерживагот в указанных высие преуделах При тггком предпочтительном ве,(:1ении процесса все необходимое для реакции количество хлористого водорода распределяют между тремя секциями, такf что 30-60% этого газа добавляют в первую и вторую секции и не больше 30% в пocлeдню э секцию. Общее количество молекулярного кислорода, необходимое для реакции, распределяют между секциями таким образом, что 30-45% газа добавляют в первую и вторую секции к от 10 до 40% в . последнюю секцию , Предпочтительно общие количества хлористого водорода и молекулярного кислорода распределяют меж,цу тремя секциями следующим образом: хлористый водород - 50%г 50%; 0% и молекулярный кислород - 40%:40%s20%, Реакция оксихлорирования протекает при температуре в пределах от 230 до З55с. Для достижения максимального срока службы катализатора и упрощения процесса желательно тем пературу в зоне реакции поддерживат Б пределах от 230 до 3150С, В большинстве случаев пригодно давление в зоне реакции от 3f5 до 7 атмосфер Предпочтительно реакционную масс охлаждают до температуры ниже при давлении от 2 до 5,5 атм до иол чения обогащенной, этиленом газовой фазы и конденсата, состоящего в основном из дихлорэтана и воды, вод удаляют и отгоняют дихлорэтан в од или нескольких колоннах. Циркуляция непрореагировавшей га зовой фазы (в основном непрореагиро вавший этилен) в значительной степ ни уменьшает проблему загрязнения атмосферы. Кроме того, при циркуляции улуч шается выход дихлорэтана из этилен Можно возвращать в зону реакции до 97% непрореагирозавшей газовой фазы. Пример. Проведен ряд опытов о оксихЛорированию этилена с примеениегд неподвижного слоя катализатоа в виде хлорида меди на носителе. Молярное отношение хлористого о.цорода к этилену в реакционной оне поддерживают ниже 0/7, молярное тношение кислород г этилеи в реакционой зоне поддерживали ниже 0,12 и ыше 0,02,, АО Оборудование и описание экспеш тентаЗона реакции состоит из трех последовательно соед.иненных секций, каждая из которых представляет собой никелевую трубу длиной 366 см с рубашкой, в верху которой псзмещается охлаждающий змеевик,. Температуру и местоположение горячей точки определяют с помощью 20 термопар, р.аспололсенных на расстоянии 18 см одна от другой в гильзе, проходящей по всей длине каждой секции реактора. 1ермопары присоединены к регкстрирукщему устройствур Четыре термопары помещают в охлаждающей рубаип-се калодой сегсцли реактора для измерения температуры циркулирующего охлаж,Еающего агента Ка;-кдая секция реактора снабжена входными отверстиями. Подачу регулируют таким образом, что этиленf хлористый водород к воздух и молекулярный водород поступают в одну любую или во все три секции в жeлae ыx -: пропорциях. Предусмотрена также циркуляция непрореагировав1г его продукта из третьей секции (обогащенная этиленом газовая фаза.) ГС входному отверстию первой секции Обеспечена, возможность смешивать исходные продукты, т.е. хлористый во7го.роД|, воздух или молекулярный кислород и обогащенную этиленом газовую фазу из третьей секции. Отбор проб на входньк и выходных линиях кажлой секции реактора дает .возможность анализировать составы указанных потоков методом газовой хромотографии, Продукт удаляемый из третьей секции, охлаждают в графитовом теплообменнике, охлаждаемом водой,и охлажденный продукт, удаляемый с третьей стадии реакции разделяют в газожидкостном сепараторе на конденсат (содержащий главным образом дихлорэтан и воду) и газовую, фазу. При применении молекулярного кислорода в качестве источника кислорода и избытка этилена по сравнению с стехисметрически необходимым количеством указанная газовая фаза содержит в основном азот. Конденсат поступает в сепаратор, яз которого удаляют дихлорэтан и волУ, которые собирают в барабанах и анализируют с целью получения материального баланса. Газовую фазу из сепаратора возвращают с помощью циркуляционного компрессора в первую секцию реактора.
Реагенты пропускают при давлении выше атмосферного через зону реакции в течение 4-12 час до устойчивой конверсии реагентов (постоянная степень конверсии хлористого водорода). Реакция протекает в зоне реакции по направлению сверху вниз. Три секции реактора расположены в вертикальной
плоскости и поток реагентов проходит со дна первой и второй секций реактора и поступает в верх второй и третьей секции соответственно. Во всех опытам все необходимое для реакции количество этилена (свежего и циркулирующего) подают в первую зону реакции совместно с хлористым
водородом и молекулярным кислородом. Поток в каждую секцию реактора регулируют таким образом, чтобы достигнуть желаемого молярного отной1ения реагентов в реакционной массе.
Б, Катализатор и загрузка катаизатора.
Катализатор оксихлорярованип состоит из смеси 15р5 вес Л- хлористой меди и 1,5 вес.% хлористого кэлия, нанесенной на окись ajiKNUiUHH с размерами частиц от 6.35 до 3,36 мм. 5 Катализатор готовят при пропитке
частиц окиси алюминия 2М полным раствором хлористой меди и хлористого калия в ут азанном весовом отношении. После пропитки в течен-ие 30 мин н стекан 5я избытка растворя частицы
0 катализатора сушат при 288°С в течение 16 час,, а затем при 3 час.
Для создания неподвижного слога катализатора в зоне реакции в трубча5тые секции реактора загружают катализатор или катализатор и инертный разбавитель.В первоп и второй сек. циях применяют разныз пропорции инертного разбавителя. Дня этого
0 частицы катализатора смешивают перед, загрузкой а реактор с разбавителем до получения желательного отношения катализатор:разбавитель. При сравнительных опытах по оксихлорированию
5 испытывают два способа загрузки катализатора, приведенные в табл.1.
Таблица 1






При всех способах загрузки катализатора в третью секцию реактора помещают неподвижный слой, содержащий 100 вес.% катализатора на носителе.
Применяют гравиметрический метод для анализа конденсата из газожидкостного сепаратора, а потоки продуктов анализируют ротаметром.
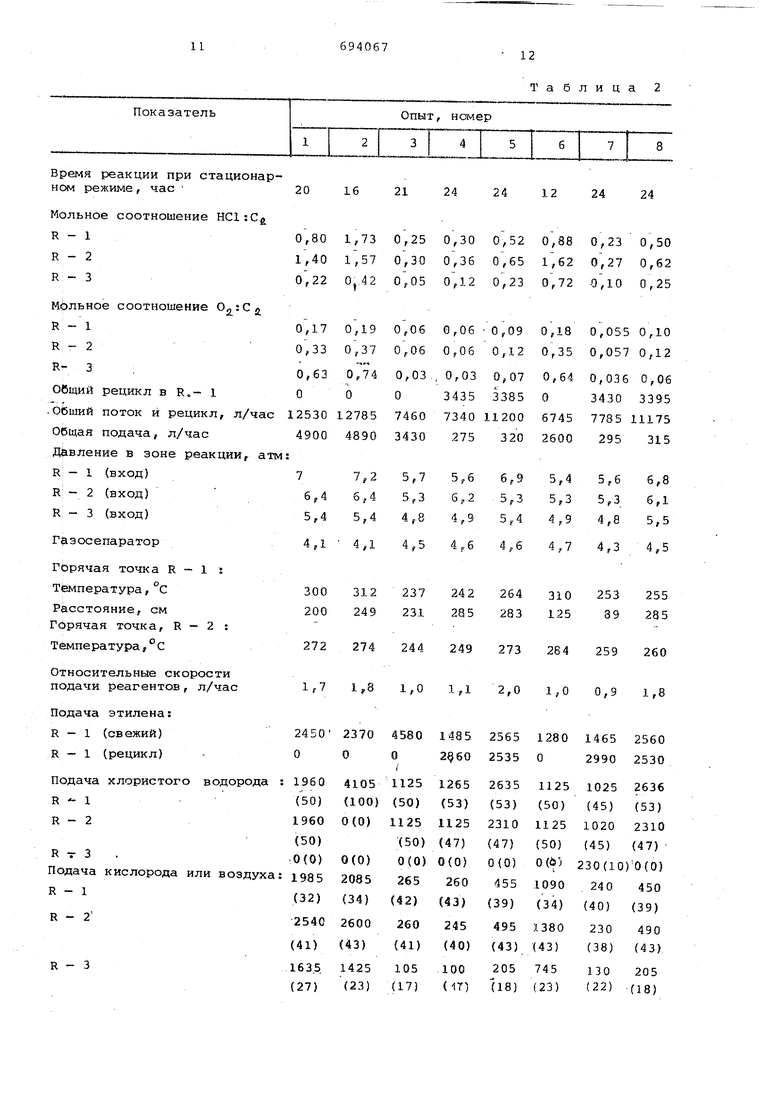
В табл.2 приведены условия полимеризации при 1-ом способе загрузки катализатора. Секции реактора в таблице обозначают следуквдим образом:
55 первая секция - R - 1; вторая секция R - 2 и третья секция R - 3. Используют следующие обозначения компонентов: этилен - С хлористый водород - НС1: кислород - Оо; азот - NjI iQ окись углерода - СО; двуокись углерода - СО; хлористый этил - ХЭ; 1,2-дихлорэтан - ДХЭ; 1,1,1-трихлорэтан ТХЭ; хлористый винил - ХВ.
694067
11
Таблица 2
Состав потока
С
СО
СОц
хэ
ДХЭ
другие
Конверсия хло водорода, %
Селективность водорода, %:
к ДХЭ
Селективность
П-ой способ загрузки катализатора,- носитсл -.ц.нуокдгсь
скобках дан процент НС1 и Оу для разли-f.HL-j; секций.
Преимущество предлагаемого способ заключается в снижении максимальной температуры горячей точки в зоне реакции при любом способе загрузки катализатора по сравнению с температурой этой точки в известном способе При одинаковых примерно скоростях прохождения раагентов температура
горячей точки в предлагаемом способе примерно на ниже чем в известное процессе.
Легкость регулирования температур горячей точки в допустимых пределах в предлагаемом процессе, обусловлена по крайней мере частично, тем фактом, что тег-шература неподвижного слоя повышается медленнее по длине этого слоя, и, по видимому.
1 ,8
99,0 98,7
98,7
98,6 97,6 98,4
о Я . п
98,2
распространяется в более широкой части слоя, чем при известных процессах, в которых в качестве источника кислорода прш 1еняется воздух.
Показана эффектнв;--ость добавления хлористого водорода к реакционной массе в более чем одной точке по длине зоны реакции. П.ри этом увеличивается избирательность этиленгч в отношении образовання дихлорэтана,
Показано, что Б результате почти полной рециркуляции продукта из зоны реакции, происходит лишь незначительное загрязнение атмосферы.
Формула изобретения
Способ получения i,-дихлорэтана путем взаимодействия зтилена, хлористого водорода и молекулярного
кислорода в паровой фазе при темпе- ратуре 230-35БС и давлении 2-10 атм в присутствии неподвижного слоя катализатора - хлористой меди на носителе, с последующим выделением из реакционной массы жидкой фазы, содсрлощей 1,2-дихлорэтан , и газообразной фазы, отличающийся TSMf что, с целью повьпяения эффективности процессаf хлористый водород и молекулярный кислород подают порциями по всей реакционной зоне, при
поддержании молярного соотношения хлористого водорода и этилена 0,050,7:.1 и кислорода и этилена 0,02 0,12;.1, а газообразную фазу рециркулируют в процесс.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1979-10-25—Публикация
1973-12-18—Подача