Предлагаемое изобретение относит ся к области эпоксидных композиций йа основе ц-иклоалифатйческих эпоксидных соединений (ЦАЭС), содержащих эпоксидированяый циклоалифатический активный, разбавитель и рекомендуемых для использования в качестве заливочных и пропиточных компаундов электротехнического назначения клеёв,- связующих для армированных пластиков.
ЦАЭС обладает рядом технически
важных свойств, которые обусловливают их широкое применение в рйДё отраслей народного хозяйства.
Известна композиция, содержащая циклоалифатическую эпоксидную смолу и ангидридный отвердитель 1.
К недостаткам композиции на основе наиболее теплостойкого 3,4-эпоксигексагидробензаЛь-з,4 бис(гидррксиметил)циклогексана зачастую относят высокую вязкость.
Полимеры на его основе имеют высокие диэлектрические свойства, теплостойкость, но повышенную хрупкость,
. Повышенная вязкость композиций на основе 3,4-эпоксигексагидробензаль-3, 4-эпокси-1, l бис(гидроксиметил)циклогексана (УП-612) обуслов0лена повышенной вязкостью самого диэпоксида.
Например, вязкость УП-612 пр.и 40°С составляет 6000-10000 сП, вяз5кость его зарубежного аналога СУ-175 при составляет 125000150000 сП.
Физико-механические свойства диэпоксида УП-612 при отверждении ан0гидридными отВердителями приведены ниже.





| название | год | авторы | номер документа |
|---|---|---|---|
| Полимерная композиция | 1976 |
|
SU653276A1 |
| Полимерная композиция | 1977 |
|
SU690044A1 |
| Клей | 1978 |
|
SU785336A1 |
| Алифатически-циклоалифатические диэпоксидные соединения в качестве разбавителей эпоксидных смол | 1978 |
|
SU789522A1 |
| Стеклопластик | 1972 |
|
SU456746A1 |
| 3,4-Эпоксигексагидробензиловые эфиры ди /3,4-эпоксигексагидробензоил/ резорциловой кислоты в качестве мономера высокопрочных термостойких эпоксиполимеров | 1976 |
|
SU667554A1 |
| Эпоксидная композиция | 1977 |
|
SU749868A1 |
| Глицидные эфиры эпоксициклоалкил3,4-эпоксигексагидрофталатов для высокопрочных теплостойких эпоксиполимеров | 1974 |
|
SU525682A1 |
| Эпоксидная композиция | 1977 |
|
SU781205A1 |
| Бис-(3,4-эпоксициклогексилметиловые) эфиры 1,3-адамантанкарбоновой кислоты в качестве мономеров для высокопрочных теплостойких эпоксиполимеров | 1976 |
|
SU598896A1 |

Предел прочности, кгс/см ;
при изгибе700 820
при сжатии1770 1880
Теплостойкость no су, С
Ч
e -. ; .
f, Ом-CM
Ангидрид метилтетрагидрофталевой кислоты. VF -V.
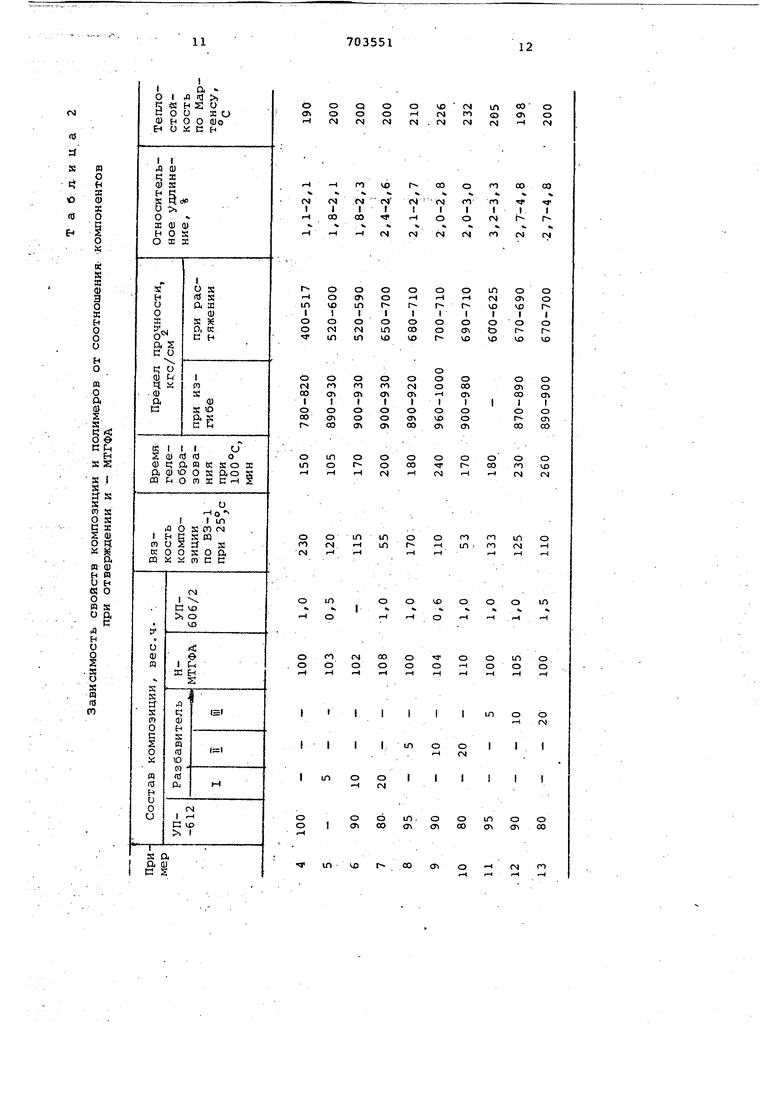
Для улучшения технологических свойств композиций совмещают УП-612 с эпоксидиановыми смолами (ЭД-16) или низковяэкими диэпоксидными соЖизнеспособность компЬзй- .
ции при 80°с ;
Теплостойкостьпо Мартен-
су, ,
г Предел прочности, кгс/см ;
при изгибе
при растяжении
при сжатии бтносительнЬе удлинение, Диэлектрические свойства при моди фикации УП-6 12 не изменяются и остайтся достаточно высокими. Вышеприведенные данные свидетельствуют , что модификация УП-б 12 §поксй ановыми и циклоалифатйчёскиШ смолами приводит к снижений теплОсФойкости полимеров практически не иэменяе 1 технологических свойств йойпозиции и физико-механических свойств полимеров на их основе. Целёсооб1райй6сть такой модификаций может бать оправдана из экономических сбображёнйй, -Ik; диеновые смолы дешевле циклоапифатических. Известен ряд моноэпоксидных разба вителей эпо ссидных смол (2 и 3, в т.ч. алифатических и циклоалифатичёских: окиси олефинов фёнилглйЦйДи220
0,0167 3,3
16
1,6-10
единениями - УП-632. Свойства получаемых при этом полимеров приведены ниже (при отверждении УП-581) . Эвтектическая смесь эндик ангиДрида с адДуктом малёинового ангидрида и антрацена. ловый и бутилглицидный эфиры, глицидилметакрилат, эллилглицидный эфир, моноокись дипентеца, окись оС-пинена, моноокись лимонена и т.д. Монозпоксидные разбавители, понижая функциональность системы и плотность сшивок, приводят к снижению теплостойкости полимеров. Незначительное увеличение прочности при этом является недостаточной компенсацией. -- -. Причиной резкого снижения теплоСТОЙКОСТИ является ТО,ЧТО МОНОЭТТОКсиДйые соединения, являясь по сути агентом обрыва цепи при отверждении, не способны образовывать пространственно сшитые структуры, т.е. после взаимодействия с отвердителем они образуют низкомолекулярныё жидкие продукты, являющиеся фактически Пластификаторами, способными зачаст йыпотевать из полимера в процессе эго эксплуатации 4. Поскольку для диэпоксида УП-612 моноэпоксидные разбавители применяют впервые, в качестве прототипа выбрана композиция на основе УП-б12 не содержащая модификаторов l . При введении известных модификаторов теплостойкость, как правило, снижается. Решение проблемы создания теплостойких полимеров чрезвычайно актуально. Однако теплостокие материалы при недостаточной технологичности композиций,, высокой хрупкЬсти и низ кой прочности полимеров на их основе не могут быть использованы в про мышлённо важных отраслях. Целью изобретения является сниже ние вязкости композиций на основе диэпоксида УП-612, при одновременно повышении прочности и эластичности полимеров, а также сохранении высокой теплостойкости. Цель достигается тем, что эпокси нал композиция, содержащая диэпоксид УП-612 и ангидрид изометилтетра гидрофталевой кислоты дополнительно содержит трис{диметиламин6ме тил) фенол и активный разбавитель, выбранный из группы, включающей 3,4-эпоксигексагидробензальоксиэтан, метил-3,4-эпоксигексагидробензоат, 3,4-эпоксициклогексан-1,1 бис(оксиметил)метан при следующем соотношении компонентов, вес.ч.: 3,4-зпоксигексагидробензаль-З, 4- (эпокси-1,1-бис)гидроксиметил/циклогексан80-100Активный разбавитель5-20Ангидрид изо-метилтетрагидрофталевойкислоты 100-110 Фрис(диметиламинометил)фенол ,5. Приготовлен ие композиции при использовании предлагаемого сочетания компонентов заключается в совмещени и.гомогенизации их смеси при ступен чатом повышении температуры от 100 до 180°С.. Примерами 1-3 демонстрируются методики синтеза используемых моноэпоксидных разбавителей. Примерами 4-13 демонстрируется зависимостьсвойств получаемых полимеров от соотношения компонентов Примерами 14-17 подтверждается увеличение адгезионных характеристи композиции в клеевом соединении. Пример 1. 3,4-эпоксициклО гексан-1,1-бис(оксиметил)-метан (оазбавитель 1). Смесь 80 вес.ч. (0,56 моля) 1,1-бис(оксиметил)циклогексена-3 и 45,7 вес.ч, (0,56 моля) 37%-го раствора формальдегида в 300 мл бензола в присутствии каталитических количеств NaHSO4 нагревают до кипения с насадкой Дина и Старка до прекращения выделения воды. После нейтрализации катализатора растворитель отгоняют, а продукт перегоняют под. вакуумом. Получают 114 вес.ч. (92,6%) циклоацеталя с т.ип. 85°С/5 мм рт.ст. и йодным числом 163 г 3/100 г. ; Вычислено: для О2иодное;.. число 165 г И /100 г. Полученный циклоацеталь растворяют в 300 мл бензола и эпоксидируют 168 вес.ч. 42%-ной надуксусной кислоты Б присутствии 16,8 вес.ч. ацетата натрия при температуре ЗО-ЗБ С с последующей выдержкой при этой температуре в течение 2,5 часов. Нижний слой сливают, а органический промывают 10%-ным раствором NaOH до рН , а затем - водой до рН 7. Растворитель отгоняют, а полученный продукт разгоняют в вакууме. Получают 118 вес.ч, (93,5%) эпоксиацеталя с т.кип. 108°С/мм рт.ст. Найдено; эпоксидное число 24,8%; П 1,4902; d 1,1764 41,83. . , Вычислено для СпК.,О„: эп.число 25,3%; 42,64. В ИК-спектрах не обнаружены частоты поглощения двойной связи (1600-1670 см) и частоты карбонильного поглощения (1730-1750 см ) и обнаружены полосы средней интенсивности в области, характерной .для ,л эпоксидных групп (800-820 см). Отсутствие в ИК-спектрах; эпоксициклоацеталя частот карбонильного поглощения и частот в области 34003700 см , характерных для свободных ОН групп, подтверждает, что при эпоксида1ровании не происходит размыкание эпоксидного кольца. Пример 2. Метил-3,4-эпок ;сигексагидробензоат (разбавитель И), К смеси 63 вес.ч. (0,5 моля) тетрагидробензойной кислоты и 80 вес.ч. (2,5 Моля) метанола при перемешивании прикапывают 37 вес.ч. концентрированной серной кислоты, затем воронку заменяют обратным холодильником и содержимое колбы кипятят в течение 6 часов. Избыток метанола отгоняют, а содержимое колбы вртряхивают в делительной воронке с водой и дают отстоя.ться. Верхний слой промывают водой, насыщенным раствором соды до рН 7 и снова водой до рН 7. Продукт разгоняют в вакууме. Получают 65 вес.ч. (91,5%) эфира с т.кип. 55-60°С/5 мм рт.ст.
найдено: йодное число - 180 г
3/100 г . число омыления 397 мг/г.
Вычислено для иодноа число 182 г а/100 г число омыления - 400 мг/г.
Полученный эфир растворяют в 200 мл бензола и эпоксндируют 143 вес.ч. 40%-ной надуксусвой кислоты в присутствии 14,3 вес.ч. ацетата натрия в условиях примера 1. Растворитель отгоняют, а полученны продукт разгоняет в вакууме. Получают 66,2 вес.ч. (93%) эпоксида с т.кип. 88-90°С/5 мм рт.ст.
2 Найдено; по|о „1,4640 d4. 1,1279 Г/СМ; эп.число 26,9%
38,23.
М
ТО Вычислено для эп.число
27,6%; MRT, 38,58,
Строение полученного соединения подтверждается анализом ИК-спектров В спектре обнаружены частоты поглощения в области 800-820 см , характерные для эпоксидных групп, а также дублетная полоса в области 17001780 , характеризующая наличие саюжно&фирной группы и отсутствуют полосы поглощения при 1654 см , подтверждающие отсутствие двойной связи.
Сравнительная характеристика полимеров
Вязкость композиции по ВЗ-1 при 25С, с
Время гелеобразования композиции при 100°С, мин
Теплостойкость по Мартенсу, ос
. 2
Предел прочности, кгс/см ;
при изгибе
при растяжении
Относительное удлинение, %
ПрочносгS клеейогб соединения СтЗ/СтЗ при сдвиге, кгс/см i Пример 3. 3,4-э.поксигексагидробензальоксиэтан (разбавитель jn)
110 вес.ч. (1 моль) тетрагидробензальдегида и 62 вес.ч. (1 моль) этИленгликоля в 400 мл бензола в присутствии каталитических количеств ЫаНЗОд. кипятят с насадкой Дина и Старка до прекращения выделения воды После нейтрализации катализатора растворитель отгоняют под вакуумом. Получают 148 вес.ч. (96%) циклоацеталя с т.кип. 76°С/5 мм рт.ст. И йодном числе 163 г 3/100 г.
Вычислено для ,. йодное число 165 г а/100 г.
148 вес.ч. (0,96 моля) циклоацеталя растворяют в 450 мл бензола и эпоксидируют 202 вес.ч. 45%-ной надуксусной кислоты в присутствии 20,2 вес.ч. ацетата натрия в условиях примера 1.
После соответствующей обработки и перегонки под вакуумом получают 156 вес.ч. (96,2%) продукта с т.кип. 125°С/6 мм рт.ст.
Найдено: эпоксидное число 24,9% п 1,4810; d4° 1,1539; , 41,98
Вычислено для эпоксидное число 25,3%; М 42,64.
В инфракрасных спектрах наблюдается серия полос в области 800820 см , характерных для эпоксидных групп и отсутствуют полосы поглощения, характерные для свободных гидроксильных групп, карбонильных групп и частоты поглощения двойной связи. Таблица
53
110
55
260
170
200
230200
210
900-930 900-980 890-900 650-700 690-710 670-700
1,0 2,4-2,6 2,0-3,0 2,7-4,8
По данным авторов.
Данные таблицы 1 свидетельствуют, что применение разбавителей снижает вязкость композиции в 2-4 раза, не изменяет теплостойкости по: 1имеров и увеличивает прочность при изгибе на 12%, при растяжении в 1,4 раза, относительное удлинение з 2,4-4,8 раза, что и представляет технический эффект изобретения.
Применение разбавителей увеличивает жизнеспособность композиций, что положительно сказывается при изготовлении армированных пластиков.
В качестве отвердителей использо703551
10 Продолжение таблицы
вание ангидридов гидроароматических дикарбоновых кислот является предпочтительным по сравнению с аромати20 чёскими ангидридами.
Поскольку свойства полимеров, получаемых в соответствии с описанием изобретения, в большей степени определяется соотношениями диэпоксида
25 УП-612 и моноэпоксидного разбавителя чем видом ангидридного отвердителя, ниже приводятся свойства полимеров, полученных при использовании только ;ангидрида изо-метилтетрагидрофтале30 вой кислоты (МТГФА).
о О1Л1Л о о ГП 01 щ о 1 (N - 1ЛГ -I in 1 СЧ -i ,н,-I
О 1Л
кВь
О
o ; Nooo-4ooino
о ООО о о -н OQ о
II I I л о о
I 1Ло оIIIII
о I ))
о
«т 1Л UJ 1 00 СГ| о - (N П
о о VD О О О 1Л
гН -Но - . -I
I1Л о о
I I
..i-l ГМ
-I (N
о о 1Я . о о 1Л о о
13
Зависимость прочности клеевых соединений от соотношения компонентов
703551j 4
Таблица 3
Авторы
Даты
1979-12-15—Публикация
1977-08-29—Подача