Изобретение относится к области аналитической химии и может быть использовано при анализе любых объектов, содержащих железо и ванадий: ферритов, феррованадия, руд и концентратов.
Известно амперометрическое последовательное определение железа и ванадия из одного раствора 1.
Однако точность этого метода не. удовлетворительна.
Наиболее близким к изобретению техническим решением является способ кулонометрического титрования электрогенерированяыми ионами Ti (III) 2. По этому способу проводят титрование железа и ванадия ионами Ti (III), генерированными в растворе электролита 7М по . и 0, 4М по TiCE на Pt электроде, и получают два перегиба на кривой титрования. Первый перегиб соответствует восстановлению V(V) до V(IY), а второй сумме восстановления V(IY) до V(III) и Fe (III) до Fe(II) . Содержание железа в этом случае определяют по разности.
Однако такой способ проведения анализа дает большие О1иибки определения железа и ванадия: t 0,44% для железа и 0,23. для ванадия.
Це.пью изобретения является повышение точности метода определения железа и ванадия и упрощение способа
Цель достигается тем, что по предлагаемому способу в качестве титранта используют электрогенерированные ионы Си (I).
Были исследованы окислительновосстановитйльные потенциалы ионных пар V(V)/V(IV), Fe (III)/Fe (dl) и Си (II)/Си (I) в среде 0,15М по НС.. 0,36М по HgSO и 0,ОШ по СиЗОд и обнаружено, что EvtY)/v(v) 0,675 В FeuIOlFe(u) 0,478 В и си.1 1Сиа 0,200 В против хлорсеребряного электрода. Из сравнения этих потенциалов видно, что ионы Си (I) будут восстанавливать ионы V(V) только до V{IV), так как стандартный электродный потенциал пары V(IV)/V(III) против хлор-серебряного электрода равен 0,047 В. Таким образом возможно последовательное титрование ионов V(V) до V(VI),a зат Fe(lIT) до Ре(II) в одном растворе электрогенерированньи.1и ионами Cu(I). Так как выход по току ионов Cu(I) в среде 0,15М по ЯСС, 0,36М по H2S04 и 0,-OlM по CuSO равен 100%, то такой способ.последовательного титрования ионов V(V) и Fe(III), наряду с
простотой и быстротой проведения анализа, обладает высокой точностью.
Разработанный способ определения железа и ванадия был применен для анализа ферритов различного состава. Навеску феррита, содержащую 240 мг переводили в раствор сплавлением с пиросульфатом калия. Сплав растворяли в воде с добавлением 20 мл концентрированной серноП кислоты и переводили раствор в мерную колбу вместимостью 200 мл. Аликвотную часть раствора 20 мл помещали в ячейку для титрования и прибавляли 0,03 п. раствор перманганата калия для окисления Fe(II) и V(IV) до появления розовой окраски раствора. Избыток перманганата восстанавливали 0,5%-ным раствором нитрита натрия, а из быток нитрита натрия связывали 0,2 г мочевины. Затем в ячейку прибавляли 100 мл раствора 0,2 М по нес и 0,01 М по CuSO и проводили кулонометрическое титрование. В качестве источника тока использовали потёнциостат П-5827М, время измеряли электросекундомером П14-2М. Генераторным рабочим электродомслужила платиновая фольга размером 9x4 см (катод), вспомогательным - серебряная спираль (анод). Конечную точку титрования устанавливали потенциометрическим методом с платиновым индикаторным электродом
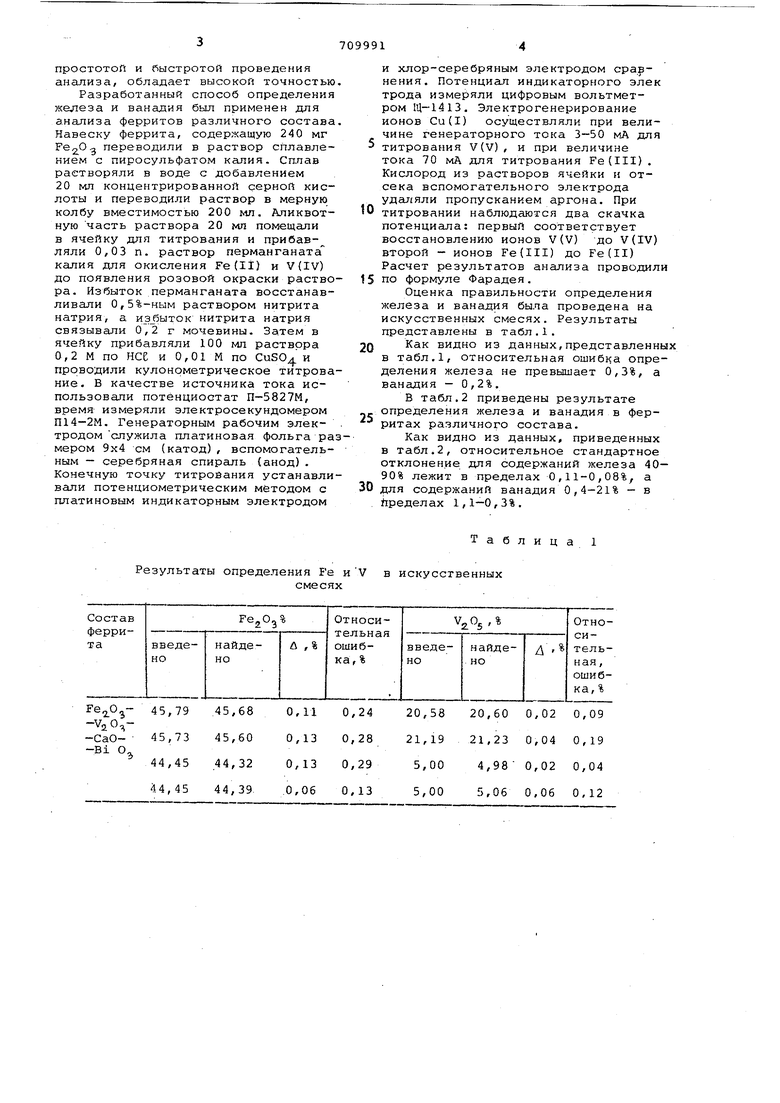
Результаты определения Fe иV в искусственных
смесях
и хлор-серебряным электродом срарнения. Потенциал индикаторного элек трода измеЕ: яли цифровым вольтметром Щ-1413. Электрогенерирование ионов Cu(I) осуществляли при величине генераторного тока 3-50 мА для 5 титрования V(V), и при величине тока 70 мА для титрования Fe(III) . Кислород из растворов ячейки и отсека вспомогательного электрода удаляли пропусканием аргона. При
титровании наблюдаются два скачка потенциала: первый соответствует восстановлению ионов V(V) до V(IV) второй - ионов Fe(III) до Fe(II) Расчет результатов анализа проводили
5 по формуле Фарадея.
Оценка правильности определения железа и ванадия была проведена на искусственных смесях. Результаты представлены в табл.1.
0 Как видно из данных,представленных в табл.1, относительная ошибка определения железа не превышает 0,3%, а ванадия - 0,2%.
В табл.2 приведены результате определения железа и ванадия в ферритах различного состава.
Как видно из данных, приведенных в , относительное стандартное отклонение для содержаний железа 40- 90% лежит в пределах 0,11-0,08%, а
0 для содержаний ванадия 0,4-21% - в пределах 1,1-0,3%.
Таблица 1
Результаты определения железа и ванадия в ферритах
Таблица

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ кулонометрического амперостатического определения ванадия | 1979 |
|
SU856993A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕХНЕЦИЯ | 1997 |
|
RU2132552C1 |
| Способ кулонометрического определения галогенидов | 1982 |
|
SU1057837A1 |
| СПОСОБ КУЛОНОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ АСКОРБИНОВОЙ КИСЛОТЫ В РАСТИТЕЛЬНОМ СЫРЬЕ И ПРЕПАРАТАХ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2010 |
|
RU2464558C2 |
| Способ индикации точки эквивалентности в кулонометрическом анализе | 1980 |
|
SU934343A1 |
| Кулонометрический способ определения гидразида дифенилфосфинилуксусной кислоты | 1990 |
|
SU1704055A1 |
| Способ потенциометрического определения мо | 1976 |
|
SU693218A1 |
| Способ кулонометрического определения рения | 1990 |
|
SU1749818A1 |
| СПОСОБ КУЛОНОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ОРГАНИЧЕСКИХ КИСЛОТ В РАСТИТЕЛЬНОМ СЫРЬЕ И ИХ ПРЕПАРАТАХ | 2010 |
|
RU2450265C2 |
| СПОСОБ ПОТЕНЦИОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ ЕМКОСТИ РАСТВОРА | 2019 |
|
RU2711410C1 |

Fe.O..-BiO,-СаО
«С 5 J
Э О -ВЮ -СаОТочность определения железа и ванадия по предлагаемому способу в 23 раза выше, чем по известным способам, что особенно важно для анализа прецезионных марок ферритов, весьма чувствительных к изменению состава. Кроме того, благодаря отсутствию подготовительных операций перед титрованием (отделение ванадия от железа, восстановление V(V) и Fa(III) предлагаемый способ является простым и быстрым. Внедрение предлагаемого способа в технологию изготовления ферритов с целью корректировки их состава позволит повысить стабильность технологического процесса и увеличить процент выхода годных изделий .
8 0,051 0,104
45,90 0,055 0,26
20,80
Формула изобретения
Кулонометрический способ определения содержания железа и ванадия из одного раствора путем титрования электрогенерированными ионами, о тличающийся тем, что, с целью повышения точности определения и упрощения способа, в качестве титранта используют электрогенерированные ионы Си(I).
Источники И 1формации, принятые во внимание при экспертизе
2,F, Cuta, зеп chni Jii Revue de chimle, 7 1 1, p, 127, 1962,
Авторы
Даты
1980-01-15—Публикация
1978-02-07—Подача