соотношении исходных реагентов
,lSl-l l,2.
в качестве растворителя использую например,диметилформамид, диметилацетамтд, N-метилпирролидон, гексаметилтриамид фосфорной кислоты в количестве 50-100 мл на 0,1 моля исходного хлорангидрида, Изменение в соотношении исходных продуктов (от 1:1 до 1;2 и 2;1) не приводит к повышению качества. Уменьшение количества растворителя нецелесообразно из-за у.веЛ«чения продолжительности реакции вслествие гетерогенности и понижения качества продуктов, увеличение расхода растворителя ведет к снижению выхода При температуре ниже 120с реакция сильно замедляется, верхний предел ограничен температурами кипения растворителей и возможностью протекания побочных реакций. Без охлаждения реакционной массы после проведения реакции выход конечного п зодукта уменьшается, нижний предел охлаждения ограничен температурой замерзания растворителя и относительно малой зависимостью растворимости конечных продуктов от температуры при температуре ниже .
Предлагаемый способ позволяет получать чистые продукты непосредственно из реакционной смеси с высокой температурой плавления, в то время Как в известных способах аналогичные или более низкие точки плавления целевых соединений получают только после дополнительной их очистки.
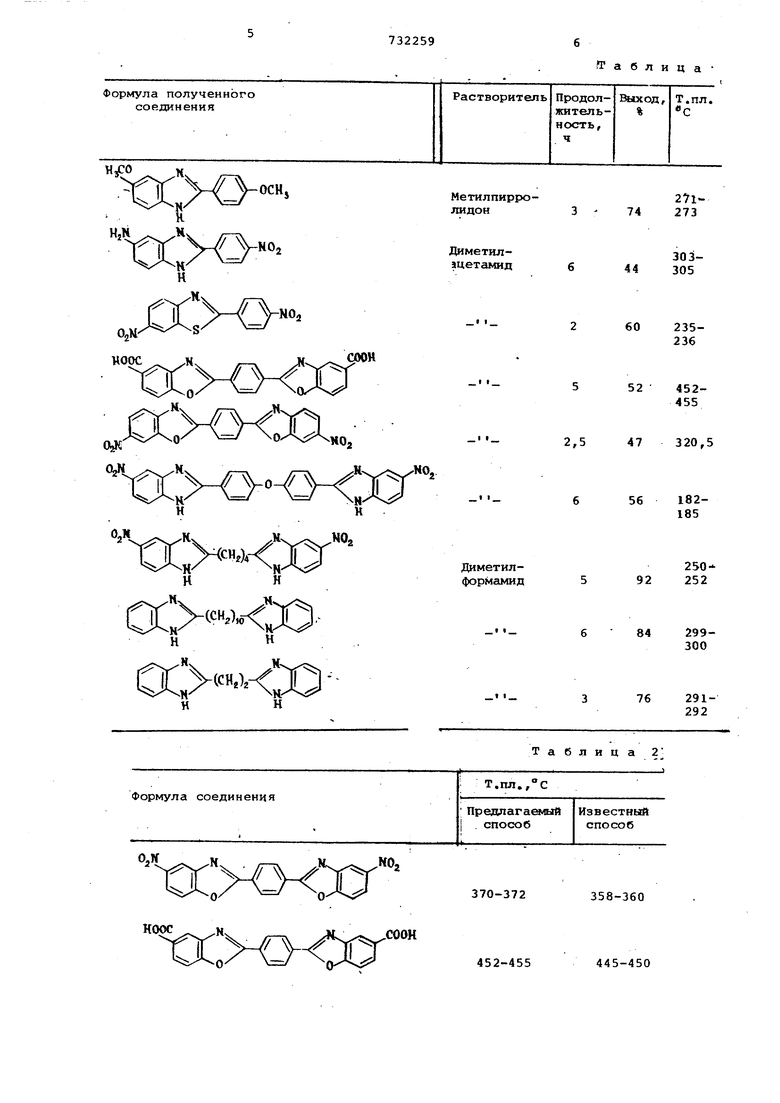
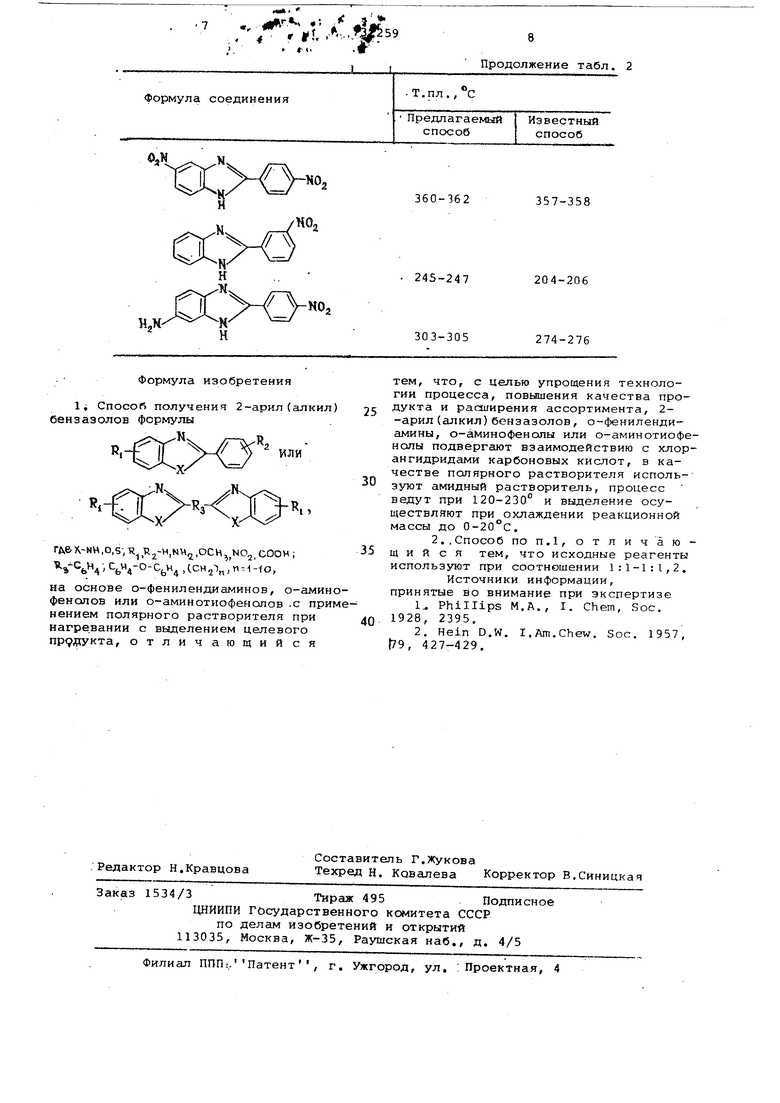
В табл.1 и в примерах представлены некоторые продукты, полученные по предлагаемому способу. В табл.2 представлены сравнительные данные по чистоте продуктов по предлагаемому способу прямо из реакционной смеси и аналогичных продуктов, полученных известными способами с последующей очисткой,например,перекристаллизацие
Из табл.2 можно сделать вывоДг что полученные по предлагаемому способу соединения по чистоте не только не уступают,но и превосходят аналогичные соединения, полученные известными способами.
Пример 1. Получение 6-нитро2-(п-нитрофенил) бензоксазола. При охлаждении растворйют 20 г (0,122 моль) 2-амино, 5-нитрофенапа в 100 мл диметилацетамида. В полученный раствор загружают 25 г (0,135 моль) п-нитробензоилхлорида. Охлаждение снимают, реакционную массу нагревают до кипения. Полученный раствор кипятят в течение 5 ч.
(Выпавший при охлаждении до осадок отфильтровывают, промывают водой и сушат.
Получают 20,9 г (60%) 6-нитро, г 2-(п-нитрофенил)бензоксазола, т.пл. 214-215С.
Найдено, %: N 14,9. С о H-jNjOj
Вычислено, % N 14,7.,
2. Получение 2,,4-фенилен(бис)-5-нитробензоксазола. В 100 мл диметилформамида растворяют 20 г (0,122 моля) 2-гилино, 4-нитрофенола и при перемешивании загружают V . 13,7 г (0,068 моля) терефталоилхлорида, 5 Реакционную массу нагревают до кипения в течение 6ч. Выпавший при охлаждении до осадок отфильтровывают, промывгиот водой и сушат.
Получают 21,5 г (76%) 2,,40 -фенилен(бис)-5-нитробензоксазола1, т.пл. 370-372° .
Найдено, %: N 13,9.
20 iD 4°6Вычислено, %: N 14,0.
Пример 3. Получение 2-(т-нитрофенил)-бензимидазола. В 50 мп .диметилацетамида растворяют 10,8 г (0,1 моля) -фен илендиамина, при
переменивании и охлаждении до
прибавляют 18,6 г (0,1 моля) т-нитробензоилхлорида, после.чего реакционную массу греют при 120с 8 ч, охлаждают до и отфильтровывают. Осадок промывают водой, сушат.
Получают 16,3 г (78%) 2-(т-нитрофенил)бензимидазола с т.пл. 204-206 Найдено, %: N 14,4. , N,0,, Вычислено, %: N 17,0.
Пример4. Получение 5-литро-2-(п-нитрофенил)бензимидазола. В 50 мл гексаметилтриамида фосфорной кислоты растворяют 15,3 г (0,1 моля) 4-нитро-о-фенилендиамина, при охлаждении добавляют 18,6г(0,1 моля) п-нитробензоилхлорида, после чего реакционную массу нагревают до кипения (232°С) 1 ч, охлаждают, отфильтровывают вьлпавший осадок, промывают растворителем и водой,
сушат.
Получают 22,5 г (80%) 5-нитро, 2-(п-нитрофенил)бензимидазола, т.пл. 360-362.
Найдено, %: N 19,7. С, HgNjO.. Вычислено, %: N 19,8.
(Таблица

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 4-теноил-0-фенилендиамина | 1981 |
|
SU1004383A1 |
| Аминооксипроизводные 2-фенилбензимидазола как мономеры для получения полиэфирамидов | 1974 |
|
SU510474A1 |
| 2-(П-аминофенил)-5-нитробензимидазол как промежуточный продукт для синтеза мономеров | 1977 |
|
SU749834A1 |
| 2-(П-Толуолсульфонил)-1,2,3,4-тетрагидропиразино(1,2-а)-бензимидазол в качестве промежуточного продукта в синтезе 2-замещенных 1,2,3,4-тетрагидропиразино(1,2-а)-бензимидазолов, обладающих биологической активностью | 1987 |
|
SU1502572A1 |
| Способ получения производных тиазолинилкетобензимидазола | 1976 |
|
SU645578A3 |
| СПОСОБ ПОЛУЧЕНИЯ 5(6)-АМИНО-2(4'-АМИНОФЕНИЛ)-БЕНЗИМИДАЗОЛА | 2005 |
|
RU2283307C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(п-АМИНОФЕНИЛ)-6-АМИНО-4H-3,1-БЕНЗОКСАЗИНОНА-4 | 1999 |
|
RU2161611C1 |
| Способ получения проивзодных бензимидазола или их солей | 1975 |
|
SU581866A3 |
| ПРОИЗВОДНОЕ БЕНЗИМИДАЗОЛА, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ И СПОСОБ МОДУЛЯЦИИ ГАМК-РЕЦЕПТОРНОГО КОМПЛЕКСА | 1996 |
|
RU2135493C1 |
| Способ получения диметилового эфира 1,4-дигидро-2,6-диметил-4-/2-нитрофенил/-пиридин-3,5-дикарбоновой кислоты | 1989 |
|
SU1766254A3 |

370-372
358-360
НООС
соон
445-450
452-455
360-362
357-358
245-247
204-206
303-305
274-276 . Формула изобретения 1; Способ получения 2-арил(ал бензазолов формулы где Х-КН ,0,5, R R..,-H,NM,j ., СООИ ; ,ССН2,ПН-(0, на основе о-фенилендиаминов, о-а фенолов или о-аминотиофенолов .с нением полярного растворителя пр нагревании с выделением целевого пр9ДУКта, отличающийс тем, что, с целью упрощения технологии процесса, повышения качества продукта и расширения ассортимента, 2-арил(алкил)бенэазолов, о-фенилендиамины, о-аминофенолы или о-аминотиофенолы подвергают взаимодействию с хлорангидридами карбоновых кислот, в качестве полярного растворителя используют амидный растворитель, процесс ведут при 120-230° и выделение осуществляют при охлаждении реакционной массы до 0-20с. 2..Способ non.l, отличающийся тем, что исходные реагенты используют при соотношении 1:1-1:1,2. Источники информации, принятые во внимание при экспертизе 1 Phillips М.А., I. Chem, Soc. 1928, 2395, 2. Hein D.W. I.Am,Chew. Soc. 1957, f79, 427-429,
Авторы
Даты
1980-05-05—Публикация
1977-06-28—Подача