(54) 2-(п-АМИНОФЕНИЛ)-5-НИТРОБЕНЗИМИДАЗОЛ КАК ПРОМЕЖУТОЧНЫЙ ПРОДУКТ ДЛЯ СИНТЕЗА Изобретение относится к новому соединению, а именно к 2-(п-аминофенил)-5-нитробензимидазолу формулы У который является промежуточным продуктом в синтезе мономеров, . 10 МОНОМЕРОВ мер 5(6)-амино-2 (п-аминофенил) бенэимидазола, 5-амино-2(п-оксифенил) бензимидазола, находящих применение для получения термостойких волокон и полиэфироамидов. Известен способ Tl} получения амидов 5(6) ё1мин6 - 2 (п-аминофенил) бензимидазола формулы
5-г№1ино-2-(п-оксифенил)-бензимидазол по известному способу получают 25 ацилированием о-нитроанилинов соответствующими хлорангидридами ароматических карбоновых кислот, восстановлением полученных нитроанилидов. путем каталитического гидрированияг ЗО
циклизацией аа;ия-о-5 енилендиаминов в присутствии минеральных кислот и диметилированием эмино-метокси-2-фенилбензикюдазЬлов бромистоводородной кислотой 2l.
Цель изобретения - получение нового промежуточного продукта, позволякадёго волее Простым способом Получать мономеры высокой степени чистоты.
Это достигается 2-(п-аА1ииофенил)-5-нитробензймидазс лом указйннбй формулы, получаемом циклизацией о-фенилендиамина, н-аминобензойной кйЬлотой в полйфрсфорной кислоте .с пос745 834
ледующим нитрованием полученного 2 Сп-аминофенил)-бензимидазола в 70 85% серной кислоте при О - 5®С.
Синтез 5(б)-аминЬ-2 (п-аминофенил) -бензимидазола с использованием заявляемого соединения происходит по
следующей схеме: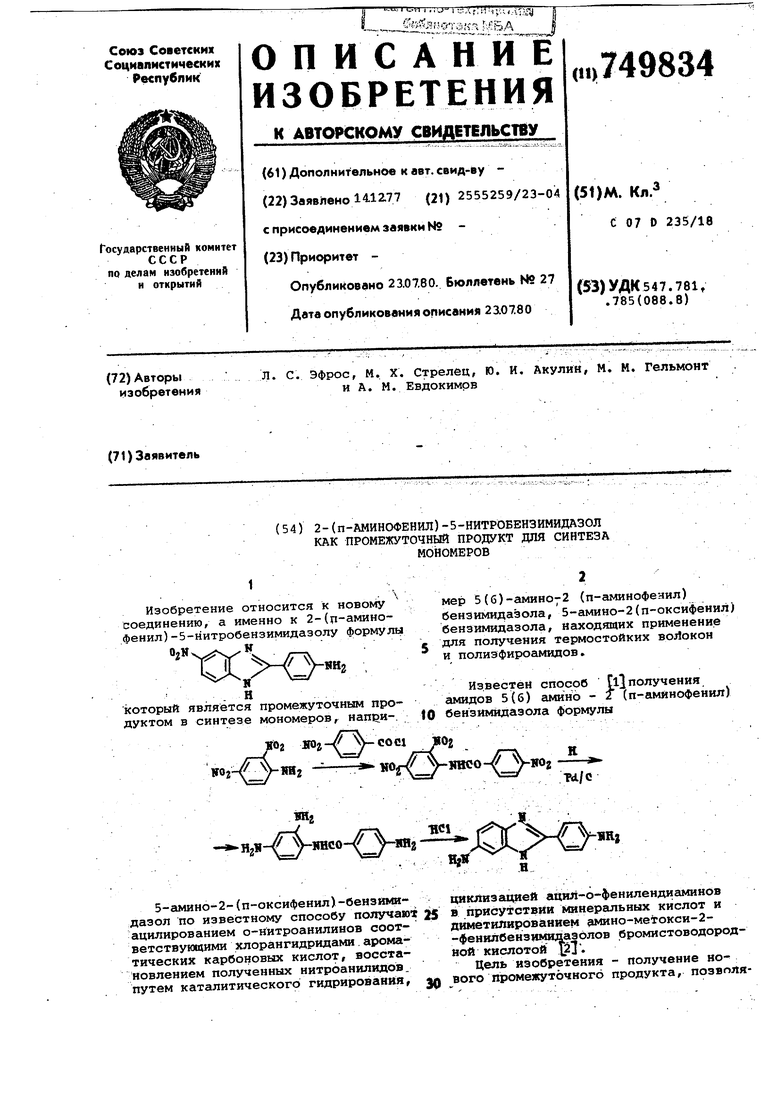


| название | год | авторы | номер документа |
|---|---|---|---|
| Аминооксипроизводные 2-фенилбензимидазола как мономеры для получения полиэфирамидов | 1974 |
|
SU510474A1 |
| Способ получения полибензимидазолохиназолинов | 1977 |
|
SU734224A1 |
| Способ получения проивзодных бензимидазола или их солей | 1975 |
|
SU581866A3 |
| Способ получения производных бензимидазола | 1971 |
|
SU472504A3 |
| ПРОИЗВОДНЫЕ 5-АМИНО-2-(N-АМИНОФЕНИЛ)БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ МОНОМЕРОВ ДЛЯ СИНТЕЗА ВЫСОКОПРОЧНЫХ ТЕРМОСТОЙКИХ АНИОНООБМЕННЫХ ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 1992 |
|
RU2074182C1 |
| Способ получения карбонилзамещенных 1-сульфонилбензимидазолов | 1977 |
|
SU685151A3 |
| Способ получения производных имидазола или их кислотно-аддитивных солей | 1983 |
|
SU1316559A3 |
| Способ получения оксипроизводных 2-арилбензазолов | 1976 |
|
SU600138A1 |
| Способ получения сульфонилбензимидазолов | 1975 |
|
SU786892A3 |
| Способ получения производных тиазолинилкетобензимидазола | 1976 |
|
SU645578A3 |

Предлагаемый способ пб лучеййяамииофенилнитробензимидаао,па позволяет 20 получать без Дополнительной перекриста ллизаций продукт высокой степени чистоты без примеси изомере, ;
Заявляемое аминонитропройзводное легко превращается в мономер 5(6)- 25 -амино-2(п-аминофенил) бензимидазол известным способом-катадитическим босстановлением (Pd/C) водородом од атмосферным давлением в среде Органического растворители, н апример л иметилформамиде и спирте с выходом 94%, т. пл. 234-235.
П реимущество заживляемого промежутрчнбгб продукта при сийтёэё данного Шомёра .состоит: во-первых, в йс- ,е пользовании менее дефицитйых о-фенилендиамина в .сравнении с 2,4-дййитроанилином, так как о-фенилендиамин получается восстановлением о-нитроаниЛииа, который образуется в качестве поббчйбгб продукта при нитровании 40 анйяина наряду с.П-нитроанйлином, назГодящим гораздо боЯёёШйрШбе применение в органическом синтеза} вовторых, в возможнрсти синтеза 2-(п-аминофенил)-5-йитробензимидазола без йримеси изомеров в-третьих, в сзущественно большем йьосоде, на стадиях 2-3-96 ,и 94% против 90 и 91% пи известному способу. Что касаетс (Синтеза другого мономера-5-аМино- м -2(п-оксифенил)-бензимидазола, то синтез его на основе предлагаемого 2- (п-аминофенил) -5-нитробенэимидазола также более прост, исключает использование дефицитных исходных продуктов, концентрированной бромйстоводороДной кислоты (см, получение Б-аМи- но-2-(п-оксифенил)-бензимидазола в примерах 4 и 5)., ,jj::i:;
На основании полученного йромежуФЪЧйого продукта можно получить и 60 другие мрнбмесш.
П р им е Р 1. 2-(п-аминофенил),
-бвНЭЙМИДаЗОЛ.:(:.;..,;..,;:-. ;;j.. I/.. .
В 300 Г пЬли рсфорнЬй-Шёйёты (124% HjPO,|) при п ереМевайвании и 65
температуре 100-120°С загружают смесь 14,0 г (0,102 моля) п-аминобёнзойной кислоты и 10,8 г (0,1 моЛя) о-фенилендиамйна, температуру реакционной мйссы повышают до 160 С, пьеле 11ёгоДс1ЮТ охладитьсй до 120- , ,Далее загрузку с последующим йагреванием до 160 повторяют. Всего за 4 приема загружают 56 г. (0,408 моля) п-амийобензойной кислоты и 43,2 г (О, моля) о-фенилендиамина. После чего перемешивают при 1бО-165 С 0,5 ч, охлаждают до 120-130®С и осyopojRHo выливают при перемешивании в 100 мл горячей воды. Полученный раствор охлгшсдают и нейтрализуют приливанйем к 1,6 л 12%-ногб водного аммиака. Белый осадок отфильтроввают, промывают водой и сушат при 150С. Выход 79 r(94%V, т. пл. 24424б«с. ;:-; ; : ; , .
П р им е р 2. 2 (п-аминофенил)-5-ййтробёнзймидазол.
В ЗОр мл серной кислоты (С-70-85%) йри охлаждении водой растворяют 62,7г (0,3 моля) 2-(п-аминофенил)бензиМидазола. Полученный раствор охлаждают до и нитруют П:РИ йерем иивании смесью 13 МП азотнрй кислоты (А ,5) (0,305 моля) в 5 О Мл Кислоты, поддерживая температуру 0-5: с. Пос-. ле окончаний прйлййанййрастврр перемешивают 1 час при и вйливаиот в смесь 1,3 л воды:и 1 Л аммиачной; воды. Оранжевый Осадок ртфильтррвывают, эАчателЬйо прокатают водой и суЫат при , т. пл. 272-274 С. Выход 74 г (96%). ,...,
Хроматография на билуфоле: метилацетат, Rr( 0,35; хлорофбрм-пропанол 10:1/ R 0,46. Спектр ПНР и Диметилацетамиде + 3% LIСI, с 4Н 8,42;, J 8,02, «JC,« 7,66;d5.B,28j( 6,73 JW 6,28; Тд 2.гц; rii; I
П p и M e p 3. 5(6)-г отно-2-(п-аминофенил)бензимидазол. В 150 мл . этанола растворяют 12,7 г (0,05 моля) 5(6) -нитро-2-(г1-.« иоАвнил) бензимидаэола, гидрируют водородом под атмосферным давлением в присутствии 2 1,7% катализатора Pd/C в течение 2 ч Раствор отфильтровывают, отгоняют 80 мл этанола, охлаждают, отфильтровывают выпавшие кристаллы; промывают 50%-ным этанолом. Получают 10,5 (94%) мономера 5(6)-амино-2-(гг-амино фенил) бензимидаэола, т. пл. 234235 с. П р и м е р 4. 5-нитро-2-(п-оксифенил) бензимидаэол. , К смеси 6 мл в 50 мл воды при перемешивании добавляют 5,1 г (20 ммоля) 2(п-аминофенил)-5-нитробензимидазола, образовавшуюся соль в суспензии диазотируют 1,3 г (20 мм ля) нитрита натрия при .. Полученную желтую суспензию диазосоедине ния постепенно приливают к 100 мл кипящей 10% H,,. После окончания выделения азота отфильтровывают ора жевый осадок, растворяет в 25% красный раствор фильтруют и нейтрал зуют соляной кислотой. Выпавший жел тый осадок отфильтровывают, промывают водой и сушат при . Получают 3,5 г (70%) 5-нитро-2-(п-оксифенил) бензимидазола, т. пл. 3383400с (разл.). Найдено: 16 ,4% , Вычислено N 16,3%. П р и м е р 5. 5-амино-2-(п-оксифенил) беиэимидазол, В 30 мл этанола растворяют 2 г 5-нитро-2(п-оксифенил)бензимидазола, гидрируют водородом под атмосферным давлением в присутствии 0,5 г катализатора Pd/C в течение 2ч. Раствор отфильтровывают, упаривают получгиот 1,5 г (85%) 5-амино-2-(п-оксифенил)-бензимидазола, т. пл. 196-197«С (лит. т. пл. ). Предлагаемое соединение позволяет получать мои(4еры высокой степени чистоты простым, доступным способс м. Формула изобретения 2-(п-аминофени)-5-нитробензимидазол формулы . .. . н - . как промежуточный продукт для синтеза мономеров. , Источники информации, принятые во внимание при экспертизе 1.Авторское свидетельство СССР 522602, кл, С 07 Р 235/04, 1974. 2.Авторское свидетельство СССР 510474, кл. С 07 D 235/18, 1974.
Авторы
Даты
1980-07-23—Публикация
1977-12-14—Подача