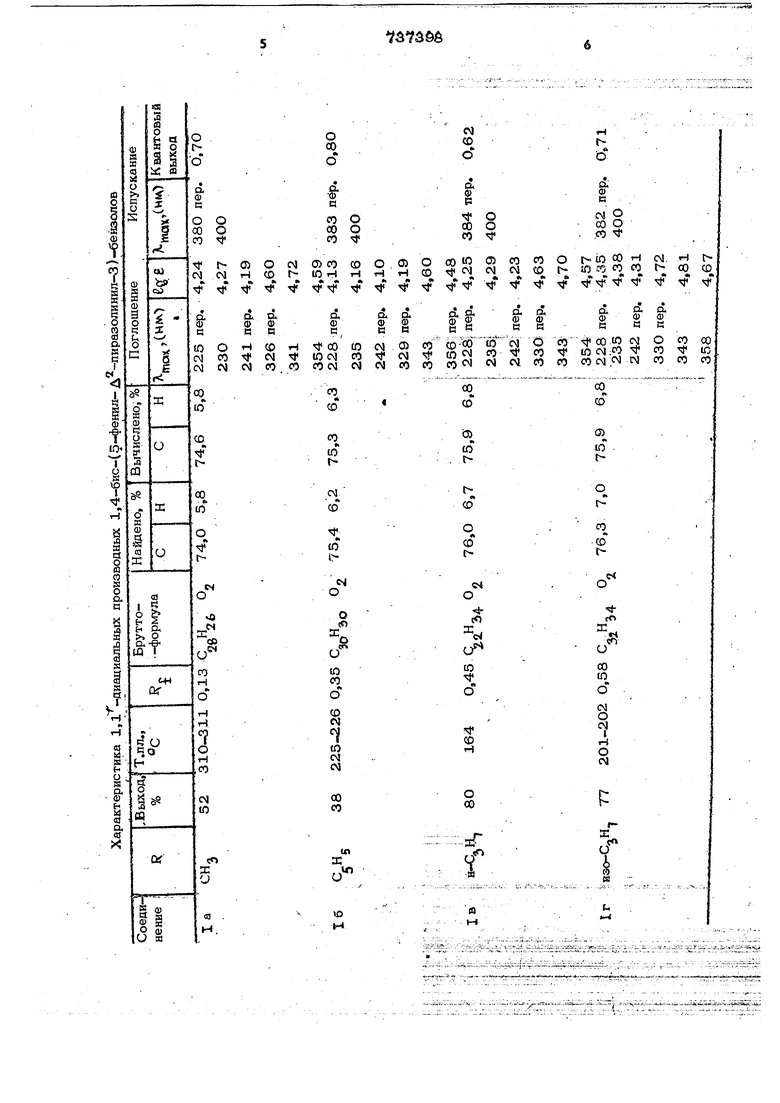
используемый одновременно в качестве растворителя и в качестве ацилнруюшвгр агента. Пример 1, 1,4-Бис-(1-ацетил-5-фешш-Д -пйраэолинил-Э)-бензол (Та Раствор 2 г {0,ОО6 моль) дибенаоиь п-диацетйлбензопа и 2,8 г (О,О55мояь гйдраэикгйярата в 110 мл ледявой уксу ной КЯСЛСУГЫ кипятят с обраггньЕМ холодильником 5 ч. Уксусную кислоту отговяют до половины объема на роторном испарителе, выпавший осадок отфипьтроБывают и парекристаллизовывают из леДяной уксусной кислоты. П р и м е р 2, 1,4-&1с-(l-nponROнШ1-5-фенил- Л пиразолвнил 3) (16). Раствор 1 г (О,003 моль) дибензаль п-йиадетилбензопа и 1,5 г (0,ОЗмоль) гидразингидрата в 10О мл пропиововой кислоты КН11ЯТ5ГГ с обратным ХОПОДШ1Ь нюсом 6 ч, охлаждают, кислоту упа рйййют на роторном испарителе, Ост&ток растворяют в 100 мл хлороформа. полученный раствор промьшают раствором соды, затем водой до нейтральной реакции, сушат над сульфатом магния и хлороформ упаривают, Попученньхй сырой продукт очищают хроматографически, пропуская его через колонку диаметром 1,5 см и длиной 40 см, наполненную силикагелем (Л 1ОО/250 мк), и используя в качестве элюента смесь бензола и эфира (1:1), Очищенный продукт перекристаллизовывают из циклогексана, П р и м е р 3, 1,4-Бис(1-бутирил5-фенил- А -пиразолинил-3)-бензол (1в). Получен аналогично примеру 2 при .кипячении компонентов в масляной кислоте,. . П р и.м е р 4, 1,4-Бис-( 1-изобутирил-5-фенил- Д -пиразолинил-3)-бензол (1 г). Получен аналогично примеру 2 при ипячении компонентов в изомасляной ислоте. Выходы и характеристики поученных соединений приведены в табице.
Хромат6графирова{ше попучейных соедвиеввй проводились на свлуфопе в системе бевзоп-эфир (1гЗ), проявле НИ€ УФ-светом,
ИЮ-спектры сняты на i1 H6opeUR-2O в табпетьах бромистого калия,,
Спёйгры поглошевия и люмивесцевн пии сняты на приборе Mi-taclii : ER$-3T в растворе ацетонитрила,, Квантовые вын ходы флуоресценции измерялись нн этом же приборе с использованием фпуороме Прической приставки (j-3 относвтедь /но стандартных растворов бисульфата хи|ШВа и 2-аминопиридина в 0,1 ч, раст- Воре серной кислоты.
Как следует из таблицы, 1,1 -диацильвые производные 1,4-бис-( А пвразолЕВИЛ-3)-бензола (1анг) внтбш:ив во флуоресцируют в ближний ультрафиолетовой области {380-46О нм), Т аксймумы флуоресценции этих совда вевий сдвинуты в кс отковолвовуто область
8
на 7О-ИО нм по сравнению с известными 1,1 -диарильными производными II. Формула изобретения
1,1-Диацильные производные 1,4 бис- {5-фенвл Л пиразол1шип-3)ензопа общей формулы
,
COR
COR
гдет СНз;С,Нд
из как люминофоры
Источники информации, принятые во внимание при экспертизе
1,Авторское свидетельство СССР
№ , кп, С 08 J 3/20, опублик. 1969.
2,Н,. А, Борисевич и др. Генерационная способность изомерных 1,4-дипиразолйвилбензопов. ЖПС, 1972, 16 (1), 45.

| название | год | авторы | номер документа |
|---|---|---|---|
| Светочувствительный полимерный материал с флуоресцентным считыванием информации, активируемый трихлорацетилпиразолином, и способ его получения | 2019 |
|
RU2725766C1 |
| Способ получения 1-арил-3- @ -гетерилпиразолонов-5 | 1984 |
|
SU1198068A1 |
| АЗАКРАУНСОДЕРЖАЩИЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2656106C1 |
| Способ получения разветвленных олигоарилсиланов на основе фенилоксазолов | 2016 |
|
RU2620088C1 |
| ПРОИЗВОДНЫЕ 1,2 -БИС (5-ФЕНИЛОКСАЗОЛИЛ-2) БЕНЗОЛА В КАЧЕСТВЕ ОРГАНИЧЕСКОГО ЛЮМИНОФОРА СИНЕГО СВЕЧЕНИЯ | 1992 |
|
RU2039744C1 |
| Способ получения бис-(3,5-диарил -пиразолинил-1)-аренов | 1973 |
|
SU477157A1 |
| Способ получения 3-[имидазо(1,2- @ )бензимидазолил-3]акриловых кислот | 1980 |
|
SU904295A1 |
| Способ получения @ , @ -дизамещенных ароматических и гетероароматических соединений | 1988 |
|
SU1750425A3 |
| Пиримидил-ди(диазадиспироалкан)ы с противовирусной активностью | 2015 |
|
RU2633699C2 |
| Способ получения производных карбоксамида оксобензотиазин-1,1-диоксида | 1975 |
|
SU664563A3 |



Авторы
Даты
1980-05-30—Публикация
1978-06-14—Подача