4;:
00
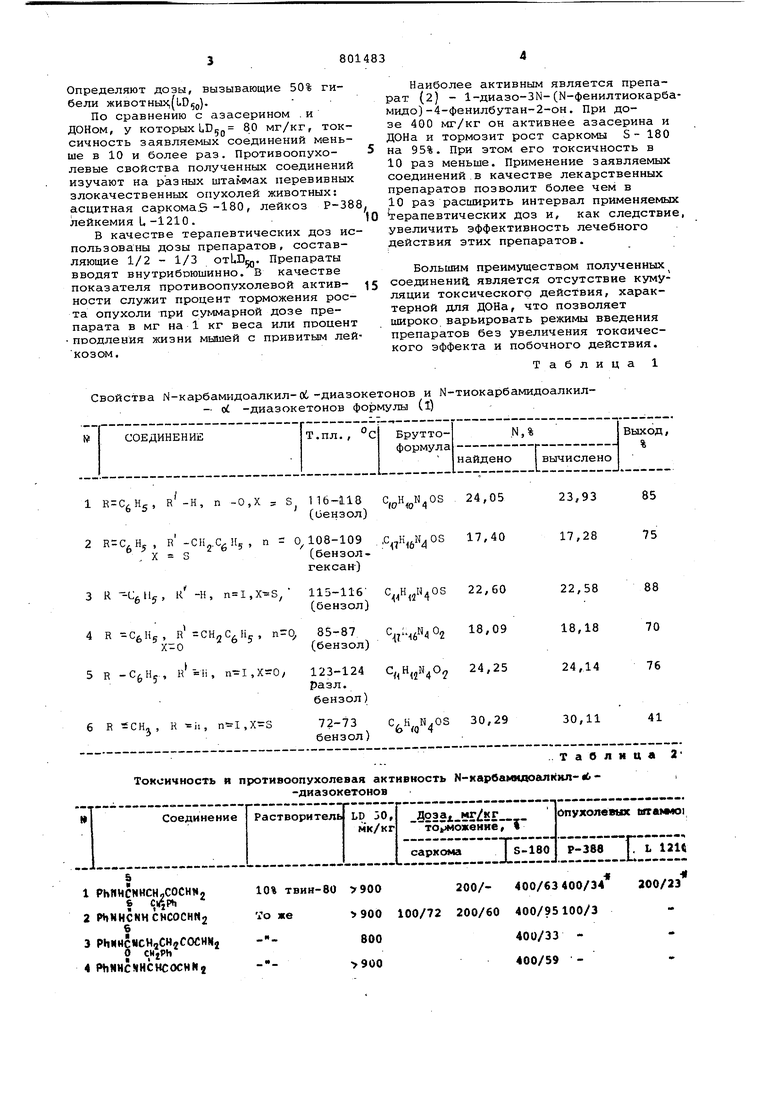
со Изобретение относится к новым хи мическим соединениям, конкретно, к производным N-карбамидоалкил-об -диазокетонов или N-тиокарбамидоалкил- oi -диазокетонов общей форму™ о II , J -13H-C-NH-CH-(CH2)j CCHN2 d где X - атом кислорода или серы; R - фенил, метил) R - атом водорода, бензил; h . 0-1. Эти соединения могут найти применение в медицине, как противоопухолевые препараты. Наиболее близким аналогом указанных соединений, обладающим противоопухолевой активностью, является аза серии, а также диазооксонорлейцин СДОН), относйщиеся к классу аминокислот. Других аналогов в литературе не выявлено. Азасерин подавляет рост некоторы перевивных опухолей мышей. Наибольший процент торможения - на саркоме S-180 (до 80%)1. Однако эти соеди нения обладают высокой токсичностью LDg 80 мг/кг) , вызывая побочные явления у крыс и мышей. В связи с этим рекомендуемая для применения доза составляет 2,5 мг на 1 кг веса (азасерин) и 0,1 мг/кг (ДОН) 2 . Кроме того, большим недостатком ДОНа являртся сильная кумуляция токсического действия, следствием чего является поражениекишечника (геморраргический энтерит . Целью изобретения является расшир ние ассортимента средств воздействия на живой организм, а именно эффективных противоопухолевых препаратов с пониженной токсичностью. Поставленная цель достигается сво ствами N-карбамидоалкил- ei -диазокето нов и N-тиокарбамидоалкил-ОС-диазоке тонов общей формулы I), получаемых известной реакцией присоединения изо цианатов или изотиоцианатов к аминам и их производным Д . Данные соединения получают взаимодействием аминоал кил-ot-диазокетонов общей формулы W О .Т1Н2-СН-(СН2) - CCHNj где R и п имеют те же значения,что и в формуле (I) ,. с изоцианатами или изотиоцианатами о щей формулы (ill): R-N где R имеют те же значения, что и в формуле (1) , в органическом растворителе при соотношении амина и изоцианата или изотиоцианата 1:1,5 при комнатной температуре с последующим выделением целевого продукта известными приемами. Как правило процесс проводят в среде хлористого метилена. Выходы конечных продуктов достигают 80%.Побочные продукты не образуются. Соотношение реагентов и температурный режим соответствуют оптимальным условиям, при которых выход продукта наибольший. Строение получаемых соединений, соответствующих формуле (1) , однозначно подтверждается ЯМР-, ИК- и УФ-спектроскопией, а также данными микроанализа. Пример. Получение 1-диазо-ЗН-(N-фенилтиокарбамидо)пропан-2-она (R-CgHj, R-H, , ) . К раствору 1,38 г (0,014 моль) 1-диазо-3-аминопропан-2-она в 100 мл хлористого метилена добавляют при перемешивании 2,5 мл (0,021 моль) фенилизотиоцианата. Смесь выдерживают в течение 10-12 ч, фильтруют, растворитель удаляют, а остаток хроматографируют на колонке с AlgO . Элюент - хлороформ. После перекристаллизации из бензола получают 2,8 г (85%), Т. пл. 116-118c.Ri 0,5 (силуфол, этилацетат-бензол 2:1). Найдено, %: N 24,(J5. C,oH,,N40S. Вычислено, %: N 23,93. П р и м е р 2. Получение 1-диазо-3N -(N -фенилтиокарбамидо)-4-фенилбутан-2-она (R -С/И, , Я-СН„СлН ,п 0, ). .. К раствору 1,95 г (0,01 моль) 1-диазо-3-амино-4-фенилбутан-2-она в 50 мл хлористого метилена при комнатной температуре добавляют при перемешивании 1,8 мл (0,015 моль) фенилизотиоцианата. Выделение продукта осуществляется методом, описанным в предыдущем примере. Остаток после хроматографирования кристаллизуется при растирании с эфиром и охлаждении до . Выход 2,5 г (75%) . Т.пл. 108-109С (бензол-гексан) . Найдено, %: С 63,08; Н 4,87, N 17,40. СпН, Вычислено, %: С 62,96, Н 4,94, N 17,28. Соединения 3, 4, 5, 6 получаются аналогично, см. табл.1. Полученные соединения были испытаны на биологическую активность. Данные испытаний приведены в табл.2. Токсичность при однократном введении определяют ча белых беспородных мышах и оценивают по методу Бернса. Препараты вводят внутрибрюшинно в виде водно-твиновых 10%) растворов. 380 Определяют дозы, вызывающие 50% гибели животных,(Ь05д). По сравнению с азасерином .и ДОНОМ, у которыхLD5g 80 мг/кг, токсичность заявляемых соединений меньше в 10 и более раз. Противоопухолевые свойства полученных соединений изучают на разных штаммах перевивных злокачественных опухолей животных: асцитная саркома.5-180 , лейкоз Р-38 лейкемия L.-1210 . В качестве терапевтических доз ис пользованы дозы препаратов, составляющие 1/2 - 1/3 OTLD. Препараты вводят внутрибоюшинно. В качестве показателя противоопухолевой активности служит процент торможения роста опухоли при суь-тмарной дозе препарата в мг на 1 кг веса или процент продления жизни мышей с привитым лей козом. Свойства Nкарбамидоалкил-об-диазокетонов и N-тиокарбамидоалкил- oi -диазокетонов формулы Cl) Наиболее активным является препарат (2) - 1-диазо-ЗК-(N-фенилтиокарбамидо)-4-фенилбутан-2-он. При дозе 400 мг/кг он активнее азасерина и ДОНа и тормозит рост саркомы S - 180 на 95%. При этом его токсичность в 10 раз меньше. Применение заявляемых соединений в качестве лекарственных препаратов позволит более чем в 10 раз расширить интервал применяемых терапевтических доз и, как следствие, увеличить эффективность лечебного действия этих препаратов. Большим преимуществом полученных соединений, является отсутствие кумуляции токсического действия, характерной для ДОНа, что позволяет широко варьировать режимы введения препаратов без увеличения токсического эффекта и побочного действия. Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Ацетиламиноалкил- @ -диазокетоны,обладающие противоопухолевой активностью | 1979 |
|
SU803351A1 |
| Аминоалкил- @ -диазокетоны в качестве полупродуктов для синтеза соединений,обладающих противоопухолевой активностью | 1979 |
|
SU839222A1 |
| 2-БИС-( β -ХЛОРЭТИЛ)АМИНО-ИЛИ 2-ФЕНОКСИ-5,7-ДИМЕТИЛ -2,6-ДИОКСО-1,3-ДИАЗА -2-ФОСФААДАМАНТАНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1985 |
|
SU1282521A1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ЖЕЛЕЗА - ФЕРРОЦЕНИЛАЛКИЛПОЛИФТОРАЗОЛЫ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2089507C1 |
| N -ФОСФОРИЛИРОВАННЫЕ ПРОИЗВОДНЫЕ 3- β -ФЕНИЛИЗОПРОПИЛСИДНОНИМИНА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2036914C1 |
| ИЗОТИУРОНИОАЗИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1991 |
|
RU2032676C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2004 |
|
RU2271209C1 |
| СРЕДСТВА, ПОДАВЛЯЮЩИЕ РОСТ РАКОВЫХ КЛЕТОК | 1993 |
|
RU2098096C1 |
| ЭТИЛОВЫЙ ЭФИР ЦИС-4-N-(N', N'- ДИМЕТИЛАМИДО-N''- ЭТИЛЕНИМИДОФОСФОРИЛ)- АМИНОЦИКЛОГЕКСАНКАРБОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1985 |
|
SU1282520A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПРОЛИФЕРАТИВНЫМ И АНТИМЕТАСТАТИЧЕСКИМ ДЕЙСТВИЕМ, ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2522449C1 |
ПРОИЗВОДНЫЕ N-КАРБАМИДОАП- КИЛ-ОС-ДИАЗОКЕТОНОВ ИЛИ И-ТИОКАРБАМИ- ДОАЛКИЛ-об-ДИАЗОКЕТОНОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ,-
Производные N-карбамидоалкил- - о(..-диазокетонов или N-тиокарбамидо- алкил- об - диазокетонов общей формулыО . о Е-ИН- С-Ш-СН-(СН^) ^CCHNjR-где, X - атом кислорода или серы',^ - фенил, метил',R' - атом водорода', бензил;И = 0-1,обладающие противоопухолевой активностью.с ?(Л
, R -Н, n -0,Х S 116-118
(бензол)
, Н , R-CH CgHj, n 0 108-109
. X S бензолгексан)
, к -H, , 115-116
(бензол)
4R CfeHj, l , n-q, 85-87
X-0(бензол)
5R , , , 123-124
разл. бензол) 72-73 6 R -СН. , К , , бензол) Токсичность n противоопухолевая активность -диаэокетонов 1Phf«HCNHCH,COCHW« 6 C/jP, 2PhNHCNHCbCOCHN2 70 же 900 3РНИйСНСНяСНйСОСНН О c/iPh 4PhNHCNHCHCOCHN
85
23,93
75
17,28
Таблица 2200/2Э800 900 С, H,N,OS 30,29 f tl , 14 л V К-карбаиидоалКкл-1б100/72 200/60 400/95100/3 400/33 400/59& PhNHCIIHCH ;CH COCI N, s .
6 СН,ИСНМСН2СНгСОСН«г HOOCCNCNjOCOCHNj
NUn
2аэасерин
Для штаммов Р-388 и 1210 приведены %% продления жизни мыней
Таблица 2
400/21
900 400/35 900
80 1,25/25 2,5/50 5/75
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Sternberg S.S | |||
| SchoIIer J., Philips F.S | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Am | |||
| Ass | |||
| Cane Res, 2, 1956, 150.2.Ларионов Л.Ф | |||
| "Химиотерапия злокачественных опухолей", Медгиз, 1962, с | |||
| Автоматическая акустическая блокировка | 1921 |
|
SU205A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Устройство для получения водяного пара и подведения его в толщу горящего топлива | 1921 |
|
SU377A1 |
Авторы
Даты
1983-08-07—Публикация
1979-07-12—Подача