Изобретение относится к аналитичес кой химии и может быть использовано для определения железа (III ) и железа (П) в ее технических материалах и различных объектах. Известны способы фотометрического определения железа с использованием органических реагентов, например способ фотометрического определения железа (П) с о-фенантролином. Молярный коэффициент поглощения при 515 нм равен 111ОО Для определения железа (III) этим способом его восстанавливают до железа (П), определ$пот общее количество железа с помощью указанного реагента, а затем количество железа (III) находят по разности til« Известен также фотометрический метод определения железа (III) в кислой среде в суммы железа (П) и железа (III) в щелочной среде с помощью сульфосалицвловсй кислоты. Молярный коэффициент поглощения для комплексов в кислой и щелочной среде равен соогветственно 18 ОО и 5800 2. Этот метод малочувствителен и не позволяет прямо определить содержание железа (П). Наиболее близким к предлагаемому по технической сущности и достигаемому результату является способ определения микроколичества железа (II) и железа (III) при повыщенном присутствии, заключающийся в том, что в одной пробе при помощи о- фенантролина определяют содержание железа (П),в другой - проводят восстановление железа (Ш) гидроксиламином до железа (П) и находят суммарное количество железа при помощи того же реагента. Количество железа (Ш) находят по разности Гз. Однако известный способ не обеспечивает прямое .определение железа (111), причем необходимо использовать два образца: первый дляопределения железа (П), второй для определения суммы железа (П)
3831738д
и железа (Ш). Кроме того, вознвка-S-10 раз, соотвегсгвенно увеличивают
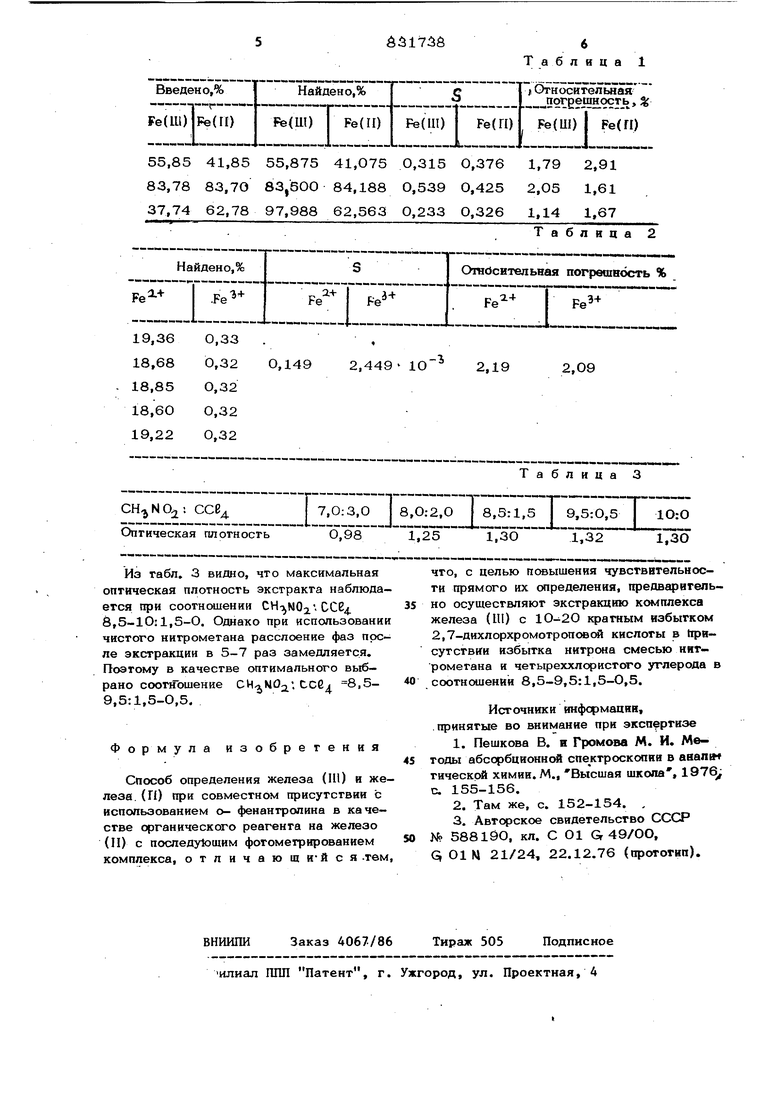
юг значительные погрешности при расче-концентрацию ДХК и нитрона и объем ратах, особенно в образцах, содержащих несоизмеримые количества железа (IU) и железа (П) за счет ошибки вычитания. Цель изобретения - определение железа (UI) и железа (П) при седаместном присутствии из одного образца, а также повьпиение чувствительности определения. Поставленная цель достигается тем, что согласно способу определения железа (III) и железа (П) при совместном присутствии .с использованием о- фенантролина в качестве органического реагента на железо (Г1) с последующим фотометрированием комплекса предварительно осуществляют экстракцию комплекса железа (И1) с 1О-2О-кратнъ1м избытком 2,7-дихлорхромотро«овой кислоты в прису тствии избытков нитрона смесью нитрометана и четъфеххлористого углерода в соотношении 8,5-9,5 : 1,5-О,5. В воднс фазе после экстракции при помощи о- фенантролина определяют содержание железа (TI). Экстракция разнолигандного комплекса железа (Ш) позволяет в предлагаемом способе исключить процесс химического восстановления железа, что повыщает точ ность определения и исключает один из источников погрешностей. Кроме того, ка видно из приведенных значений молярных коэффициентов поглощения (для разноли.пигандного комплекса 2ОООО, для двойного с о- фенантролином 1111О) чувствительность реакции определения железа (Ш) повышается примерно в. два раза. Сущность способа заключается в следующем. Для анализа отбирают аликвоту исследуемого раствора, содержащую до бОмкГ железа (П) и до 1ОО мкг железа Ш). Для анализа объектов на основе железа (П) отбирают аликвоту, содержащую до 1ОО мкг железа (Ш), водную фа эу после экстракции переносят в мерную колбу, раствор разбавляют и отбирают аликвбту для определения железа (П). Для анализа объектов на основе желе за (UI) отбирают аликвоту железа (Ш), содержащую до 60 мкг железа (П) и до 10О мкг железа (Ц1), и увеличивают в створнтеля для экстракции; при необходимости увеличивают также толшину фотометриру(емого слоя железа (П) с о- фенантрслином. Пример. Навеску соли PeSQ,-7H(p около О,ОО7ОО г быстро переносят в мерную колбу емкостью 25 мл, растворяют и доводят до метки О,1 Н сернсй кислотой, добавляют- щепотку NaHCC. В делительную воронку емкостью 1ОО мл вводят 5 мл полученного раствора, прибавл51ют 2 мл 5%-ной ДХК: Змоль 0,1М сульфата нитрона, доводят объем водной фазы аммиачно- ацетатным буферным раствором рН 6,6 до 15 мл и экстрагируют разнолигандный комплекс железа (IU) Ю мл смеси нитромеТана и че- тьфеххлористого углерода в соотношении 9: в течение 2 мин. Экстракт фильтруют сухой беззольный фильтр в кювету 1 см и измеряют оптическую плотность на фотоэлектрокалориметре с красным светофильтром. В качестве раствора сравнения используют экстракт реагентов. Содержание железа (III) находят по градуировочному графику. Водную фазу, оставшуюся после экстракции, фильтруют в мерную колбу емкостью 25 мл и допивают до метки свежепрокипяченную дистиллированную воду. 5 мл полученного раствора иомещают в мерную колбу емкостью 25 мл. прибавляют 5 мл О,25%-ного раствора -фенантролина, доливают водой до метхй и перемешивают. Через 40 мин измеряют оптическую плотность раствора на фотоэлектрикалориметре с зеленым Светофильтром в кювеТе 2 см. В качестве раствора сравнения используют дистиллированную воду. Содержание железа (П) находят по градуировочному графику. В табл. 1 и 2 приведены результаты определения Fe (III) и Fe(II) в стандартных растворах и в соли Fe 5%-Н О соответственно. В табл. 3 представлена зависимость между оптической плотностью и соотношением растворителей.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ экстракционно-фотометрического определения ванадия | 1978 |
|
SU791601A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА В ТОНКИХ МАГНИТНЫХ ПЛЕНКАХ | 1991 |
|
RU2025719C1 |
| Способ определения меди | 1982 |
|
SU1096577A1 |
| Способ определения свинца | 1990 |
|
SU1755185A1 |
| Способ фотометрического определения железа | 1973 |
|
SU570820A1 |
| Способ определения железа | 1982 |
|
SU1096578A1 |
| Способ определения железа в водных растворах | 1989 |
|
SU1709195A1 |
| Способ определения марганца (п) | 1980 |
|
SU929569A1 |
| Способ спектрофотометрического определения железа (п) в присутствии железа (ш) | 1980 |
|
SU990676A1 |
| Способ спектрофотометрического определения титана | 1982 |
|
SU1018909A1 |

55,85 41,85 55,875 41,075 0,315 83,78 83,7О 83,5ОО 84,188 О,539 37,74 62,78 97,988 62,563 О,233 Из габл. 3 видно, что максимальная оптическая плотность экстракта наблюдается при соотношении . ССЕ. 8,5-10:1,5-0. Однако при использовании чистого нитрометана расслоение фаз после экстракции в 5-7 раз замедляется. Поэтому в качестве оптимального выбрано соотношение ССбд 8,59,5:1,5-0,5. Формула изобретения Способ определения железа (HI) и же леза. (ГО при совместном присутствии с использованием о- фенантролина в качестве органического реагента на железо (II) с последуЬщим фотометрированием комплекса, отличающимися .тем О,376 1,79 2,91 0,425 2,05 1,61 О,326 1,14 1,67 что, с целью повышения чувствительности прямого их определения, предваригельно осуществляют экстракцию комплекса железа (111) с кратным избытком 2,7-дихлорхромотроповсй кислоты в 1фясутствни избытка нитрона смесью интрометана и четыреххлористого углерода в соотношении 8,5-9,5:1,5-0,5. Источники информации, .принятые во внимание при экспертизе 1.Пешкова В. и Громова М. И. Методы абсорбционной спе ктроскопии в aaaniw тическрй химии. М., Высшая школа , 1976 с. 155-156. 2.Там же, с. 152-154. , 3.Авторское свидетельство СССР М 588190, кл. С О1 Gr 49/ОО, Q 01 М 21/24, 22.12.76 (прототип).
Авторы
Даты
1981-05-23—Публикация
1979-04-02—Подача