Однако определению ванадия указанным способом мешают титан, никель, кобальт и большие количества железа, следовательно, невозможно определить концентрацию ванадия в сплавах, например в легированных сталях. Цель изобретения - повышение избирательности и полноты отделения ванадия от сопутствукядих элементов. Достигается это тем, что раствор 4- (2-пиридил-эзо) - резорцина в нитрометане вводят после экстракции комплекса ванадия с 2-100-кратным избытком нитрона, а экстракцию этого комплекса осуществляют смесью нитроме тана и четыреххлористого углерода в соотношении 8,5-9,5:1,5-0,5. Сущность способа заключается в том, что сначала ванадий переводят в двойной комплекс с нитроном, который/ затем экстрагируют смесью нитро метана и четыреххлористого углерода в соотношении 8,5-9,5:1,5-0,5 в виде ионного ассоциата анионных форм ванадия с нитроном при рН 4-7 и 2-100кратном избытке нитрона. При этом ион металлов, не образующие анионные фор мы (железо, кобальт, никель, титан « др.), остаются в растворе. Для опре деления концентрации ваиадия к экстракту, ванадата нитрона прибавляют раствор 4- (2-пиридилазЬ) -резорцина нитрометане, смесь перемешивают. При этом в экстракте образуется трехкомпонентный комплекс ванадия с 4- (2-пиридилазо) - резорцином и нитроном. Молярный коэффициент поглощения 3700 Таким образом, повышение избирательности метода достигается новой последовательностью применения извес ных технических приемов: получением вначале двойного комплекса и отделение ванадия от сопутствующих элементов, а затем введением третьего комп нента и получением окрашенного тройного фотометрируемого соединения, способ осуществляется следующим образом. П р и -м е р 1. К раствору, содержа .тему 5 мкг ванадия,прибавляют по 500 мкг титана, никеля, кобальта, молибдена , 0,5 г железа, 2 мл ОД М нитр та, аммиак 1:1 до рН 4-5, аммиачноацетатный буферный раствор рН 5,0 до объёма водной фазы 40 мл и экстрагирует соединение ванадия с нитроном 10 мл смеси нитрометана и четыреххлористого углерода (см.таб.1 в течение 2 мин. Экстракт отделяют и к нему прибавляют 2 мл 0,025%-ного раствора 4-(2.-пиридилазо) - резор цина в нитрометане, смесь перемешивают 2 мин до образования в экстракте окрашенного трехкомпонентного ком плекса ванадия с 4-(2-пиридилазо)резорцином и нитроном. Экстракт филь руют в кювету 1 см и измеряют оптическую плотность на фотоэлектроксло риметре ФЭК-М с синим светофиотром тносительно раствора холостого опыа, который выполняют аналогично, но ез ванадия. Концентрацию ванадия опрееляют по градуировочному графику. Для определения оптимального сосава растворителя по методике, излоенной в примере 1, выполнено неколько опытов и в табл.1 приведеы результаты определения 5,0 мкг анадия. Таблица Из табл. 1 видно, что оптимальным ля определения ванадия является расторитель, состоящий из смеси ССЬ в соотношении 8,5-9,5:1,5-0,5. ри сх)отношении 4:1 ванадий экстрагиуется не полностью, а при использовании чистого нитроме.тана процесс разделения происходит в 4-5 раз медленнее. Экспериментальные данные подтверждают, что оптимальньиии условиями экстракции ванадия с нитроном является рН 4-7 и не менее , чем 2-кратный избыток нитрона. П р и м е р 2. Определение ванадия в легированных сталях. Навеску стали 0,1 г растворяют в 20 мл серной кислоты (1:4), после растворения разрушают карбиды азотной кислотой (,40), приливая по каплям до прекращения вспенивания и выпаривают до паров серной кислоты. Соли растворяют в 200 мл воды при нагревании, раствор охлаждают и переводят в мерную колбу емкостью 500 мл, доводят водой до метки и перемешивгиот.; Аликвоту раствора 2 мл перенЬсят в делительную воронку емкостью 50 мл, прибавляют 18 мл аммиачноацётатного буферного раствора рН 6,2 мл 0,1 М нитрона и 10 мл смеси нитрометана и четыреххлористого углерода (9:1). Экстрагируют 1-2 мин. Отстоявшийся нижний СЛОЙ переносят в другую длительную воронку, прибавляют . мл 0,025%-ного 4- (2-пиридилазо) - резорцина в нитрометане и перемешивают 1-2 мин. Экстракт фильтруют через сухой фильтр в кювету 1 см и измеряют оптическую плотность с синим светофильтром на фоне экстракта реагенTqs.Концентрацию ванадия определяют.ло градуировочному графику.
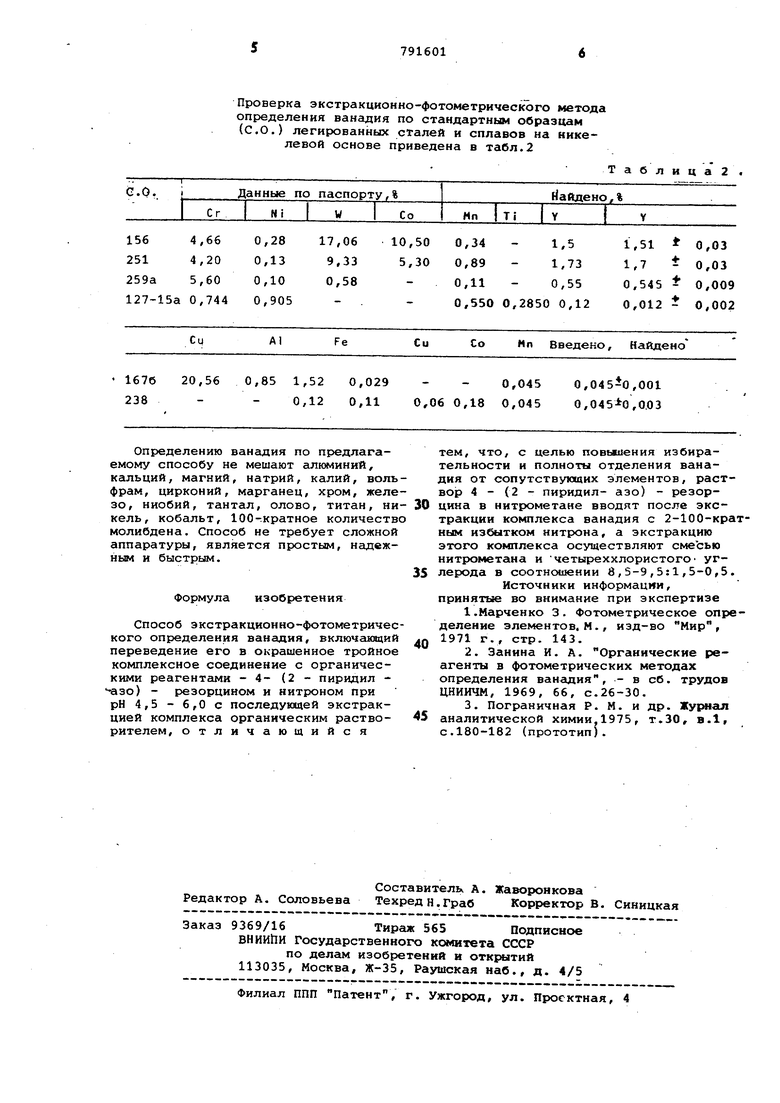
Проверка экстракцнонно-фотометрического метода определения ванадия по стандартным образцам (с.О.) легированных сталей и сплавов на никелевой основе приведена в табл.2
Таблица 2

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения железа /ш/и же-лЕзА /п/ пРи COBMECTHOM пРиСуТСТВии | 1979 |
|
SU831738A1 |
| Способ фотометрического определения ванадия | 1991 |
|
SU1797050A1 |
| Способ фотометрического определения кобальта | 1986 |
|
SU1370558A1 |
| Способ определения железа /п/ | 1975 |
|
SU592757A1 |
| Способ комплексонометрического определе-Ния МЕди(п) | 1979 |
|
SU833526A1 |
| Экстракционно-фотометрический способ определения ниобия | 1977 |
|
SU716982A1 |
| Способ определения германия | 1990 |
|
SU1734010A1 |
| Реагент для фотометрического определения висмута ( @ ) | 1983 |
|
SU1161873A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТИТАНА (IV) | 2009 |
|
RU2407002C1 |
| Способ определения высших третичных аминов и четвертичных аммониевых оснований | 1981 |
|
SU976355A1 |

Определению ванадия по предлагаемому способу не мешают алюминий, кальций, магний, натрий, калий, вольфрам, цирконий, марганец, хром, железо, ниобий, тантал, олово, титан, никель, кобальт, 100-.кратное количество молибдена. Способ не требует сложной аппаратуры, является простым, надежным и быстрым.
Формула изобретения
Способ экстракционно-фотометрического определения ванадии, включающий переведение его в окрашенное тройное комплексное соединение с органическими реагентами - 4- (2 - пиридил ) - резорцином и нитроном при рН 4,5 - 6,0 с последующей экстракцией комплекса органическим растворителем, отличающийся
тем, что, с целью повыиения избирательности и полноты отделения ванадия от сопутствующих элементов, раствор 4 - {2 - пиридил- азо) - резорцина в нитрометане вводят после экстракции комплекса ванадия с 2-100-кратиым избытком нитрона, а экстракцию этого комплекса осуществляют смесью нитрометана и четыреххлористого углерода в соотношении 8,3-9,5:1,5-0,5.
Источники информации, принятые во внимание при экспертизе
0
5 аналитической химии,1975, Т..ЗО, в.1.
алалп ичас ЧП п л.пггпп л.
С.180-182 (прототип).
Авторы
Даты
1980-12-30—Публикация
1978-09-25—Подача