(54) СПОСОБ ПОЛУЧЕНИЯ НЕСИММЕТРИЧНЫХ N-ФЕНИЛ-N-ЗАМЕЩЕННЫХ П-ФЕНИЛЕНДИАМИНОВ
прерывном режимах. Температура реакции и давление в реакционном сосуде не так существенны. Способ осуществляется при нормальном давлении и комнатной температуре, однако вследствие влияния давления и температуры на скорость реакции целесообразно осуществлять его при повышенной температуре и увеличенном давлении. Рекоменду тся работать в температурном режиме от 20 до . Температура реакции aS-laS C, лучше 40-100 С. Давленив водорода может колебаться в широких пределах, например в интервале 1-150 бар. Его величина составляет 5-15 бар, лучше 7-12 бар. Время реакции 15 миН - 5 ч, предпочтительно 0,5-3 ч.
Получаекые соединения используются в промышленности в больших количествах в качестве антиоксидантов резин и веществ, препятствукядих деструкции резин под действием озона.
Примеры 1-9 (сравнительные примеры) .
Реакции проводят в стеклянных автоклавах объемом 1 л, снабженных отводным вентилем, расположенным в днище, трубкой для ввода газ.а, жидкостным краном и лопастной мешалкой ( перемешивание с помощью магнитной мешалки). Для проведения реакции берут 20 г (93,2 ммоль) п-нитрозодифенилгидроксиламина (НДГА) и 200 мл ацетона. Реакцию проводят в интервале от 30 до , давление водорода 9-10 бар, продолжительность реакции 1 ч и скорость перемешивания 1500 ирт Автоклав сначала откачивают, затем наполняют водородом. Затем автоклав наполовину заполняют реакционной средой и, наконец, суспендируют пнитрозодифенилгидроксиламин,(ндгА) и катализатор, состоящий из палладия на угле, в остатке реакционной среды и полученную смесь, дозированно вводят через впускной .вентиль. Затем давление водорода в автоклаве доводят до 9-10 бар и осторожно нагревают. В зависимости от количества палладия реакция протекает при температуре от 20 до . После прекращения тепловыделения автоклав продолжают греть при 75°С, так что cyt/яларное время реакции составляет 1ч.
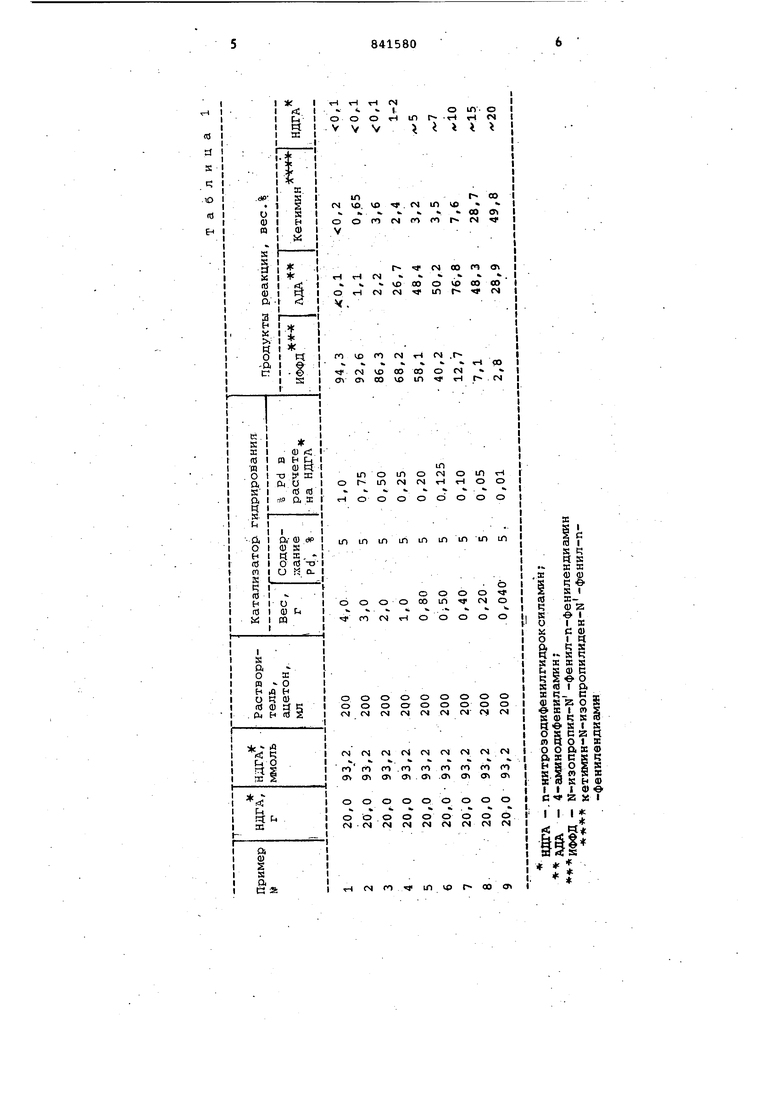
В табл. 1 показано влиян.ие количества благородного металла на выход М-изопропил-М-фенил-п-фенилендиамина (ИФФД). В табл. 1 приведены: состав катализатора, состоящего из палладия на угле, количество металла в расчете на количество введенного в реакцию п-нитрозодифенилгидроксиламина, а также выходы.несимметричного Н-фенил-М-замещенного п-фенилендиамина и образукяцихся в качестве побочных продуктов кетиминов и непроалкилированных производных п-фенилендиамина.
(С
а
S
с;
о
(О
е-1
Результаты этих сравнительных опытов убедительно показывают, что при использовании катализатора в количестве соответствупщем 1 вес. % палладия относительно количества введенного в реакцию п-нитрозодифенилгидроксиламина, восстановительное ёшкилирование протекает со сравнительно более высокой селективностью образования требуемого N-изопропил-N-фенил-п-фенилендиамина. При исг пользовании более низких количеств катализатора селективность образования Н-изопропил-м-фенил-п-фенилен-. диамина вновь падает. При использовании катализатора в количестве, соответствугацем 0,20 вес.% палладия, селективность лежит значительно ниже 10%.
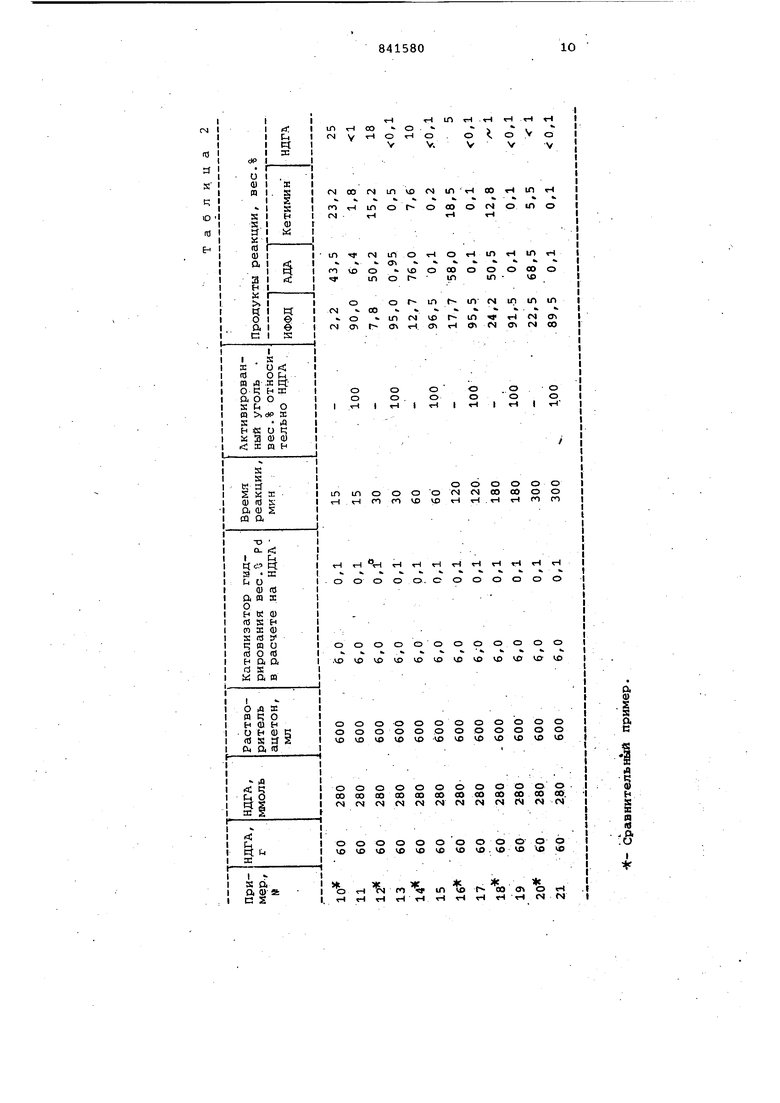
Примеры 10-21. Достигаемое повышение выхода, а также селективности за счет добавления активированного угля с удельной поверхностью не менее 700 и зольность менее 7,5 вес.% видно из примеров и сравнительных примеров табл. 2.
Пример, 7 из табл. 1 повторяют один раз с добавлением и один- раз без добавления активированного угля и количественно определяют конверсию исходного и выход целевого продуктов в зависимости от продолжительности реакции.
В кадцом случае вз-аимодействию подвергают 60 г (280 ммоль) и-нитрозодифенилгидроксиламина и 600 лл ацетона в присутствии 6,0 г палладиево-угольного катализатора фирмы Degussa с содержанием палладия 1,.%, удельной поверхностью угля: 1100 .и зольностью 0,5вес.% по методике, описанной в примерах 1-9.
В примерах 17, 19 и 21 выходы N-изопропил-N-фенил-п-фенилендиамина ниже, чем, например, в примере 15, так как вследствие большей продолжительности реакции часть требуемого продукта уже подвергалась дальнейшему восстановлению до N-изопропил-N -циклогексил-п-фенилендиамина.
1Л fN
NCO(NulVO Nm-r400
п
(N
1Л« CN 1ЛО ОгЧ .
ЮО kVOOOOOOOOO «т1Г о t 1Л1Л VO о 1Л МЧ5Г-1Л |т-4(1а1 (IOO
гН гН
СО О О I
о V
гН О Н О
о
VV.
V
V
V
тН 1Л
1Г1 О t О а О О 1Л
1Л «Н 1Л Ч
оoi irvt- uifNioirt
00 - . 





| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N'-ФЕНИЛ-ПАРА-ФЕНИЛЕНДИАМИНОВ | 2012 |
|
RU2502725C1 |
| Способ получения п-аминодифенила-МиНА | 1979 |
|
SU828961A3 |
| Способ получения -бис (1,3-диметилбутил)п-фенилендиамина | 1978 |
|
SU676586A1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-НИТРО И/ИЛИ 4-НИТРОЗОДИФЕНИЛАМИНА, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-АМИНОДИФЕНИЛАМИНА И СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЛКИЛИРОВАННОГО П-ФЕНИЛЕНДИАМИНА | 1992 |
|
RU2102381C1 |
| Способ получения -фенил- -/1,3диметилизобутил/-п-фенилендиамина | 1976 |
|
SU639859A1 |
| Способ получения катализатора для гидрогенизационной переработки алифатических и ароматических соединений | 1980 |
|
SU1060096A3 |
| Способ получения N-1,3-диметилбутил-N-фенил-п-фенилендиамина | 1980 |
|
SU891639A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ИЗОПРОПИЛ-N'-ФЕНИЛ-П-ФЕНИЛЕНДИАМИНА | 2018 |
|
RU2670975C1 |
| КАТАЛИТИЧЕСКОЕ ГИДРИРОВАНИЕ НИТРОБЕНЗОЛА С ОБРАЗОВАНИЕМ 4-АМИНОДИФЕНИЛАМИНА | 1998 |
|
RU2213088C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АЛКИЛ-6-МЕТИЛ-N-(1'-МЕТОКСИ-2'-ПРОПИЛ)-АНИЛИНА И 2-АЛКИЛ-6-МЕТИЛ-N- (1'-МЕТОКСИ-2'-ПРОПИЛ)-N-ХЛОРАЦЕТАНИЛИДА | 1993 |
|
RU2127253C1 |

гН гН tH гНгНгЧ гЧгНгМ НгН
ооооо. соооооо
оооооооооооо
.ЧО VO VO VO VO VO VO VO О
оооооооооооо оооооооооооо
VO VD VO Ю VO VO v VO Л VO VO
о о о о о о о о о о о о оо QO 00 оо оо 00 со .со 00 со . со со
(NtNlCNtSrvlfMCMfvJtNNriltM
о о о о о о о о о о- о р
VO VO VO VO VO VO VO VO . VO VO VO viD
li Irvj fO «г гН гЧ Н и гН
о о
о о
о о
о о о
о .
I тН I v4I гЧ 1
гН
о о о о о о inoooo N seooooo
tHnrOVDVOrHi-l.rHvHfOm
4с . Це . 1к
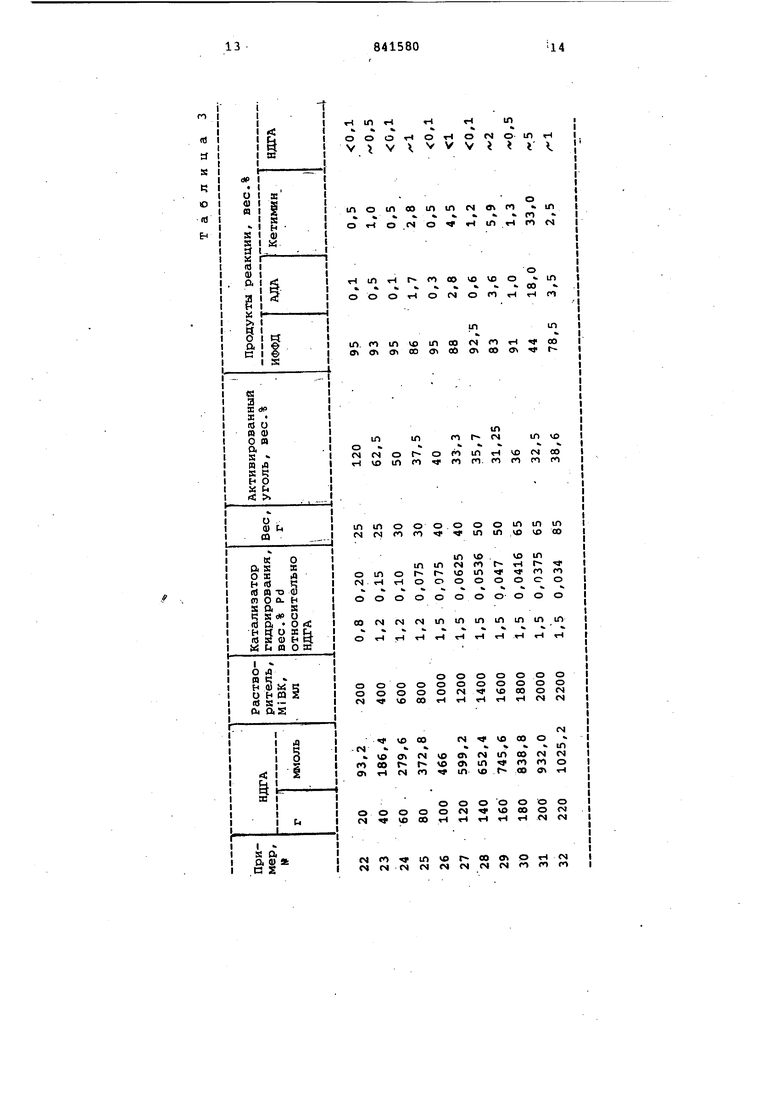
1Л VO f 00 Л о гЧ тН тН тН «ч тН мм Примеры 22-32: В стеклянный автоклав объемом 1,5 л, снабженный лопастной мешалкой, термометром, .трубкой для ввода газа, манометром, жидкостным краном, вентилем для отвода газа, отводным вентилем, расположенным в днище, и фильтровальным пальцем фильтрбужа, загружают суспензию 20 г п-нитррзодифенил гидроксиламина и 0,8 г палладиевоугольного катализатора (EIOP фирмы Oegussa с содержанием палладия 5% и 0,20% палладия в расчете на количество п-нитрозодифенилгидроксиламина), а также 25 г активированного угля (фирмы Merk порошкообразного, высушенного с удельной поверхностью 1050 и содержанием золы менее 5 вес.% и 200. мл метилизобутилкетона. После многократного откачивания и продувания водородом реакций начинают при давлении водорода 9 10 бар. Восстановительное алкилирова ние происходит при температуре около 40с и после завершения экзотермичес кой реакции, во время протекания кот рой реакционную смесь охлагкдают, автоклав выдерживают при и скорос ти перемешивания 1500 ирт, так чтобы суммарная продолжительность реакции составляла 1 ч. После завершения реакции субстрат с помощью фильтрбужа под давлением водорода отделяют от катализатора гидрирования и активированного угля - катализатора и последние вместе с Метилизобутилкетоном возвращают в автоклав. После этого подвергают взаимодействию вновь в течение 1 ч при 75-80 С и давлении водорода 9-10 бар новую порцию, состоящую, из 20 г п-нитрозодифенилгидроксиламина, 200 г метилизобутилкетона (суммарное количество), а также активированного угля-катализатора и в соответствукяцих случаях свежего катализатора гидрирования. Таким образом осуществляют 10 циклов, в течение которых удается подвергнуть восстановительному алкилированшо в итоге 220 г п-нитрозодифенилгидроксиламина. Количество катализатора гидрирования,, а также активированного угля-катализатора выраженные в вес. % палладия относительно суммарного количества введенного в реакцию п-нитрозодифенилгидроксиламина, а также достигнутые выходы N-(1,3-диметилбутил)-N-фенил-п-фенилендиамина (ДБФФД), п-амино-дифениламина (АДА) и кетимина приведены в табл. 3. Результаты свидетельствуют о том, что после нескольких реакционных циклов количества добавляемых свежего катализатора гидрирования и активированного угля значительно снижаются.
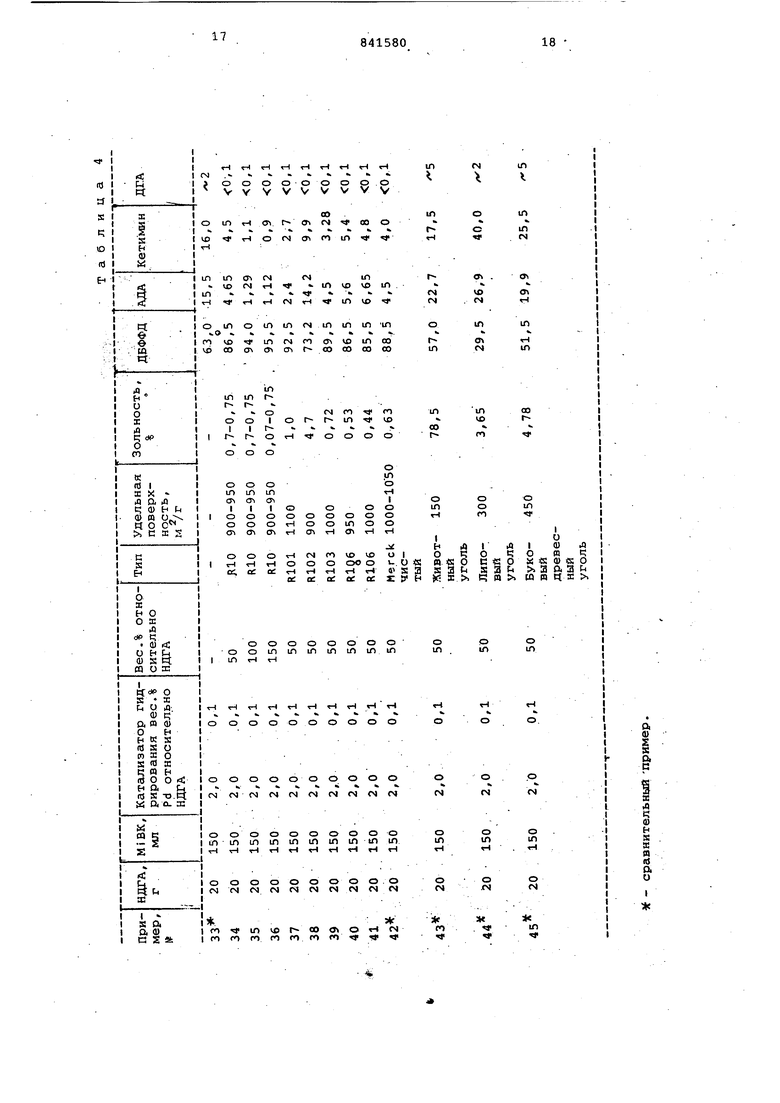
ПримерыЗЗ-45. Примеры 33 - 36 показывают как влияние количества добавленного активированного угля, так и влияние типа активированного угля (примеры 37 - 45) на протекание процесса восстановительного алкилирования.
Реакции проводят по методике, описарной в примерах 1 - 9. В каждом случае в реакцию вводят 20 г п-ни.трозодифенилгидроксиламина (НДГА) и 150 iJin метилизобутилкетона (МИБК) . В качестве катализатора гидрирования используют палЛадиево-угольный катализатор (Е 106R фирмы 0еди55а с содержанием палладия 1,02 вес.%).
в качестве активиропан-ных углей используют синтетические активированные угли фирм Degusse и Merck с различными величинами удельноП поверхности и зольности, а также различные активированные угли из природного сырья.
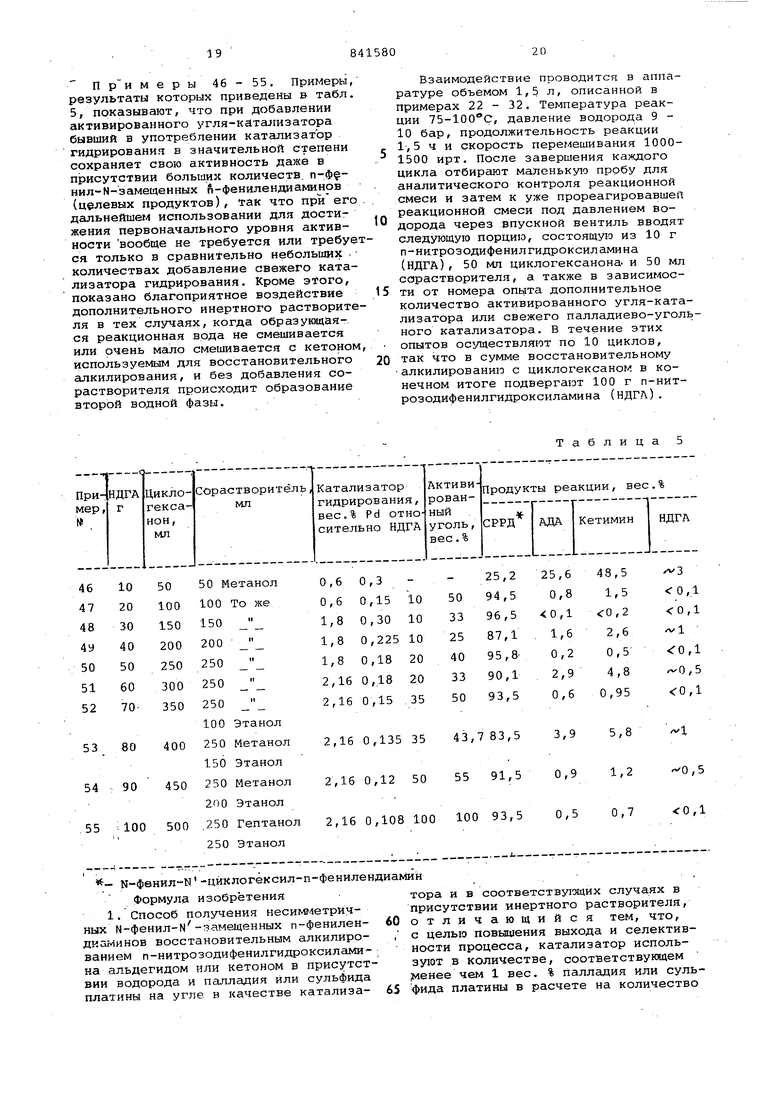
Примеры 42-45 показывают, что как в случаях слишком низкой удельной поверхности, так и в случаях слишкой высокого содержания золы активированных углей выходы N-(1,3-диметилбутил)-М-фенил-п-фенилендиамина (ДБФФД) ниже. Примеры 46-55. Примеры результаты которых приведены в табл 5, показывают, что при добавлении активированного угля-катализатора бывший в употреблении катализатор гидрирования в значительной степени сохраняет свою активность даже в присутствии больших количеств, п-ф нил-М- замещенных ft-фенилендиаминов (целевых продуктов), так что при его дальнейшем использовании для достижения первоначального уровня активности вообще не требуется или требуе ся только в сравнительно небольших количествах добавление свежего катализатора гидрирования. Кроме этого, показано благоприятное воздействие дополнительного инертного растворите ля в тек случаях, когда образующаяся реакционная вода не смешивается или очень мало смешивается с кетоном используемым для восстановительного алкилирования, и без добавления сорастворителя происходит образование второй водной фазы. t ц-фенил-Н-цйклогексил-п-фенилен Формула изобретения 1. Способ получения нecим / eтpичныхН-фенил-н-замещенных п-фенилендиаминов восстановительным алкилированием п-нитрозодифенилгидроксилами на альдегидом или кетоном в присутст вии водорода и палладия или сульфида платины на угле в качестве катализаТаблицаВзаимодействие проводится в аппаратуре объемом 1,5 л, описанной в примерах 22 - 32. Температура реакции 75-100с, давление водорода 9 10 бар, продолжительность реакции 1,5 ч и скорость перемешивания 10001500 ирт. После завершения каждого цикла отбирают маленькую пробу для аналитического контроля реакционной смеси и затем к уже прореагировавшей реакционной смеси под давлением водорода через впускной вентиль вводят следующую порцию, состоящую из 10 г п-нитрозодифенилгидроксиламина (НДГА) , 50 МП циклогексанона. и 50 мл сорастворителя, а также в зависимости от номера опыта дополнительное количество активированного угля-катализатора или свежего палладиево-угольного катализатора. В течение этих опытов осуществляют по 10 циклов, так что в сумме восстановительному алкилированию с циклогексаном в конечном итоге подвергают 100 г п-нитрозодифенилгидроксиламина (НДГД). ин тора и в соответству1свдих случаях в присутствии инертного растворителя, отличающийся тем, что, с целью повышения выхода и селективности процесса, катализатор используют в количестве, соответствукядем ;менее чем 1 вес. % палладия или суль фида платины в расчете на количество
введенного в реакцию п-нитрозодифенилгидроксиламина с добавкой активированного угля с удельной поверхностью не менее 700 м /г и зольностью менее 7,5 вес. %,
2,Способ по п, 1, отличающийся тем, что катализатор гидрирования используют в количествах, соответствующих 0,05-0,2 вес. % палладия или сульфида платины в расчете на количество введенного в реакцию п-нитрозодифенилгидроксилг№ ина.
3,Способ по пп. 1 и 2, отличающийся тем, что количество активированного угля-катализатора составляет 10-.200 вес. % в расчете на количество введенного в реакцию п-нитрозодифенилгидроксиламина.
4,Способ по пп. 1-3, о т л и чаюций-ся о тем, что количество .альдегида или кетона составляет
2-10 экв. на каждый.эквивалент п-нитpoзoдифeнилгидpoкcилa Iинa.
ч а ю щ и -и с я тем, что взаимодействие проводят при 40-100с и давлении водорода 7-12 атм.
Источники информации, принятые во внимание при экспертизе 0 1. Патент Великобритании №1295672, кл. С 2 С, опублик. 08.10.72 (протоТ1 -
Авторы
Даты
1981-06-23—Публикация
1979-04-13—Подача