Изобретение относится к усовершенствованному способу получения 2-алкил-6-метил-(1'-метокси-2'-пропил)-анилина и к способу получения 2-алкил-6-метил-N-(1'-метокси-2'-пропил)-N-хлорацетанилида.
Производные N-алкиланилина могут быть использованы в промышленности при приготовлении активных веществ для сельского хозяйства, в частности гербицидов, как описано, например, в патенте США 3937730. Пути приготовления вкраце описаны в патенте США 3937730, однако способ восстановительного алкилирования не подтвержден примерами и не описан в деталях.
В патенте Чехословакии 270548 описан способ получения 2-этил-6-метил-N-(1-метокси-2-пропил)-анилина с помощью восстановительного алкилирования 2-этил-6-метиланилина в присутствии платинового катализатора гидрирования и неорганической кислоты в качестве катализатора присоединения протона. Недостатки этого процесса состоят в том, что эта реакция не доходит до конца без дополнительного добавления свежего катализатора, и при возвращения катализатора в цикл теряется значительная каталитическая активность. Трудно фильтровать катализатор, который мелко измельчен, так как фильтр забивается. Это приводит к длительному времени фильтрования. Дополнительный недостаток с точки зрения экологии состоит в использовании избытка метоксиизопропанола в качестве растворителя.
Было необходимо найти способ получения 2-алкил-6-метил-N-(1'-метокси-2'-пропил)-анилина, который применим в промышленном масштабе и который обеспечивает экологическое и экономическое преимущества над известными способами. Требуется лучший способ удаления катализатора и сокатализатора путем фильтрования, каким является устранение дополнительного активированного угля и растворителя.
В данном случае удивительным образом было обнаружено, что без всякой потери выхода и чистоты достигается существенно улучшенное отделение катализатора гидрирования, кислотного катализатора и конечного продукта путем проведения известного способа приготовления при использовании дополнительных количеств воды во время восстановительного алкилирования и при добавлении основания к реакционной смеси до отделения готового продукта. Также было обнаружено, что повторно используемый катализатор проявляет только незначительные потери активности в течение многих циклов, в результате чего не должен добавляться совсем свежий катализатор или должны добавляться его только незначительные количества для поддержания полной активности.
Целью настоящего изобретения является создание усовершенствованного способа получения 2-алкил-6-метил-N-(1'- метокси-2'-пропил)-анилина формулы I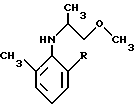
в которой R обозначает метил или этил,
путем каталитического восстановительного алкилирования, при котором по крайней мере один моль-эквивалент метоксиацетона формулы II
CH3C(O)CH2-O-CH3
вводят в реакцию с одним моль-эквивалентом 2-алкил-6-метил-анилина формулы III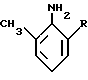
в жидкой среде без дополнительного растворителя, в присутствии катализатора на базе платиносодержащего углерода и в присутствии водорода, а также в присутствии кислотного сокатализатора при давлении водорода в пределах от 2•105 до 1•106 Па при температуре в пределах от 20 до 80oC, отличающегося тем, что реакционная смесь содержит воду с начала реакции и после гидрирования, добавляют основание, реакционную смесь фильтруют для разделения катализатора и соединения формулы I, извлекаемого из фильтра.
R предпочтительно обозначает этил.
Исходные соединения имеются в продаже на рынке или могут быть получены известными способами. Метоксиацетон формулы II может быть приготовлен, например, каталитической дегидрогенизацией метоксиизопропанола, а водород извлекают для использования на этапе гидрирования данного процесса, который здесь описан.
Содержание воды в реакционной смеси может быть о 15 до 30 вес.% по отношению к метоксиацетону. Наиболее предпочтительно метоксиацетон формулы II используется непосредственно в качестве его азеотропа с водой, и он содержит примерно 25 вес.% воды.
Реакция конденсации происходит в водной среде, подкисленной кислотным сокатализатором. Используемый кислотный сокатализатор может представлять собой, например, H3PO4 или H2SO4, при этом предпочтительна серная кислота. Пригодны небольшие количества кислоты, например, от 0,001 до 0,08 моль-эквивалентов по отношению к количеству присутствующего 2-алкил-6-метил-анилина.
Реакция между соединениями формул II и III является экзотермической и допускается повышение температуры реакционной смеси предпочтительно до 35 - 60oC, более предпочтительно до 40 - 50oC, причем ее поддерживают на этом уровне, например, с помощью внешнего охлаждения, при необходимости, для гидрирования.
Катализатор, используемый для гидрирования, представляет собой платину на носителе из активированного угля, иногда называемого платиносодержащим углем. Металлическая платина присутствует в количестве от 3 до 6%, предпочтительно от 4 до 5% от веса носителя. Было обнаружено, что этот катализатор является повторно используемым свыше 100 раз без вредного влияния на его активность или селективность реакции. Согласно предпочтительному варианту осуществления катализатор повторно используется, например, в более, чем 10 - 15 циклах. После этого повторного использования может быть целесообразным добавлять незначительные количества свежего катализатора.
Воздух должен быть вытеснен из автоклава перед реакцией. Это может быть осуществлено с помощью промывания автоклава инертным газом, например, неоном, аргоном, гелием или азотом. Азот предпочтителен.
Этот процесс может быть осуществлен в удобном варианте в автоклаве, оснащенном отдельными впускными клапанами для газа, например, клапаном для водорода, клапаном для азота и при определенных условиях клапаном для впуска воздуха. Гидрирование проводят при давлении водорода предпочтительно от 3 до 7 бар, более предпочтительно от 4 до 6 бар (1 бар = 1•105 Паскалей).
Основание, добавляемое после гидрирования, может представлять собой KOH или NaOH, и предпочтительно NaOH. Добавляют достаточное количество основания для нейтрализации кислотного сокатализатора, который может быть извлечен из водной фазы, например, в виде ее соли.
До фильтрования желательно вытеснить непрореагировавший водород в автоклаве инертным газом, например, одним из вышеперечисленных газов, хотя предпочтительным является водород. Реакционной смеси дают выйти из автоклава через фильтр. Выгодно создавать разность давлений, например, пониженное давление ниже фильтра, или давление может быть подано выше фильтра, имея в виду сторону автоклава. Предпочитают подводить давление азота внутри автоклава для выдавливания смеси полностью, а также снизить время фильтрования. Катализатор на базе платиносодержащего угля может промываться водой и высушиваться под потоком газообразного азота, например, азота технической степени чистотой, или смеси воздух/азот, до его повторного использования в следующей реакции. Целевое соединение образует органическую фазу, и его отделяют от водной фазы известными методами, и оно может быть очищено или использоваться непосредственно в последующем процессе, например, для получения активных веществ для сельского хозяйства.
Еще одним предметом изобретения является способ изготовления соединений формулы IV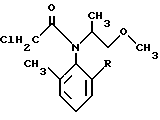
в которой R обозначает метил или этил, при котором
а) на первом этапе проводят каталитическое восстановительное алкилирование, при котором по крайней мере один моль-эквивалент метоксиацетона формулы II
CH3C(O)CH2-O-CH3
вводят в реакцию с одним моль-эквивалентом 2-алкил-6-метил- анилина формулы III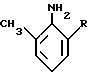
в жидкой среде без дополнительного растворителя, в присутствии катализатора на базе платиносодержащего угля и водорода и в присутствии кислотного сокатализатора при давлении водорода в пределах от 2•105 и 1•106 Па при температуре в пределах от 20 до 80oC, и
б) на втором этапе вводят в реакцию соединение формулы IV, отличающийся тем, что на первом этапе реакции а) реакционная смесь содержит воду с начала реакции и после гидрирования добавляют основание, реакционную смесь фильтруют для отделения катализатора.
Предпочтения для первого этапа а) такие же, что и вышеуказанные для получения соединений формулы I.
Этап реакции б) приводит к соединениям формулы IV, что описано, например, в заявке на канадский патент 1176659.
Хлорангидрид монохлоруксусной кислоты может быть использован в эквимолярном количестве или в избыточном количестве до 20 моль/моль соединения формулы I. Предпочтителен избыток от 5 до 15 молей/моль. Реакция может быть осуществлена в присутствии инертного растворителя, такого, как, например, ароматические растворители, такие, как бензол, толуол, ксилол.
Особенно целесообразно использование избыточного количества хлорангидрида монохлоруксусной кислоты в качестве растворителя для реакции без какого-либо дополнительного сорастворителя.
Температура реакции может варьироваться в пределах от 50 до 130o Цельсия. Целесообразно проводить реакцию в температурном диапазоне от 70oC до температуры флегмы реакционной смеси, предпочтительно при температуре флегмы реакционной смеси.
Промывка продукта, полученного после того, как будет отогнан избыток хлорангидрида монохлоруксусной кислоты, может быть осуществлена водой при температуре от 50 до 100oC. Целесообразно проводить промывку повторно, несколько раз. Также целесообразно добавлять к промывочной воде такое количество щелочи, в частности, едкого натра или едкого кали, чтобы довести значение pH воды до 4 - 10. Продукт в последующем сушат нагревом при 100 - 120oC в вакууме.
Этап б) реакции может быть осуществлен периодически или в непрерывном режиме. При проведении процесса непрерывно целесообразно добавлять хлорангидрид монохлоруксусной кислоты и соединение формулы I одновременно в реакционный сосуд и непосредственно после концентрирования смеси в вакууме. Хлористый водород, образованный во время реакции, отделяется в газообразной форме и может быть сжат и подаваться в стальные цилиндры или растворен в воде для получения концентрированной соляной кислоты.
Процесс по этапу а) согласно изобретению, кроме того, является удивительным, если рассмотреть обсуждение восстановительного алкилирования автором M.Freifelder на стр. 346 - 349 "Practical Catalytic Hydrogenation" (Wiley Interscience 1971). Удаление воды, участвующей в реакции, например, над безводной неорганической солью, как сообщается, увеличивает выходы путем сдвига равновесия в сторону продукта конденсации, например, азометина.
Преимущества способа с этапом а) согласно изобретению суммируются следующим образом: высокий оборот платинового катализатора достигается без значительной потери активности или селективности; более легкое отделение целевых продуктов; более легкое отделение катализатора; не используется органический растворитель для добавки к реагентам.
В нижеследующих примерах изобретение иллюстрируется более подробно.
Пример 1: 2-этил-6-метил-N-(1'-метокси-2'-пропил)-анилин. 236,1 г (2,01 молей) свежеприготовленного метоксиацетона (75% метоксиацетона, 25% воды) смешивают 233,9 г (1,73 моля) 2-метил-6-этил-анилина (100%) в автоклаве. 3,7 г Pt-C (5%), предварительно выдержанного в воде, добавляют в автоклав с 20 г воды. 4,3% 96%-ной H2SO4 осторожно добавляют по каплям при перемешивании смеси. Автоклав закрывают и воздух вытесняют заполнением N2 технической степени частоты до 5 бар, вакуумируют автоклав и повторно заполняют азотом три раза. Азот технической степени чистоты содержит в пределах от 0,1 до 0,5 вес.% кислорода.
Азот вытесняют продувкой водородом, удаляют и повторяют заполнение водородом до давления 5 бар. Реакционную смесь перемешивают и температуре дают возрасти до 40 - 45oC, причем на этом уровне ее поддерживают. Давление H2 удерживают путем использования регулятора давления в пределах от 4,8 до 5,0 бар. Поглощение H2 реакционной смесью прекращается спустя примерно 4 часа, после чего реакционную смесь охлаждали до 20oC. Водород вытесняют с использованием азота путем вытеснения сильным напором струи, удалением и заполнением N2 до давления 5 бар, с повторением 3 раза. Затем давление N2 снижают до атмосферного давления и автоклав открывают. При перемешивании реакционной смеси добавляют 18,75 г NaOH (20%).
Автоклав закрывают, вновь закачивают в него азот и содержимое перекачивают через фильтр, используя давление азота, слегка превышающее атмосферное давление. Отжатый осадок представляет собой катализатор из платиносодержащего угля. В автоклав добавляют 20 г воды, которые пропускают в атмосфере N2 сквозь отфильтрованный катализатор для его промывки. Влагу, остающуюся в катализаторе, удаляют выпариванием в потоке азота в течение нескольких минут. Отфильтрованную органическую фазу отделяют от водной фазы с использованием разделителя фаз и получают 354,1 г соединения, указанного в заголовке (98,7% от теоретического). Катализатор удаляют из фильтра и возвращают в автоклав с дополнительными 20 г воды. Автоклав вновь заполняют азотом до того, как проводить процесс.
Влияние возврата в цикл на активность катализатора.
В серии из 20 каталитических реакций гидрирования были получены следующие результаты при повышенных условиях при времени реакции 4,5 часа.
2-этил-6-метил-N-(1'-метокси-2'-пропил)-анилин сокращенно обозначается НАА, а метилэтиланилин обозначается МЭА.
Пример 2: 2-этил-6-метил-N-(1'-метокси-2'-пропил)-N-хлорацетанилид.
9,7 г (0,047 молm) 2-этил-6-метил-N-(1'-метокси-2'-пропил)-анилина согласно примеру 1 и 5,05 г (0,05 моль) триэтиламина смешивают с 30 мл свободного от воды бензола. 5,65 г (0.05 моль) хлорацетилхлорида в 10 мл бензола добавляют по каплям и смесь промывают несколько раз водой. После разделения органической фазы и водной фазы органическую фазу сушат, а растворители удаляют под вакуумом. Продукт получают количественно, и он имеет показатель преломления n

Способ получения 2-алкил-6-метил-N-(11-метокси-21-пропил)-анилина путем каталитического восстановительного алкилирования, при котором по крайней мере один моль-эквивалент метоксиацетона вводят в реакцию с одним моль-эквивалентом 2-алкил-6-метил-анилина в жидкой среде без добавления растворителя, в присутствии платиносодержащего угольного катализатора и водорода и в присутствии кислотного сокатапизатора при давлении водорода в пределах от 2 х 105 до 1 х 106 Па при температуре в пределах от 20 до 80°С, отличающийся тем, что реакционная смесь содержит воду от начала реакции и после гидрирования добавляют основание, реакционную смесь фильтруют для отделения катализатора, и соединение, указанное в названии изобретения, извлекают из фильтрата. Способ особенно применим для получения N-замещенных хлорацетанилидных гербицидов, при этом улучшается отделение катализатора гидрирования, кислотного сокатализатора и целевого соединения при сохранении выхода и чистоты целевого продукта. 2 с. и 30 з.п. ф-лы, 1 табл.
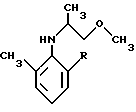
где R означает метил или этил,
путем каталитического восстановительного алкилирования, при котором по крайней мере один моль-эквивалент метоксиацетона формулы II
СН3С(О)СН2-О-СН3
вводят в реакцию с одним моль-эквивалентом 2-алкил-6-метил-анилина формулы III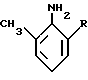
в жидкой среде в присутствии водорода, катализатора - платины на угле и кислотного сокатализатора под давлением водорода, равном 2•105-1•106 Па, при температуре 20-80oC, отличающийся тем, что процесс ведут в водной среде, после окончания реакции добавляют основание, реакционную смесь фильтруют для отделения катализатора и соединение формулы I выделяют из фильтрата.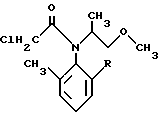
где R означает метил или этил,
при котором на первой стадии проводят каталитическое восстановительное алкилирование, когда по крайней мере один моль-эквиалент метоксиацетона формулы II
СН3С(О)СН2-О-СН3
вводят в реакцию с одним моль-эквивалентом 2-алкил-6-метил-анилина формулы III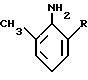
в жидкой среде в присутствии водорода, катализатора - платины на угле и кислотного сокатализатора при давлении водорода, равном 2•105-1•106 Па, при температуре 20-80oC, и на второй стадии полученное соединение формулы I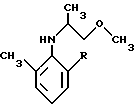
где R - метил или этил,
вводят во взаимодействие с хлорангидридом монохоруксусной кислоты и отделяют соединение формулы IV, отличающийся тем, что первую стадию процесса ведут в водной среде, после окончания реакции добавляют основание и реакционную смесь фильтруют для отделения катализатора.
| US, патент, 3937730, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| CS, патент, 270548, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1999-03-10—Публикация
1993-12-23—Подача