I
Изобретение относится к способу получения новых кортикоидов о&цей формулы
CH.2R2
„„OCHjOTSi
Цель изобретения - расширение средств воздействия на живой организм.
Указанная цель достигается спосогсобом получения новых кортикоидов общей формулы 1, в которой --.. , Y, Z, V, R и R, обладают вышеуказанными значениями, основанным на известной реакции присоединения галоида или хлорноватистой кислоты к двойной связи и заключающимся в том, что к 9,11 дегидростероиду общей формулы присоединяют хлор или хлорноватистую кислоту и выделяют целевой продукт. Пример 1,5,0 г 21-ацетокси-17с1-метоксимегокси 4,9 (П )-прегнадиен-3 20-диона суспендируют в 50 мл тетрагидрофурана и при смешивают с 20,5б мл 1 н, раствора перхлорной кислоты и 2,78 г М-хлорсукцинимида. Реакционную смесь перемешивают в течение 2 ч, при этом добавляют еще 3,52 мл перхлорной кислоты. Реакционную смесь высаживают в раство ре из 5,1+ г сульфита натрия, и 350 мл ледяной воды. Осадок отфильтровывают промывают водой и влажные кристаллы перекристаллизовывают из смеси метанол-вода. Получают 1,5 г 21-ацетокси-9с1 хлор-1 К -окси- - -метоксиметокси-4-прегнен-З,20-диона который после кристаллизации из этилацетата и ацетона плавится при 189192°С. Пример 2. а). Суспензию 6,0 г 21-ацетокси-17с1-окси-1,4,9-прег натриен-3,20-диона в мл безводного ацетонитрила смешивают с 11,5 мл метоксиэтоксиметилхлорида и 11,5 мл Ди изопропилэтиламина и перемешивают в течение 7,5 ч при . После высаживания вледяной воде выделенный осадок растворяют в метиленхлориде, промывают водой и сушат, после чего растворитель отгоняют. Очистку реак Й1ИОННОГО продукта производят хроматографией на 800 г силикагеля в сиетеме этилацетат-гексан (0-30 этилaцeтaтa) . Получают 4,9 Г21-ацетоксй-1 7с1- (1 ,3,6-триоксагептил) 1,4,9 -прегнатриен-3,20-диона, т.пл. 140 С в). Раствор 1,0 г 21-ацетокси-17 i- (1 ,3,6-триоксагептил) 1,4,9-прегнатриен-3,20-диона в 10 мл диоксана смешивают с 900 мг N-хлорсукцинимида и 5 мл 10%-ной перхлорной кислоты. Перемешивают 3,5 ч при комнатной тем пературе и выливают на смесь леДяная вода - поваренная соль - бисульфит натрия. Осадок отфильтровывают,раств ряют в метиленхлориде, промывают водой и после высушивания над сульфаТОМ натрия растворитель отгоняют. Сы рой продукт очищают хроматографией н 100 г силикагеля в системе метиленхлорид-ацетон (0-15 ацетона). Получают 7бО мг 21-ацетокси-9Ы.-хлор-11 (1-окси-17с1- (1 ,3,6-триоксагептил)-1 ,4-прегнадиен-3,20-диона, т.пл. 204°С, а также 180 мг 21-ацетокси-9с1, хлор-1 7cL- (1, 3.6-триоксагептил)-1 ,-прегнадиен-3,20-диона, т,пл. Ц8°С, Пример 3. а). ,0 г 21-аметокси-17с1-окси-1,4,9-прегнатриен-3,20-диона растворяют в 28 мл безводного метиленхлорида и 18 мл формальдегиддиметилацеталя, смешивают с добавляемой порциями смесью из 6,0 г кизельгура и г полупятиокиси фосфора и перемешивают s течение 45 мин при комнатной температуре. Осадок фильтруют и экстрагируют еще раз метиленхлоридом, который содержит триэтиламина. Сырой продукт очищают хроматографией на 750 г силикагеля в системе метиленхлорид-ацетон (0-12 ацетона). Получают 3,3 г 21-ацетокси-17оЬ-метоКсиметокси-1,4,9 прегнатрйен-3,20дирна, т.пл. 160°С. Ь) . 1 ,6 г 21-ацетокси-1 7с1-метоксиметокси-1,Ц,9 прегнатриен-3,20-диона растворяют в 16 мл диоксана и смешивают с 1,5 г N-хлорсукцинимида. После добавления порциями 8 мл водной перхлорной кислоты реакционную смесь перемешивают в течение 3 ч при комнатной температуре и выливают на насыщенный раствор поваренной соли и бисульфита натрия в ледяной воде. Осадок отфильтровывают, сырой продукт очищают хроматографией на 175 г силикагеля в системе метиленхлоридацетон (0-12 ацетона). Получают 1,1 г 21-ацетокси-9а1 хлор-11|Ь-окси-1 7с1.метоксиметокси-1 ,4-прегнадиеН-3,20-диона, т.пл. 224°С, и 250 мг 21-ацетокси-9си 11f диxлop-17(i-мeтoксиметокси-1,4-прегнадиен-3,20-диона, т.пл. 162С. Пример 4. а). 3,2 г трис(т|5ифенилфосфин(родий (1)-хлорида растворяют в смеси из 100 мл метанола и , йОО мл бензола и предварительно гид-i рируют в течение 6,5 ч при нормальном давлении. Раствор упаривают на ротационном испарителе и остаток очищают хроматографией на 400 г силикагеля в системе метиленхлорид-ацетон (0-12 ацетона). Получают 2,1 г 21-ацетокси-17с1-метоксиметокси-4 ,9-прегнадйен-3,20-диона. Ь). Аналогично примеру ЗЬ 1,1 г 21 - ацетокси-17cL- метокси меток си- 4,9 -прегнадиен-3,20-диона обрабатывают с N-хлорсукцинимидом и перхлорной кислотой. После очистки выделяют 430 мг 21-ацетокси-9с1-хлор-1 1(Ь-окси- 1 7ci-метоксиметокси-4-прегнен-З,20-диона, т.пл. . 59 Пример 5. а). 17,5 г 21-хлор-17сС окси-4,9 прегнадиен-3,20-диона обрабатывают аналогично при- . меру За 236 мл формальдегиддиметилаце таля. Сырой продукт очищают хроматографией на 2,25 «г силикагеля в сис теме метиленхлорид-ацетон (0-k% ацетона). Получают 7,6 г 21-хлор-17с1-метоксиметокси-«,9-прегнадиен-3,20-диона, т.пл. . Ь) . 1 ,8 г 21-хлор-17 1-метоксиметокси-,9 лрегнадиен-3,20-диона обрабатывают аналогично примеру 3 Ь N-хлорсукциниммдом и перхлорной кислотой. Сырой продукт очищают хроматографией на 100 г силикагеля . системе метиленхлорид-ацетон (0-10% аце тона). Выделяют 126 мг 9(1,21-дихлор-11р-окси-17о1-метоксиметокси-А-прегнен-3,20-диона, т.пл. 197°С с разло жением . Пример 6, а). 3,0 г 21-фтор-17с1 окси-1 , ,9-прегнатриен-3,20-диона аналогично примеру обрабатываюг Ц мл формальдегиддиметилацеталя. Сырой продукт очищают хроматографией на 450 г силикагеля в системе метилен хлорид-ацетон (0-8% ацетона ). Полу чаю 1,5 г 21-фтор-17А-метоксиметокси U ,9-прегнатриен-3,20-диона. Ь). В условиях примера ЗЬ 500 мг 21-фтор- 17 -метоксиметокси-1 ,, натриен-3,20-диона обрабатывают М-хлорсукцинимидом и перхлорной кислотой. После описанной выше методики пе реработки и очистки хроматографией на силикагеле выделяют +20 мг 9с1-хлор-21-фтор- 11(1-окси-17с1-метоксиметокси-1 ,4-прегнадиен-3,20-диона, т.пл. . Пример 7. а). 1,0г 17с1-окси-1,k,9-прегнатриен-3,20-диона в условиях примера За обрабатывают форм альдегиддиметилацеталем. Выделяют 823 мл 17 А метоксиметокси-1 ,,9 пpeгнaтpиeн-3,20-диoнa в виде сырого продукта. Ь). 823 мг названного выше сырого продукта обрабатывают аналогично примеру 3bN-хЛорсукцинимидом и перхлорной кислотой, очищают аналогичным об- разом. Получают мг 9(1 хлор-11(i-окси-17о1- метоксиметокси-1 ,-прегнадиен-3,20-диона, т.пл. 227°С. Пример 8. а). Аналогично примеру 7 из 7,6 г 21-фтop-17ot.-oкcи-,9-пpeгнaдиeн-3,20-диона и 68 мл формальдегиддиметилацеталя получают 36 8, г 21-фтор-17с1-метоксиметокси-4,9 прегнадиен-3,20-диона. Ь). В условиях примерз 5а 1, г 21-фт6р- 17о1-метоксиметокси- ,9 прегнадиен-3,20-диона обрабатывают N-хлорсукцинимидом и перхлорной кислотой. Сырой продукт очищают хроматографией на 100 г силикагеля в системе метиленхлорид-ацетон (0-10 ацетона). Получают 380 мг 9с1-хлор-21-фтор-1 Ш-окси-17с1-метоксиметокси-+-прегнен-3,20-диона, т.пл. 21t С (с разложением) . Новые кортикоиды общей формулы I при локальном применении отличаются выраженным антивоспалительным действием и обладают эффективным различием между желательным локальным действием и нежелательным системным побочным действием. Локальное действие определяют с помощью теста на сужение сосудов следующим образом. Тест проводили со здоровыми крысами по 8 штук обоего пола, которые за последние две недели не получали локальной кортикостероидной обработки. Сужение сосудов оценивали визуально через i и 8 ч с помощью проверки по следующим степеням действия: 1 абсолютное побледнение, 2 небольшая остаточная эритема, 3 средней степени эритема, интенсивность эритемы в средней области необработанной и неповрежденной кожи, эритема с небольшими.осветлениями, 5 никакого побледнения или усиления эритемы. В каждом ряду опытов в качестве сравнительного вещества применяли дифлюкортолон-21 -валерианат (66-,9с(и-дифтор-1111-окси- 1бс1-метил-21 -валерилокси-1 , -прегнадиен-3,20-дион - ДФВ). Определяли разность д в средних степенях действия ДФВ, наблюдавшихся в отдельных рядах исследований, и тестового вещества. Положительные отклонения показывают благоприятнуюоценку тестового вещества в сравнении с ДФВ, отрицательные отклонения неблагоприятную оценку. Системное действие соединений определяли с помощью теста на дополняющий отек следующим образом. Крыс весом от 130 до 150 г для получения очага воспаления инъекцировали 0,1 мл 0, суспензии МусоЬасterium butyrtcum в правую заднюю лапу. Перед инъекцией измеряли объем
79271
лапы у крыс. Через 2k ч после инъекции еще раз измеряли объем лапы для определения оазмера отека. Затем орально или подкожно крысам вводили различные количества испытываемого 5 вещества, растворенного в смеси из 29 бензилбензоата и касторового масла. После последующих 2 ч вновь определяли объем лапы.
Контрольные экземпляры обрабатыва-О ли аналогично с той разницей, что им инъекцировали не содержащую испыты3а
ваемого вещества смесь бензилбензоата с касторовым маслом.
Из полученного объема лапы определяли количество испытываемого вещества, необходимого для достижения 50 ;-иого уменьшения объема экспериментально полученного отека лапы.
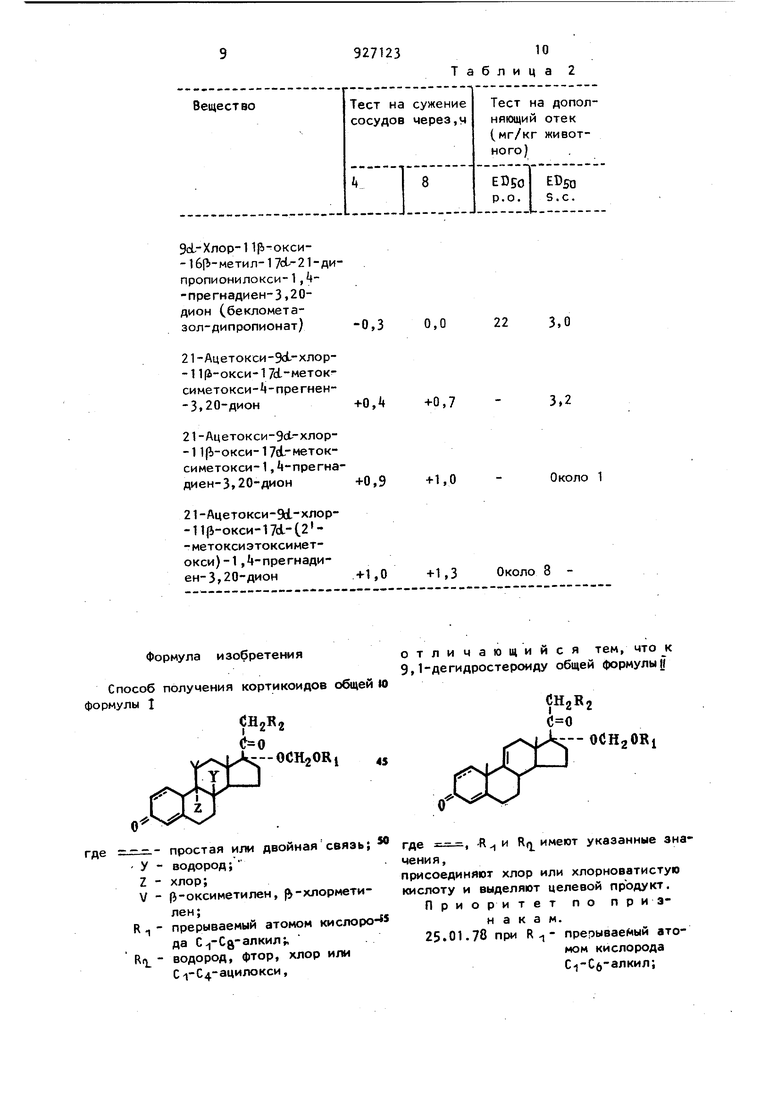
В табл. 1 и 2 приведены результаты тестов, полученные при обработке крыс соответственно производными преднизолона и 9-хлоркортикоидами, содержащими 0,1 ч/млн активного вещества.
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения кортикоидов | 1979 |
|
SU876060A3 |
| Способ получения производных 9-фторпреднизолона | 1978 |
|
SU862829A3 |
| Способ получения производных 9-хлорпреднизолона | 1977 |
|
SU743581A3 |
| Способ получения кортикоидов | 1979 |
|
SU890979A3 |
| Способ получения кортикоидов | 1979 |
|
SU880253A3 |
| Способ получения 17 @ -алкоксиметоксикортикоидов | 1979 |
|
SU1103797A3 |
| Способ получения кортикоидов | 1977 |
|
SU730311A3 |
| Способ получения производных 6 -фтор-16 ,18-диметил-1,4прегнадиен-3,20-диона | 1971 |
|
SU468409A3 |
| Способ получения производных прегнановой кислоты | 1975 |
|
SU615863A3 |
| Способ получения кортикоид -21- СульфОпРОпиОНАТОВ или иХ СОлЕй | 1979 |
|
SU818489A3 |

11(Ь,17 1--21-триокси-1, «-прегнадиен-3,20-дион (преднизолон}
11(Ь,21-диокси-17 1-метоксиметокси-1,4 прёгнадиен-3,20-дион
21-Ацетокси-11|1|-окси-17с1-мётокси-1,-прегнадиен-3,20-дион.
21-Бутирилокси-1 lfi-окси-17dL-MeTOKсиметокси-1,4-прегнадиен-3,20-дион
8,6 2,6
-0,8
9,8
-0,3
з ()
+0,
+0,2
Около 3
0,30,0223 0 +Q,,7 +0,9+1,0
+1,0+1,3Около 8 Формула изобретения
Способ получения кортикоидов общей Ю
формулы 1
CH2R2
--OCHjORl45
простая или двойная связь;
де
- У Z V
водород;
хлор;
р-оксиметилен, { -хлорметилен;
прерываемый атомом кислоро-
RI Ч
да С- -Са-алкил;,
водород, фтор, хлор или
С-1-С4 ацилокси,
3,2
Около 1
отличающийся тем, что к 9,1-дегидростероиду общей формулы((
СНгКг
r-OCHgORi
где -- -, -R и Rq имеют указанные значения,
присоединяют хлор или хлорноватистую кислоту и выделяют целевой продукт. Приоритет по признакам.
1192712312
19«12.78 при R- прерываемый это- 1. Машковский М.Д. Лекарственные мои кислорода средства, т.2. М., Медицина, 1972, C-j-Ce-алкил. c.. .
Источники информации, s кие реакции, т. 1. М., Мир, 1973, принятые во внимание при экспертизе с. 08.

Авторы
Даты
1982-05-07—Публикация
1979-12-11—Подача