Изобретение касается нового способа получения известных производных фенилгуанидина, которые обладают антигельминтной активностью и применяются в ветеринарной терапии.
Изобретение относится к получению активных ингредиентов общей формулы I: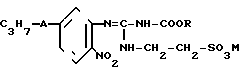
(1) где R - C1-C4-алкильные группы;
М - атом водорода или ион натрия, калия или кальция;
A - -S-, -,-SO- или -SO2-группа.
Простейший способ получения гуанидинов - взаимодействие солей S-алкил-изотиурония с аммиаком или аминами (I). Обычно используют соли S-метилизотиурония; при этом существенным недостатком является образование побочного продукта метилмеркаптана, который имеет неприятный запах, а также весьма токсичен. Кроме того, недостатком является и то, что реакционная способность S-метилгруппы очень низка и реакция может длиться несколько дней.
Патенты, защищающие получение фенилгуанидинов общей формулы I, описывает взаимодействие N-метокси-карбонил-N'-(2-нитро-4-пропил-тиофенил)-S-метилзотиокар- бамида и N'-(2-аминоэтил)-N'-циано-N''-метилгуанидина в течение 24 ч с амином (2 моль-эквивалента) в ацетонитриле (2).
Этот способ при получении целевого продукта общей формулы I даже при времени реакции, составляющем несколько дней, позволяет достичь выход всего 45% . По-видимому, это объясняется тем, что S-метилгруппа очень медленно взаимодействует с нуклеофильным заместителем и реакция приводит в итоге к получению побочных продуктов.
Изобретение касается получения производных гуанидина общей формулы I методом, заключающимся в том, что производное тиокарбамида общей формулы II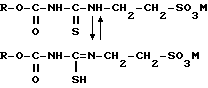 окисляется необязательно в присутствии неорганического или органического растворителя и полученное при этом новое производное сульфокислоты общей формулы III
окисляется необязательно в присутствии неорганического или органического растворителя и полученное при этом новое производное сульфокислоты общей формулы III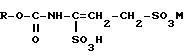 реагирует с производным анилина общей формулы IV
реагирует с производным анилина общей формулы IV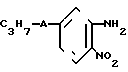 в присутствии органического растворителя.
в присутствии органического растворителя.
Изобретение основано на утверждении, что новое соединение общей формулы III, содержащее SO3-группу, взаимодействует с производным анилина общей формулы IV значительно быстрее, чем соответствующие производные, содержащие SH-группу (скорость реакции выше более, чем в 15 раз). Кроме того, утверждается, что новое соединение общей формулы III может быть получено очень простым способом - окислением соответствующего H-производного общей формулы II.
Окисление преимущественно проводят кислородом, пероксидом водорода, метапериодатом натрия, перманганатом калия, хлоратами, некоторыми надкислотами в присутствии воды и/или органического растворителя.
В случае окисления с помощью пероксида водорода может использоваться в качестве растворителя вода, а температура процесса 0-45оС. Для ускорения реакции применяют катализатор, например, каталитическое количество молибдата натрия.
Согласно изобретению, окисление может также проводиться с применением органической надкислоты: надуксусной кислоты, надбензойной кислоты, мета-хлор-надбензойной кислоты или надфталевой кислоты.
Производное сульфокислоты общей формулы III может взаимодействовать с производным анилина общей формулы IV в присутствии ацетонитрила, диметилсульфоксида при температурах до 0оС до температура кипения реакционной смеси.
Амин общей формулы IV преимущественно используют в избытке 5-30%.
Согласно изобретения, преимущественно способа в том, что он прост и не приводит к получению пахнущих или токсичных побочных продуктов, а выделенные полупродукты стабильны при комнатной температуре. Процесс идет с хорошим выходом (около 70%) при незначительном времени реакции.
Соединения общей формулы II и IV известны в практике и могут быть получены хорошо известными методами при соответствующей квалификации.
Способ, описанный в изобретении, сопровождается следующими примерами (не ограничивающими изобретение).
П р и м е р 1. В 100 мл суспендируют 31,33 г N-(метоксикарбонил-N'-(2-этилсульфокислота)-тиокарбомида, прибавляют 3 г хлорида натрия и 0,5 г молибдата натрия и охлаждают до 0оС. Затем прикапывают 43 мл 33%-ного раствора пероксида водорода, причем 28 мл прибавляют при температуре не более 20оС, а остальное количество - при температуре не более 40оС. Продолжительность прикапывания около 1 ч. Смесь охлаждают до 10оС, фильтруют, промывают осадок насыщенным раствором хлорида натрия и сушат.
Полученный продукт добавляют к 32 г 2-нитро-4-пропилтиоанилина в 100 мл ацетонитрила и кипятят смесь с обратным холодильником до отсутствия исходной сульфокислоты. (Тонкослойная хроматография: твердая фаза - Polygram Sil G/UV254 смесь растворителей: метанол, уксусная кислота, хлороформ в отношении 95:5:5). Растворитель отгоняют в вакууме. К остатку добавляют 10 г гидроксида натрия, растворенного в 100 мл воды; раствор фильтруют с небольшим количеством древесного угля и доводят pH фильтрата до 1,5. Отфильтрованные кристаллы промывают ацетоном. Получают 42,6 г N-(метоксикарбонил)-N'-((2-нитро-5-пропилсульфенил)фенил)-N''-(2-этилсульфок ислота)-гуанидина. Т.пл. 214-215оС.
П р и м е р 2. В 30 мл эфира суспендируют 2,41 г N-(метоксикарбонил)-N'-(2-этилсульфокислота)-тиокарбамида. При температуре до 20оС прибавляют 5,5 г м-хлорнадбензойной кислоты, растворенной в 20 мл эфира. Полученный раствор после 10-минутной выдержки смешивают с 3 x 50 мл 5%-ного раствора гидрокарбоната натрия, сушат над сульфатом магния и упаривают. Получают 2,5 г N-(метоксикарбонил)-N'-(2-этилсульфокислота)амино-имино-метансульфокисло-ты. Т.пл. 211-216оС.
П р и м е р 3. В 50 мл уксусной кислоты суспендируют 2,4 г N-(метоксикарбонил)-N'-(2-этилсульфокислота)-тиокарбамида. При 0оС прибавляют 2,3 г надуксусной кислоты, растворенной в 20 мл уксусной кислоты. Смесь перемешивают в течение 2 ч при комнатной температуре, после чего упаривают в вакууме досуха. К остатку добавляют 50 мл диметилацетамида и 3,2 г 2-нитро-4-пропилсульфониланилина. Смесь кипятят с обратным холодильником до отсутствия сульфокислоты, что контролируется тонкослойной хроматографией. Затем смесь выпаривают в вакууме досуха, остаток смешивают с 50 мл ацетона, фильтруют и полученные кристаллы промывают ацетоном.
Получают 3,75 г N-(метоксикарбонил)-N'-(2-нитро-5-пропилсульфонил)фенил-N''-(2-этилсульфокис лота)-гуанидина). Т.пл. 240-245оС.
П р и м е р 4. В растворе 0,42 г гидроксида натрия в 80 мл воды растворяют 4,2 г N-(метоксикарбонил)-N'-((2-нитро-5-пропил-сульфенил)фенил)-N''-(2-этилсульфо кисло- та)-гуанидина. Добавляют раствор 2,7 г персульфата калия в 10 мл воды. Реакционную смесь перемешивают в течение 3 ч, после чего выпаривают в вакууме досуха. Остаток суспендируют в 100 мл горячего метилового спирта и охлаждают до 20оС. Осажденные кристаллы фильтруют и промывают метиловым спиртом. Получают 3,96 г натриевой соли N-(метоксикарбонил)-N'-(2-нитро-5-пропилтионил)-фенил-N''-(2-этил-сульфокис- лота)-гуанидина. Т.пл. 147-150оС.
П р и м е р 5. В растворе 0,42 г гидроксида натрия в 80 мл воды растворяют 4,2 г N-(метоксикарбонил)-N''-(2-нитро-5-пропил- сульфенил)-фенил-N''-(2-этилсульфокисло-та)-гуанидина. К раствору при 20оС прикапывают 6 мл 33% -ного раствора пероксида водорода. После перемешивания в течение 8 ч к реакционной смеси прибавляют 2,2 г хлорида кальция в 10 мл воды. После 20-минутного перемешивания образовавшиеся кристаллы фильтруют, промывают холодной водой и высушивают.
Получают 3.97 г кальциевой соли N-(метоксикарбонил)-N''-((2-нитро-5-пропил-суль- фонил)-фенил)-N''-(2-этилсульфокислота)- гуанидина. Т. пл. 330оС.
П р и м е р 6. К 1 г N-(метоксикарбонил)-N'-(2-этилсульфокислота)-амино-имино-ме- тансульфокислоты, полученной в соответствии с примером 2, прибавляют 1 г 2-нитро-5-пропил-тиониланилина и 5 мл ацетонитрила. Смесь кипятят с обратным холодильником до отсутствия исходной сульфокислоты, что контролируется тонкослойной хроматографией. Затем смесь упаривают досуха и к остатку добавляют 20 мл 1-нормального раствора гидроксида натрия. Раствор осветляют с древесным углем и доводят pH фильтрата до 1,5 с помощью соляной кислоты. Получают 1,62 г N-(метоксикарбонил)-N'-(2-нитро-5-пропил-тионил)фенил-N''-(2-этил- сульфокислота)-гуанидина. Т.пл. 146-148оС.
П р и м е р 7. К 1 г N-(метоксикарбонил)-N'-(2-этилсульфокислота)-амино-имино-ме- тансульфокислоты прибавляют 1 г 2-нитро-5-пропилсульфониланилина и 10 мл ацетонитрила. Смесь кипятят с обратным холодильником до отсутствия исходной сульфокислоты, что контролируется тонкослойной хроматографией. Затем смесь выпаривают досуха и остаток смешивают с 10 мл 1-нормального раствора гидроксида натрия. Раствор осветляют с древесным углем и доводят pH фильтрата до 1,5. Полученные при этом кристаллы отфильтровывают.
Получают 1,39 г N-(метоксикарбонил)-N'-(2-нитро-4-пропилсульфонил)фенил-N''-(2-этилсульфокис лота)-гуанидина. Т.пл. 241-244оС.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ | 1988 |
|
RU2014331C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1988 |
|
RU2049783C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПАРГИЛАММОНИЙХЛОРИДА | 1994 |
|
RU2130450C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АМИДОКСИМА О-(2-ГИДРОКСИ-3-ПИПЕРИДИНО-1-ПРОПИЛ)-НИКОТИНОВОЙ КИСЛОТЫ И ИХ СОЛЕЙ (ВАРИАНТЫ), ЧИСТОЕ КРИСТАЛЛИЧЕСКОЕ ОСНОВАНИЕ АМИДОКСИМА О-(2-ГИДРОКСИ-3-ПИПЕРИДИНО-1-ПРОПИЛ)-НИКОТИНОВОЙ КИСЛОТЫ | 1990 |
|
RU2074854C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИНОЛИНКАРБОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ И СОЕДИНЕНИЕ | 1990 |
|
RU2044734C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛАЛКИЛАМИНОВ ИЛИ СОЛЕЙ ЭТИХ СОЕДИНЕНИЙ | 1990 |
|
RU2015960C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ИЗОФЛАНОВЫХ ПРОИЗВОДНЫХ | 1991 |
|
RU2036918C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛАЛКИЛАМИНОВ ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1989 |
|
RU2007384C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ 13,14-ДИГИДРО-15(R)-17-ФЕНИЛ-18,19,20-ТРИНОР PGF2 13,14-ДИГИДРО-15(R)-17-ФЕНИЛ-18,19,20-ТРИНОР PGF2 СОЕДИНЕНИЯ. | 1993 |
|
RU2099325C1 |
| АНТИМИКРОБНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2030913C1 |
Сущность изобретения: продукт - производные фенилгуанидина ф-лы 1 (3-NO2) , (50-A-C3H7)-C6H3-N=C(NH-CH2-CH2SO3M)-NH-COOR, где R-алкил; MH, Na, K, Ca; A- группа S, SO, SO2 . Реагент 1: тиокарбамид ф-лы II 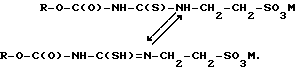 Реагент 2: окислитель. Продукт 3 (новое): R-O-C(O)-NH-C(SO3H)=N-CH2-CH2-SO3M обрабатывают соответствующим производным нитроанилина.
Реагент 2: окислитель. Продукт 3 (новое): R-O-C(O)-NH-C(SO3H)=N-CH2-CH2-SO3M обрабатывают соответствующим производным нитроанилина.
Способ получения производных фенилгуанидина общей формулы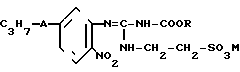
где R - C1 - C4-алкил;
М - водород, натрий, калий или кальций;
А - группа - S -, - SO - или SO2 -,
отличающийся тем, что, с целью интенсификации процесса и повышения выхода целевого продукта, производное тиокарбамида общей формулы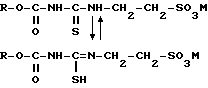
где R и М имеют указанные значения,
подвергают окислению с последующей обработкой полученного при этом производного сульфокислоты общей формулы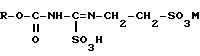
где R и М имеют указанные значения,
производным анилина общей формулы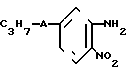
где А имеет указанные значения,
в присутствии органического растворителя при температуре от комнатной до температуры кипения реакционной смеси.
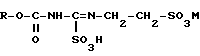
| Способ получения безгрунтовой эмали на железных изделиях | 1932 |
|
SU50286A1 |
Авторы
Даты
1994-07-15—Публикация
1991-02-20—Подача