Изобретение относится к органическому синтезу и касается получения новых фенилалкиламинов, обладающих биологической активностью и используемых в качестве активно-действующего начала в фармацевтических препаратах, стимулирующих центральную нервную систему.
Из патента США 40 25 624 известны фармацевтические смеси, содержащие аспирин и, главным образом фенил-алкил-мочевины или фенилалкиламины (последние - в очень ограниченном объеме). Эти смеси используют для лечения воспалительных процессов, причем утверждается, что снижается желудочное кровотечение.
В частности, в колонках 5 и 6 указанного патента указаны соединения F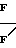 C
C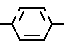 CH2-
CH2-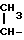 NHC2H5
NHC2H5
и 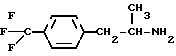
Эти соединения не входят в объем данного изобретения (соединения, где R1 - группа СН3, полностью исключены вообще).
В патенте США не говорится, как получать фенилалкиламины, которые не были известны до даты подачи данной заявки и не описывает каких-либо их свойств. В описании к патенту только говорится (колонка 4, строки 42-42): "Фенилалкиламины, используемые в данном изобретении, хорошо известны и включают фенфлурамин и норфенфлурамин", т. е. , в этом тексте четко выражено, что речь идет только об известных фенилпропиламинах. В противоположность этому соединения по изобретению являются новыми.
В соответствии с изобретением предлагается получение биологически активных фенилалкиламинов общей формулы I и их солей.
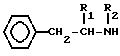 (I) где R1 обозначает алкил с прямой или разветвленной цепью, содержащей 2-8 углеродных атомов; фенилалкил, содержащий 7-10 углеродных атомов; фенил или циклоалкил, содержащий 3-8 углеродных атомов;
(I) где R1 обозначает алкил с прямой или разветвленной цепью, содержащей 2-8 углеродных атомов; фенилалкил, содержащий 7-10 углеродных атомов; фенил или циклоалкил, содержащий 3-8 углеродных атомов;
R2 обозначает группу -CH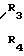 , где
, где
R3 - атом водорода или алкил С1-С7, который может быть замещен галогеном, гидроксилом, алкокси-группой с 1-4 атомами углерода или фенилалкилом (C2),
R4 - атом водорода; или группа 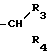 может вместе образовать циклоалкильное кольцо с 3-8 атомами углерода, при условии, что группы R1 и R2 совместно содержат по меньшей мере 5 атомов углерода и в том случае, когда R1 означает этил, R2 не может означать изобутил, или фармакологически приемлемых солей этих соединений.
может вместе образовать циклоалкильное кольцо с 3-8 атомами углерода, при условии, что группы R1 и R2 совместно содержат по меньшей мере 5 атомов углерода и в том случае, когда R1 означает этил, R2 не может означать изобутил, или фармакологически приемлемых солей этих соединений.
Согласно изобретению фенилалкиламины получают тем, что вводят во взаимодействие амин общей формулы II 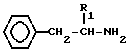 c cоединением общей формулы III O
c cоединением общей формулы III O C
C где R1, R3 и R4 имеют указанные значения, в присутствии восстановителя, такого как амальгама алюминия, газообразный водород и металлический катализатор гидрирования, боргидрид щелочного металла, с последующим выделением целевого продукта в виде свободного основания и фармацевтически приемлемой соли.
где R1, R3 и R4 имеют указанные значения, в присутствии восстановителя, такого как амальгама алюминия, газообразный водород и металлический катализатор гидрирования, боргидрид щелочного металла, с последующим выделением целевого продукта в виде свободного основания и фармацевтически приемлемой соли.
Соединения общей формулы 1, полученные по изобретению, представляют собой в форме свободных оснований липоидрастворимые маслоподобные вещества, которые при желании можно подвергнуть конверсии в кристаллические водорастворимые соли. Процесс получения соли можно проводить с использованием фармацевтически приемлемых неорганических или органических кислот (например соляной кислоты, бромистоводородной кислоты, серной кислоты, фосфорной кислоты, муравьиной кислоты, уксусной кислоты, щавелевой кислоты, малеиновой кислоты и тому подобного). Соединения общей формулы I можно выделить из кислых аддуктов по обычным методам. Соединения общей формулы I и их биологически приемлемые кислые аддукты могут быть использованы в качестве активно действующих веществ при приготовлении фармацевтических композиций для человека.
Указанные фармацевтические композиции на основе новых соединений могут быть приготовлены по известным в фармацевтической промышленности методам. Активно действующее вещество можно использовать в обычных дозированных формах (например, в форме таблеток, пилюль, драже, капсул, препаратов для инъекций и тому подобного). Указанные фармацевтические композиции могут быть включать в себя обычные носители, добавки, смазывающие вещества, наполнители, вспомогательные агенты и тому подобное.
Соединения общей формулы I заметно ингибируют инициируемое тирамином выделение норадреналина из плазматических пор нейронов за счет ингибирования процесса поглощения тирамина. В противоположность известным фенилалкиламинам соединения общей формулы I не проявляют эффекта выделения норадреналина. Одновременно с этим соединения формулы I сильно подавляют нейронное поглощение норадреналина и допамина, значительно усиливая катехоламинергическое действие, но в отличие от амфетамина и метамфетамина не оказывают влияния на серотонергическое действие даже при введении в организм в больших дозах.
Соединения общей формулы I являются стимуляторами центральной нервной системы, которая проявляет стимулирующий эффект в фармакологических испытаниях на обучение и антидепрессивность, лишь в умеренной степени усиливают подвижность и метаболизм, не демонстрируют заметного аноректального эффекта и только в слабой степени токсичны.
В противоположность основной группе известных психоэнергетических агентов соединения общей формулы I не обладают действием, ингибирующим моноамино-оксидазу (МАО). Если рассматривать механизм их действия и химическое строение, они значительно отличаются от известных трициклических антидепрессантов.
Основываясь на вышеизложенном, можно утверждать, что фенилалкиламины общей формулы I составляют психофармаконовую группу с новым механизмом действия, приемлемым для повышения психической активности (обучение, сохранение памяти) и для медицинского лечения клинических моделей депрессии, а также заболеваний, сопровождающихся заметными дефектами способности к обучению и запоминанию, подобно болезни Альцгеймера, предположительно без проявления побочных эффектов, свойственных известным стимуляторам, которые вызывают выделение катехоламина.
В соответствии с активностью соединений изобретения способ лечения предусматривает лечение здоровых или больных людей фармацевтической композицией, содержащей эффективное количество соединения общей формулы I или ее фармацевтически приемлемого кислого аддукта.
Предпочтительные ежедневные дозы составляют приблизительно 10-150 мг, в частности примерно 30 мг. Такие фармацевтические композиции предпочтительнее вводить в организм перорально, парентерально или сублингвально.
Благодаря своей низкой токсичности соединения общей формулы I можно также использовать для лечения детей в соответствующим образом пересчитанной дозировке.
1. Примеры на получение.
П р и м е р 1. 16,3 г (0,1 моля) 1-фенил-2-пентил-амина растворяют в 100 мл метанола и добавляют смесь 5,8 г (0,1 моля) пропионового альдегида и 20 мл метанола при 10оС. Реакционную смесь перемешивают 2 ч, затем добавляют 8 г (0,21 моля) боргидрида натрия. Реакция проходит при комнатной температуре в течение 12 ч. После этого смесь выливают в 200 мл 10% -ной уксусной кислоты при охлаждении и встряхивают с бензолом. Водную метанольную фазу нейтрализуют 40% -ным раствором гидроокиси натрия. Отделяющееся масло экстрагируют бензолом и органический слой осушают над сульфатом натрия, отфильтровывают и выпаривают. Остаток дистиллируют в вакууме. Вес дистиллята (основная фракция) составляет 14,35 г (70% ).
Температура кипения при остаточном давлении 7 мм рт. ст. составляет 112-120оС, nD20 = 1,5030.
Этилацетатный раствор указанного основания подкисляют добавлением в него этанола, содержащего соляную кислоту. Выпавший в осадок гидрохлорид очищают и сушат. Температура плавления: 122-124оС (смесь этанола с диэтиловым эфиром).
П р и м е р 2. 16,3 г (0,1 моля) 1-фенил-2-пентиламина растворяют в 100 мл метанола, добавляют раствор 5,8 г (0,1 моля) пропионового альдегида в 20 мл метанола. После перемешивания в течение 2 ч реакционную смесь гидрируют в присутствии 3 г катализатора "палладий на активированном угле". По завершении реакции катализатор отфильтровывают и реакционную смесь обрабатывают аналогично описанному в примере 1. После дистилляции получают 15,4 г (75% ) N-пропил-1-фенил-2-пентиламина.
Примеры 1-13 приведены в табл. 1.
П р и м е р 14. 16,3 г (0,1 моля) 1-фенил-2-пентиламина растворяют в 100 мл метанола и при 10оС добавляют раствор 5,8 г (0,1 моля) ацетона в 20 мл метанола. Через 2 ч реакционную смесь выливают в 700 мл 96% -ного этанола. В эту смесь добавляют маленькими порциями алюминиевую фольгу, активированную HgCl2 (7,3 г), затем перемешивают при комнатной температуре 24 ч. Спирт отгоняют при пониженном давлении. Оставшаяся смесь разделяется на две фазы - водную и масляную. Масляную фазу экстрагируют бензолом, экстракт осушают над сульфатом натрия, фильтруют и концентрируют. Остаток растворяют в этаноле, содержащем хлористоводородную кислоту, и раствор концентрируют. Неочищенный продукт, кристаллизуют из смеси этанола и эфира. Получают 16,8 г N-изопропил- 1-фенил-2-пентиламин-гидрохлорид (см. пример 3).
11. Биологические примеры
11/1. Определение эффекта выделения норадреналина ин виво на кошках (in vivo).
Состояние мигательной перепонки, подвергнутой анестезии кошки, постоянно регистрируется с помощью ауксотонического самопишущего кимографа. Выделение норадреналина инициирует сжатия мигательной перепонки в зависимости от дозы вещества. Внутрибрюшинное введение 1 мг/кг ФЭА инициирует сокращение мигательной перепонки. Доза 1 мг/кг амфетамина и метамфетамина вызывают такое сокращение в течение длительного периода времени. В ходе проведения вышеуказанного испытания соединения общей формулы I не вызывает никакого сокращения перепонки. (Метод: J. Knoll. Monoamin Oxidase and Its Inhibition (Eds. Wolstenholme and Knight), Elsevier, 1976г. , стр. 131).
11/2. Определение психостимулирующего эффекта на крысах.
а) Модифицированное прыжковое испытание [J. Knoll and B. Knoll, Arch. Int. Pharmacodyn. 148, 200, 1964 г. ] .
В ходе проведения данного испытания небольшие дозы амфетамина [до 1-2 мг/кг] улучшают, тогда как повышенные дозы амфетамина [более 3 мг/кг] ухудшают способность к обучению и запоминанию в зависимости от конкретной дозы. Соединений общей формулы I улучшают характеристики в дозировке 0,5 - 15 мг/кг в зависимости от конкретной дозы. Таким образом, новые соединения свободны от ухудшающего эффекта, который характерен в больших дозах для амфетамина вследствие активации серотонергической системы. [Дозы, превышающие 10 мг/кг, рассматриваются как очень большие] .
b) Испытание с челночной камерой (Метод: B. Knoll, J. Knoll; Pol. J. Pharmacol. Pharm. , 34, 17-23, 1982 г. ).
В соответствии с данной методикой испытания ежедневное введение в организм дозы в 1 мг/кг подкожно амфетамина вызывает значительное усиление желания в выработке условного рефлекса и его сохранения в течение тяти дней наблюдения. Однако усиление способности сопровождается неестественно сильной реакцией на промежуточные сигналы. Эффект более высоких доз амфетамина (5-10 мг/кг) даже невозможно оценить в челночной камере вследствие возникновения явления исключительно высокой общей подвижности.
Ежедневное введение в организм 0,5 мг/кг соединения в соответствии с примером 1 позволяет значительно повысить способность по сравнению с контрольным экспериментом без признаков усиления общей подвижности.
Соединение в соответствии с примером 1 усиливало способность к обучению и сохранение навыков с самого первого дня и в течение всего периода испытания даже при введении в организм крайне высокой ежедневной дозы в 15 мг/кг. В то время как способность подопытных животных оказывается необычно высокой, усиление рефлекса на промежуточные сигналы можно рассматривать как умеренное, если принимать во внимание исключительно высокую способность к обучению. Животные, которым соединение в соответствии с примером 1 вводили в организм в дозе 15 мг/кг, полностью сохраняют способность, достигнутую по завершении однонедельного периода обучения, даже спустя 6 недель после завершения курса введения лекарства. В соответствии с результатами упомянутых испытаний соединения изобретения позволяют достичь исключительно резкого эффекта усиления способности к обучению, причем указанный эффект является очень сильным и широким, но достигается по другому механизму в сравнении с механизмом действия амфетамина.
11/3. Определение антагонизма к депрессии, вызванной действием тетрабеназина, в ходе испытаний по обучению крыс.
а) Прыжковое испытание. Метод: J. Knoll, B. Knoll, Arzneimittel Forschung 8, 339, 1958 г. , 9, 633, 1959 г.
Закрепленный условный рефлекс, достигаемый в ходе прыжковых испытаний, не может быть ингибирован соединениями общей формулы I даже в больших дозах [например, в дозе 15 мг/кг соединения в соответствии с примером 8] . Такой рефлекс может быть полностью подавлен только большими дозами тетрабеназина [5 мг/кг] , тогда как депрессивному эффекту тетрабеназина может эффективно противодействовать соединение в соответствии с примером 8 в дозе 15 мг/кг.
b) Испытание с челночной камерой. Метод: B. Knoll, J. Knoll, Pol, J. , Pharmacol. , Pharm. 34, 17 - 23, 1982 г.
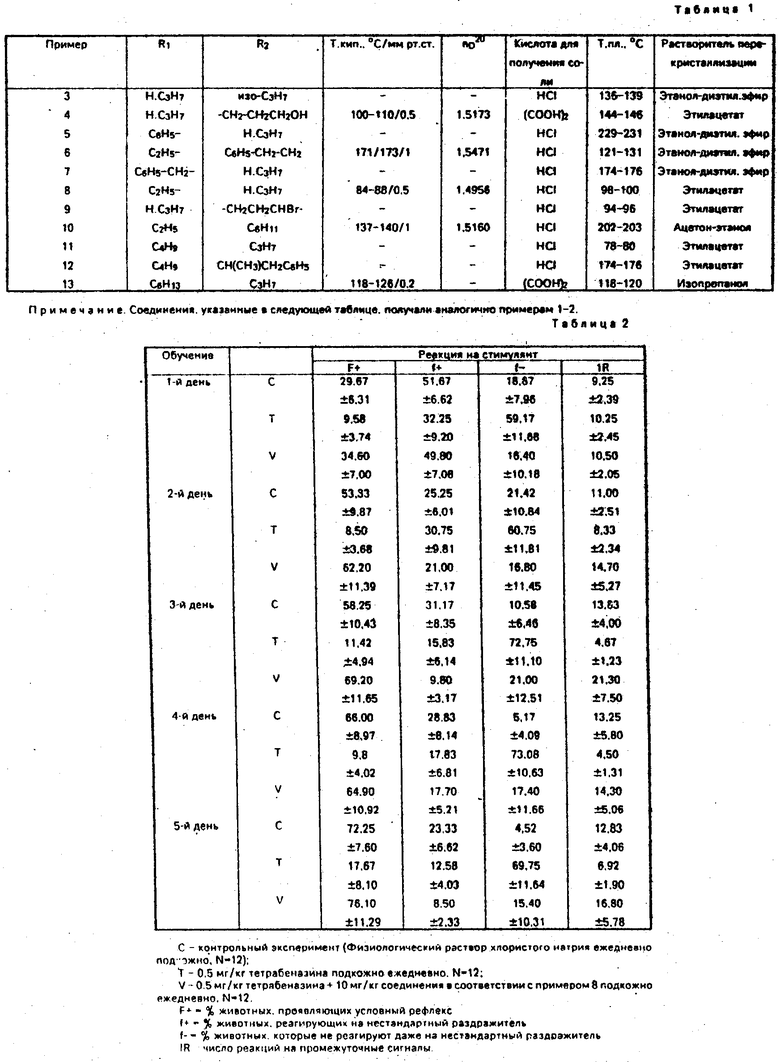
В соответствии с результатами данного испытания депрессии, вызванной тетрабеназином, можно противостоять с помощью соединений общей формулы I. В табл. 2 приведены числовые значения, полученные в ряде испытаний, проведенных с использованием соединения в соответствии с примером 8.
Аналогичные результаты получают при применении соединений в соответствии с примерами 1 и 13.
11/4. Определение эффекта, оказываемого на подвижность крыс.
Испытание проводят в челночной камере без подачи тока и света. Регистрируют и суммируют с помощью прибора число самопроизвольных перемещений от одной стенки камеры до другой в течение 30 мин. Данное испытание проводят с группой животных, которая включает в себя 112 крыс расы CFY обоих полов массой по 180-200 г каждая. Перед началом испытания подкожно животным вводят испытываемое соединение общей формулы I совместно соответственно с тетрабеназином и десметилимипрамином (ДМИ), используемым в качестве сравнительного соединения.
В соответствии с результатами данного испытания, соединения примеров 1 и 8 не повышают подвижность в дозе 10 мг/кг, тогда как соединения примеров 1, 6 и 13 в определенной степени превышают подвижность. Эффекту повышения подвижности, вызванному 1 мг/кг тетрабеназина, заметно противостоит соединение примера 8 в дозе 2,5 мг/кг и полностью противодействует соединение примера 1 уже в дозе 1 мг/кг. В ходе данных испытаний ДМИ проявляет скорее ингибирующий сам по себе эффект, чем антагонистическое действие в отношении депрессии подвижности, вызванной тетрабеназином.
11/5. Определение влияния, оказываемого на метаболизм у крыс.
Метод: B. Issekutz, B. Issekutz, Jr. , Naymyn. Schiedebero 2Arch Pharmac 306, 1942 г.
В ходе проведения данного испытания соединения общей формулы I ускоряют обмен веществ в значительно меньшей степени в течение более короткого периода времени, чем либо амфетамин, либо 1-депренил.
11/6. Определение влияния на потребление пищи у крыс
Введение перорально или подкожно сытым животным при хорошем их кормлении соединения в соответствии с примером 7 в дозе 15 мг/кг не изменяет количества потребляемой ими пищи (амфетамин проявляет аноректический эффект уже в дозе 1 мг/кг). При аналогичной дозе он не оказывает влияния на количество потребляемой пищи крысами, которым на давали есть в течение 96 ч, у которых чувство голода полностью подавляется амфетамином в течение 3-4 ч при дозе 2-5 мг/кг.
Доза в 5 мг/кг соединений в соответствии с примерами 1 и 13 вызывает эффект подавления чувства голода, который приблизительно идентичен эффекту, вызываемому амфетамином в дозе 0,5 мг/кг в течение первого часа.
11/7. Определение ин виво поглощения 3Н-норадреналина надосадочным слоем кортекса крыс (in vivo).
Кортекс гомогенизируют в 0,32 М растворе сахарозы с помощью тефлонового горшочка, ядра клеток седиментируют центрифугированием при температуре 0оС в течение 20 мин в количестве 1000 г. Для испытаний используют выделенный таким образом надосадочный слой. Процесс поглощения проводят в растворе Кребса-Хейнзелейта, насыщенном карбогеном, в конечном объеме 1 мл при концентрации 3Н-норадреналина 5,10-8 мол. Операции прединкубирования и инкубирования проводят при температуре 37оС в течение 5 мин каждую. Реакцию прекращают добавлением 4 мл охлажденного льдом раствора Кребса и ткань отделяют GF/B-фильтрованием. Относительное поглощение определяют с использованием 10-4М раствора низоксетина при температуре 37оС. Радиоактивность GF/B-фильтровальной бумаги определяют измерением сцинтилляции жидкости в смеси толуол-РРО-РОРОР-продукт "тритон".
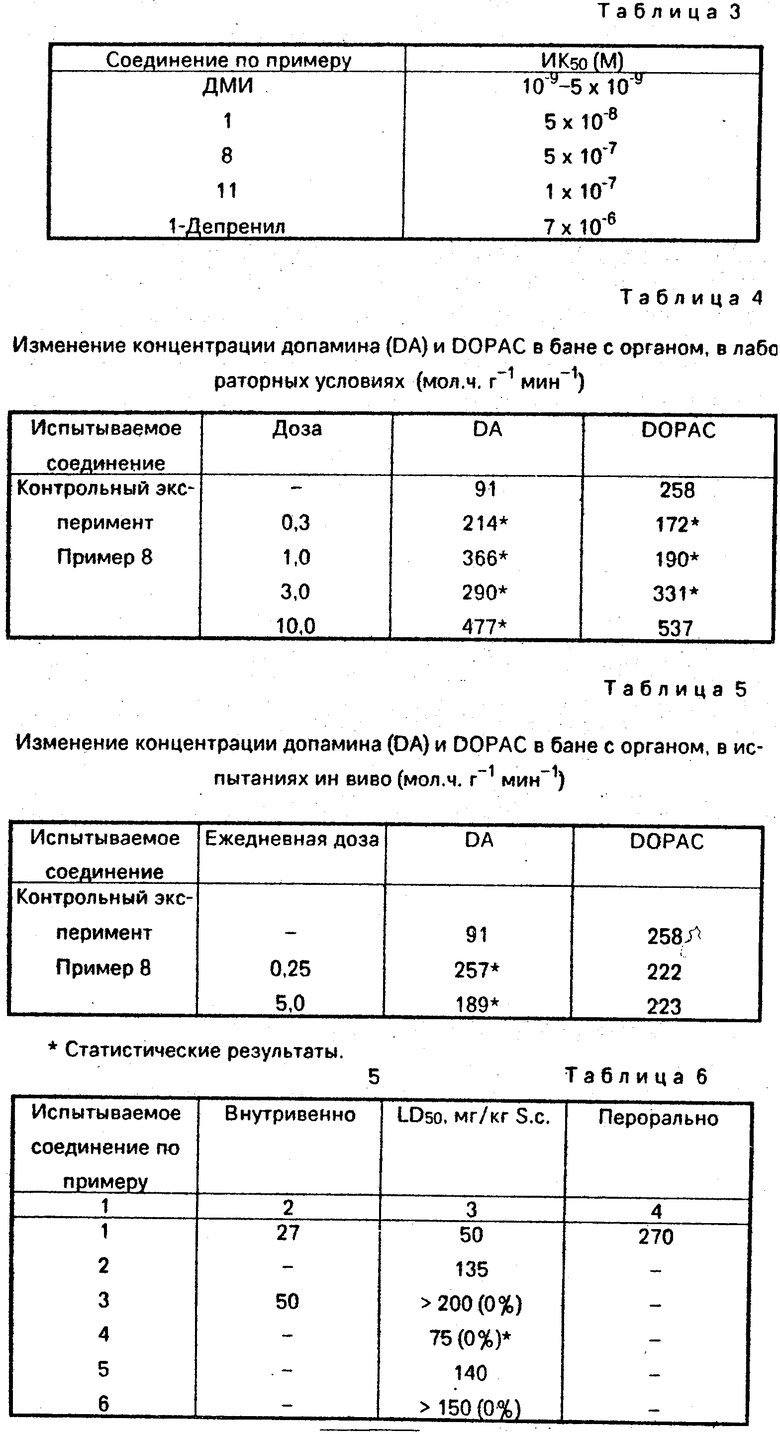
Полученные результаты приведены в табл. 3.
Определение эффекта усиления допаминеринового действия на изолированных крысиных стриатумных препаратах.
Метод: Kerecsen и др. , Chromatography, the State of the Art, (Eds. Kalasz, Ettre) Akademial Kiado Budapest, 1985. , стр. 195-203.
В ходе проведения экс виво испытаний на животных им вводят подкожно в организм соединения в течение 3 недель, а спустя 2 ч после заключительной инъекции орган удаляют.
Полученные результаты сведены в табл. 4 и 5.
11/8. Острая токсичность (на крысах).
Полученные результаты сведены в табл. 6. (56) Байганд-Хильгетаг. Методы эксперимента в органической химии. М. : Химия, 1968, с. 378, 470, 480.
Патент США N 4025624, кл. 424-233, 1977.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛАЛКИЛАМИНОВ ИЛИ СОЛЕЙ ЭТИХ СОЕДИНЕНИЙ | 1990 |
|
RU2015960C1 |
| Способ получения фенилалкиламинов или их фармакологически приемлемых солей | 1988 |
|
SU1746882A3 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ, РАЗВИВАЮЩИХСЯ ВСЛЕДСТВИЕ НЕЙРОДЕГЕНЕРАТИВНЫХ ПРОЦЕССОВ | 1992 |
|
RU2125448C1 |
| АНТИМИКРОБНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2030913C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ | 1988 |
|
RU2014331C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОВЫХ КИСЛОТ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1988 |
|
RU2049783C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧИСТЫХ ИЗОФЛАНОВЫХ ПРОИЗВОДНЫХ | 1991 |
|
RU2036918C1 |
| КЛАТРАТ 7-ИЗОПРОПОКСИИЗОФЛАВОНА И ЦИКЛОДЕКСТРИНОВОГО ПОЛИМЕРА, ПРОЯВЛЯЮЩИЙ АКТИВНОСТЬ ПРОТИВ ОСТЕОПОРОЗА И ОСТЕОМАЛЯЦИИ | 1987 |
|
RU2022970C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ФЕНИЛГУАНИДИНА И ПРОИЗВОДНЫЕ СУЛЬФОКИСЛОТЫ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ В СИНТЕЗЕ ПРОИЗВОДНЫХ ФЕНИЛГУАНИДИНА | 1991 |
|
RU2015963C1 |
| РАЦЕМИЧЕСКИЕ ИЛИ ОПТИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ | 1991 |
|
RU2090559C1 |

Использование: в фармацевтической промышленности как соединения, обладающие способностью стимулировать центральную нервную систему. Сущность изобретения: способ получения фенилалкиламинов общей формулы: 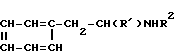 где R1 - прямой или разветвленный алкил (C2-C8), фенилалкил (C7-C10), фенил или циклоалкил (C3-C8), R2 - группа
где R1 - прямой или разветвленный алкил (C2-C8), фенилалкил (C7-C10), фенил или циклоалкил (C3-C8), R2 - группа 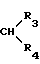 где R3 - Н или алкил (C1-C7), который может быть замещен галогеном, гидроксилом, алкокси-группой C1-C4, или фенил - C2 - алкил, R4 - водород, или группа -
где R3 - Н или алкил (C1-C7), который может быть замещен галогеном, гидроксилом, алкокси-группой C1-C4, или фенил - C2 - алкил, R4 - водород, или группа - 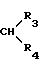 вместе означает циклоалкильное кольцо C3-C8 при условии, что группы R1 и R2 совместно содержат по меньшей мере 5 углеродных атомов и, в том случае, когда R1 - этил, R2 не может обозначать изобутил, или их фармакологически приемлемых солей. Реагент 1: амин - C6H15-CH2CHR1NH2. Реагент II:
вместе означает циклоалкильное кольцо C3-C8 при условии, что группы R1 и R2 совместно содержат по меньшей мере 5 углеродных атомов и, в том случае, когда R1 - этил, R2 не может обозначать изобутил, или их фармакологически приемлемых солей. Реагент 1: амин - C6H15-CH2CHR1NH2. Реагент II: 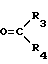 . Процесс ведут в присутствии восстановителя, такого, как амальгама алюминия, газообразный водород и металлический катализатор гидрирования, боргидрид щелочного металла. 8 табл.
. Процесс ведут в присутствии восстановителя, такого, как амальгама алюминия, газообразный водород и металлический катализатор гидрирования, боргидрид щелочного металла. 8 табл.
Способ получения фенилалкиламинов общей формулы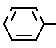 CH2-
CH2-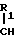 -NHR2
-NHR2
где R1 - прямой или разветвленный алкил C2 - C8, фенилалкил C7 - C10, фенил или циклоалкил C3 - C8;
R2 - группа
-CH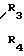
где R3 - водород или алкил C1 - C7, который может быть замещен галогеном, гидроксилом, алкоксигруппой C1 - C4 или фенилалкилом C2,
R4- водород или группа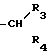
месте - циклоалкильное кольцо C3 - C8, при условии, что группы R1 и R2 совместно содержат по меньшей мере 5 атомов углерода, и в том случае, когда R1 - этил, R2 не может обозначать изобутил, или их фармакологически приемлемых солей, отличающийся тем, что амин общей формулы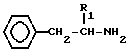
де R1 имеет указанные значения,
подвергают взаимодействию с соединением общей формулы
O C
C
где R3 и R4 имеют указанные значения,
в присутствии восстановителя, такого, как амальгама алюминия, газообразный водород и металлический катализатор гидрирования, боргидрид щелочного металла, с последующим выделением целевого продукта в виде свободного основания или фармакологически приемлемой соли.
Авторы
Даты
1994-02-15—Публикация
1989-11-23—Подача