Изобретение относится к медицине, в частности к клинической биохимии, и может быть использовано в медицинской практике при изучении биохимических показателей крови в клинике и эксперименте.
Известны способы депротеинизации крови при ферментативном определении глюкозы, включающие использование осаждающих реактивов: гидроксида цинка, хлорной кислоты или трихлоруксусной кислоты.
Однако все эти методы неудобны (трудоемки) в плане практического применения для проведения массовых анализов. При использовании гидроксида цинка осаждение форменных элементов и белков цельной крови происходит в слабощелочной среде, что обеспечивает специфичность ферментативной реакции и достаточно высокую точность определения глюкозы, однако требует использования только свежеприготовленного реактива (т.е. в каждой пробирке непосредственно перед забором крови готовят суспензию гидроксида цинка, сливая растворы сульфата цинка и гидроксида натрия). При использовании хлорной и трихлоруксусной кислот из-за неблагоприятного воздействия кислой среды на ферментативную реакцию для обеспечения достаточной точности определения глюкозы необходимо вводить дополнительную стадию доведения pH реакционной смеси до значений 7,0-8,4.
Наиболее близким техническим решением к изобретению является способ депротеинизации цельной капиллярной крови с использованием в качестве осаждающего реактива 0,0037 М раствора уранилацетата, который практически не влияет на pH среды и не требует специального приготовления.
Однако данный метод не дает достаточно высокой точности при использовании глюкозооксидазно-пероксидазного определения глюкозы. Кроме того, уранилацетат является радиоактивным и труднодоступным реактивом, а точность определения глюкозы при его использовании существенно зависит от состава ферментативной системы.
Целью изобретения является повышение точности определения глюкозы.
Поставленная цель достигается способом депротеинизации цельной капиллярной крови при ферментативном определении глюкозы, включающим добавление осаждающего форменные элементы крови реактива и отделение осадка, при этом в качестве реактива используют 0,1-0,4 М перхлорат лития в физиологическом растворе.
Раствор перхлората лития не влияет на pH среды, устойчив в течение трех месяцев хранения при 4-8оС и в течение месяца при комнатной температуре, не обладает ингибирующим действием по отношению к ферментативным системам определения глюкозы, включая ферментативный реактив фирмы Lachema, Labsystems и используемый в отечественной клинической практике.
П р и м е р 1. Определение содержания глюкозы в сыворотках с известной концентрацией в присутствии депротеинирующего реактива.
К 20 мкл сыворотки, содержащей известную концентрацию глюкозы (5,2 мМ), приливают 200 мкл депротеинирующего реактива (0,2 М перхлорат лития в 0,9% -ном растворе NaCl либо 0,0037 М раствор уранилацетата, либо суспензию: 200 мкл 0,45% сульфат цинка в смеси с 40 мкл 0,1 M NaOH, либо 0,33 М раствор хлорной кислоты), затем перемешивают, суспензию центрифугируют при 15000 об/мин в течение 6 или 15-20 мин при 5000-6000 об/мин (осадок должен быть плотным). Затем к 100 мкл супернатанта добавляют 1000 мкл ферментного реактива, рекомендованного для отечественной клинической практики, состоящего из глюкозооксидазы 18 ед/мл, пероксидазы 1 ед/мл, 4-аминоантипирина 0,72 мМ, фенола 11 мМ, фосфатного буфера pH 7,0, перемешивают и инкубируют смесь при комнатной температуре в течение 40 мин. Одновременно таким же образом обрабатывают 10 мМ раствор глюкозы (эталон). После инкубации измеряют оптическую плотность А пробы и эталона против контрольного раствора и концентрацию глюкозы в пробе рассчитывают по формуле:
глюкоза мМ = 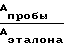 × 10 ..
× 10 ..
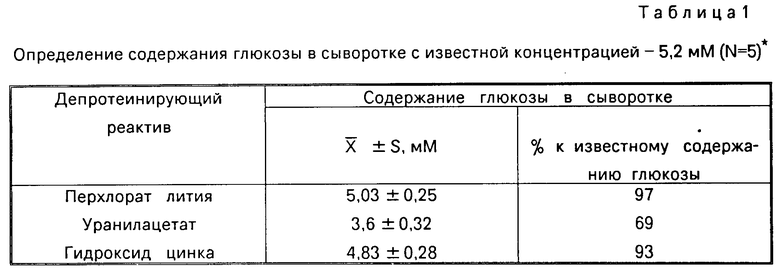
Результаты приведены в табл.1.
Как видно из табл. 1, при определении глюкозы в контрольной сыворотке наиболее точные результаты получены при использовании в качестве депротеинирующего реактива перхлората лития.
П р и м е р 2. Оценка воспроизводимости определения глюкозы предлагаемым методом.
Определение содержания глюкозы ведут в одном эталонном растворе глюкозы с концентрацией 10 мМ (эталон приготовлен в 0,2%-ной бензойной кислоте из глюкозы, высушенной до постоянного веса при 37оС) ежедневно в течение 10 дней аналогично описанному в примере 1. По данным анализа рассчитывают среднее арифметическое 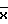 , среднеквадратичное отклонение S и коэффициент вариации V. Результаты представлены в табл.2.
, среднеквадратичное отклонение S и коэффициент вариации V. Результаты представлены в табл.2.
Как видно из табл.2, коэффициент вариации для перхлората лития не превышает 4%, в то время как для уранилацетата эта величина равна 8%, что свидетельствует о более высокой точности предлагаемого способа определения глюкозы.
П р и м е р 3. Определение содержания глюкозы в цельной капиллярной крови здоровых лиц и больных сахарным диабетом.
К 200 мкл депротеинирующего реактива (см. пример 1) добавляют 20 мкл цельной капиллярной крови (для определения глюкозы пробы крови берутся непосредственно из пальца), перемешивают и центрифугируют. Дальнейшее определение ведут аналогично описанному в примере 1. Результаты представлены в табл.3.
Как видно из табл. 3, величина доверительного интервала концентраций глюкозы при определении у здоровых лиц с помощью перхлората лития соответствует общепринятым нормам для глюкозооксидазного метода - 3,5-5,7 мМ. Для уранилацетата и хлорной кислоты определенное количество глюкозы соответственно достоверно занижает или превышает определяемую величину. Перхлорат лития правильно определяет содержание глюкозы и в крови больных сахарным диабетом (сравнение величин концентраций глюкозы, полученных при использовании перхлората лития и суспензии гидроксида цинка, показывает отсутствие достоверных различий).
П р и м е р 4. Определение содержания глюкозы в одной порции цельной крови различными глюкозооксидазно-пероксидазными методами.
Определение глюкозы ведут в одной порции цельной венозной крови, к которой для предотвращения свертывания добавляют 3,8%-ный раствор цитрата натрия (1 ч. раствора цитрата натрия и 9 ч. крови по объему), перемешивают. К 20 мкл крови добавляют 200 мкл раствора депротеинирующего реактива, перемешивают и центрифугируют. Далее определение глюкозы ведут аналогично описанному в примере 2. При этом в качестве ферментативной системы используют либо рекомендованную для отечественной клинической практики (см. пример 1), либо набор готовой аналитической формы фирмы Lachema, либо Labsystems. (Набор фирмы Lachema: глюкозооксидаза - 4 ед/мл, пероксидаза - 1 ед/мл, 4-аминоантипирин - 0,8 мМ, 4-хлор-3-крезол-0,6 мМ, буфер pH 8,4; набор фирмы Labsystems: глюкозооксидаза - 20 ед/мл, пероксидаза - 10 ед/мл, 4-аминоантипирин - 0,6 мМ, п-гидроксибензолсульфонат - 20 мМ, фосфатный буфер pH 7,0). Результаты представлены в табл.4.
Как видно из табл.4, перхлорат лития позволяет получать правильные результаты по определению глюкозы при использовании различных ферментативных методов.
П р и м е р 5. Выбор оптимального интервала концентраций перхлората лития.
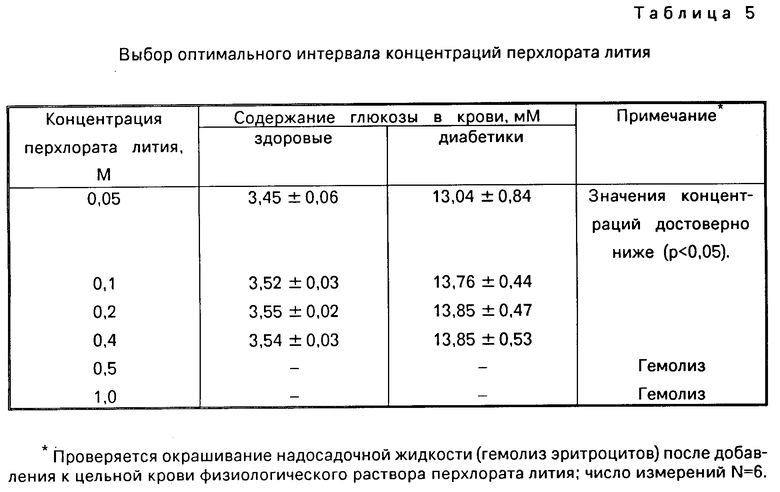
Определение глюкозы ведут в одной порции цельной венозной крови аналогично описанному в примере 4, используя отечественный ферментативный набор реактивов (см. пример 1) и меняя концентрацию перхлората лития от 0,05 М до 1,0 М. Результаты представлены в табл.5.
Как видно из табл.5, оптимальный интервал концентраций перхлората лития составляет 0,1-0,4 М. При значениях ниже 0,1 М определяемые величины концентраций достоверно ниже (p<0,05) значений, определяемых в оптимальном интервале. При значениях выше 0,4 М наблюдается гемолиз эритроцитов (красное окрашивание), мешающий проведению анализа.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕАКТИВ ДЛЯ ОПРЕДЕЛЕНИЯ ГЛЮКОЗЫ В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1991 |
|
RU2009499C1 |
| Реагент для определения концентрации глюкозы в сыворотке крови | 1990 |
|
SU1776692A1 |
| Способ иммобилизации фрагментов нуклеиновых кислот на полимерной подложке | 1991 |
|
SU1808014A3 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pUR 290 S ΔE, КОДИРУЮЩАЯ ГИБРИДНЫЙ ПОЛИПЕПТИД β -ГАЛАКТОЗИДАЗА-NS 1-БЕЛОК ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА, И СПОСОБ ЕЕ КОНСТРУИРОВАНИЯ | 1989 |
|
RU1679798C |
| СПОСОБ ПОЛУЧЕНИЯ 1 -> 3, 1 -> 6-БЕТА-D-ГЛЮКАНА, ОБЛАДАЮЩЕГО ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1993 |
|
RU2095417C1 |
| 3'-ФОСФАТ, N, P-НЕЗАЩИЩЕННЫЕ ФОСФОТИОАТНЫЕ ОЛИГОДЕЗОКСНУКЛЕОТИДЫ В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ ФОСФОТИОАТНЫХ, ОЛИГОНУКЛЕОТИДНЫХ РЕАГЕНТОВ ДЛЯ БИОТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ, ФОСФОТИОАТНЫЕ ОЛИГОНУКЛЕОТИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ 3'- И/ИЛИ 5'-СВЯЗАННЫЕ ХИМИЧЕСКИЕ ГРУППИРОВКИ В КАЧЕСТВЕ ФОСФОТИОАТНЫХ ОЛИГОНУКЛЕОТИДНЫХ РЕАГЕНТОВ ДЛЯ БИОТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2069214C1 |
| Н-ФОСФОНАТЫ ГИДРОКСИЛСОДЕРЖАЩИХ СТЕРОИДОВ В КАЧЕСТВЕ РЕАГЕНТА ДЛЯ ТВЕРДОФАЗНОГО СИНТЕЗА СТЕРОИДНЫХ ПРОИЗВОДНЫХ ОЛИГОНУКЛЕОТИДОВ ИЛИ ИХ АНАЛОГОВ | 1991 |
|
RU2009147C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОТИНМЕЧЕННЫХ ОЛИГОДЕЗОКСИРИБОНУКЛЕОТИДОВ | 1994 |
|
RU2083584C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ГЕНОМНОЙ ДНК ИЗ КЛЕТОК МИКРООРГАНИЗМОВ | 2000 |
|
RU2177035C2 |
| СПОСОБ ДЕТЕКЦИИ РНК ВИРУСА ГЕПАТИТА А | 1992 |
|
RU2031126C1 |

Использование: в медицине, в клинической биохимии. Цель: повышение точности способа. Сущность изобретения: используют для депротеинизации 0,1 - 0,4 М перхлорат лития в физиологическом растворе при применении глюкозооксидазно-пероксидазного определения глюкозы. Положительный эффект: применение способа позволяет на 4% повысить точность способа. 5 табл.
СПОСОБ ДЕПРОТЕИНИЗАЦИИ ЦЕЛЬНОЙ КАПИЛЛЯРНОЙ КРОВИ ПРИ ФЕРМЕНТАТИВНОМ ОПРЕДЕЛЕНИИ ГЛЮКОЗЫ, включающий добавление осаждающего форменные элементы крови реактива и отделение осадка, отличающийся тем, что, с целью повышения точности способа, при использовании глюкозоксидазно-пероксидазного метода определения глюкозы в качестве реактива применяют 0,1 - 0,4 М перхлорат лития в физиологическом растворе.
| Инструкция по применению набора реактивов для определения глюкозы фирмы ЛаХеМа, ЧССР. |
Авторы
Даты
1994-08-30—Публикация
1990-01-11—Подача