Изобретение относится к органической химии, конкретно к производным нитроглицерина, а именно алкокситринитратгептантриолов общей формулы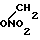 -
-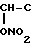 H2O-CH
H2O-CH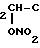 H2OR обладающих кардиотонической активностью, что предполагает применение их в медицинской практике. Заявляемые соединения в литературе не описаны.
H2OR обладающих кардиотонической активностью, что предполагает применение их в медицинской практике. Заявляемые соединения в литературе не описаны.
В настоящее время наиболее применяемыми препаратами для этой цели являются сердечные гликозиды (строфантин, дигоксин) и адреномиметики. Эти препараты, проявляя высокую активность (10-6 м/л) являются высокотоксичными, обладают кумулятивным действием и другими побочными эффектами. Поиск новых кардиотоников негликозидного происхождения ведется, как правило, среди синтетических веществ различных классов [1, 4].
Наиболее близким аналогом по химической структуре является нитроглицерин, вызывающий выраженную разгрузку сердца и улучшение коронарного кровообращения, а также обладающий кардиoстимулирующим действием (увеличение сократимости миокарда на 22% в концентрации 10-4 м/л [2]. Вместе с тем, кратковременность действия нитроглицерина (до 15 мин), выраженная гипотензивная реакция и слабый кардиотропный эффект, не позволяют использовать его в клинике в качестве кардиотонического средства [3].
Целью изобретения является поиск новых производных нитроглицерина, обладающих более высокой кардиотонической активностью и низкой токсичностью по отношению к теплокровным животным.
Поставленная цель достигается модификацией молекулы нитроглицерина с удлинением углеродной цепи, введением липофильной алкоксифторсодержащей группы и кислородного мостика между атомами углерода. Последнее дало возможность в молекуле заявляемых соединений удалить одну от другой нитрогруппы. В результате были синтезированы заявляемые соединений (V, а, б), проявляющие выраженные кардиотонические свойства.
Заявляемые соединения получают по следующей схеме: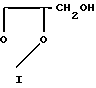 +
+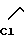
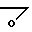
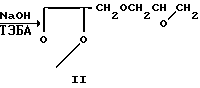
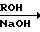
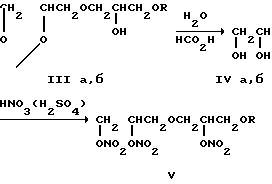 CH2OCH
CH2OCH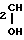 CH2OR где R = CH2CF3(a), R = CH2CF2CHF2 (б).
CH2OR где R = CH2CF3(a), R = CH2CF2CHF2 (б).
По приведенной выше схеме α -этилиденглицериновый эфир (I) в присутствии едкого натра и триэтилбензиламмония хлорида (ТЭБА) реагирует с эпихлоргидрином, превращаясь в эпоксид (II), который при действии спиртов раскрывается с образованием соединений (III). Изопропилиденовая защита вицинальных диольных групп снимается при нагревании спирта (III) с разбавленной муравьиной кислотой. При этом образуются триолы (IV), которые при нитровании нитрующей смесью дают целевые продукты (V, а, б).
П р и м е р 1. Синтез 1,2 изопропилиден-4-окса-6,7- эпоксигептандиола (II).
К смеси 40 г (1 моль) NaOH, 92,5 г (1 моль) эпихлоргидрина, 2 г ТЭБА и 10 мл воды прибавляют при перемешивании при 40-45оС в течение 30 мин 26,4 г (0,2 моль) α -глицеринового эфира (I), после чего перемешивают при 35оС 2 ч. Реакционную смесь охлаждают, соли растворяют добавлением к смеси 100 мл воды. Отделившийся слой экстрагируют эфиром, упаривают и перегоняют.
Выход 27,5 (73%) эпоксида (II); т.кип. 113-115оС; n20D 1,4405,
Найдено, %: С 57,42; Н 8,53.
С9Н16О4.
Вычислено, %: С 57,43; Н 8,57.
П р и м е р 2. Синтез 1-(1,1,1-трифторэтилокси)-2-гидрокси-4-окса-6,7-изопропи- лиденгептан (III а).
Смесь 27,5 г (0,146 моль) эпоксида (II), 30 г (0,3 моль) трифторэтанола, 50 мл 10% -ного NaOH перемешивают при 80оС 4 ч. Реакционную смесь охлаждают, экстрагируют эфиром, сушат К2СО3, эфир и избыток трифторэтанола отгоняют, остаток перегоняют. Выход 30 г (71%) спирта (III a). т.кип. 147-150оС (10 мм рт.ст.).
Найдено, %: С 45,78; Н 6,65; F 19,68.
C11H19F3O5
Вычислено, %: С 45,89; Н 6,59; F 19,79.
Аналогично получают спирт (III б). Выход 73%, т.кип. 108-110оС/0,1 мм рт.ст.
Найдено, %: C 44,68; H 6,18; F 24,13.
C12H20O5F4
Вычислено, %: C 45,00; H 6,29; F 23,73.
П р и м е р 3. 1-(1,1,1-Трифторэтилокси)-4-окса-2,6,7-тригидроксигептан (IV a).
Смесь 30 г (0,4 моль) спирта (III a), 20 мл воды и 3 мл 85%-ной муравьиной кислоты перемешивают при 90оС 4 ч до полной гомогенизации реакционной смеси, после чего упаривают в вакууме, а остаток перегоняют. Выход 18,6 г (72%), т.кип. 148-150оС/0,07 мм рт.ст.; n20D 1,4203.
Найдено, %: C 38,67; 6,02; F 22,89.
C8H15F3O5
Вычислено, %: С 38,70; Н 6,09; F 22,98.
Спектр ПМР (ГМДС, d6-ацетон): 4,2 м (1Н, СН); 4,0 м (2Н, СН2); 3,85 м (1Н, СН); 3,67 м (3Н, СН); 3,62 т (2Н, ОСН2CF3); 3,46 м (6Н, 30СН2). ИК спектр (пленка, см-1): 3300 (ОН).
Аналогично получают тригидроксигептан (IV б). Выход 78%; т.кип. 150-152оС/0,07 мм рт.ст.).
Найдено, %: C 38,24; H 5,70; F 27,57.
C9H16F4O5
Вычислено, %: C 38,29; H 5,67; F 27,65.
ПМР спектр (ГМДС, d6-ацетон): 6,05; 6,26; 6,53 три триплета (1Н, CF2CF2H); 4,3 м (1Н, СН); 4,08 (1Н, СН); 3,9 (2Н, СН2); 3,7 м (3Н, ОН); 3,64 т (2Н, ОСН2CF2CF2), 3,48 м (6Н, 30СН2).
ИК спектр: (пленка, см-1). 3300 (ОН).
П р и м е р 4. Синтез 1-(1,1,1-трифторэтилокси)-4-окса-2,6,7-тринитратгептантри-ола (V, а).
К 40 мл охлажденной до 5оС Н2SO4 при перемешивании прибавляют 13,26 мл 95% -ной HNO3 (уд. вес 1,5), так чтобы температура была не выше 10оС. После прибавления всей HNO3 смесь перемешивают при 10оС 5 мин, затем прибавляют 12,4 г (0,05 моль) соединения (IV a) в течение 10 мин при 10-15оС. Затем смесь перемешивают при этой температуре 40 мин. Органический слой отделяют, промывают 3 раза по 50 мл воды; затем 2 раза по 50 мл 3%-ным раствором NaHCO3, водой, 3 раза по 30 мл нагретым до 40оС 5%-ным раствором этанола. Органический слой отделяют, растворяют в эфире сушат MgSO4, эфир упаривают. Выход 13,4 г (70%) целевого тринитрата (V а). n20D 1,4328.
Найдено, %: С 25,06; Н 3,10; N 10,90; F 14,75
C8H12F3N3O11
Вычислено, %: С 25,07; Н 3,15; N 10,96; F 14,87.
ПМР спектр (ГМДС, d6-ацетон): 5,61 (1Н, СН); 5,45 м (1Н, СН); 4,71-4,81 квартет, 4,92-5,00 дублет дублетов (2Н; СН2ONO2); 4,05 т (2Н; ОСН2CF3); 3,84-3,96 (4Н, СН2ОСН2 2Н СН2ОСН2CF3).
ИК спектр: (пленка, см-1) 1630 (ONO2). 1000-1100 (C-F). Аналогично при нитровании триола (IV б) получают с выходом 75% тринитрат (V б). n20D 1,4318.
Найдено, %: С 25,94; Н 3,13; N 10,05; F 18,20
C9H13N3F4O11
Вычислено, %: С 26,03; Н 3,15; N 10,11; F 18,30
ИК спектр (пленка, см-1): 1630 (ONO2), 1000-1100 (С-F).
Спектр ПМР (ГМДС, d6-ацетон): 5,95; 6,22; 6,48 три триплета (1Н, CF2CF2H); 5,63 м (1Н, СН); 5,46 м (1Н, СН); 4,73-5,00 м 2Н, CH2ONO2); 4,06 т (2Н, ОСH2CF2CF2); 3,84-3,91 м (6Н, СН2ОСН2).
П р и м е р 5. Исследование кардиотропных свойств предлагаемых соединений.
Влияние данных соединений и эталонных препаратов на сократимость миокарда оценивали в экспериментах на изолированном миокарде, сокращающемся в изометрическом режиме под действием электрической стимуляции. Папиллярную мышцу левого желудочка крыс помещали в проточную камеру и перфузировали оксигенированным раствором Тироде (95% 02 и 5% СО2) при 29оС. Электрическую стимуляцию осуществляли с помощью платиновых электродов, расположенных параллельно мышце. Использовали импульсы прямоугольной формы от электростимулятора КЗМО длительностью 5 мс, напряжением, превышающем пороговое на 10-25% с частотой 1 Гц. Для оценки сократительной способности миокарда использовали показатели развиваемого напряжения (Т, мг) и скорость развития и спада напряжения (dT/dt, мг/с). Регистрацию осуществляли на Polygraph System-6000 (Япония) при скорости записи 1 и 25 мм/с. Перфузию мышц проводили раствором Тироде с содержанием соединений V а, б или эталонного препарата в концентрациях от 10-8 до 10-4 м на 1 л. Для растворения соединения использовали 1-2 мл полиэтиленгликоля-300 (Loba Feinchemie Austranal) с последующей обработкой ультразвуком на аппарате УЗДМ-2Т. В перфузируемом растворе содержание растворителя составляло не более 1:100 и не оказывало влияния на сократимость миокарда. Сравнение проводили с аналогами по структуре - нитроглицерином и по действию - строфантином. Результаты экспериментов приведены в таблице.
Влияние соединений V а, б и нитроглицерина и строфантина на сократимость миокарда
Представленные в таблице данные показывают, что заявляемые соединения Va и Vб проявляют выраженные кардиотонические свойства, увеличения сократимость миокарда в концентрациях 10-7 м/л на 20-60%, причем соединение V а проявляет несколько большую активность, по сравнению с V б. Наиболее распространенным в настоящее время кардиотоником является гликозид природного происхождения строфантин. При сравнительном анализе кардиотонического действия строфантина и заявляемых соединений, установлено, что активность соединения Va превышает активность строфантина, а соединения V б несколько ниже активности строфантина. Однако следует признать, что оба заявляемых соединения обладают достаточно высокой кардиостимулирующей активностью при низкой токсичности. В результате проведенных фармакологических исследований установлено ЕС50, м/л: Va 1 ˙ 10-6 Vб 1 ˙ 10-5 Строфантин 8 ˙ 10-6
Вышеизложенные данные позволяют заключить, что соединения Va и Vб являются высокоактивными кардиотоническими соединениями, синтетического происхождения.
П р и м е р 6. Изучение токсичности.
Исследование токсичности соединений проводили на белых беспородных мышах массой 20-25 г. Заявляемые соединения и эталонные препараты вводили внутрижелудочно в дозах от 10 до 3000 мг/кг массы тела. Учет проводили в течение 24 ч с последующим наблюдением в течение 10 сут после введения. Результаты опытов подвергали статистической обработке по методу Личфилда-Уилкинсона в модификации Рота.
Результаты испытаний выявили следующую токсичность: LD50 строфантина 17 мг/кг; LD50 соединений а, б составляла 2000 мг/кг.
Смертельная доза нитроглицерина внутрь для кошек - 6 мг, для кролика - 2 мг.
Таким образом, предлагаемые соединения обладают значительно меньшей токсичностью, по сравнению с препаратом подобного типа действия - строфантином - и могут быть отнесены к нетоксичным соединениям.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2,6-ДИМЕТИЛ -3,5-БИС (АЛКОКСИКАРБОНИЛ) -4-[ПОЛИФТОРАЛКОКСИ(МЕТОКСИ) -ФЕНИЛ] -1,4-ДИГИДРОПИРИДИНЫ, ПРОЯВЛЯЮЩИЕ КАРДИОТОНИЧЕСКОЕ И ГИПЕРТЕНЗИВНОЕ ДЕЙСТВИЕ | 1992 |
|
RU2036907C1 |
| 4,5-ДИМЕТИЛ-2-Н-ПРОПИЛТИО-2-ω-Н-ПЕРФТОРБУТИЛ -3Н, 6Н-ТИАИН, ОБЛАДАЮЩИЙ ИНОТРОПНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2054426C1 |
| 3-ОКСОТИАЗОЛИДИНО [3,2-A] ПИПЕРАЗИНЫ ИЛИ ИХ ГИДРОХЛОРИДЫ, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1991 |
|
SU1823452A1 |
| 1S,3R-2,2-ДИМЕТИЛ-3-(2-МЕТИЛ-2-ОКСИПРОПИЛ)ЦИКЛОПРОПАНКАРБОНИТРИЛ В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ В СИНТЕЗЕ ПИРЕТРОИДНОГО ИНСЕКТИЦИДА-ДЕЛЬТАМЕТРИНА И СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ | 1989 |
|
RU1679761C |
| Ациклические @ -изопреноидные кетоацетали в качестве синтонов полипренолов | 1981 |
|
SU1026415A1 |
| ДИГИДРОХЛОРИДЫ N-[β-(1,2,5-ТРИМЕТИЛ-4-АРИЛПИПЕРИДИН-4-ИЛ)ЭТИЛ]-N-АЛКИЛ-N-(3,4-ДИМЕТОКСИБЕНЗИЛ)АМИНОВ, ЯВЛЯЮЩИЕСЯ ИНГИБИТОРАМИ КАЛЬЦИЙ-КАЛЬМОДУЛИНЗАВИСИМЫХ ПРОЦЕССОВ | 1991 |
|
SU1829346A1 |
| Дихлорметилацетилены как промежуточные продукты для получения 1-хлор-1-алкинилциклопропанов и способ их получения | 1982 |
|
SU1131174A1 |
| Способ получения изоцианатов | 1988 |
|
SU1555325A1 |
| 1,1-Диацетоксиалкан-4-оны в качестве промежуточных продуктов в синтезе 2-замещенных циклопент-2-енонов | 1987 |
|
SU1520062A1 |
| Способ получения 1-пропионилокси-3,7-диметилокта-2 @ ,7-диена | 1982 |
|
SU1155579A1 |
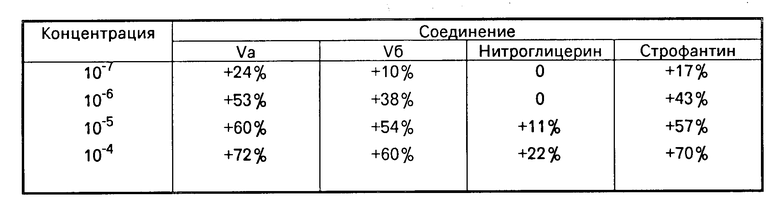
Использование изобретения: в качестве кардиотонического средства в медицине. Сущность изобретения: продукт - 7-алкокси-4-окса-1,2,6-тринитратгептантриол ф-лы CH(ONO)2CH(ONO2)CH2OCH2CH(ONO2)CH2OR , указано R; БФ; n
7-АЛКОКСИ-4-ОКСА-1,2,6-ТРИНИТРАТГЕПТАНТРИОЛЫ, ОБЛАДАЮЩИЕ КАРДИОТОНИЧЕСКОЙ АКТИВНОСТЬЮ.
7 - Алкокси-4-окса-1,2,6-тринитратгептантриолы общей формулы I: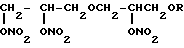
где Ia) R = CH2CF3;
Iв) R = CH2CF2CHF2,
обладающие кардиотонической активностью.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Братусь В.В., Безусько А.Г | |||
| Влияние нитроглицерина на сократимость миокарда при различном его кислородном обеспечении | |||
| Физиологич | |||
| фурнал СССР им.И.М.Сеченова, т.74, N8, с.390-395. | |||
Авторы
Даты
1995-01-27—Публикация
1991-06-24—Подача