Изобретение относится к способам получения биологически активных 5-хлор-2-аминозамещенных бензгидрилмочевин, эффективно действующих на монокооксигеназную систему печени и проявляющих высокую антигипоксическую активность.
Известен способ получения галогензамещенных бензгидрилмочевин, обладающих высокой противосудорожной активностью /1/, путем взаимодействия соответствующих бензгидриламинов с нитромочевиной в водной среде с выходом до 70%.
Недостатками приведенного способа получения проявляются в том, что исходные бензгидриламины являются малодоступными веществами, а также нитромочевина не выпускается крупнотоннажной промышленностью.
Известен способ получения м-хлорбензгидрилмочевины (оригинального отечественного антиконвульсанта "галодиф") реакцией м-хлорбензгидрилформамида с мочевиной в водном растворе в присутствии соляной кислоты при 135-140оС с выходом 89% /2/
Сравнительно высокая температура ведения процесса и использование относительно труднодоступного производного дифенилметана в качестве органического субстрата, вызывают неудобства для промышленного освоения способа получения.
Наиболее близким по технической сущности к заявляемому изобретению является способ получения монозамещенных бензгидрилмочевин /3/, взятый за прототип, который заключается в том, что 0,045 моля бензгидрола и 0,27 моля мочевины в среде уксусной кислоты в присутствии 0,19 молей серной кислоты конденсируют с образованием бензгидрилмочевин с выходами 78-92%.
Однако этот достаточно простой способ получения бензгидрилмочевин оказался неприемлемым для осуществления конденсации мочевины именно с 5-хлор-2-аминобензгидролами с целью получения соответствующих 5-хлор-2-аминобензгидрилмочевин, так как в этом случае наряду с целевыми продуктами в значительной степени образуются 5-хлор-2-аминобензгидроловые эфиры уксусной кислоты, а также продукты гетероциклизации по орто-аминогруппам (производные "4-фенил-тетрагидрохиназолинона).
Целью изобретения является разработка метода синтеза 5-хлор-2-аминозамещенных бензгидрилмочевин и упрощение способа получения.
Согласно изобретению, поставленная цель достигается тем, что мочевину и серную кислоту (d=1,84) предварительно выдерживают в течение 10-15 мин при 75-90оС, к полученной смеси добавляют 5-хлор-2-аминозамещенные бензгидролы, после чего расплав перемешивают 6 ч при следующих молярных соотношениях реагентов : 5-хлор-2-аминозамещенные бензгидролы : мочевина : серная кислота =1:(8-9):(4-4,3).
П р и м е р 1. В трехгорлую колбу, снабженную обратным холодильником, мешалкой и термометром, загружают 7,7 г (0,13 молей) мочевины и 3,4 (0,064 моля) серной кислоты (d=1,84) и перемешивают в течение 10 мин, после чего добавляют 4 г (0,016 моль) 5-хлор-2-N-метиламинобензгидрола и нагревают при 80оС 6 ч. Конец реакции определяют по исчезновению пятна 5-хлор-2-N-метиламинобензгидрола. По окончании реакции смесь охлаждают до 20оС при перемешивании, добавляют 50 мл холодной воды и нейтрализуют 5%-ным раствором карбоната натрия до рН 7. Образующийся осадок отфильтровывают, промывают 50 мл воды и 40 мл четыреххлористого углерода и перекристаллизовывают из 55% -ного водного этанола, получают 2,8 г 5-хлор-2-N-метиламинобензгидрилмочевины /I/, что составляет 79% в расчете на 5-хлор-2-N-метиламинобензгидрол.
П р и м е р 2. Синтез, выделение и очистку 5-хлор-2-аминобензгидрилмочевины /II/ проводят аналогично примеру 1. Получают из 4,1 г (0,07 молей) мочевины, 1,83 мл (0,034 молей) серной кислоты и 2 г (0,008 молей) 5-хлор-2-аминобензгидрола 1,85 г (77%) 5-хлор-2-аминобензгидролмочевины /II/.
П р и м е р 3. Синтез, выделение и очистку 5-хлор-2-N-ацетиламинобензгидрилмочевины /III/ проводят аналогично примеру 1. Получают из 5,1 г (0,09 молей) мочевины, 2,3 мл (0,04 моля) серной кислоты и 3 г (0,01 моль) 5-хлор-2-ацетиламинобензгидрола 3,7 г (80%) 5-хдор-2-N-ацетиламинобензгидрилмочевины /III/.
Влияние молярных соотношений реагентов и температуры на выход 5-хлор-2-N-метиламинобензгидриломочевины приведены в табл. 1.
По сравнению с прототипом, заявляемый способ получения предусматривает проведение процесса конденсации 5-хлор-2-аминозамещенных бензгидролов с мочевиной в расплаве в отсутствии растворителей. Использование распространенных органических растворителей (октан, бензол, этанол, диоксан) в качестве гомогенизирующей среды реакции не приводит к возникновению целевых продуктов, а применение ледяной уксусной кислоты, как в прототипе вызывает ряд нежелательных процессов - образование аминобензгидроловых эфиров уксусной кислоты и азагетероциклов тетрагидрохиназолинового ряда. Образование 6-хлор-4-фенилхиназолинонов подтверждено методом тонкослойно-хроматографического анализа путем сравнения с аутентичными образцами, синтезированных по способу 4. Контроль за индивидуальностью полученных веществ и анализ реакционной смеси производили на пластинах Силуфол-УФ-254, элюирующая смесь бензол: этанол=8:2, детектирование под УФ-светом и обработкой пластины реактивом Эрлиха.
Для заявляемого способа получения немаловажное значение придается строгому соблюдению молярных соотношений реагентов, что иллюстрируется экспериментальными данными реакции 5-хлор-2-N-метиламинобензгидрола с мочевиной в присутствии серной кислоты (таблица). Так, например, снижение количества мочевины до 5-7 молей на 1 моль исходного гидрола существенно снижает выходы 5-хлор-2-N-метиламинобензгидрилмочевины (53-72%, синтезы 1-3). А увеличение же количества мочевины свыше 9 молей на 1 моль гидрола делает процесс невозможным из-за плохого смешения реагентов (не образуется расплав). Синтезы 6-9 демонстрируют влияние количества серной кислоты на выход целевого продукта. Если расход серной кислоты составляет менее 4 моль на 1 моль гидрола (синтезы 6, 7), то выход продукта реакции несколько падает за счет плохого смешения реагентов. При увеличении расхода серной кислоты свыше 4,3 молей на 1 моль гидрола также снижает выход целевого продукта за счет параллельного протекания побочных реакций, приводящих в конечном итоге к смеси, не поддающейся разделению и анализу.
Синтезы 10-14 отражают значительность температурного фактора ведения процесса на выход 5-хлор-2-N-метиламинобензгидрилмочевины. Как видно из экспериментальных данных, при температурах ниже 75оС наряду с падением выхода продукта наблюдается параллельное увеличение времени проведения реакции (синтезы 10, 11). При температуре свыше 70оС (синтезы 14) заметное уменьшение выхода целевого продукта происходит из-за прогрессирующего образования побочного производного тетрагидрохиназалинона.
Синтезированные нами соединения показали выраженное действие на монооксигеназную систему печени и проявили высокую антигипоксическую активность. В настоящее время, полученные вещества проходят стадию углубленного биохимического исследования в Институте фармакологии ТНЦ АМН СССР.
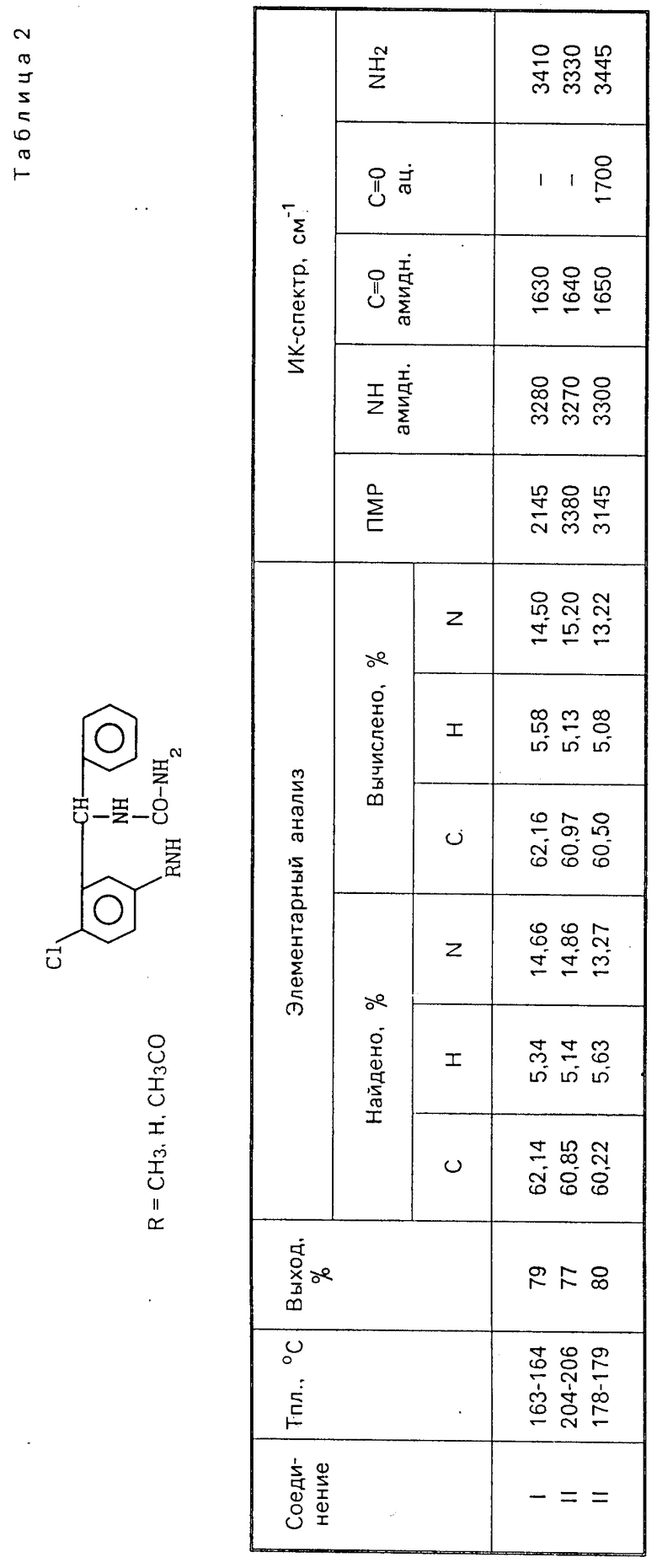
Структура и состав 5-хлор-2-аминозамещенных бензгидрилмочевин на основании данных ИК-спектров, элементного и тонкослойно-хроматографического анализа приведена в табл. 2.
Данный способ получения 5-хлор-2-аминозамещенных бензгидрилмочевин по сравнению с прототипом содержит ряд технико-экономических преимуществ, которые заключаются в том, что упрощается процесс за счет исключения образования побочных продуктов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СЕРНОКИСЛАЯ СОЛЬ 2-N-МЕТИЛАМИНО-5-ХЛОРБЕНЗГИДРИЛМОЧЕВИНЫ, ПРОЯВЛЯЮЩАЯ ПРОТИВОСУДОРОЖНУЮ АКТИВНОСТЬ | 1991 |
|
RU2033411C1 |
| N-БЕНЗГИДРИЛ-N`-(ТРИФТОРАЦЕТИЛ)МОЧЕВИНА, ПРОЯВЛЯЮЩАЯ ПРОТИВОСУДОРОЖНУЮ АКТИВНОСТЬ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1991 |
|
RU2033412C1 |
| N,N'-ДИ(БЕНЗГИДРИЛ)-N-(ТРИФТОРАЦЕТИЛ)МОЧЕВИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОСУДОРОЖНУЮ И ФЕРМЕНТИНДУЦИРУЮЩУЮ АКТИВНОСТЬ | 1991 |
|
RU2024501C1 |
| БРОМЗАМЕЩЕННЫЕ N-БЕНЗГИДРИЛ-N-(ТРИФТОРАЦЕТИЛ)МОЧЕВИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОСУДОРОЖНУЮ АКТИВНОСТЬ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2070039C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-5-ХЛОРБЕНЗГИДРОЛА, 2-N-МЕТИЛАМИНО-5-ХЛОРБЕНЗГИДРОЛА И МЕТАХЛОРБЕНЗГИДРОЛА | 1992 |
|
RU2065435C1 |
| СПОСОБ ПОЛУЧЕНИЯ М-ХЛОРДИФЕНИЛМЕТИЛМОЧЕВИНЫ | 1992 |
|
RU2092478C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-ДИНИТРО-3,7-ЭНДОМЕТИЛЕН-1,3,5,7-ТЕТРАЗАЦИКЛООКТАНА | 2001 |
|
RU2198886C1 |
| ГАЛОГЕНЗАМЕЩЕННЫЕ N-БЕНЗГИДРИЛ- N -(ТРИФТОРАЦЕТИЛ) МОЧЕВИНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОСУДОРОЖНУЮ АКТИВНОСТЬ | 1991 |
|
SU1829341A1 |
| ОПТИЧЕСКИЕ ИЗОМЕРЫ (+) И (-)-БЕНЗГИДРИЛМОЧЕВИН И (+) И (-)-1-[(3-ХЛОРФЕНИЛ)-ФЕНИЛ-МЕТИЛ]МОЧЕВИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2537361C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АДАМАНТАНКАРБОНОВОЙ КИСЛОТЫ | 2009 |
|
RU2412930C1 |

Использование в производстве медицинских препаратов. Сущность изобретения: новый способ получения новых, ранее неописанных 5-хлор-2-аминозамещенных бензгидрилмочевин. Реагент 1 -мочевина. Реагент 2- 5-хлор-2-аминозамещенные бензгидролы. Условия реакции: реакцию проводят в концентрированной серной кислоте при соотношении реагента 1,2 и серной кислоты (8-9):1: (4-4,3). Выход 70-80%. 2 табл.
СПОСОБ ПОЛУЧЕНИЯ 5-ХЛОР-2-АМИНОЗАМЕЩЕННЫХ БЕНЗГИДРИЛМОЧЕВИН общей формулы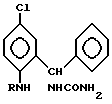
где R = CH3, H, CH3CO
отличающийся тем, что мочевину обрабатывают концентрированной серной кислотой при 75 - 90oС в течение 10 - 15 мин с последующим добавлением в полученную смесь соответствующего 5-хлор-2-аминозамещенного бензгидрола, реакционную массу выдерживают при 70 - 90oС в течение 6 - 8 ч, при молярном соотношении 5-хлор-2-аминозамещенного бензгидрола, мочевины и серной кислоты 1 : 8 oC 9 : 4 oC 4,3.
| СПОСОБ ПОЛУЧЕНИЯ М-ХЛОРДИФЕНИЛМЕТИЛМОЧЕВИНЫ | 1985 |
|
SU1334658A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-03-10—Публикация
1990-10-22—Подача