Изобретение относится к медицине, а именно к кардиологии.
Известен индивидуализированный подбор лекарств для лечения ишемической болезни сердца (ИБС), в частности антиаритмиков, основанный на анализе клинического эффекта. Однако, несмотря на использование при инфаркте миокарда (ИМ) лучшего из антиаритмиков-лидокаина, смертность от фибрилляции желудочков сердца сохраняется высокой.
Известна также перспективность применения синтетических аналогов регуляторных пептидов стресс-лимитирующих как антиаритмиков. Так даларгин (Д) аналог лей-энкефалина, уменьшал количество экстрасистол при перевязке коронарной артерии у собак. Д в настоящее время проходит клинические испытания как средство для ограничения зоны некроза при ИМ. Как известно при ИМ может наблюдаться как дефицит, так и избыток опиоидных пептидов. Поэтому целесообразность применения Д в клинике во многом зависит от эндогенного количества лей-энкефалина и пептидов, аналогичных ему по действию. Показана возможность характеризовать пептидный баланс в организме, определяя на парамециях токсичность спиртоворастворимой фракции сыворотки крови в присутствии Д и пептида дельта-сна. Для этого 0,02 мл раствора спирто-водорастворимой фракции сыворотки крови соединяют с физиологическим раствором и вторую каплю с раствором Д (или другого пептида). В обе капли добавляют примерно 30 особей инфузорий, подсчитывают время парамецийной реакции-ВПР. При его увеличении под воздействием препаратов констатируется дефицит того пептида и его аналогов в организме, с которым производили биотестирование.
Цель изобретения профилактика фибрилляции желудочков сердца у больных ИМ.
Эта цель достигается тем, что на основании клинических данных больным ИБС, угрожаемым по развитию фибрилляции, как часто имеющим дефицит стресс-лимитирующих пептидов, назначается дополнительно Д в дозе 0,1 мг/кг, продолжается его ежедневное введение в той же или большей дозе 3 и более дней при наличии стимулирующего эффекта Д на ВПР в сыворотке крови больного или ее спирто-водорастворимой фракции, но доза препарата уменьшается или он отменяется при отсутствии такого действия.
Дозировка и показания к применению уточняются практически у постели больного с помощью простого быстроосуществимого теста на культуре парамеций.
П р и м е р. Выписка из истории болезни N 10667 больного П. 38 лет. Поступил в палату интенсивной терапии 23.06.89 г. с подтвержденным общепринятыми критериями диагнозом острого трансмурального переднего ИМ. Отмечалась из осложнений редкая экстрасистолия. Учитывая молодой возраст больного, наличие экстрасистолии при имеющемся диагнозе констатировали угрозу фибрилляции желудочков. Назначен даларгин 0,015 мг/кг. Это была первоначальная дозировка, с которой проводились клинические испытания Д как средства ограничения зоны некроза. Для уточнения дозировки 0,02 мл сыворотки крови больного соединили с 0,01 мл физиологического раствора (контроль). На том же предметном стекле такую же каплю сыворотки соединили с 0,01 мл раствора Д (0,8 мг/мл). Добавили в каждую каплю по 25-30 особей инфузории туфельки в 0,02 мл культуральной среды. Под микроскопом наблюдали за состоянием клеток в обоих каплях. Установили, что в контроле они погибли через 5 мин, а в опыте на 6 мин позже. Это свидетельствует о высокой степени дефицита энкефалинов у больного и малой вероятности достаточности использованной дозы Д у больного. Повторное аналогичное исследование сыворотки крови больного после окончания инфузии Д показало нетипичную сохранившуюся высокую потребность в Д. Разница между контролем и опытом составила 4 мин. Дозу Д сразу не скорректировали. Через час после окончания введения Д у больного развивалась фибрилляция желудочков, которая была сразу купирована электрической дефибрилляцией. Больной сразу пришел в себя. После дефибрилляции потребность в Д снизилась (до 2 мин в данном тесте). Д вводился в последующие 4 дн. Потребность в Д исчезла. Других осложнений не было. Больной отправлен в санаторий на реабилитацию.
Это единственный случай развития фибрилляции в исследовании у больного, получающего Д. Развитие фибрилляции связали с индивидуально недостаточной дозой Д. Но очевидно, частичное устранение резко выраженного дефицита стресс-лимитирующих пептидов привело к устранению выраженного дефицита стресс-лимитирующих пептидов, привело к успеху реанимационных мероприятий. Наблюдение демонстрирует необходимость индивидуального подбора Д.
Доказательства достижения положительного эффекта основаны на экспериментальном материале, показавшем антифибрилляторный эффект Д и высокий дефицит стресс-лимитирующих пептидов при угрозе фибрилляции, а также на клинических наблюдениях.
Однако индивидуализированное назначение Д связано не только с угрозой фибрилляции. Оно связано и с неблагоприятным течением репаративных процессов на фоне дефицита стресс-лимитирующих пептидов. Получены предварительные данные, подтвеpждающие это положение. Больным ИМ, получавшим и не получавшим Д (контроль), проводили прекардиальное картирование в 35 отделениях. Как видно из табл.1, исходно в группе с Д-терапией и в контроле показатели повреждения и площади некроза по ЭКГ в подгруппах с и без дефицита Д достоверно не отличались (р 0,05). Хотя имелась тенденция к меньшей площади некроза в группах без дефицита Д. Не было достоверных различий между контрольной и опытной группами по соответствующим подгруппам. Не произошло также достоверных сдвигов с 1 по 4-5-й дн болезни в динамике изучаемых показателей в обеих подгруппах в контроле и опыте. Однако на 4-5 сутки появилась достоверная разница (р 0,05) в площади зоны некроза в группе с дефицитом пептидов в нашем тесте. На фоне дефицита в группе с Д-терапией площадь некроза оставалась большей, чем в группе без дефицита. В контроле, а также для показателя площади повреждения имелась тенденция к такой же динамике. Следовательно доза 15 мкг/кг в среднем не была достаточной. Таким образом, индивидуализированное назначение должно предусматривать и выбор индивидуальной дозы.
Обобщая весь приведенный экспериментальный и клинический материал, можно отметить, что Д повышает порог фибрилляции желудочков сердца и поэтому целесообразен при ИМ с угрозой фибрилляции, но при отсутствии тяжелой сердечной недостаточности, особенно с артериальной гипотонией, брадикардией, синоаурикулярными и антриовентрикулярными блоками. Учитывая идентичность эффектов Д эндогенно образующемуся лей-энкефалину и ряду других аналогичных по действию стресс-лимитирующих пептидов, терапия им особенно целесообразна под контролем активности пептидов. Парамеции оказались культурой, чувствительной к изучаемым регуляторным пептидам человека. Поэтому предложенный тест с ними может быть целесообразен в силу доступности для индивидуализированного лечения Д ишемической болезни сердца.
Из 228 пациентов 63 получали Д в дозе 100 мкг/кг 3 дня внутривенно капельно I группа, 51 человек 15 мкг/кг 5 дней II группа. Остальные 114 его не получали III группа. Применяли Д, произведенный на экспериментальном предприятии медико-биологических препаратов ВКНЦ АМН СССР. Там же получено и плацебо для Д. У 25-и больных I группы и 25-и больных III группы исследование проводилось методом двойного плацебо. Дозы Д соответствовали рекомендациям Фармакокомитета МЗ СССР.
Как видно из табл.2, сравниваемые группы на момент поступления были репрезентативными. Кроме Д лечение больных в 3 сравниваемых группах было одинаковым, традиционным. У небольшого числа пациентов в первые дни заболевания использовали лидокаин или его аналоги. По данному признаку сравниваемые группы также значимо не отличались. Поэтому статистические сопоставления в дальнейшем представляются правомерными.
Для доказательства того, что использование предложенного теста повышает эффективность лечения ИМ Д, разделили больных ИМ, которым исследовали ИПО, на 4 группы в зависимости от результатов исследования ИПР. Две основные группы, получивших Д: c положительными результатами ИПР (Д с ИПРП) и без них (Д без ИПРП), а также две соответственно контрольные группы (К с ИПРП и К без ИПРП). ИПР определяли на момент поступления больных, до лечения. Создание соответствующих по ИПР основных и контрольных групп обусловлено тем, что по предварительным данным пациенты с ИПРП представляют собой контингент с прогностически неблагоприятным течением ИМ, если ИПР не будет скорректирован, например, Д. Данные 4 группы формировались по тем же принципам, что и описанные группы из их числа.
Как видно из табл. 3, на момент поступления 4 сравниваемых группы представлялись репрезентативными. В группе Д с ИПРП в первые 3 ч заболевания поступило 17 больных, от 3 до 6 ч 9 человек, позже 6 ч 14 больных; в группе К с ИПРП соответственно 14,8,12 пациентов; в группе Д без ИПРП 13,7,14; в группе К без ИПРП 9,4,7 соответственно.
Методы исследования. Наряду с анализом общепринятых клинических показателей, определяли активность аспартат- и аланин-аминотрансфераз (АсАТ и АлАТ, м/моль/сл) с помощью стандартных наборов реактивов фирмы Био-ДА-Тест, активность креатининфосфокиназы (КФК, ед/л) наборами фирмы ЛАХЕМА, активность лактатдегидрогеназы и ее фракций (ЛДГ, микрокатал/л, ЛДГ-1 и ЛДГ-2,) по А.А. Пыркову и соавт. (1970) реактивами фирмы "Ренал". Винилинминдальную кислоту в моче (ВМК, в мкмоль/сут) исследовали по методу В.В.Меньшикова, Т.Д.Большакова (1966). У больных с передними ИМ проводили прекардиальное картирование ЭКГ (ПКК) по методу Maroco (1972). Вегетативный индекс Кердо (ВИ,) рассчитывали по формуле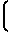 1
1  100, где АДД-АД диастолическое.
100, где АДД-АД диастолическое.
АД систолическое обозначали АДС.
Анализировали число лимфоцитов (лим.) и в абсолютных цифрах (лим, абс, 109 л) в общем анализе крови, индекс сдвига лейкоцитов (ИСЛ) соотношение полиморфно-ядерных и мономорфно-ядерных лейкоцитов. Статистическая обработка результатов проводилась на электронном вычислительном комплексе МС20102 с использованием критериев Стьюдента или Вилкоксона в зависимости от распределения в ряду. Достоверность различий по числу осложнений в группах в заявке вычисляли по критерию Стьюдента. В данных материалах с учетом рекомендаций ВКНЦ применяли и критерий х2, двухсторонний точный критерий Фишера.
Как видно из табл.3, в исходно репрезентативных группах Д с ИПРП и К с ИПРП достоверно более низкой оказалась летальность в группе Д с ИПРП (6,3; Р 0,05). В этой же группе имелась тенденция к меньшему числу аневризм при передних распространенных трансмуральных ИМ при отсутствии значимых отличий по другим признакам. При сравнении групп Д без ИПРП и К без ИПРП не было существенных отличий по летальности, аневризмам и другим анализируемым признакам. Следовательно, Д реализовывал свой лечебный эффект именно в контингенте больных с положительным ИПРП. Этот контингент при сравнении групп К с ИПРП и К без ИПРП представлялся как более тяжелый. При исходной репрезентативности этих групп в группе К с ИПРП достоверно чаще формировались аневpизмы при передних ИМ, имелась тенденция к более высокой летальности.
В общей совокупности пациентов с Д отмечалась более низкая летальность в основном за счет сохранения жизни больным с ИПРП. Наиболее вероятная причина снижения летальности устранение дефицита стресс-лимитирующих пептидов Д, что видно по данным ВПР, ИПР. Как известно при равной площади некроза прогноз ИМ может быть разным. Он зависит от факторов реактивности организма, участвующих в ответе на некроз, от уровня стресс-лимитирующих пептидов. Первоначально снижение летальности связали с профилактикой Д фибрилляции желудочков. Имеющийся материал защищает положение по летальности в целом, причем у больных ИМ, поступивших в 1-е сут с сердечной недостаточностью не выше I степени, при наличии ИПРП. В общей контрольной группе умерло 16 пациентов, от отека легких, шока 6, от фибрилляции 2, разрывов миокарда 7, тромбэмболии легочной артерии 1. Причем 9 больных умерло в остром периоде ИМ. В группе с Д в остном периоде погибло 2 больных без ИПРП (отек легких и разрыв миокарда).
Следовательно, механизмы влияния Д на летальность оригинальны, судя по ИПР, связаны с его действием на биологическую активность стресс-лимитирующих пептидов. Они до конца не изучены, связаны с дозировкой Д. Они отличаются от традиционных, когда снижение летальности при неосложненном в 1-е сут ИМ достигается за счет ограничения очага поражения, профилактики опасных аритмий, причем часто недифференцированно, у всех таких больных. Д реализует свой эффект примерно у половины таких пациентов с ИМ когда, судя по ИПР, биологическая активность стресс-лимитирующих пептидов снижена. Имеется аналогия с реализацией лечебного эффекта инсулина только при гипергликемии. Д не может быть отвергнут по той причине, что его действие не соответствует традиционным взглядам на механизмы снижения летальности при ИМ. Дифференцированное использование Д при ИМ может быть новым направлением в борьбе за выживаемость больных ИМ, поступивших в стационар в первые сутки заболевания без тяжелых осложнений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА | 1989 |
|
RU2006039C1 |
| СПОСОБ ОГРАНИЧЕНИЯ ЗОНЫ ПОРАЖЕНИЯ И УСКОРЕНИЯ РЕПАРАТИВНЫХ ПРОЦЕССОВ ПРИ ИНФАРКТЕ МИОКАРДА | 1991 |
|
RU2086979C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВОВ АНГИНОЗНОЙ БОЛИ ПРИ ИНФАРКТЕ МИОКАРДА | 1993 |
|
RU2113856C1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| СПОСОБ ВОСПРОИЗВЕДЕНИЯ КАРДИОГЕННОГО ШОКА НА МЕЛКИХ ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2003 |
|
RU2239874C1 |
| СПОСОБ ДИАГНОСТИКИ И ПРОФИЛАКТИКИ ЧАСТЫХ РЕЦИДИВОВ ГЕРПЕСА ПРОСТОГО | 1997 |
|
RU2159632C2 |
| АНТИАНГИНАЛЬНОЕ СРЕДСТВО | 2001 |
|
RU2200026C2 |
| Способ периоперационной органопротекции у больных опухолями области головы и шеи | 2023 |
|
RU2822968C1 |
| СПОСОБ ЛЕЧЕНИЯ АРИТМИЧЕСКОГО СИНДРОМА ПРИ ПРОГРЕССИРУЮЩЕЙ СТЕНОКАРДИИ | 2004 |
|
RU2266130C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНОГО ИСХОДА ГИПЕРТРОФИЧЕСКОЙ КАРДИОМИОПАТИИ | 2013 |
|
RU2527768C1 |


Изобретение относится к медицине, в частности к кардиологии, и может быть использовано для лечения больных инфарктом миокарда в остром периоде. Цель - профилактика фибрилляции желудочков сердца и снижение летальности. Для этого в терапии инфаркта используют даларгин в дозе 0,1 мг/кг, определяют пептидный баланс организма по парамецийному тесту с даларгином и при наличии дефицита стресс-лимитирующих пептидов дозу даларгина увеличивают, а при отсутствии уменьшают до 0,015 мг/кг. 3 табл.
СПОСОБ ЛЕЧЕНИЯ ИНФАРКТА МИОКАРДА, включающий введение даларгина, отличающийся тем, что, с целью профилактики фибрилляции желудочков сердца и снижения летальности, даларгин вводят в дозе 0,1 мг/кг, определяют пептидный баланс организма по парамецийному тесту с даларгином и при наличии дефицита стресслимитирующих пептидов дозу увеличивают, а при отсутствии дефицита уменьшают до 0,015 мг/кг.
| Г.К.Золоев и др | |||
| Кардиология | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
Авторы
Даты
1995-04-10—Публикация
1990-08-13—Подача