Изобретение касается способа получения новых производных бензгидрилоксиэтил-пиперазина, которые могут найти применение в медицине.
Известны производные бензгидрола, общей формулы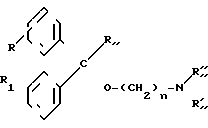 в которой RR1 представляют, независимо один от другого, водород, алкил, алкокси или галоген, Rll представляет водород или алкил, группа NRll'' Rll' означает замещенную группу диалкиламино, алкиламино, пирролидино, пиперидино, морфолино или пиперазино. Эти соединения воздействуют на центральную нервную систему и, в частности, оказывают седативный эффект. [См. нижеприведенные документы: -BURGER, MEDICINAL CHMISTRY 4-е издание, том III, Manfred WOLFF, стр. 559-564 WIL EYN.Y. Eds -I.M.MELON и А. BuZAS Fr 74.23.262 и Fr 76.13.592 -GOOTIES I. и Coll Е.Р. 0.099.148]
в которой RR1 представляют, независимо один от другого, водород, алкил, алкокси или галоген, Rll представляет водород или алкил, группа NRll'' Rll' означает замещенную группу диалкиламино, алкиламино, пирролидино, пиперидино, морфолино или пиперазино. Эти соединения воздействуют на центральную нервную систему и, в частности, оказывают седативный эффект. [См. нижеприведенные документы: -BURGER, MEDICINAL CHMISTRY 4-е издание, том III, Manfred WOLFF, стр. 559-564 WIL EYN.Y. Eds -I.M.MELON и А. BuZAS Fr 74.23.262 и Fr 76.13.592 -GOOTIES I. и Coll Е.Р. 0.099.148]
Цель изобретения разработка новых соединений, имеющих противогистаминную активность, идентичную или же превышающую противогистаминную активность названных производных, но не имеющих седативного действия.
Эта цель достигается предлагаемым способом получения производных бензгидрилоксиэтил-пиперазина общей формулы I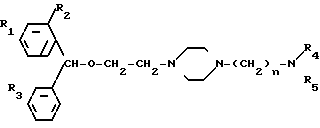
где R1 водород, галоид, низший алкил, низший алкокси или трифторметилрадикал;
R2 водород или галоид;
R3 водород, галоид или трифторметилрадикал;
n целое число между 2 и 6 включительно;
R4 и R5 представляют один атом водорода и другой группу бензоила, замещенную нитро или метокси, или R4 и R5 образуют вместе с атомом азота, с которым они связаны, гетероциклическую группу, выбираемую из групп: сукцинимидил, 4-фенилсукцинимидил, 2-оксобензимидазолинил, 3-бензил-2-оксобензимидазолинил, 1,2,3,4-тетрагидро-2,4-диоксохинахолинил, 3,4-дигидро-4-оксохиназолинил, 3,4-дигидро-4-оксо-2-метилхиназолинил, 3,7-дигидро-1,3-диметил-2,6-диоксо-1Н-пуринил, 3,7-дигидро-3,7-диметил-2,6-диоксо-1Н-пу- ринил, отличающийся тем, что соединение общей формулы II
X-(CH2)n-N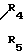 где n, R4 и R5 имеют определенные значения и Х представляет группу галогена или тозила, подвергают взаимодействию с избытком бензгидрилоксиэтил-пиперазина общей формулы III
где n, R4 и R5 имеют определенные значения и Х представляет группу галогена или тозила, подвергают взаимодействию с избытком бензгидрилоксиэтил-пиперазина общей формулы III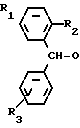 -(CH2)2-N
-(CH2)2-N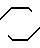 NH где R1-R3 имеют приведенные значения в среде инертного апротонного растворителя, такого как толуол, и в случае необходимости, полученный целевой продукт превращают в кислые аддитивные соли.
NH где R1-R3 имеют приведенные значения в среде инертного апротонного растворителя, такого как толуол, и в случае необходимости, полученный целевой продукт превращают в кислые аддитивные соли.
Кислые аддитивные соли соединений по изобретению получают классическим способом путем взаимодействия с фармацевтически приемлемыми кислотами, такими как, например, уксусная кислота, хлористоводородная кислота, торфторуксусная кислота, метансульфокислота.
Соединения по изобретению имеют ценные фармакологические свойства, в частности, противогистаминные и антиспазматические свойства и могут применяться, в частности, для лечения спазматических состояний и аллергий.
Полученные производные идентифицированы и охарактеризованы с помощью спектров ядерного магнитного резонанса и инфракрасного спектра, а также их элементным анализом.
П р и м е р 1. 1-[2-(Бензгидрилокси)этил]-4-[2-(фталимидо)этил]пиперазиндиметансу -льфонат (формула I, R1=R2=R3=H;
NR4R5= -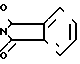 n=2;)
n=2;)
В реактор загружают 15,3 г бромоэтилфталимида, 36 г бензгидрилоксиэтил-пиперазина, 500 мг йодистого калия в 250 мл безводного толуола. Реакционную смесь нагревают в течение 6 ч до 120оС. Поглощают остаток 100 мл воды, экстрагируют 100 мл толуола. Сушат и выпаривают растворители. Таким путем получают 27 г масла, которое кристаллизуют из этанола. Твердое вещество обезвоживают и получают 25,5 г кристаллов (Т.пл.101оС).
К этим 25,5 г полученного твердого вещества, растворенного в 100 мл ацетона, добавляют 10,5 г метансульфокислоты. Обезвоживают и получают таким путем 34 г диметансульфоната (Т.пл.124оС) эмпирической формулы:
С29Н31N3О3, 2(СН4О3S)
Вычислено, С 59,26; Н 5,94; N 6,35; S 9,69.
Найдено, С 59,24; Н 5,99; N 6,36; S 9,79.
Спектр ЯМР (основание в растворе в СDСl3, этанол ТМ С):
7,6 ппм (m), 4Н, (фталимидо); 7,1 ппм (m), 10Н, (Ф2С);
5,3 ппм (S), 1Н, (СН-0); 3,8 ппм (t), 2Н (СН2-N-С=0);
3,5 ппм (t), 2Н, (СН2-0); 2,5 ппм (m), 12Н, (СН2-N).
Спектр ИК (1%в КВr)
1780 см-1 (С= 0 асимметр.); 1710 см-1 (С=0 симметр.): 1200 см-1 (SO2); 1070 см-1 (SO2).
П р и м е р 2. 1-[2-(Бензгидрилокси)этил]-4-[2-(окси-бензамидо)этил]-пиперазин-диметансульф онат (формула 1, R1=R2=R3=Н; n=2;
NR4R5= -NH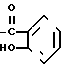
В реактор помещают 8,4 г N-(2-бром-этил)-3,4-дигидро-2,4-диоксо-2Н-1,3-бензо- ксазина (0,0311 моль), 18,4 бензгидрилоксиэтилпиперазина В (0,0622 моль) и 250 мг йодида калия в 150 мл толуола. Реакционную смесь нагревают в течение 6 ч при 120оС и остаток гидролизуют 100 мл воды, декантируют и снова экстрагируют водную фазу 50 мл толуола. Высушенные толуольные фракции объединяют и растворитель выпаривают. Таким образом получают 16 г сырого масла, которое очищают путем хроматографии на колонке с силикагелем. Чистый продукт выделяют и получают 6,65 г целевого продукта. К этим 6,65 г масла, растворенных в ацетоне (50 мл) добавляют 2,3 эквивалента метансульфокислоты. Кристаллы отсасывают и таким образом получают 7,8 г диметансульфоната брутто-формулы
С28Н33N3O3˙2СН3SO3H.
Cпектр ЯМР (растворитель СDСl3; этанол ТМС)
2,2 2,9 (m), 12Н, СН2 N; 3,4 (t), 2Н,O-CH2; 3,6(t), 2Н, СН2-N-СH; 5,2(S), 1Н, СН 0; 6,5 8,1(m), 14Н, аром. 7,6 (m), 1Н, NH; 9,2 (m), 1Н, ОН.
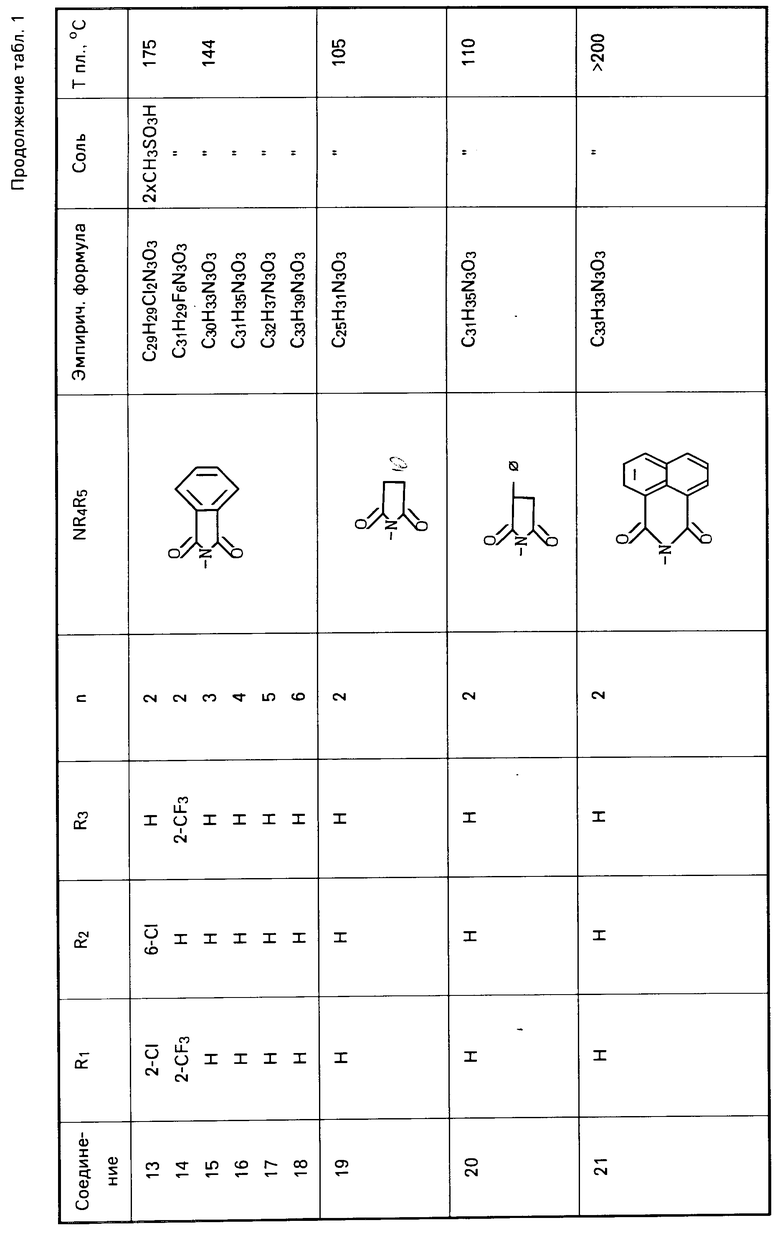
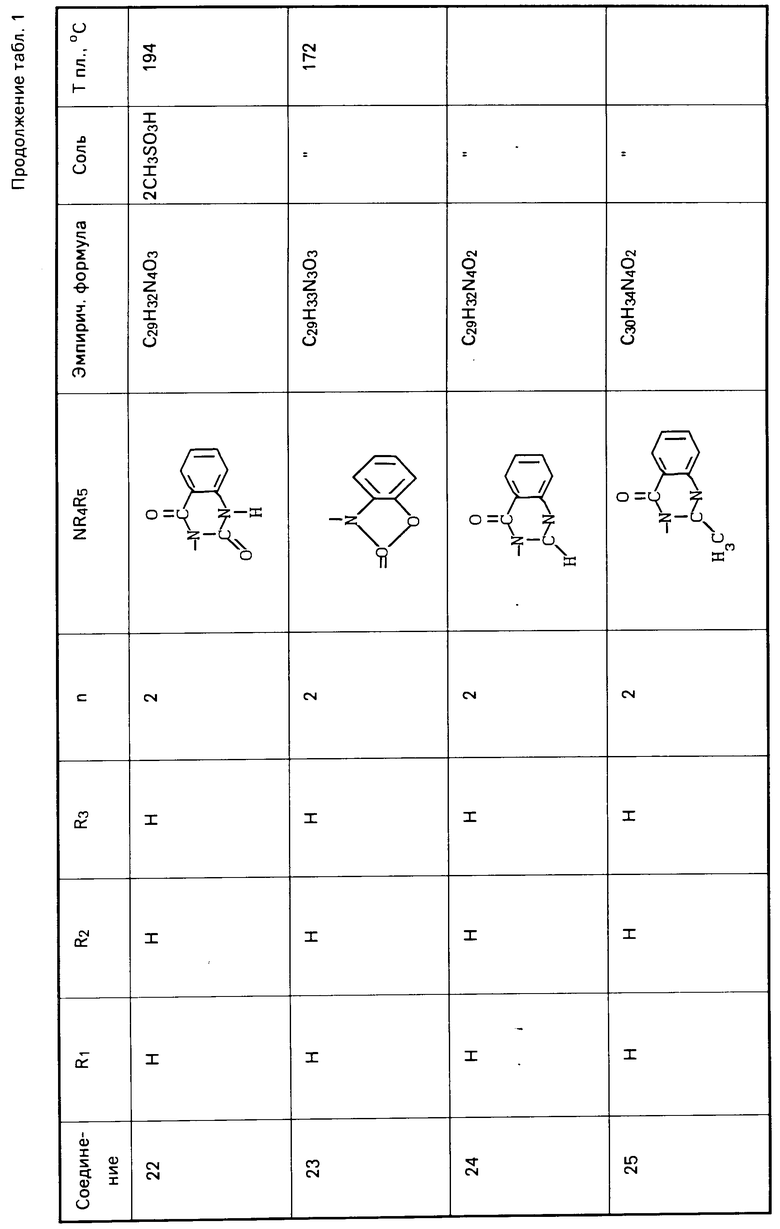
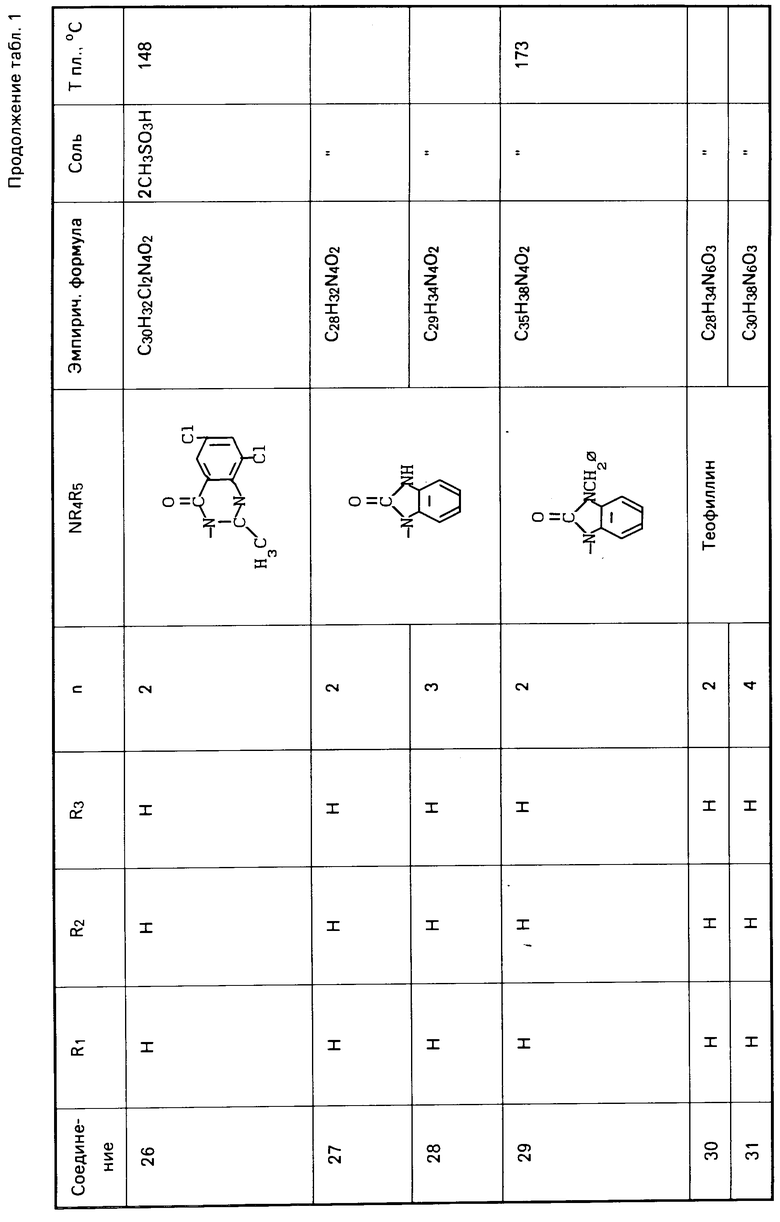
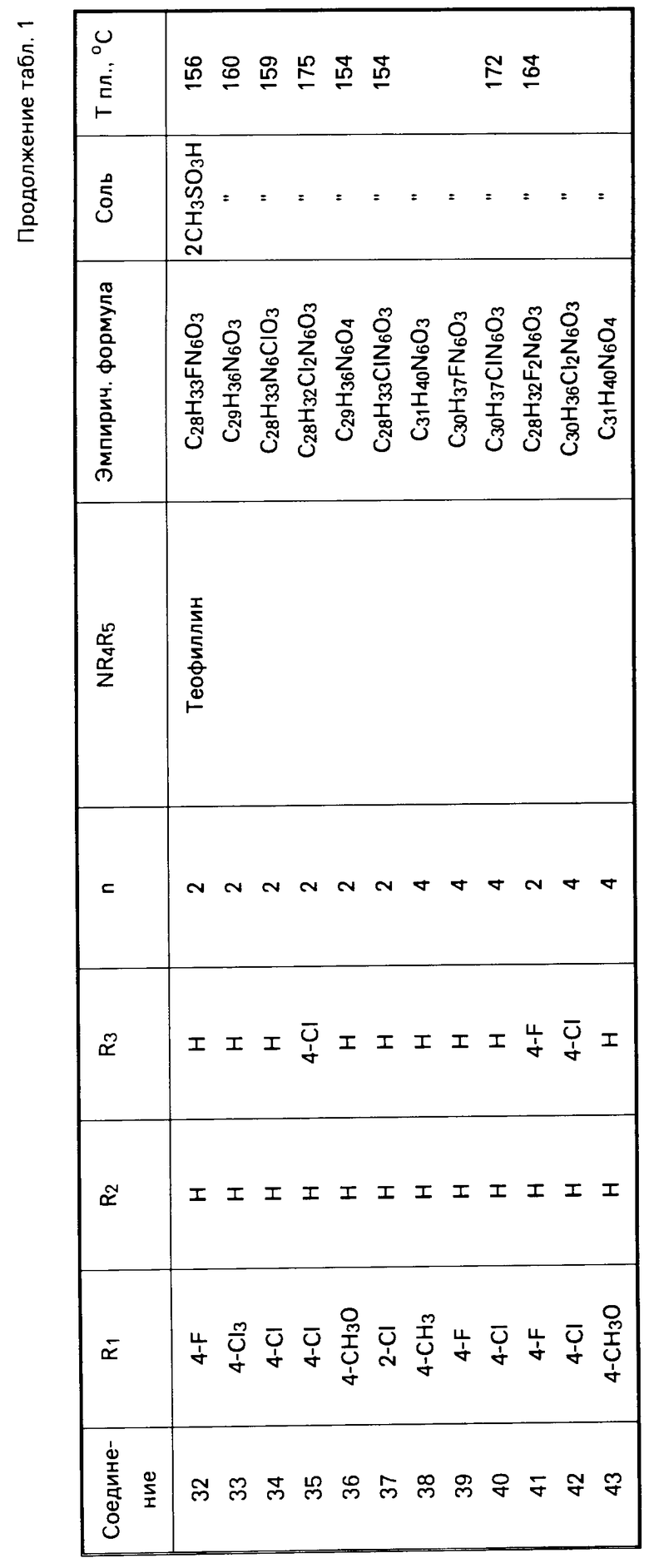
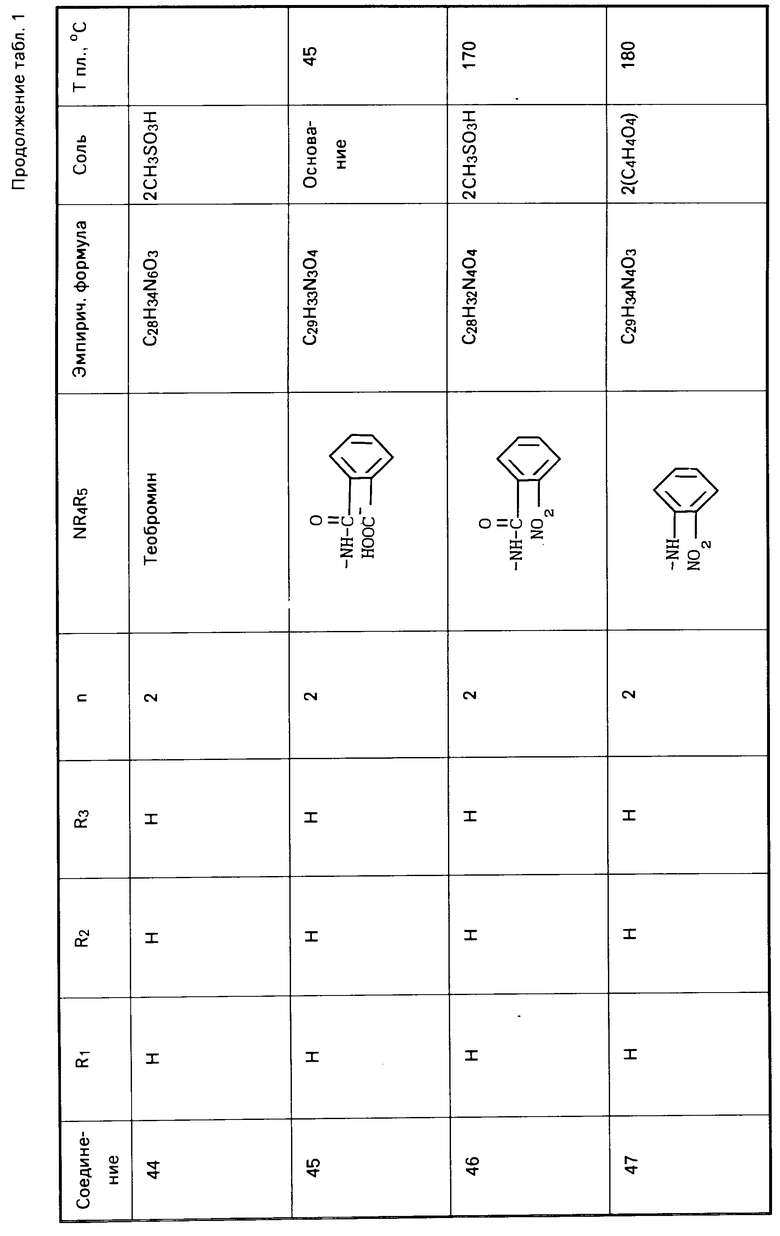
Действуя по аналогичной методике, получают следующие соединения, указанные в табл. 1. Результаты ЯМР-анализа полученных соединений приведены ниже.
5 2.1 2.7 (m), 12Н, СН2-N; 3.4 (t), 2Н, СН2-О;
3.5 (s), 3H, CH3-O; 3.6 (t), 2H, CH2-N- C=O;
5.1 (s), 1Н, СН-О; 6.7 (m), 4Н, arom;
7.0 (s), 5H, аром; 7.1-7.8 (m), 4Н, аром.
8 2.3-2.7 (m), 12H, CH2-N; 3.5 (t), 2Н, О-СН2;
3.7 (t), 2Н, СН2-N-C=0; 5.2 (s), 1H, CH-O;
7.0-7.4 (m), 4H, аром; 3.0-7.6 (m), 4H, CH2-N-C=0.
14 2.2-2.7 (m), 12H, CH2-N; 3.5 (t), 2H, O-CH2;
3.7 (t), 2H, CH2-N-C=O; 5.3 (s), 1H, CH-O;
6.9-7.8 (m), 12H, аром.
16 1.4-1.9 (m), 4H, C-CH2-CH2-C;
2.1-2.7 (m), 12H, CH2-N; 3.5 (t), 2H, CH2-O.
3.6 (t) 2H, CH2-N-C=O; 5.2 (s), 1H, CH-O;
7.1 (m), 10H, аром. 7.3-7.6 (m), 4H, аром.
17 1.0-1.9 (m), 6H, C-(CH2)3-C; 2.0-2.8 (m), 12H, CH2-N;
3.4 (t), 2H, CH2-O; 3.5 (t), 2H, CH2-N- C=O;
5.1 (s), 1H, CH-O; 7.0 (s), 10H, аром;
7.2-7,6 (m) 4H, аром.
18 1.1-1.8 (m), 8H, C-(CH2)4 C; 1.9-2.7 (m), 12H, CH2-N.
3.4(t); 2H, CH2-O; 3.5 (t), 2H, CH2-N- C=O;
5.1 (s), 1H, CH-O; 7.0 (s) 10H, аром;
7.2-7.6 (m), 4H, аром.
24 2.2-2.8 (m), 12H, CH2-N; 3.4 (t), 2H, CH2-O
3.9(t), CH2-N-C; 5.2 (s), 1H, CH-O; 6.9 (s), 10H, аром;
6.8-8.0 (m), 5H, аром.
25 2.2-2.6 (m), 12H, CH2-N; 2.4 (s), 3H, CH3;
3.4 (t), 2H, O-CH2;
3.9 (t), 2H, CH2-N-C;
5.1 (s), 1H, CH-O; 7.0 (s), 10H, аром;
6.8-8.0 (m), 4H, аром.
27 2.1-2.7(m), 12H, CH2-N; 3.4(t), 2H, CH2-O;
3.8(t), 2H, CH2-N-C; 5.1(s), 1H, CH-O;
6.7(m), 4H, аром; 7.0(m), 10H, аром; 6.9(s), 1H, NH.
28 1.7(m), 2H, C-CH2-C; 2.4-2.7(m), 12H, CH2-N;
3.4(t), 2H, CH2-O; 3.8(t), 2H, CH2-N-C;
5.1(s), 1H, CH-O;
6.6-7.2(m), 15H, аром, NH.
30 2.3-3.0(m), 12H, N-CH2; 3.2(s), 3H, N-CH3;
3.3(t), 2H, CH2-O; 3.4(s), 3H, N-CH3;
4.2(t), 2H, CH2-N; 5.2(s), 1H, CH-O;
7.0(s), 10H, аром; 7.3(s), 1H, CH=N.
31 1.2-1.9(m), 4H, C-(CH2)2-C; 2.0-2.4(t), 2H, CH2-N;
3.2(s), 3H, CH3-N; 3.3(t), 2H, CH2-O;
5.1(s), 1H, CH-O; 7.1(s), 10H, аром; 7.9(s), CH=N.
38 1.2-2(m), 4H, C-CH2-CH2-C; 2.1(s), 3H, CH3 (arom);
2.3-2.7(m), 12H, CH2-N; 3.3(s), 3H, CH3- N;
3.4(t), 2H, CH2-O; 4.2(t), 2H, CH2-N;
5.1(s), 1H, CH-O; 7.0(m), 9H аром;
7.2(s), 1H, CH=N
39 1.2-1.9(m), 4H, C-CH2-CH2-C;
2.3-2.8(m), 12H, CH2-N; 3.3(s), 3H, CH3- N;
3.4(t), 2H, CH2-O; 3.5(s), 3H, CH3-N;
4.2(t), 2H, CH2-N; 5.3(s), 1H, CH-O;
6.9(m), 4H, аром; 7.1(s), 5H, аром;
7.4(s), 1H, CH=N
42 1.3-2(m), 4H, C-CH2-CH2-C; 2.3-2.6(m), 12H, CH2-N;
3.3(s), 3H, CH2-N; 3.4(t), 2H, CH2-O;
3.5(s), 3H, CH3-N; 4.2(t), CH2-N; 5.2(s), 1H, CH-O;
7.1(m), 8H, аром; 7.4(s), 1H, CH=N.
43 1.2-2.0(m), 4H, C-CH2-CH2-C
2.3-2.8(m), 12H, CH2-N; 3.2(s), 3H, CH3- N;
3.3(t), 2H, CH2-O; 3.4(s), 3H, CH3-N;
3.6(s), 3H, CH3-O; 4.1(t), 2H, CH2-N;
5.1(s), 1H, CH-O; 6.7(m), 4H, аром; 7.0(s), 9H, аром.
44 2.3-2.7(m), 12H, CH2-N, 3.3(s), 3H, CH3-N;
3.4(t), 2H, CH2-O; 3.7(s), 3H, CH3-N;
4.1(t), 2H, CH2-N; 5.1(s), 1H, CH-O;
7.0(s), 10H, аром; 7.2(s), 1H, CH=N.
Описание фармакологических тестов
1) Актиметрия
Двигательная активность мышей определялась при помощи фотоэлектрического актиметра Буассье и Симона.
Помещали по пять мышей в коробку, закрытую крышкой, с проходящими через нее двумя перпендикулярными лучами света, которые мыши пересекали при передвижении.
Эти передвижения подсчитывались компьютером через тридцать минут и один час.
Планка с отверстиями.
Через 30 мин после внутрибрюшинного введения производных, соответствующих изобретению, каждую мышь помещали на 5 мин на автоматизированную планку с отверстиями и отмечали по минутам количество обследованных отверстий.
Эффективная доза 50 вычисляется как функция полученных результатов.
Фенилбензохинон (ФБХ).
Боль в брюшине у мышей вызывается внутрибрюшинной инъекцией фенилбензохинона (ФБХ). Уменьшение болевого синдрома, характеризующегося скрюченным положением животного, исследуют при помощи инъекции испытуемого продукта за 30 мин до введения ФБХ.
Эффективная доза 50 вычисляется как функция процентного отношения ослабления болевого синдрома к контрольным животным.
Антагонизм к бронхоспазму, вызванному гистамином.
Морских свинок помещали в замкнутое пространство, где распыляли гистамин и оставляли только тех животных, у которых ясные признаки асфиксии возникали в течение 4 мин.
Исследуемое вещество вводится партии морских свинок за 30 мин до нового помещения их в камеру для контроля за резистентностью к гистамину. Морская свинка считается защищенной, если она выдерживает десять минут, оставаясь в аэрозоле гистамина, без появления признаков асфиксии.
Средняя эффективная доза рассчитывается как функция полученных результатов.
Противогистаминная активность.
Определяли дозу, защищающую 50% морских свинок относительно смертельной дозы гистамина.
Продукт вводится за 30 мин до внутривенной инъекции солянокислого гистамина. Эффективная доза 50 высчитывается, как функция полученных результатов.
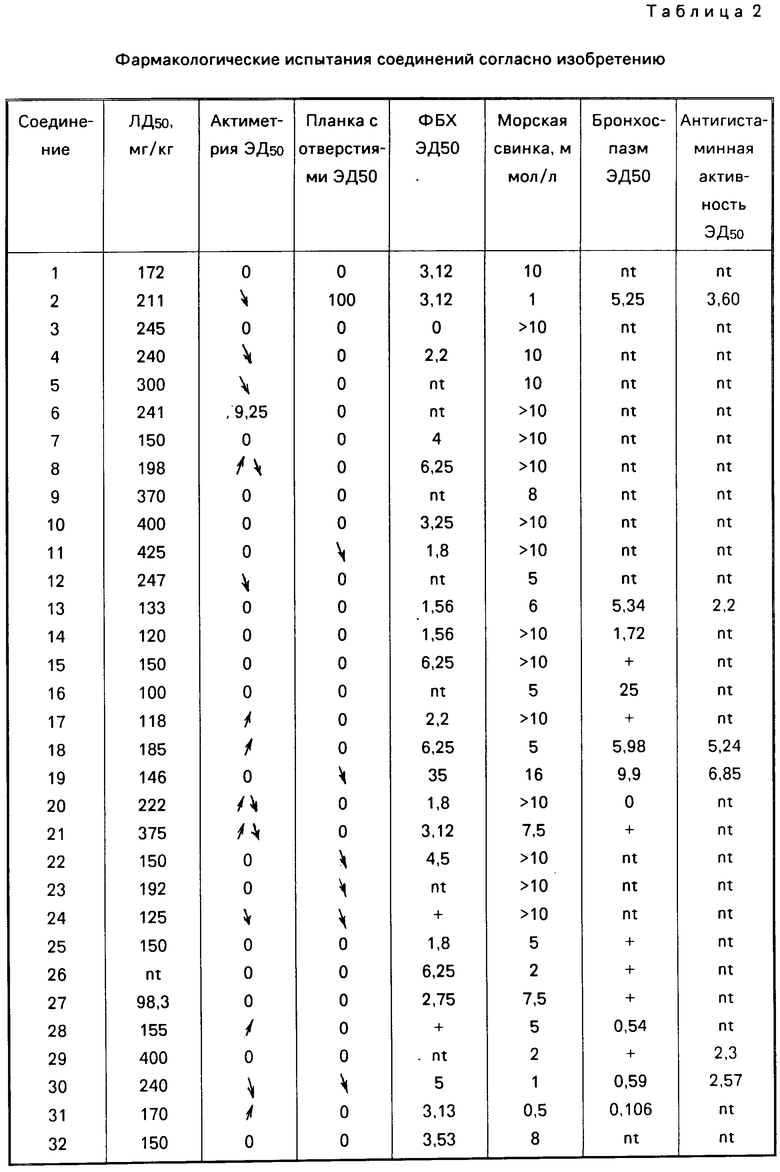
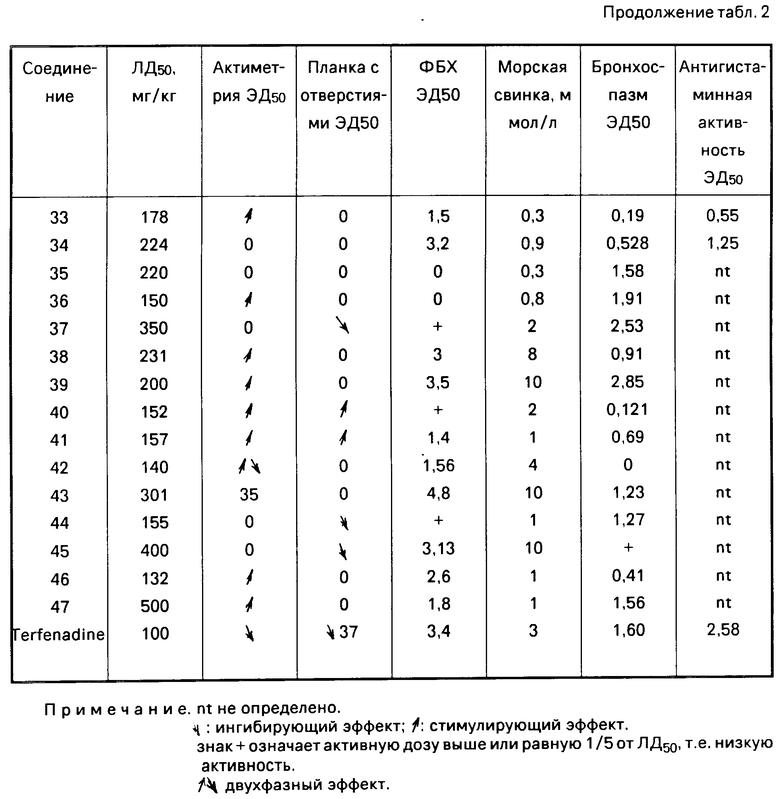
Результаты приведены в табл. 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИПЕПТИДНОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2165423C2 |
| ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА СО ВСТРОЕННЫМИ В УГЛЕВОДОРОДНУЮ ЦЕПЬ ОСТАТКАМИ ЦИКЛОПЕНТАНА | 2014 |
|
RU2589054C2 |
| Оксазолидиноны на основе производных пиридоксина, обладающие антибактериальной активностью | 2024 |
|
RU2836570C1 |
| НОВЫЕ ПИРРОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2607788C2 |
| 7-АЦИЛАМИНОЦЕФАЛОСПОРИНЫ, ЗАМЕЩЕННЫЕ В ПОЛОЖЕНИИ 3 ЦИКЛИЧЕСКИМИ АМИНОГУАНИДИНОВЫМИ ГРУППАМИ | 1999 |
|
RU2245884C2 |
| ИНГИБИТОРЫ ТРОМБИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ЗАЩИЩЕННОЕ ПРОИЗВОДНОЕ | 1996 |
|
RU2176645C2 |
| АНАЛОГИ ВИТАМИНА D, СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2153491C2 |
| СПИРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА | 2008 |
|
RU2484092C2 |
| СОЕДИНЕНИЯ, ПРИГОДНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ TRPM8 | 2011 |
|
RU2608109C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИФЕНИЛАЗЕТИДИНОНА | 2005 |
|
RU2380361C2 |
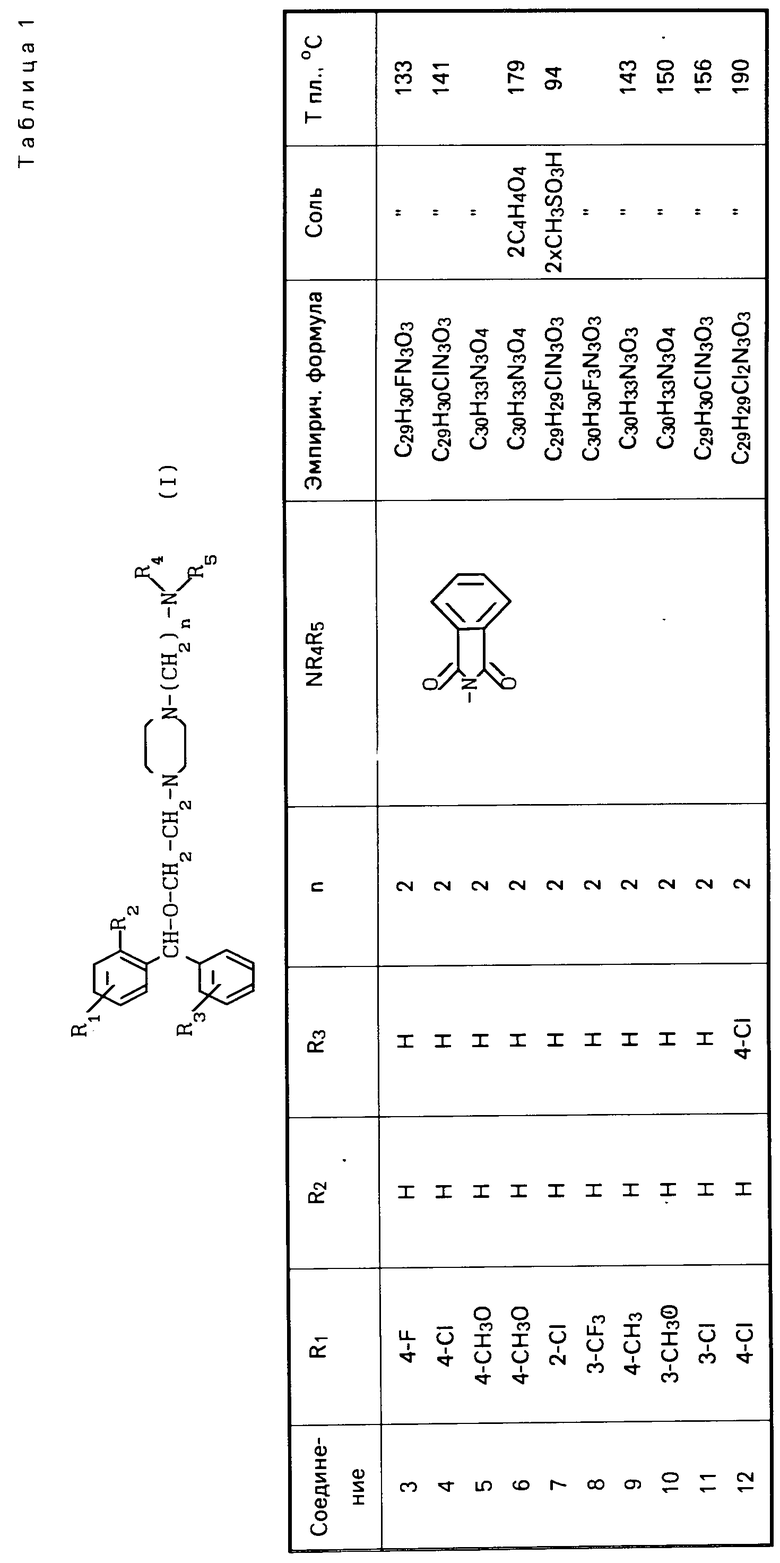
Сущность изобретения: продукт-производные бензгидрилоксиэтилпиперазина ф-лы 1, где R1-H, Hal низший алкил, низший алкокси, трифторметил; R2-H, Hal; R3-H, Hal, CF3; n - целое число 2 - 6, R4 и R5 - один Н, другой бензоил, замещенный NO2 или CH3O или R4 и R5 вместе с атомом азота, с которым они связаны, гетероциклическую группу, как-то сукцинимидил, 4-фенилсукцинимидил, 2- оксобензимидазолинил, 3- бензил -2- оксобензимидазолинил,1,2,3,4- тетрагидро -2,4- диоксохин - азолинил,3,4-дигидро-4- оксохиназолинил,3,4- дигидро-4-оксо-2-метилхиназолинил, 3,7-дигидро-1,3-диметил- 2,6-диоксо-1Н-пуринил, 3,7-дигидро-3,7-диметил-2,6-диоксо-1Н-пуринил. Реагент 1: амин ф-лы X-(CH2)n-NR4R5, где x-Ha1, тозил. Реагент 2: бензгидрилоксиэтилпиперазин. Условия реакции: избыток реагента указанного амина, апротонный растворитель. Соединения обладают противогистаминной активностью без побочного седативного действия. Структура соединения ф-лы 1 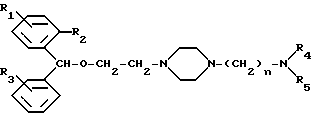 2 табл.
2 табл.
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗГИДРИЛОКСИЭТИЛПИПЕРАЗИНА общей формулы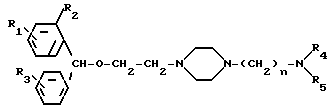
где: R1 водород, галоид, низший алкил, низший алкокси или трифторметилрадикал;
R2 водород или галоид;
R3 водород, галоид или трифторметилрадикал;
n-2-6 целое число;
R4 и R5 один водород, другой группа бензоила, замещенная нитро или метокси, или R4 и R5 образуют вместе с азотом, с которым они связаны, гетероциклическую группу, выбираемую из группы: сукцинимидил, 4-фенилсукцинимидил, 2-оксобензимидазолинил, 3-бензил-2-оксобензимидазолинил, 1,2,3,4-тетрагидро-2,4-диоксохиназолинил, 3,4-дигидро-4-оксохиназолинил, 3,4-дигидро-4-оксо-2-метилхиназолинил, 3,7-дигидро-1,3-диметил-2,6-диоксо-1H-пуринил, 3,7-дигидро-2,7-диметил-2,6-диоксо-1H-пуринил,
отличающийся тем, что соединение общей формулы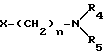
где n, R4 и R5 имеют указанные значения;
X группа галогена или тозила,
подвергают взаимодействию с избытком бензгидрилоксиэтил-пиперазина общей формулы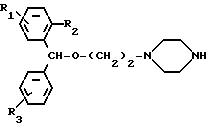
где R1 R3 имеют указанные значения,
в среде инертного апротонного растворителя, такого, как толуол, и в случае необходимости полученный целевой продукт превращают в кислые аддитивные соли.
| Патент США N 4068069, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-04-10—Публикация
1987-07-09—Подача