Изобретение относится к способу получения нового соединения группы 6-(4)-тиопиримидинов, конкретно тиопиримидина, содержащего цианэтильную группу при циклическом атоме азота, а в 4-м и 5-м положении молекулы OCH3 и NH2-группы соответственно формулы 1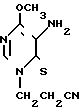 (I)
(I)
Известен предполагаемый синтез 4-карбметокси-5-(N-формил-N-(2-цианоэтил-амино)-1,2,3-тиадиазола формулы (А)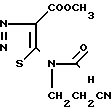 (A) Проведено изучение биологической активности соединения (А). Установлено, что оно обладает высокой биологической активностью.
(A) Проведено изучение биологической активности соединения (А). Установлено, что оно обладает высокой биологической активностью.
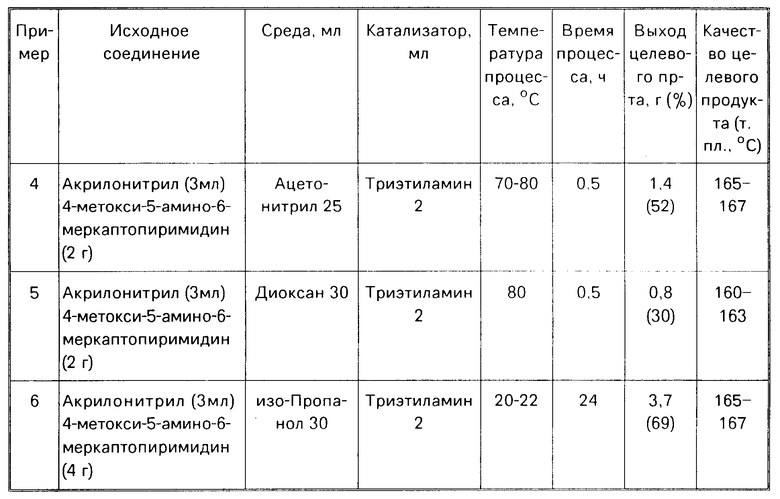
Для синтеза соединения I, которое относится к группе тиопиримидинов, использована реакция цианэтилирования. В ряду производных пиримидина реакция цианэтилирования известна для соединений, содержащих оксо-группы во 2,4 и 6-м положениях молекулы пиримидина [1] Эта реакция проходит с использованием основного катализатора в водной среде или в среде органического растворителя при комнатной или повышенной температуре.
Однако цианэтилирование производных пиримидина, молекула которых содержит одновременно три различных реакционных центра (NH2, SH, N-циклический) не известно.
Цель изобретения способ получения нового производного 4-(6)-тиопиримидина формулы I, содержащего цианэтильную группу при циклическом атоме азота в положении 1 пиримидинового цикла.
Поставленная цель достигается благодаря исходному соединению формулы II, в качестве которого предлагается использовать 6-тиопиримидин, молекула которого, наряду с NH2-группой в 5-м положении, содержит заместитель в 4-м положении цикла метоксильную группу, позволяющий провести реакцию цианэтилирования целенаправленно, в именно по циклическому атому азота, находящемуся в положении 1 пиримидинового цикла.
Заявляемый способ получения 1-(21-цианоэтил)-4-метокси-5-амино-6-тио-1,6-ди- гидропиримидина (I) осуществляют следующим образом.
Исходный 4-метокси-5-амино-6-меркаптопиримидин подвергают взаимодействию с акрилонитрилом или его предшественником-нитрилом 3-галогенпропионовой кислоты в среде растворителя в присутствии основного катализатора в температурном интервале 20 80оС. Целевой продукт выделяют известным способом.
Схема заявляемого способа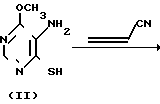
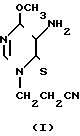
Впервые охарактеризовано и установлено строение соединения I. Данные элементного анализа, физико-химические константы I приведены в таблице.
Исходное соединение 4-метокси-5-амино-6-меркаптопиримидин формулы II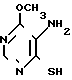 (II)
(II)
Его получают известным способом [2] 4-метокси-5-нитро-6-хлорпиримидин последовательно подвергают действию NaSH и Na2S2O4. В качестве растворителя используют H2O или органические растворители, например низшие спирты, циклические простые эфиры, нитрилы карбоновых кислот. В качестве основных катализаторов используют гидроокиси щелочных металлов, третичные амины (триэтиламин).
Известно, что взаимодействие гетероциклических соединений, содержащих группировку формулы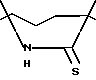 с акрилонитрилом или нитрилом β-галогенпропионовой кислоты проходит неоднозначно, так как приводит к образованию различных продуктов (N- или S-цианэтильных производных [3] или их смеси [4]) в зависимости от наличия и характера заместителей в исходном соединении. Этот факт подтвержден впервые для соединений ряда 5-амино-6-меркаптопиримидина. Установлено, что введение в соединение II CH3-группы в положение 2 цикла приводит к образованию только S-цианэтильного производного по схеме
с акрилонитрилом или нитрилом β-галогенпропионовой кислоты проходит неоднозначно, так как приводит к образованию различных продуктов (N- или S-цианэтильных производных [3] или их смеси [4]) в зависимости от наличия и характера заместителей в исходном соединении. Этот факт подтвержден впервые для соединений ряда 5-амино-6-меркаптопиримидина. Установлено, что введение в соединение II CH3-группы в положение 2 цикла приводит к образованию только S-цианэтильного производного по схеме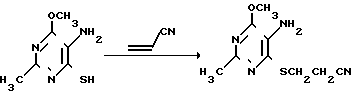 При замене в исходном соединении II заместителя в 4-м положении (OCH3-группу) на N(CH3)2 образуется продукт только N-цианэтилирования
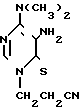
При замене в исходном соединении II заместителя в 4-м положении (OCH3-группу) на N(CH3)2 образуется продукт только N-цианэтилирования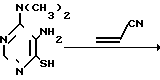
 Однако в случае, если исходное соединение II содержит в 4-м положении OCH3-группу, а в 5-м NH2-группу, то в результате его цианэтилирования образуется смесь S- и N-цианоэтильных производных. При этом основным продуктом является N-циаэтильное производное согласно схеме:
Однако в случае, если исходное соединение II содержит в 4-м положении OCH3-группу, а в 5-м NH2-группу, то в результате его цианэтилирования образуется смесь S- и N-цианоэтильных производных. При этом основным продуктом является N-циаэтильное производное согласно схеме: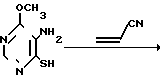
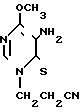
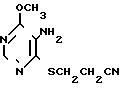 +
+ 
Таким образом, впервые найдена возможность введения цианэтильных групп по циклическому атому азота пиримидинового цикла в ряду производных 4-(6)-тиопиримидина.
Ранее в литературе не были описаны способы алкилирования по циклическому атому азота для тиопиримидинов.
Примеры иллюстрируют заявляемый способ получения соединения I.
П р и м е р 1. 1-(2'-Цианоэтил)-4-метокси-5-амино-6-тио-1,6-дигидропиримидин.
К суспензии 4 г 4-метокси-5-амино-6-меркаптопиримидина (II) в 30 мл изопропанола прибавляют 5 мл акрилонитрила и 3 мл триэтиламина. Реакционную массу нагревают до 80оС и перемешивают при этой температуре 25-45 мин. Через 15 мин образуется темно-коричневый раствор. Ход процесса контролируют хроматографически (силуфол, элюент хлороформ-метанол 10:1, Rf исходного 0,45). Процесс считают законченным, когда пятно исходного практически исчезает. Для этого в среднем требуется 35 мин. Реакционную массу охлаждают до 10-15оС и выпавший осадок 1 отфильтровывают, промывают 10 мл изо-пропилового спирта, затем 50 мл воды и сушат на воздухе.
Получают 3,2 г (60%) 1-(21-цианоэтил)-4-метокси-5-амино-6-тио-1,6-дигидропирими- дина (I). Более кристаллическое вещество, т.пл. 165-167оС (водный этанол).
Найдено, C 45,95; H 4,65; N 26,59; S 15,20.
C7H10N4OS
Вычислено, C 45,70; H 4,80; N 26,65; S 15,25.
ИК-спектр, см-1: 3440, 3334 (NH2), 2252 (CN)
УФ-спектр, λmax (lg ε), нм: 230,5 (4,09); 310,0 (3,90); 356,9 (4,15).
Спектр ПМР: 3,34 м.д. (CH2CN), 4,81 м.д. (N-CH2). Фильтрат после отделения I, а также изопропиловый спирт от промывки упаривают досуха, обрабатывают водой.
Получают 1 г 4-метокси-5-амино-6-цианоэтилтиопиримидина. Белое кристаллическое вещество, т.пл. 68оС (гексан).
Найдено, C 46,01; H 4,86; N 26,56; S 15,09.
M+ 210 C7H10N4OS
Вычислено, C 45,70; H 4,80; N 26,65; S 15,25.
М 210
ИК-спектр, см-1: 3436, 3346 (NH2), 2242 (CN).
УФ-спектр, λmax (lg ε), нм: 220,0 (4,09); 261,1 (3,78); 298,5 (3,96).
Спектр ПМР: 3,43 м.д. (CH2CN); 2,87 м.д. (S-CH2).
П р и м е р 2. К раствору 1 г 4-метокси-5-амино-6-меркаптопиримидина в 20 мл воды, содержащей 1 г КОН, при энергичном перемешивании прибавляют 2 г акрилонитрила, смесь перемешивают в течение 6 ч при температуре 20-22оС. Выпавший осадок отфильтровывают и промывают водой до нейтральной реакции.
Получают 0,8 г (59,2%) 1-(21-цианоэтил)-4-метокси-5-амино-6-тио-1,6-дигидропири- мидина (I), т.пл. 162-164оС.
Фильтрат после отделения I подкисляют разбавленной H2SO4 и выделяют 0,2 г исходного пиримидина.
П р и м е р 3. К раствору 1 г 4-метокси-5-амино-6-меркаптопиримидина в 30 мл метанола, содержащего 10 мл триэтиламина, при перемешивании прибавляют раствор из 1 г 3-хлорпропионитрила в 10 мл метанола. Смесь перемешивают при 60оС в течение 2 ч. Упаривают досуха и остаток обрабатывают водой. Осадок отфильтровывают.
Получают 0,7 (52%) соединения I, т.пл. 165-166оС.
П р и м е р 7. Получение 4-карбметокси-5-(N-формил-N-(2-цианоэтил-амино)-1,2,3-тиадиазола (соединение А).
К раствору 2 г (9,5 ммоль) 1-(2'-цианоэтил)-1,6-дигидро-4-метокси-5-амино-6-тио- пиримидина в 60 мл 10%-ного раствора соляной кислоты при интенсивном перемешивании и температуре (-5) 0оС прибавляют раствор 1,3 г (18,8 ммоль) нитрита натрия в 6 мл воды. Смесь выдерживают при комнатной температуре и перемешивании в течение 1,5 ч, затем экстрагируют этилацетатом (5х50 мл), экстракт сушат сульфатом натрия и упаривают под вакуумом. Получают 1,5 г смеси целевого продукта и его деформилированного производного. Смесь очищают колоночной хроматографией на силикагеле (элюент хлороформ). Получают 0,75 г (32,7%) указанного в заголовке продукта в виде кристаллического порошка, т.пл. 105-107оС, растворимого в диметилформамиде, диметилсульфоксиде, ацетоне, хлороформе, при нагревании в спирте, нерастворим в воде, устойчив при хранении на воздухе.
Использование: в синтезе биологически активных соединений. Сущность изобретения: способ получения 1-( 2′ -цианоэтил)-4-метокси-5-амино-6-тио-1,6-дигидропиримидина, C7H10N4OS , белое кристаллическое вещество, т.кип. 165 - 166°С (водный этанол). Реагент 1: 4-метокси-5-амино-6-меркаптопиримидин. Реагент 2: акрилонитрил или 3-галогенпропионитрил. Процесс ведут в водной среде или в органическом растворителе в присутствии основного катализатора при 20 - 80°С. Выход 52 - 69%. 1 табл.
СПОСОБ ПОЛУЧЕНИЯ 1-(2'-ЦИАНОЭТИЛ)-4-МЕТОКСИ-5-АМИНО-6-ТИО-1,6-ДИГИДРОПИРИМИДИНА формулы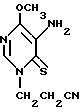
отличающийся тем, что 4-метокси-5-амино-6-меркаптопиримидин обрабатывают нитрилом акриловой кислоты или 3-галогенпропионитрилом в водной среде или среде органического растворителя в присутствии основного катализатора при 20
80oС.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Whitehead C.W., Traverso J.J | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J.Am | |||
| Chem | |||
| Soc | |||
| Приспособление для строгания деревянных полов, устраняющее работу на коленях | 1925 |
|
SU1956A1 |
Авторы
Даты
1995-05-20—Публикация
1992-04-10—Подача