Изобретение относится к способу получения 3-(гексадекансульфинил- и сульфонил-2-метоксиметилпропил)-(2-триметилоаммониоэтил)фосфата и его солей.
Известны пропил(триалкиламмониоалкил)фосфаты, которые замещены в положении 3 алкилмеркапто-, алкилсульфинил- и алкилсульфонил остатками, соединения, которые в положении 3 содержат алкилмеркапто-группу, например (3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат (Илмофозин), который обладает превосходными противоопухолевыми свойствами.
В настоящее время найдено, что аналогичные сульфинил- и сульфонилсоединения, а также соответствующие гептадецил- и октадецилпроизводные, подпадают под расширенную формулу изобретения, неожиданно обладают ин виво еще более лучшим действием, чем Илмофозин, в особенности оба соединения: (3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат и (2-метоксиметил-3-октадекансульфонилпропил)-(2-триметиламмониоэтил)фосфат.
Предметом изобретения является способ получения соединения общей формулы I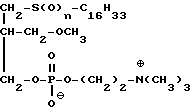 (I) в которой n 1 или 2 и их стереоизомеры, а также их фармакологически безопасные (совместимые) соли.
(I) в которой n 1 или 2 и их стереоизомеры, а также их фармакологически безопасные (совместимые) соли.
При этом предпочтительны соединения общей формулы I, в которых n 1 или 2.
Особенно предпочтительны (3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат и (2-метоксиметил-3-октадекансульфонилпропил)-(2-триметиламмониоэтил)фосфат.
Предметом изобретения являются все стереоизомерные соединения формулы I, которые получаются на основании асимметрического атома углерода или сульфоксидной группы.
Соединения общей формулы (I) получают известными способами;
соединение общей формулы II, которое может быть в виде рацемата или в виде энантиомера,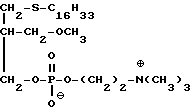 (II)
(II)
В качестве окислителя используют предпочтительно 30%-ную перекись водорода в ледяной уксусной кислоте. При использовании эквимолярных количеств получают сульфоксиды, с трех-, пятикратным избытком окислителя получают соответствующие сульфоны. Для окисления также можно использовать органические перекиси, например м-хлорнадбензойную кислоту, причем применяют инертные растворителя, например метиленхлорид. Температура реакции составляет 0-50о С, предпочтительно 20о С.
Фармакологические совместимые соли получают известным способом, например путем нейтрализации соединений формулы I с помощью нетоксических неорганических или органических кислот, например соляной, серной, фосфорной, бромводородной, уксусной, молочной, лимонной, яблочной, салициловой, малоновой, малеиновой или янтарной.
Предлагаемые в изобретении новые вещества общей формулы I и их соли могут вводиться в жидкой или твердой форме кишечно или парентерально. При этом принимают во внимание все обычные формы введения, например таблетки, капсулы, драже, сиропы, растворы, суспензии и т.д. В качестве инъекционной среды используют предпочтительно воду, которая содержит обычные в случае инъекционных растворов добавки, как стабилизаторы, агенты растворения и буферы.
Такого рода добавки тартратные и цитратные буферы, этанол, комплексообразователи (как этилендиаминотетрауксусная кислота и ее нетоксичные соли) и высокомолекулярные полимеры (как жидкий полиэтиленоксид) для регулирования вязкости. Жидкие носители для инъекционных растворов должны быть стерильны и предпочтительно защиты в ампулы. Твердые носители представляют собой, например, крахмалы, лактозу, маннит, метилцеллюлозу, тальк, высокодисперные кремниевые кислоты, высокомолекулярные жирные кислоты (как стеариновые кислота), желатина, агар-агар, фосфат кальция, стеарат магния, животные и растительные жиры и твердые высокомолекулярные полимеры (как полиэтиленгликоли). Пригодные для орального применения композиции в желательном случае могут содержать вкусовые и подслащивающие вещества.
Дозировка может зависеть от различных факторов; способ введения, вид, возраст и/или индивидуальные состояния. Суточно вводимые дозы составляют примерно 0,05-100 мг/кг массы тела.
Действие веществ испытывалось на модели ин виво на индуцированной метилхлорантреном фибросаркоме мыши.
Описание опыта.
Самкам СУ6F4-мышей в день инъекцируют подкожно 1х105 мет-А-клеток. Терапию осуществляют ежедневно, начиная с 1 дня вплоть до 21 дня с помощью 2,5,10 и 40 мг/кг перорально. Число животных на группу 1, В качестве параметров определяют:
1) объем опухоли в 7, 14, 21 и 28 день после инокуляции опухолевых клеток.
2) масса опухоли в 28 день.
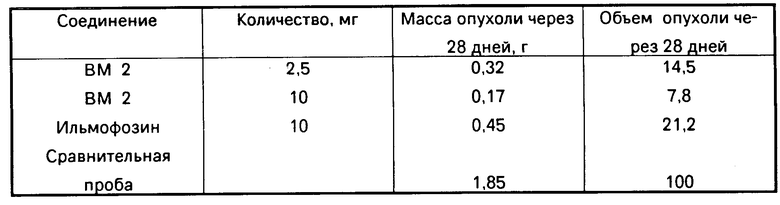
В качестве сравнительного вещества выбирают не окисленное на сере соединение (3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат (Илмофозин) и соединение (3-октадецилокси-2-метоксипропил)-(2-триметиламмониоэтил)фосфат (ЕТ-18-ОСН3); в качестве позитивного контроля берут циклофосфамид (см. таблицу).
При рассмотрении объема опухоли отчетливо видно, что 2,5 мг ВМ 2 (=(3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат а) обладают такой же эффективностью, как и 10 мг Илмофозина. Вес опухоли в 28 день показывает тот же результат. ВМ 2 отчетливо эффективнее, чем Илмофозин.
П р и м е р 1. (3-Гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат.
К 7,56 г (14 моль) (3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфата в 70 мл уксусной кислоты добавляют 4,2 мл (42 ммоль) 30%-ной перекиси водорода и перемешивают при комнатной температуре. Спустя 24 ч добавляют еще раз 1,4 мл перекиси водорода и перемешивают в целом 72 ч. раствор концентрируют на ротационном испарителе при 20о С, остаток смешивают с диэтиловым эфиром и оставляют стоять в течение ночи в холодильнике. Декантируют эфирный раствор от вязкого осадка, растворяют его в 1 мл воды и раствор подвергают сушке вымораживанием. Получают таким образом 5,2 г (65%) желательного соединения в аморфной форме с 1 моль воды; Rf значение на RF-18-силикагелевой пластине с помощью смеси растворителей ацетон (7)) вода (3)) 0,1% ледяной уксусной кислоты: 0,35. SO-производное: 0,39. Исходный материал: 0,28.
Аналогичным образом путем применения (-)-, соответственно, (+)-энантиомерного простого тиоэфира получают сульфонильные производные:
а) (-)-(3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосф ат;
б) (+)-(3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосф ат;
в) (3-октадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат;
г) (-)-(3-октадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфа т;
д) (+)-(3-октадекансульфонил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфа т.
П р и м е р 2. (3-Гексадекансульфинил-2-метоксиметилпропио)-(2-триметиламмониоэтил)фосфат.
К 10,8 г (20 ммоль) (3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонилэтил)фосфата в 100 мл ледяной уксусной кислоты добавляют 2 мл (20 ммоль) 30% -ной перекиси водорода и раствор оставляют стоять при комнатной температуре в течение 144 ч. Раствор концентрируют на ротационном испарителе, остаток, смотря по обстоятельствам, обрабатывают дважды толуолом и снова концентрируют. Затем остаток перемешивают с 250 мл ацетона, отфильтровывают от небольшого количества нерастворимой части и фильтрат медленно испаряют. После того, как испарилась примерно половина ацетона, осаждается осадок. Отсасывают и получают 3,0 г (27%) желательного продукта. Т.пл. 235-240о С; Rf-значение на RP-18-силикагелевой пластине с помощью смеси растворителей ацетон (7)) вода (3)) 0,1% ледяной уксусной кислоты: 0,39, SO2-производное: 0,35; исходный материал: 0,28.
Аналогичным образом путем применения (-)- соответственно (3)-энантиомерного простого тиоэфира получают следующие сульфоксиды:
а) (-)-(3-гексадекансульфинил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосф ат;
б) (-)-(3-гексадекансульфинил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосф ат.
П р и м е р 3. Аналогично примеру 2 путем использования соответствующего октадецильного производного получают: (3-октадекансульфинил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфат и путем применения соответствующего (-)- соответственно (+)- энантиомерного простого тиоэфира получают:
а) (-)-(3-октадекансульфинил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфа т;
б) (+)-(3-октадекансульфинил-2-метоксиметилпропил)-(2-триметиламмониоэтил)фосфа т.
П р и м е р 4. Таким же образом, как и в примере 1, с использованием в качестве исходного соединения (-)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмтнийэтил)фосфа т ( [α]D20-6,1о; с 1, в метаноле) получают (-)-(3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосф ат, выпадающий в осадок с 1 моль воды. Выход 85% p [α]D20 -1,9о, с 1, в метаноле.
П р и м е р 5. Таким же образом, как и в примере 1, с использованием в качестве исходного соединения (+)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфа т ( [α]D20 +5,9о, с 1, в метаноле) получают (+)-(3-гексадекансульфонил-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосф ат, образующийся с 1 моль воды с выходом 79% [α]D20 + 1,7о, с 1, в метаноле.
П р и м е р 6. Использующиеся в примерах энантиомеры получают следующим образом:
А) 43 г этилового эфира (±) 3-гексадецилмеркапто-2-метоксиметилпропионовой кислоты в смеси со 100 мл диоксана и 200 мл 10н. серной кислоты нагревают в течение 18 ч при 130оС. После охлаждения раствор упаривают и остаток растворяют в 500 мл изогексана. Раствор оставляют стоять в течение некоторого временим при -20о С и отсасывают затем выпадающий осадок. В результате получают 25,3 г (56%) (+)-гексадецилмеркапто-2-метоксиметилпропионовой кислоты. Т.пл. 37-40о С.
Б) 25 г (+)-3-гексадецилмеркапто-2-метоксиметилпропионовой кислоты растворяют в 250 мл метиленхлорида с добавкой 10 капель диметилформамида и смешивают раствор с 10,4 мл тионилхлорида. Смесь перемешивают в течение 3 ч при комнатной температуре в атмосфере азота, упаривают в ротационном выпарном аппарате, растворяют осадок в 100 мл толуола, снова упаривают и повторяют процесс еще дважды. В результате получают 25,7 г хлорангидрида ( )=-3-гексадецилмеркапто-2-метоксиметилпропионовой кислоты в виде маслянистой жидкости.
В) К 9,2 г (-)-фенилглицинола, растворенного в 220 мл абсолютного диоксана, добавляют 11,2 мл триэтиламина и добавляют к смеси по каплям при охлаждении льдом при 10о С раствор 25,07 г полученного в соответствии с пунктом Б хлорангидрида кислоты в 200 мл диоксана. Охлаждение прекращают и смесь перемешивают в течение ночи. Выпадающий осадок отсасывают и фильтрат упаривают. Остаток разделяют на 800 г силикагеля (подвижная фаза: смесь ацетона и толуола в объемном соотношении 1:5). В результате получают оба диастереомера амида N-[(-)-(2-окси-1-фенилэтил] -3 -гексадецилмеркапто-2-метоксиметилопропионовой кислоты.
Выходящий первым диастереомер получается в количестве 9,7 г (58%). Т.пл. 81-84о С; [α]
Выходящий с меньшей скоростью диастереомер получается в количестве 11,1 г (выход 66%). Т.пл. 82-84о С; [α]
Г) Оба диастереомера разделяли на энантиомеры следующим образом; 3 г диастереомера растворяют в 30 мл абсолютного диоксана и смешивают раствор с 7,5 мл 2н. серной кислоты. Смесь нагревают при интенсивном перемешивании в течение 10 ч при 100о С, затем охлаждают, разделяют фазы, органическую фазу дважды встряхивают в делительной воронке с водой, высушивают и упаривают. Остаток растворяют в 30 мл изогексана, охлаждают раствор до -20о С и через 2 ч отсасывают выпадающий осадок. В результате получают 1,97 г (выход 87%) соответствующего энантиомера (без примеси другого энантиомера) 3-гексадецилмеркапто-2-метоксиметилпропионовой кислоты. Т.пл. 38-40о С.
Из выходящего с большей скоростью диастереомера получают (-)-энантиомеp. [α]D20: 6,2о, с= 1, метанол.
Из выходящего с меньшей скоростью диастереомера получают (+)-энантиомер. [α]D20 +5,9о, с 1, метанол.
Д) К 220 г литийалюминийгидрида в 20 мл абсолютного диэтилового эфира добавляют по каплям 1,85 г энантиомера 3-гексадецилмеркапто-2-метоксиметилпропионовой кислоты, растворенного в 150 мл абсолютного диэтилового эфира, и кипятят с обратным холодильником в течение 2 ч. После охлаждения добавляют небольшое количество воды для разложения, раствор высушивают с помощью сульфата натрия и упаривают. Остаток подвергают очистке на 100 г силикагеля (подвижная фаза: смесь диэтилового эфира и гексана в объемном соотношении 1: 1). В результате 1,2 г (выход 68%) 3-гексадецилмеркапто-2-метоксиметилпропанола в виде воскообразного вещества.
Из (-)-кислоты получат (+)-спирт. [α]D20 +5,7о, с 1, метиленхлорид.
Из (+)-кислоты получают (-)-спирт. [α]D20 -6,0о, с 1, метиленхлорид.
Е) К 1,08 г изомера 3-гексадецилмеркапто-2-метоксиметилпропанола в 10 мл метиленхлорида добавляют при -10о С вначале 1,3 мл триэтиламина, а затем по каплям раствор 1,3 г 2-хлор-2-оксо-1,3,2-диоксофосфолана в 5 мл метиленхлорида и продолжают перемешивать смесь без охлаждения в течение 3 ч. После этого ее упаривают и остаток обрабатывают диэтиловым эфиром. Нерастворимый остаток отфильтровывают, а фильтрат упаривают. В результате получают 1,35 г маслянистой жидкости, которую растворяют в 25 мл насыщенного триметиламином ацетонитрила. Раствор перемешивают в течение 48 ч, отсасывают выпадающий осадок, тщательно промывают его ацетонитрилом и ацетоном и подвергают очистке с помощью колоночной хроматографии на силикагеле (подвижная фаза; смесь метиленхлорида, метанола и воды в объемном соотношении 65:24:4). В результате получают 0,56 г (выход 34% от теоретического) целевого продукта.
Из (-)-спирта получают (+)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфа т с 1 моль воды. [α]D20 + 5,9о, с 1, метанол.
ИЗ (+)-спирта получают (-)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфа т с 1 моль воды. [α]D20 -6,1о, с 1, метанол.
П р и м е р 7. Таким же образом, как и в примере 2, с использованием (-)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфа та ( [α]D20 -6,1о, с )= 1, метанол) получают (-)-(3-гексадекансульфинил-2-метоксиметилпропил)-(2-триметилоаммонийэтил)фос фат, образующийся с 1 моль воды. Выход 91% [α]D20 -4,7о, с 1, метанол.
П р и м е р 8. Таким же образом, как и в примере 2, с использование в качестве исходного соединения (+)-(3-гексадецилмеркапто-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфа та ( [α]D20 +5,9о с 1, метанола) получают (+)-гексадекансульфинил-2-метоксиметилпропил)-(2-триметиламмонийэтил)фосфат, образующийся с 1 моль воды. Выход 87% [α]D20 +4,4о, с 1, метанол.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 2-аммонийэтилфосфатов | 1983 |
|
SU1376948A3 |
| ЦИКЛОГЕКСАНОЛНИТРАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1991 |
|
RU2106339C1 |
| НОВЫЕ ТИАЗОЛИДИНДИОНЫ И СОДЕРЖАЩИЕ ИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 1994 |
|
RU2122002C1 |
| Способ получения N-замещенных производных азиридин-2-карбоновой кислоты или натриевой соли кислоты | 1985 |
|
SU1431676A3 |
| Способ получения производных индазола | 1977 |
|
SU680643A3 |
| СРЕДСТВО ДЛЯ КОЛОРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ АНАЛИТА | 1989 |
|
RU2015513C1 |
| Способ получения 2-циано-6-оксибензтиазола и его варианты | 1980 |
|
SU1055332A3 |
| Способ получения сульфонамидов алкилфенилкарбоновых кислот | 1981 |
|
SU1088664A3 |
| Способ получения производных феноксиалкилкарбоновой кислоты,их солей,сложных эфиров и амидов | 1979 |
|
SU1052157A3 |
| Способ получения производных резоруфина | 1986 |
|
SU1621811A3 |
Сущность изобретения: продукт ф-лы: C16H33-S(O)n-CH2-CH(CH2-OCH3)-CH2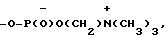 где n-1 или 2. Выход 27%. Т.пл. 235-240°С. Реагент 1: C16H33-S-CH2-CH(CH2-OCH3)-CH2
где n-1 или 2. Выход 27%. Т.пл. 235-240°С. Реагент 1: C16H33-S-CH2-CH(CH2-OCH3)-CH2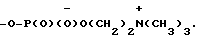 Реагент 2: окислитель. Условия реакции: CH3COOH лед. 1 табл.
Реагент 2: окислитель. Условия реакции: CH3COOH лед. 1 табл.
Способ получения 3-(гексадекансульфонил- или сульфинил-2-метоксиметилпропил)-(2-триметиламмонио-этил)-фосфата общей формулы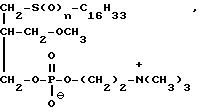
где N 1,2,
их стереоизомеров или фармакологически приемлемых солей, отличающийся тем, что соединение формулы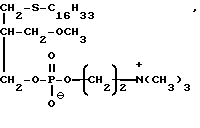
в виде рацемата или энантиомера обрабатывают окислителем с последующим переводом в случае необходимости в оптические изомеры и/или фармакологически приемлемые соли.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ВЕСЫ ДЛЯ АВТОМАТИЧЕСКОГО ВЗВЕШИВАНИЯ СЫПУЧИХ ТЕЛ | 1945 |
|
SU69968A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-05-20—Публикация
1990-03-02—Подача