Изобретение относится к области органической химии, конкретно к новому химическому соединению комплексу бис- [1(3)-изобутилтиоэтил-6-метилурацилу] PtCl2 формулы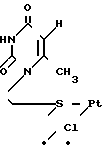
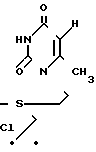 (Х 989) проявляющему иммунотропную активность.
(Х 989) проявляющему иммунотропную активность.
Аналогом по строению и назначению является 6-метилурацил, синтез и свойства которого описаны в литературе [1]
6-Метилурацил получают путем перемешивания мочевины, ацетоуксусного эфира, этилового спирта и концентрированной соляной кислоте с последующим выделением β-ураминокротонового эфира, который обрабатывают раствором едкого натра, кипятят 2-3 ч при 95оС, охлаждают и подкисляют соляной кислотой при 65оС, выпавшие кристаллы при охлаждении отфильтровывают. Общий выход 6-метилурацила равен 50-55% [1]
Недостаток 6-метилурацила в том, что он достоверно стимулирует реакцию ГЗТ (гипрочувствительность замедленного типа) к ДНФБ (2,4-динитробензол).
Целью изобретения является расширение средств воздействия на живой организм, характеризующихся выраженной иммунотропной активностью и разработка способа получения.
Поставленная цель достигается синтезом нового комплекса PtCl2 с бис-[1(3)-изобутилтиоэтил-6-метилурацила] Номер регистрационного удостоверения 9991390 от 05.10.90. Способ получения комплекса заключается во взаимодействии K2PtCl4 в водной ацетоновой среде с 1(3)-изобутилтиоэтил-6-метилурацилом в течение 3 ч при комнатной температуре, при молярном соотношении компонентов 1,2:2,0.
Исследования проводили на белых беспородных мышах массой 15,0-17,0 г, полученных из питомника лабораторных животных "Рапполово" АМН СССР.
Острая токсичность определялась на беспородных мышах обоего пола при однократном внутрибрюшинном введении. Вводились дозы от 5 до 1600 мг/кг. После введения токсических доз через 5-10 мин у животных наблюдалось угнетенное состояние, вытягивание конечностей, снижение подвижности. Смерть наступала от остановки дыхания.
Параметры токсичности определяли по методу Кербера. При внутрибрюшинном введении ЛД50 соединения составила 400,0±36,2 мг/кг.
На основании классификации токсичности веществ при введении под кожу и в брюшную полость данное соединение относится к малотоксичным. Влияние соединения Х-989 на иммунную систему изучали на модели гиперчувствительности замедленного типа (ГЗТ) и антителообразования.
Гиперчувствительность замедленного типа к 2,4-динитрофторбензолу (ДНФБ) воспроизводили сенсибилизацией животных нанесением на кожу живота 25 мкл 0,5% -ного раствора ДНФБ в смеси ацетона с оливковым маслом (4:1). Через 5 сут после сенсибилизации на предварительно измеренные микрометром уши капали по 20 мкл 0,25%-ного раствора ДНФБ. Реакцию оценивали по приросту толщины ушей через 24 ч после нанесения разрешающей дозы ДНФБ. Соединение вводили в дозе 40 мг/кг (1/10 ЛД50) в течение 4 сут, начиная с первого дня после сенсибилизации.
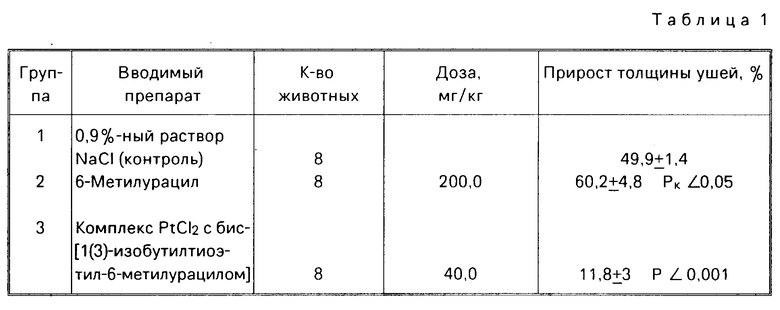
Влияние соединения и метилурацила на реакцию ГЗТ у мышей дано в табл. 1.
Таким образом, значение толщины прироста ушей в опытной группе существенно ниже (P  0,006), чем в контрольной, что позволяет говорить о наличии у комплекса PtCl2 с бис-[1(3)-изобутилтиоэтил-6-метилурацилом] выраженного супрессирующего влияния на клеточное звено иммунитета, в отличие от структурного аналога метилурацила, который достоверно стимулирует реакцию ГЗТ к ДНФБ.
0,006), чем в контрольной, что позволяет говорить о наличии у комплекса PtCl2 с бис-[1(3)-изобутилтиоэтил-6-метилурацилом] выраженного супрессирующего влияния на клеточное звено иммунитета, в отличие от структурного аналога метилурацила, который достоверно стимулирует реакцию ГЗТ к ДНФБ.
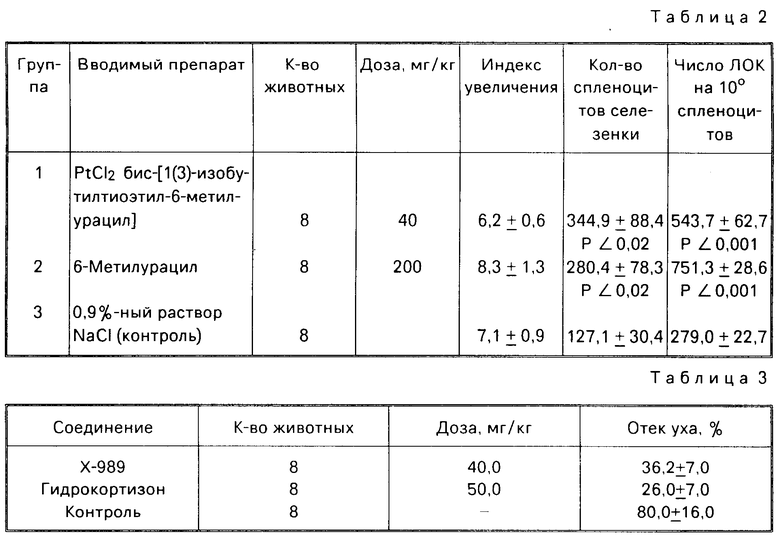
Влияние соединения Х-989 на образование АОК в селезенке беспородных мышей-самцов дано в табл. 2.
Соединение также, как и метилурацил, существенно стимулирует образование АОК, не влияя на массу селезенки, но увеличивая количество спленоцитов.
П р и м е р 1. В плоскодонную колбу емкостью 50 мл засыпают 1 г K2PtCl4, приливают 10 мл воды, перемешивают до растворения и прибавляют по каплям при перемешивании на магнитной мешалке 1,167 г (0,0048 моль) 1(3)-изобутилтиоэтил-6-метилурацила в 10 мл ацетона. Полученную реакционную смесь перемешивают 3 ч, ацетон отгоняют на испарителе ИР-1М в вакууме водоструйного насоса, сливают воду декантацией с выпавшего комплекса в воде светло-желтого цвета в виде мази, промывают водой для удаления солей и экстрагируют хлороформом, хлороформ отгоняют на роторном испарителе ИР-1М в вакууме водоструйного насоса и получают 1,622 (90%) комплекса PtCl2 c бис-[1(3)-изобутилтиоэтил-6-метилурацила]-цис-конфигурации, хорошо растворимого в ацетоне, хлороформе.
Найдено, C 33,50; H 4,50; N 6,29; S 8,50; Cl 10,0; Pt 25,7.
Вычислено для C22H36 N4O4S2, С 35,20; H 4,83; N 7,46; Cl 9,45; S 8,54; Pt 25,99; O 8,53.
ИК-спектр (ν, см-1): 332,318 (валентные колебания PtCl2), 307 (вал. колец, Pt-S).
Иммунотропная активность соединения иллюстрируется следующими примерами.
П р и м е р 2. В качестве модели клеточного иммунитета использовали реакцию гиперчувствительности замедленного типа (ГЗТ) у беспородных мышей. Реакцию ГЗТ воспроизводили известным способом, сенсибилизируя мышей нанесением на выстриженный живот 25 мкл 0,5%-ного раствора 2,4-динитрофторбензола (ДНФБ) в смеси ацетона с оливковым маслом (4:1). Разрешающую дозу (20 мкл 0,25% -ного раствора ДНФБ) наносили на 4-е сут после сенсибилизации на уши с предварительно измеренной толщиной. Соединения вводили внутрибрюшинно в дозе 1/10 ЛД50с +1 по +4 день. Всего 4 введения. Структурный аналог соединения 6-метилурацил, взятый в качестве эталона, вводили в общепринятой дозе (200 мг/кг) по той же схеме.
П р и м е р 3. Влияние соединения на гуморальное звено иммунного ответа определяли по методу N.K. Jerne, A.A. Nordin [2] в модификации A. Cunningham [3] Мышей иммунизировали внутрибрюшинным введением нориммунной дозы эритроцитов барана за 4 полных суток до опыта. Взвесью эритроцитов барана и комплемента морской свинки в соотношении 1:1:2 заполняли камеры. После инкубации в термостате при температуре 37оС в течение 1,5 ч подсчитывали визуально число зон гемолиза, соответствующее количеству антителообразующих клеток (АОК). Производили перерасчет АОК на 106 спленоцитов. Соединение вводили на +1 +4 сутки поcле иммунизации в дозе 1/10 ЛД50, метилурацил в дозе 200 мг/кг по той же схеме.
Соединение Х-989 также, как и метилурацил, существенно стимулирует образование АОК, не влияя на массу селезенки, но увеличивая количество спленоцитов.
П р и м е р 4. Острая токсичность комплекса PtCl2бис-1(3)-изобутилтиоэтил-6-метилурацил определялась на беспородных мышах обоего пола массой 18-20 г при однократном внутрибрюшинном введении. Вводились дозы от 50 до 1600 мг/кг. После введения токсических доз через 5-10 мин у животных наблюдалось угнетенное состояние, вытягивание конечностей, снижение подвижности. Смерть наступала от остановки дыхания.
Элементный анализ целевого продукта сделан повторно после сушки в вакууме при 70оС.
Найдено, C 35,00; H 4,45; N 7,31; S 8,50; Cl 9,60; Pt 25,78.
Вычислено для C22H36N4O4S2 PtCl2, C 35,20; H 4,83; N 7,46; Cl 9,45; S 8,54; Pt 25,99; O 8,53; М.м. 750,6692, Т.пл. 204-205оС.
Для установления положения заместителя 1(3)-изобутилтиоэтил-6-метилурацила проведено исследование УФ-спектра при рН 1-12. рН 1 λmin 231,65 λmax 262,50 рН 7 λmin 231,85 λmax 262,50 рН 12 λmin 245,65 λmax 281,15
Установлено, что максимум поглощения УФ-спектров с изменением рН среды от 1 до 12 дает батохромный сдвиг на 18,65.
Параметры токсичности определяли по методу Кербера. При внутрибрюшинном введении ЛД50 соединения составила 400,0 ± 36,2 мг/кг. На основании классификации токсичности веществ при введении под кожу и в брюшную полость, данное соединение относится к малотоксичным.
Таким образом, малотоксичное соединение комплекс PtCl2˙бис-[1(3)-изобутилтиоэтил-6-метилурацил] характеризуется выраженной иммунотропной активностью, подавляя клеточное звено иммунитета и стимулируя антителогенез, что характерно для урацилов, замещенных по третьему атому азота цикла.
Следовательно, заместитель должен находиться в 3-ем положении и называться 3-изобутилтиоэтил-6-метилурацил или 2,4-диоксо-3-(5-метил-3-тиагексил)-6-метил-1,2,3,4-тетрагидропиримидин.
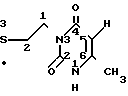
Поскольку комплекс PtCl2 с указанным лигандом образуется за счет связи с серой, то комплекс цис-PtCl2 ˙ 2L будет называться по женевской номенклатуре бис-[2,4-диоксо-6-метил-1,2,3,4-тетрагидропиримидин-3-(5-метил-3- тиагексил)-S] -цис-дихлорилатина или биc-[1-(2,6-диоксо-4-метил- 1,2,3,6-тетрагидропиримидин-1-ил)-5-метил-3-тиагексил-S] цис-дихлорилатина.
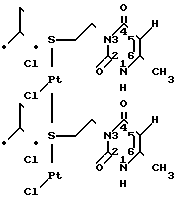
Структура целевого продукта устанавливается с помощью ИК-, ПМР-спектров, а также по аналогии со структурной известного продукта.
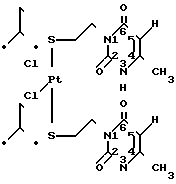
Известны полученные комплексные соединения Pt (II) и Pd (II) с 5-аминоурацилом и его метильными производными с монодентатной координацией лигандов только через атом азота экзоциклической аминогруппы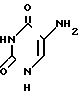
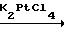
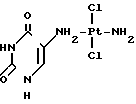
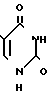
Строение доказано ИК-спектрами.
Известны комплексные соединения, соединенные через N3-платина пиримидин-2,4-диона и второй лиганд через экзоциклический кислородный атом цис-Pt(NH3)2 (1 MeU)2 и цис-Pt(NH3)2 (1 MeT)2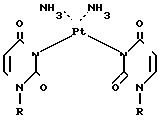
Известна серия двухядерных комплексов (X2)PtL2 M(Y2)Z ˙ n H2O L-1-метилурациланион (1-MeU, C5H5N2O2) или 1-метил- тиминанион (1-MeT, C6H7N2O2) связь Pt через N3 положение и второй металл через О4 положение
X2 и Y2 (NH3)2, этилендиамин, ен; 2,2-бипиридин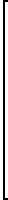
 P
P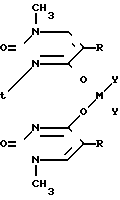
 Z·nH2O комплексы охарактеризованы элементным анализом, спектроскопическими методами.
Z·nH2O комплексы охарактеризованы элементным анализом, спектроскопическими методами.
В нашем случае комплекс PtCl2 образуется за счет связи с серой В ИК-спектре комплекса имеются две очень сильные полосы в области 318, 332 см-1, относящиеся к валентным колебаниям связи PtCl и однозначно свидетельствующие об образовании координационного соединения типа цис-PtCl2 ˙ 2L (L монодентатный лиганд). Полосы поглощения в области 305-310 см-1 принадлежат валентным колебаниям связи Pt-S. Полосы поглощения в области 3130 см-1 характерны для валентных колебаний ν (N-1)H, полосы поглощения в области 1660, 1720 характерны для кольца урацила (νC2=0, νC4=0,
В ИК-спектре комплекса имеются две очень сильные полосы в области 318, 332 см-1, относящиеся к валентным колебаниям связи PtCl и однозначно свидетельствующие об образовании координационного соединения типа цис-PtCl2 ˙ 2L (L монодентатный лиганд). Полосы поглощения в области 305-310 см-1 принадлежат валентным колебаниям связи Pt-S. Полосы поглощения в области 3130 см-1 характерны для валентных колебаний ν (N-1)H, полосы поглощения в области 1660, 1720 характерны для кольца урацила (νC2=0, νC4=0,  N-C=0).
N-C=0).
ПМР-спектр 3-изобутилтиоэтил-6-метилурацила (δ, м.д. CDCl3): 0,99 (д, J 6,5; 6Н2g), 1,6 (м, 1Н2); 2,046 (с, 3Н3 или С6-СН3) 2,32 (м, 2Нв); 2,58 (м, 2Нб), 3,88 (м, 2На), 5,475 (с, 1Ни), 10,729 (с, 1Нк).
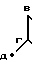
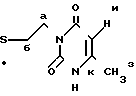 ПМР-спектра комплекса бис-(3-изобутилтиоэтил)-6-метилурацил-3) цис-дихлорплатина
ПМР-спектра комплекса бис-(3-изобутилтиоэтил)-6-метилурацил-3) цис-дихлорплатина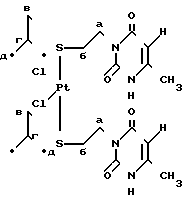 1,04 (д, J 6,5, 12Н4д); 2,08 (м. 2Н2г); 2,18 (с, 6Н, 2С6 СН3); 3,01 (м, 4Н2в); 3,28 (м, 4Н2б), 4,36 (м, 4Н2а); 5,66 (с, 2Н2и); 10,45 (с, 2Н2к).
1,04 (д, J 6,5, 12Н4д); 2,08 (м. 2Н2г); 2,18 (с, 6Н, 2С6 СН3); 3,01 (м, 4Н2в); 3,28 (м, 4Н2б), 4,36 (м, 4Н2а); 5,66 (с, 2Н2и); 10,45 (с, 2Н2к).
О том, что комплексообразование осуществляется за счет образования координационной связи Pt-S, свидетельствует спектр ЯМР 1Н комплекса, в которой, по сравнению со спектром лиганда, наибольший дополнительный химсдвиг имеется для сигналов -протонов метиленовых групп при атоме серы в области слабого поля (0,7 м.д.)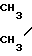 CH-
CH-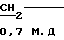 S
S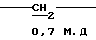 CH2_N
CH2_N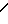
Изучили иммунотропные свойства комплекса бис-[2,4-диоксо-3-(5-метил-3-тиагексил)-6-метил-1,2,3,4-тетрагидропиримидин- S] цис-дихлорплатины дис PtCl2˙L2.
Для изучения биологической активности комплекса в качестве аналога был взят 6-метилурацил, так как он обладает выраженной иммунотропной активностью.
Установлено, что комплекс цис-PtCl˙L2 обладает выраженным супрессирующим эффектом на клеточное звено иммунитета (на модели ГЗТ).
В связи с тем, что комплекс цис-PtCl2˙L2 обладает выраженным супрессирующим эффектом на клеточное звено иммунитета (на модели ГЗТ), проведена серия опытов в сравнении с гидрокортизоном, который обладает свойствами иммунодепрессанта.
Реакцию ГЗТ воспроизводили обычным способом, сенсибилизируя мышей нанесением на выстриженный живот 25 мкл 0,5%-ного раствора 2,4-динитрофторбензола (ДНФБ) в смеси ацетона с оливковым маслом (4:1). Через 5 сут после сенсибилизации на предварительно измеренные микрометром уши капали по 20 мкл 0,25% -ного раствора ДНФБ. Реакцию оценивали по приросту толщины ушей через 24 ч после нанесения разрешающей дозы ДНФБ. Соединение вводили в дозе 40 мг/кг (1/10 LД50) в течение 4 сут, начиная с первого дня после сенсибилизации.
Влияние соединения и гидрокортизона на реакцию ГЗТ у мышей дано в табл. 3.
Структурный аналог гидрокортизон, взятый в качестве эталона, вводили в общепринятой дозе 50 мг/кг по известной схеме.
Таким образом, соединение Х-989 обладает выраженным супрессирующим эффектом на клеточное звено иммунитета (на модели ГЗТ), причем его действие аналогично) супрессирующим свойствам известного иммуносупрессора гидрокортизона.
Исследованное соединение Х-989 может найти практическое применение как стимулятор гуморального звена иммунной системы, так как достоверно увеличивает количество АОК, и как иммуносупрессор на моделях, аналогичных реакции ГЗТ.
| название | год | авторы | номер документа |
|---|---|---|---|
| [2,4-ДИОКСО -1,3- БИС (5-МЕТИЛ -3-ТИАГЕКСИЛ) -6-МЕТИЛ-1,2,3,4- ТЕТРАГИДРОПИРИМИДИН-S,S] ЦИC-ДИXЛOPПЛATИHA , ПPOЯBЛЯЮЩAЯ ИMMУHOTPOПHУЮ AKTИBHOCTЬ | 1991 |
|
RU2028300C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-6-МЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2028295C1 |
| 3-ИЗОБУТИЛТИОЭТИЛ-6-МЕТИЛУРАЦИЛ, ОБЛАДАЮЩИЙ ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2035456C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-5-ГИДРОКСИ-6-МЕТИЛУРАЦИЛ, ОБЛАДАЮЩИЙ ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2028296C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-5-ИЗОБУТИЛТИОЭТИЛОКСИ-6-МЕТИЛ-УРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2027710C1 |
| 5-ГИДРОКСИ-3,6-ДИМЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2035455C1 |
| 1,3-(2,6-ДИГИДРОКСИ-4-ТИАГЕПТАМЕТИЛЕН)-6-МЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ АКТИВНОСТЬ | 1992 |
|
RU2034839C1 |
| ПИРИМИДИНОВЫЕ АЦИКЛОНУКЛЕОЗИДЫ, ПРОЯВЛЯЮЩИЕ ИММУНОТРОПНУЮ И ПРОТИВОВОСПАЛИТЕЛЬНУЮ АКТИВНОСТЬ | 1992 |
|
RU2051150C1 |
| 2-МЕТИЛ-4-АМИНО-6-ОКСИПИРИМИДИН И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1998 |
|
RU2165926C2 |
| КАЛИЕВАЯ СОЛЬ 2-[1-(1,1ДИОКСОТИЕТАНИЛ-3) БЕНЗИМИДАЗОЛИЛ-2-ТИО]-УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩАЯ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1996 |
|
RU2115652C1 |
Использование: в медицине как препарат, проявляющий иммунотропную активность. Сущность изобретения: PtCl с бис-[1(3)-изобутилтиоэтил-6-метилурацила] -цис-конфигурации C22H36N4G2 , выход 1,62 г (90%). Реагент 1: водный раствор K2PtCl4 . Реагент 2: ацетоновый раствор 1(3)-изобутилтиоэтил-6-метилурацила. Условия реации: при перемешивании в течение 3 ч. 3 табл.
Бис[2,4 диоксо-6-метил-1,2,3,4 тетрагидропиримидин-3 (5-метил- 3 - тиагексил)-S цис дихлорплатина формулы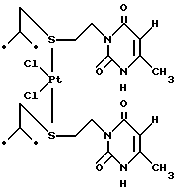
проявляющая иммунотропную активность.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Cunningham A.J., A method of increased sensitivity for detecting single antibody forming cells | |||
| Nature, 1965, v.207, N 5001, p.1106-1107. | |||
Авторы
Даты
1995-05-20—Публикация
1991-03-11—Подача