Изобретение относится к области органической химии, конкретно к способу получения 2-метил-4-амино-6-оксипиримидину формулы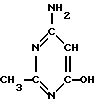
проявляющему иммунотропную активность.
Аналогом по строению и назначению выбран оксиметилурацил
синтез и свойства которого даны ниже.
Известен способ получения оксиметилурацила (Hurst D.T., Aplication of the Elbs Persulfate Oxidation to the Preparation of 5-Hydroxypyrimidines // Austr. J. Chem. 1983. - 36. - p. 1285-1289).
Оксиметилурацил получают методом окисления 6-метилурацила персульфатом аммония в щелочной среде (реакция Эльбса) с последующим гидролизом соляной кислотой при 100oC.
Недостаток этого способа в том, что он приводит к получению 5-гидрокси-6-метилурацила с выходом 50% и чистотой 80-90%.
Оксиметилурацил усиливает реакцию иммунитета и эффективен при терапии инфекций, препарат не токсичен, не вызывает побочных явлений, проявляет универсальные антисептические свойства, способствует заживлению ран, трофических язв и ожогов, ослабляет вредное влияние радиации, защищает от отравления алкоголем, нитратами, фосфорорганическими веществами, нормализует количество лейкоцитов, усиливает гуморальный и клеточный иммунитет, обладает антистрессовым, кардиостимулирующим и антитоксическим действием.
Оксиметилурацил является более активным иммуностимулятором, чем метилурацил, поэтому взят в качестве аналога. Недостаток его в том, что он очень плохо растворим в воде (0,1%).
Создание иммуномодуляторов имеет важное значение для современной иммунологии и практической медицины, так как открывает возможность лечения и профилактики ряда заболеваний и патологических состояний человека. В последние годы получен и исследован целый ряд природных и синтетических соединений, обладающих иммуномодулирующими свойствами. Однако препаратов, способных оказывать иммуномодулирующее влияние, полностью безопасных и дающих однонаправленный эффект с точным механизмом действия, в настоящее время практически нет. Поэтому остается актуальным поиск малотоксичных иммуномодуляторов.
Работами школы проф. Д.Н. Лазаревой показано, что к числу перспективных классов иммуномодуляторов относятся производные пиримидина. Наличие у некоторых из них антиоксидантных свойств рассматривается как важное звено в механизме их иммуномодулирующего действия. Обладая весьма низкой токсичностью (LD50 3-4 г/кг), они стимулируют нуклеиновый и белковый обмен, ускоряют пролиферацию и дифференцирование клеток, оказывают противовоспалительное действие, повышают резистентность организма к инфекции. Среди изученных производных пиримидина наиболее активными стимуляторами фагоцитарной активности in vivo и in vitro оказались такие как 5-оксиметилурацил, метилурацил, пентоксил, 5-окси-6-метилурацил, суперацил (2-амино-4-метил-6-оксипиримидин), повышающие поглотительную способность.
Схема синтеза 2-метил-4-амино-6-оксипиримидина
Целью изобретения является расширение ассортимента препаратов, проявляющих иммунотропную активность, и разработка способа получения 2-метил-4-амино-6-оксипиримидина.
Поставленная цель достигается синтезом 2-метил-4-амино-6-оксипиримидина путем сливания смесей (смесь 1-солянокислого ацетамидина, циануксусного эфира и метанола) и метилата натрия с последующим отделением выпавшего осадка NaCl, отгонкой метанола, растворением осадка в воде, подкислением уксусной кислотой.
Поставленная цель также достигается тем, что к раствору метилата натрия в метаноле по каплям добавляют смесь, содержащую солянокислый ацетамидин, циануксусный эфир и метанол при температуре 10-55oC в течение 1-5 часов, полученную смесь нагревают, затем отгоняют метанол, растворяют остаток в воде, подкисляют уксусной кислотой и выделяют целевой продукт.
Иммунотропные свойства и острая токсичность предлагаемого соединения изучены в лаборатории новых лекарственных средств института органической химии УНЦ РАН.
Острую токсичность соединения определяем на беспородных мышах обоего пола массой 18-20 г при однократном внутрибрюшинном и внутрижелудочном введении, полученных из питомника лабораторных животных "Рапполово". Величину LD50 при внутрибрюшинном введении определяли по методу Кербера и при внутрижелудочном введении по Литчфильду и Уилкоксону LD50 = 5500 (4740 ± 6380) мг/кг. На основании классификации токсичности веществ 2-метил-4-амино-6-оксипиримидин (МАОП) относится к малотоксичным соединениям (Постановление Государственного комитета стандартов Совета Министров СССР).
В качестве модели первичного гуморального иммунного ответа использовали метод локального гемолиза в геле по методу N.K. Jerne, E.A.Nordin в модификации A. G. Cunningham. Беспородных мышей иммунизировали внутрибрюшным введением нормиммунной дозой (2 · 108) эритроцитов барана за 4 полных суток до эксперимента. Количество антителообразующих клеток (АОК) определяли по числу зон гемолиза в камерах. Проводили перерасчет АОК на 106 спленоцитов. Соединения вводили внутрижелудочно в дозах 25 и 50 мг/кг с 1 по 4 сутки. Сравнивали вливание 2-метил-4-амино-6-оксипиримидина на АОК с эффектом оксиметилурацила.
Соединение III стимулирует образование АОК в 2 раза меньшей дозе (25 мг/кг - 1/220 доли от LD50), чем оксиметилурацил (50 мг/кг), а в дозе 50 мг/кг МАОП активнее стимулирует АОК, чем оксиметилурацил (ОМУ) (табл. 1).
МАОП способен стимулировать образование АОК и на фоне иммуносупрессии, вызванной циклофосфаном и преднизолоном.
МАОП на фоне иммуносупрессии, вызванной преднизолоном, в 2 раза эффективнее оксиметилурацила стимулирует образование АОК, а на фоне иммуносупрессии, вызванной циклофосфаном, МАОП аналогично оксиметилурацилу стимулирует образование АОК в селезенке.
Изучено влияние МАОП на клеточный иммунитет на модели реакции гиперчувствительности замедленного типа (ГЗТ) к 2,4-динитрофторбензолу и к эритроцитам барана и показано, что МАОП в дозе 25 мг/кг не оказывает влияния на ГЗТ к ДНФБ и к эритроцитам барана.
Изучено влияние МАОП на течение экспериментальных инфекций при лечебном и профилактическом введении. Применение МАОП и оксиметилурацила совместно с антибиотиками в лечебном режиме, т.е. после заражения животных, эффект был маловыражен. При профилактическом введении пиримидинов в течение 7 дней и лечебном режиме после заражения значительно повысили эффективность лечения антибиотиками экспериментальных инфекций, вызванных стафилококком, протаем, кишечной и синегнойной палочками. Показано, что МАОП более значительно, чем оксиметилурацил, повышает эффективность антибиотикотерапии экспериментальных инфекций. При иммуносупрессии, вызванной преднизолоном и иммураном, МАОП более значительно, чем оксиметилурацил, повышал эффективность антибиотикотерапии экспериментальных инфекций. МАОП более значительно, чем оксиметилурацил стимулирует поглотительную способность РЭС. На фоне угнетения различными факторами МАОП аналогично оксиметилурацилу стимулирует поглотительную способность фагоцитов и усиливает наработку кислородных радикалов в фагоцитах. МАОП аналогично оксиметилурацилу не изменяет реакцию трансплантант против хозяина (ТППХ). МАОП на фоне иммуносупрессии, вызванной гидрокортизоном более значительно, чем оксиметилурацил стимулируют выработку агглютининов и повышает протективные свойства сыворотки крови.
Таким образом, проведенные экспериментальные данные исследования показали, что 2-метил-4-амино-6-оксипиримидин - малотоксичное соединение и обладает выраженными иммуномодулирующими свойствами, превышающими по эффективности оксиметилурацил, препарата, прошедшего клиническую апробацию.
Данное изобретение иллюстрируется примерами.
Пример 1. Способ получения 2-метил-4-амино-6-оксипиримидина. 35 г металлического натрия растворяют в 250 мл абсолютного метанола в течение 2-х часов, охлаждают до 30oC.
Готовят смесь из 27,7 г (0,293 моля) высушенного ацетамидина солянокислого, 35 мл (0,309 моля) циануксусного эфира, перегнанного при 205oC и 59 мл абс. метилового спирта (перегнанного). Эту смесь тоже хорошо охлаждают в бане со льдом. Обе смеси слиты (5 мл), сразу же выпадает белый осадок - это NaCl (выбросить). Вся реакционная смесь поставлена на водяную баню на 2 часа (с обратным холодильником).
Маточный раствор перелит в колбу Фаворского и от него водоструйным насосом отогнан метиловый спирт. В колбе сухой осадок.
Утром (на другой день) раствор разогрет на водяной бане и теплым отфильтрован (это делают для того, чтобы было больше свободного спирта, а то вся реакционная смесь за ночь превращалась в гель).
Прозрачный спиртовой раствор поставлен на водяную баню и из него отогнан метиловый спирт.
Осадок высушен, растворен в минимальном количестве воды, разбавлен водой вдвое и прибавлена 98% уксусная кислота до слабокислой реакции (избыток нельзя). Выпавший осадок, отфильтрован и промыт водой, высушен т.пл. 275oC (низкая) (должна быть Т. пл. 292oC).
Осадок перекристаллизован из воды. Т.пл. 288oC (в опыте N 562 Т. пл. была 292oC). Осадок поставлен еще сушиться. Вес 13,5 г (37,2% Т. пл. 288oC (разл.)).
Пример 2. Синтез 2-метил-4-амино-6-оксипиримидина (III).
35 г металлического натрия растворяют в 250 мл абсолютного метанола в течение 2 ч, охлаждают до 30oC, ставят мешалку и прибавляют по каплям смесь (I), содержащую 36,3 г (0,384 моль) солянокислого ацетамидина, 42 мл циануксусного эфира и 50 мл абсолютного метанола, в течение 1 ч, температура в колбе поднимается до 45oC. Реакционную смесь нагревают на водяной бане в течение 1 ч при 45-55oC и оставляют на ночь. На следующий день от реакционной смеси отгоняют метанол в вакууме водоструйного насоса при температуре бани 70-78oC. Остаток растворяют в 400 мл воды, подкисляют уксусной кислотой до pH 6-7 (65 мл). Выпавший осадок отфильтровывают, промывают ацетоном, полученные кристаллы перекристаллизовывают из воды с углем, получают 37,8 г (78,7%) 2-метил-4-амино-6-оксипиримидина с т. пл. 295oC, растворимого в воде (1%), в ДМФА - 1%, в ДМСО - 3-5%.
Пример 2а аналогичен примеру 1 за исключением того, что прибавление смеси (1) ведут при 10oC в течение 5 ч. Реакционную смесь нагревают до кипения метанола и перемешивают при этой температуре 1 ч и оставляют на ночь. Обработка аналогична опыту 2. Получают 33,6 г (70%) 2-метил-4-амино-6-оксипиримидина.
Пример 2б аналогичен примеру 1 за исключением того, что прибавление смеси (I) ведут при 50oC в течение 1 ч. Реакционную смесь нагревают до кипения метанола и перемешивают при этой температуре 1 ч и оставляют на ночь. Обработка аналогична опыту 2. Получают 45,6 г (95%) 2-метил-4-амино-6-оксипиримидина.
Пример 2в аналогичен примеру 1, за исключением того, что прибавление смеси (I) ведут при температуре 40oC в течение 2 ч. Реакционную смесь нагревают до кипения метанола и перемешивают при этой температуре 1 ч и оставляют на ночь. Обработка аналогична примеру 2. Получают 38,4 г (80%) 2-метил-4-амино-6-оксипиримидина.
Чистота и строение полученного соединения доказано ЯМР 1H и 13С спектрами, а также ИК-, УФ и элементным анализом.
Найдено, %: C 47,32; H 5,86; N 33,23. C5H7N3O. Вычислено %: C 47,99; H 5,64; N 33,58. УФ спектр λmax1 = 212,8; λmix1 = 232; λmax2 = 258,4.
В спектре ЯМР 13C соединения III имеются сигналы 21 (CH3-C2); 164,38 (C4); 163,63 (C2), 159,04 (C6); 82,99 (C5).
В ИК спектре соединения III имеются полосы поглощения в области 648 см-1 (RCH= CHR1); 808(ωNH2); 1288 (VCN); 1380(δSCH3); 1608, 1616, 1628 (VC=O, = N-C=O); 3064 (VC=C); 3344(δ
Пример 3. В качестве модели первичного иммунного ответа использовали метод локального гемолиза в геле N.K. Jerne, A.A. Nordin (Science, 1963. V. 140. - N 3565, P. 405) в модификации A.G. Cunningham (1965. V. 207. - N 5001. - P. 1106-1107).
Беспородных мышей иммунизировали внутрибрюшинным введением нормиммунной дозы (2·108) эритроцитов барана за 4 полных суток до эксперимента. Количество антителообразующих клеток (АОК) определяли по числу зон гемолиза в камерах. Проводили пересчет АОК на 106 спленоцитов.
Пример 4. В качестве модели клеточного иммунитета использовали реакцию гиперчувствительности замедленного типа (ГЗТ) у беспородных мышей. Реакцию ГЗТ воспроизводили обычным способом (Phanuphak, J.W.Moocheod, N.A. Clemon. J. Immunol. 1974. N 112. P. 115-123), сенсибилизируя мышей нанесением на выстриженный живот 25 мкл 0,5% раствора 2,4-динитрофторбензола (ДНФБ) в смеси ацетона с оливковым маслом (4:1). Разрешающую дозу (20 мкл 0,25% раствора ДНФБ) наносили на 4 сутки после сенсибилизации на уши с предварительным измерением толщины уха микрометром. Соединение вводили внутрибрюшинно в дозе 25 мг/кг и 50 мг/кг с +1 по +4 день. Всего 4 введения. Структурный аналог соединения - оксиметилурацил, взятый в качестве эталона, вводили в общепринятой дозе 50 мг/кг по той же схеме.
Пример 5. Острая токсичность соединения 2-метил-4-амино-6-оксипиримидина определялась на беспородных мышах обоего пола массой 18-20 г при однократном внутрибрюшинном введении, полученных из питомника лабораторных животных "Рапполово". После введения токсических доз через 5-10 мин у животных наблюдалась вялость, вытягивание конечностей, смерть наступала от остановки дыхания.
Параметры токсичности определяли по методу Литчфилъду и Уилкоксону. При внутрибрюшинном введении 2-метил-4-амино-6-оксипиримидина LD50 = 5500 (4740 ± 6380) мг/кг. На основании классификации токсичности веществ при введении под кожу и брюшную полость (Н. Ф. Измеров, Н.В. Саноцкий, К.К. Сидоров "Медицина", М. , 1977, О.Н. Елизарова. "Медицина", М., 1971 г. и Постановление Государственного комитета стандартов Совета Министров СССР) 2-метил-4-амино-6-оксипиримидин (МАОП) относится к малотоксичным соединениям.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРИМИДИНОВЫЕ АЦИКЛОНУКЛЕОЗИДЫ, ПРОЯВЛЯЮЩИЕ ИММУНОТРОПНУЮ И ПРОТИВОВОСПАЛИТЕЛЬНУЮ АКТИВНОСТЬ | 1992 |
|
RU2051150C1 |
| 1,3-(2,6-ДИГИДРОКСИ-4-ТИАГЕПТАМЕТИЛЕН)-6-МЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ АКТИВНОСТЬ | 1992 |
|
RU2034839C1 |
| БИС[2,4-ДИОКСО-6-МЕТИЛ-1,2,3,4 -ТЕТРАГИДРОПИРИМИДИН-3-(5-МЕТИЛ-3- ТИАГЕКСИЛ)-S]ЦИС-ДИХЛОРПЛАТИНА, ПРОЯВЛЯЮЩАЯ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2035467C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-5-ИЗОБУТИЛТИОЭТИЛОКСИ-6-МЕТИЛ-УРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2027710C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-5-ГИДРОКСИ-6-МЕТИЛУРАЦИЛ, ОБЛАДАЮЩИЙ ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2028296C1 |
| 1,3-БИС(ИЗОБУТИЛТИОЭТИЛ)-6-МЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2028295C1 |
| 5-ГИДРОКСИ-3,6-ДИМЕТИЛУРАЦИЛ, ПРОЯВЛЯЮЩИЙ ИММУНОТРОПНУЮ АКТИВНОСТЬ | 1991 |
|
RU2035455C1 |
| 3-ИЗОБУТИЛТИОЭТИЛ-6-МЕТИЛУРАЦИЛ, ОБЛАДАЮЩИЙ ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2035456C1 |
| [2,4-ДИОКСО -1,3- БИС (5-МЕТИЛ -3-ТИАГЕКСИЛ) -6-МЕТИЛ-1,2,3,4- ТЕТРАГИДРОПИРИМИДИН-S,S] ЦИC-ДИXЛOPПЛATИHA , ПPOЯBЛЯЮЩAЯ ИMMУHOTPOПHУЮ AKTИBHOCTЬ | 1991 |
|
RU2028300C1 |
| ПРОИЗВОДНЫЕ 4-ОКСО-1,4-ДИГИДРОПИРИМИДИНА, ОБЛАДАЮЩИЕ ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2037491C1 |


Изобретение относится к новому 2-метил-4-амино-6-оксипиримидину формулы I и способам его получения. Предлагаемое соединение проявляет иммунотропную активность и может быть использовано в медицине. Первый способ заключается в том, что сливают смеси (смесь 1-солянокислого ацетамидина циануксусного эфира и метанола) и метилата натрия с последующим отделением выпавшего осадка NaCl, отгонкой метанола, растворением осадка в воде и подкислением уксусной кислотой. Второй способ заключается в том, что к метилу натрия при температуре 10 - 55oC прибавляют по каплям смесь солянокислого ацетамидина, уксусного эфира и абсолютного метанола в течение 1 - 5 ч с последующей отгонкой метанола, растворением остатка в воде, подкислением уксусной кислотой. 3 c.п.ф-лы, 2 табл. 
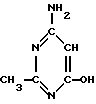
проявляющий иммунотропную активность.
отличающийся тем, что сливают смеси: смесь 1-солянокислого ацетамидина, циануксусного эфира и метанола и метилата натрия с последующим отделением выпавшего осадка NaCl, отгонкой метанола, растворением осадка в воде, подкислением уксусной кислотой.
отличающийся тем, что к раствору метилата натрия в метаноле по каплям добавляют смесь, содержащую солянокислый ацетамидин, циануксусный эфир и абсолютный метанол при температуре 10 - 55oC в течение 1 - 5 ч, полученную смесь нагревают, затем отгоняют метанол, растворяют остаток в воде, подкисляют уксусной кислотой и выделяют целевой продукт.
| SU 1342417 А3, 30.08.1987 | |||
| УСТРОЙСТВО для ЗАГРУЗКИ | 0 |
|
SU199649A1 |
| ВОЛНОВОДНЫЙ ФАЗОВЫЙ ДЕТЕКТОР | 0 |
|
SU205894A1 |
| DE 1140580 А, 11.06.1963 | |||
| Устройство для измерения амплитуды вибрации | 1979 |
|
SU890076A1 |
Авторы
Даты
2001-04-27—Публикация
1998-11-25—Подача