Изобретение относится к новым химическим соединениям трилитиевым солям (1 R,5 R)-3 -аза-1 -(2-амино-1,6-дигидро-6- оксо- пуринил-9)-аза-3 дезокси-3 -(азидонафталин-1-суфамидо)гексопиранозил-6 -трифос- фатов общей формулы
H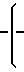 O
O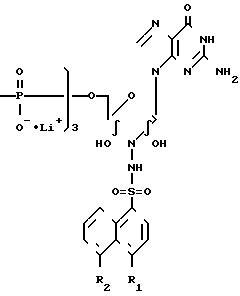 где R1 N3 и R2 Н (I) или R1 Н и R2 N3 (II), как специфическим фотоактивируемым необратимым ингибиторам РНК-полимеразы.
где R1 N3 и R2 Н (I) или R1 Н и R2 N3 (II), как специфическим фотоактивируемым необратимым ингибиторам РНК-полимеразы.
Указанные соединения могут быть использованы в биохимии, биофизике и молекулярной биологии для изучения строения и механизма действия РНК-полимеразы.
Наиболее близким к описываемым является известное соединение (1 R,5 R) -3 -аза-1 -(2-амино-1,6-дигидро-6-оксопуринил -9)-3 -дезокси-3 -(2-гидроксибензамидо)гек- сопиранозил-6 -трифосфат, оказывающий специфическое ингибирующее действие на РНК-полимеразу и обладающий флуоресцентными свойствами (1).
Однако данный ингибитор обладает следующими недостатками:
недостаточно высокой эффективностью ингибирующего действия;
отсутствием реакционноспособной группировки в составе молекулы, что исключает возможность селективного введения в активный центр фермента флуоресцентной метки, образующей ковалентную связь с белком, с последующим отделением от избытка несвязанного модификатора, что существенно ограничивает область его применения.
Цель изобретения создание новых соединений в ряду производных 5 -гуаниловых нуклеотидов, оказывающих более выраженное ингибирующее действие на РНК-полимеразу и позволяющих более эффективно проводить изучение данного фермента с помощью спектрофлуориметрии.
Цель достигается трилитиевыми солями (1 R,5 R)3 -аза-1 -(2-амино-1,6-дигидро-6-ок- сопуринил-9)-3 дезокси-3 -(азидонафталин-1-сульфамидо)гексопиранозил-6 -три- фосфатов вышеуказанной общей формулы как специфическими фотоактивируемыми необратимыми ингибиторами РНК-полимеразы.
Соединения I и II получают способом, основанным на известной реакции циклизации продуктов периодатного окисления рибонуклеотидов с гидразидами аренсульфокислот в водноорганической среде при рН 4,5-5 [1]
Исходные 4- и 5-азидонафталин-1-сульфонилгидразины получают способом, основанным на следующих известных реакциях:
замещения диазогруппы азидной у диазониевых производных соответствующих аминонафталин-1-сульфокислот при взаимодействии с азидом натрия [2]
хлордегидроксилирования промежуточных азидонафталин-1-сульфокислот пятихлористым фосфором [2]
гидразинолиза аренсульфонилхлоридов избытков гидразина [3]
П р и м е р 1. Трилитиевая соль (1 R,5 R)-3 -аза-1 -(2-амино-1,6-дигидро-6-оксо-пури- нил-9)-3 дезокси-3 -(4-азидонафталин-1-сульфамидо)гексопиранозил-6 -трифосфата (I).
К раствору 64 мг (0,1 ммоль) натриевой соли оксо-гуанозин-5 -трифосфата, очищенной от примеси иодата натрия, в 5 мл 1 М литий-ацетатного буфера (рН 5,0) при перемешивании и красном свете добавляют раствор 34 мг (0,13 ммоль) 4-азидонафталин-1-сульфонилгидразина в 7 мл диоксана. Полученный раствор перемешивают в течение 2 ч при комнатной температуре, защищая от света, затем упаривают при пониженном давлении до объема ≈0,5 мл и обрабатывают 5 мл охлажденной смеси безводный этанол безводный диэтиловый эфир (3:1, об.). Выпавший осадок отделяют центрифугированием, промывают безводным диоксаном, затем безводным диэтиловым эфиром и высушивают в вакууме в присутствии фосфорного ангидрида. По- лучают 50 мг целевого продукта (выход 63,5%).
Физико-химические свойства полученного соединения представлены в табл.1.
П р и м е р 2. Трилитиевая соль (1 R,5 R)-3 -аза-1 -(2-амино-1,6-дигидро-6-оксо-пури- нил-9)-3 -дезокси-3 -(5-азидонафталин-1-су- льфамидо)гексопиранозил-6 -трифосфата (II).
В условиях, описанных в примере 1, используя 34 мг (0,13 ммоль) 5-азидонафталин-1-сульфонилгидразина, получают 46 мг целевого продукта (выход 58% ).
Физико-химические свойства полученного соединения представлены в табл.1.
Изучение ингибирования РНК-полимеразы описываемыми соединениями проводили следующим образом.
ДНК-зависимую РНК-полимеразу фага Т7 выделяли из штамма-продуцента Е.coli. Активность фермента определяли по образованию /32Р/-РНК из /32Р/-нуклеозидтрифосфатов.
Инкубационная смесь для определения активности содержит 50 мМ Трис-НСl, рН 7,8; 10 мМ МgСl2; 5 мМ LiCl; 10 мМ β -меркаптоэтанол, раствор плазмиды рGЕМ-2 ("Рromega Biochem.", США) 20-40 мкг/мл; аденозин-5 -трифосфат (АТФ), уридин-5 -трифосфат (УТФ), цитидин-5 -трифосфат (ЦТФ) и гуанозин-5 -трифосфат (ГТФ) по 0,4 мкмоль/мл; /α -32P/-АТФ или /α -32Р/-УТФ (200000 имп./мин на пробу); фермент 0,2-0,5 мкг в пробе. При определении ингибирующего действия в среду инкубации при красном свете вносят изучаемое соединение для получения раствора требуемой концентрации. Общий объем пробы 25 мкл. Реакцию проводят при 37оС в течение 20 мин. Определение количества образовавшейся РНК (кислотонерастворимого материала) проводят известным способом.
Значение I50 определяют из графика зависимости активности фермента от концентрации ингибитора.
Используемый препарат ДНК-зависимой РНК-полимеразы фага Т7 имеет активность 130000-160000 ед. и характеризуется следующими значениями Км для нуклеозид-5 -трифосфатов: КмГТФ 0,16 мМ; КмАТФ 0,04 мМ; КмЦТФ 0,08 мМ; КмУТФ 0,06 мМ. Инициирующим реакцию нуклеозидтрифосфатом является ГТФ.
В указанных условиях (при красном свете) значение I50 для соединений I и II составляло 0,35 и 0,18 мМ соответственно. Ингибирование носило обратимый характер.
Под действием света (λ320±10 нм) происходит необратимое связывание ингибиторов с ферментом в результате генерации высокореакционноспособного нитренового радикала. Свободнорадикальный механизм реакции делает возможным ковалентное взаимодействие ингибиторов практически с любыми аминокислотными остатками в связывающем участке белка.
Эффект ингибирования РНК-полимеразы описываемыми соединениями в условиях фотолиза увеличивается с течением времени и не уменьшается после их удаления из среды преинкубации (гель-фильтрация), что указывает на необратимое связывание ингибиторов с ферментом. Препарат фермента, модифицированного соединениями I и II, после гель-фильтрации обладал выраженными флуоресцентными свойствами (λ mахвозб.=350 и 360 нм, λ mахфлуор.425 и 450 нм, соотв.), что также свидетельствует о необратимом связывании ингибиторов I и II с РНК-полимеразой.
При совместной преинкубации РНК-полимеразы с соединениями I и II и 5 мМ (субстрат РНК-полимеразы) наблюдается защитный эффект от действия ингибиторов, что указывает на их специфическое взаимодействие с активным центром фермента.
Ингибирование РНК-полимеразы соединениями I и II (в условиях фотолиза), а также наиболее близким структурным аналогом (1 R, 5 R)-3 -аза-1 -(2-амино-1,6-дигидро-6-оксопуринил-9)-3 -дезокси-3 -(2-гид- роксибензамидо)гексопиранозил-6 -трифо- сфатом (III), охарактеризовано данными, приведенными в табл. 2. Ингибирующее действие соединений I,II и III на РНК-по- лимеразу.
При изучении изменения интенсивности флуоресценции ковалентных фермент-ингибиторных комплексов в результате осуществленного щелочного гидролиза (рН 12, 0оС, 48 ч) морфолинового фрагмента остатков ингибиторов I и II было обнаружено увеличение интенсивности флуоресценции ≈в 1,5 раза.
Как вытекает из сравнения указанных данных, описываемые соединения I и II оказывают значительно более выраженное необратимое ингибирующее действие на РНК-полимеразу по сравнению с известным соединением III и расширяют арсенал специфических необратимых ингибиторов фермента, позволяющих проводить его изучение с помощью спектрофлуориметрии. Описываемые соединения I и II могут быть использованы для локализации ГТФ-связывающих центров в белках.
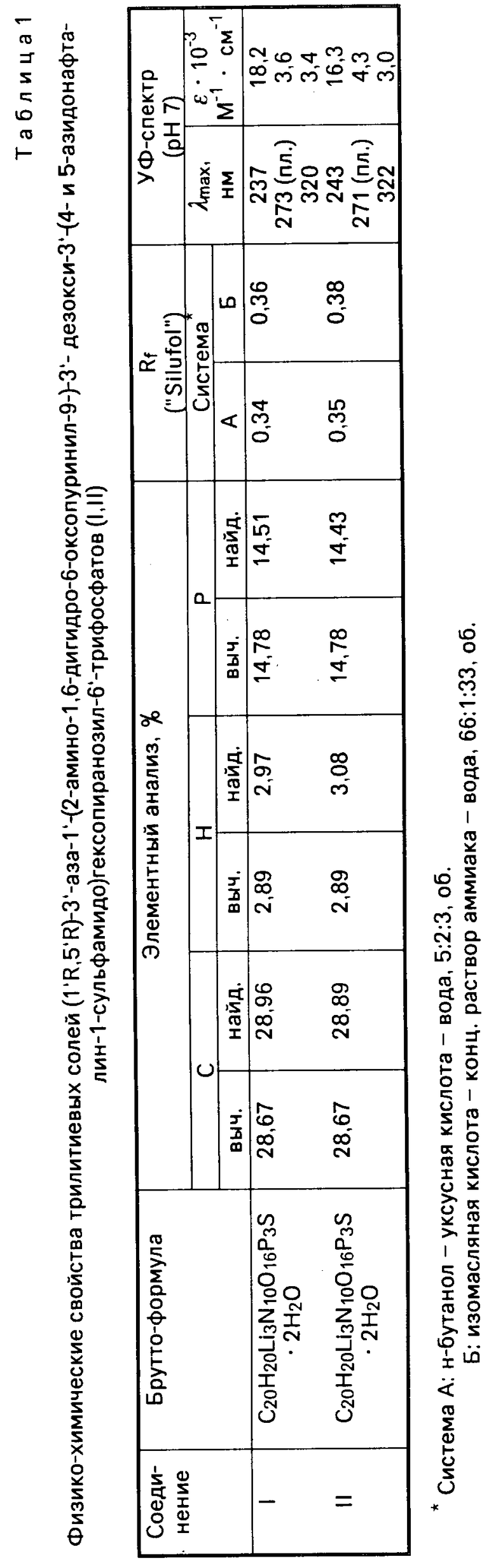

Использование: в качестве специфических фотоактивируемых необратимых ингибиторов РНК - полимеразы. Сущность: продукт - трилитиевые соли (1′R,5′R)-3′ -аза- 1′ -(2-амино-1,6-дигидро-оксопуринил-9)- 3′ -дезокси 3′ (азидонафталин-1-сульфамидо)гексопиранозил- 6′ -трифосфатов. Выход 58 - 63% БФ C20H26Li3N10O16P3S·2H2O Реагент 1: 4- или 5-азидонафталин-1-сульфонилгидразин. Реагент 2: натриевая соль оксо-гуанозин- 5′ -трифосфат в присутствии литий-ацетатного буфера. Условия реакции в среде диоксана при pH 4,5 - 5. 2 табл.
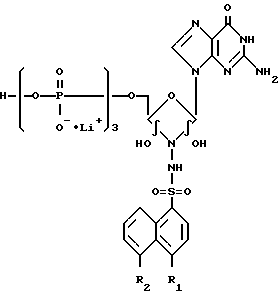
где R1 N3; R2 H;
или R1 H;
R2 N3,
в качестве специфических фотоактивируемых необратимых ингибиторов РНК-полимеразы.
| Progress in thin-layer shromatography and related methods | |||
| A.Niederwieser, G.Pataki, eds | |||
| V.-J | |||
| Acad | |||
| Press | |||
| NY, 1970, р.108-110. |
Авторы
Даты
1995-06-09—Публикация
1991-05-22—Подача