Изобретение относится к производным бензохинона, которые проявили превосходную активность как лекарства.
Более подробно, данное изобретение касается новых производных бензохинона, пригодных в качестве терапевтических агентов для лечения болезней печени.
Поскольку причина, образ и патофизиология каждой из гепатических болезней различны и включают немало неизвестных факторов, очень трудно разработать терапевтический агент для этих болезней.
В настоящее время характерные представители этих лекарств, широко использующиеся для лечения и предупреждения гепатических болезней и клинически оцененных, включают глицирризиновые рецептуры.
Хотя, как полагают, они должны быть эффективны против гепатических расстройств, циррозов или гепатитов и для постоперационной защиты печени, и т.д. их действенность не так сильна и что хуже они проявляют побочные стероидные эффекты. Кроме того, они применяются в форме внутривенных инъекций и неблагоприятно неактивны при употреблении орально.
Поэтому крайне требуется разработать лекарство, которое является безопасным и может проявлять активность даже при оральном применении.
При данных обстоятельствах начали тщательные научные исследования с целью разработки терапевтического агента для гепатических болезней.
В результате установили, что производные бензохинона, которые будут описаны ниже, удовлетворяют цели изобретения.
Примеры бензохиноновых производных, которые показали фармацевтическую активность, включают также и те, которые описаны в японских патентах NN 223150/1987, 223150/1987, 177934/1983.
Бензохиноновое производное, которое описано в патенте Японии N 223150/1987 отличается от соединения (1) изобретения по химической структуре и достоверно имеет антиастматическую активность, таким образом является отличным от соединения представленного в настоящем изобретении по фармацевтической активности.
Японский патент N 177934-1983 также раскрывает бензохиноновое производное, которое, однако, отличается от соединения, заявляемого настоящим изобретением, как по эффективности, так и по структуре.
Более того, японский патент N 185921/1988 представляет терапевтический агент для гепатических болезней, который, однако, отличается от соединения изобретения по химической структуре.
Изобретение относится к бензохиноновым производным описываемым следующей общей формулой (1) и к их фармакологически приемлемым солям:
A-CH 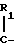 COR2 где А это группа представленная формулой:
COR2 где А это группа представленная формулой: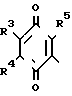 (где R3 и R4 могут быть идентичны, либо отличаться друг от друга, представляя собой каждый метокси или этокси группу, R5 означает метил либо группу представленную формулой:
(где R3 и R4 могут быть идентичны, либо отличаться друг от друга, представляя собой каждый метокси или этокси группу, R5 означает метил либо группу представленную формулой: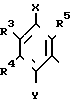 (где R3, R4 и R5 имеют значения, указанные выше, Х и Y также могут быть идентичны или отличаться друг от друга, являясь гидроксильной группой, группой формулы -(ОСН2)n OR6, где n равно 0 или 1, R6 низший алкил).
(где R3, R4 и R5 имеют значения, указанные выше, Х и Y также могут быть идентичны или отличаться друг от друга, являясь гидроксильной группой, группой формулы -(ОСН2)n OR6, где n равно 0 или 1, R6 низший алкил).
R1 является группой С9Н19, С5Н11, бензилом, циклогексилметилом, фенилом, группой -СН2-СН2-(СН3)СН-СН3, -СН2-СН2-СН2-СН2-СN, -СН2-СН2-СН2-S-СН3 или группой -CH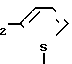 R2 представляет группу ОR8, где R8 атом водорода или низший алкил.
R2 представляет группу ОR8, где R8 атом водорода или низший алкил.
Примеры фармакологически приемлемых солей включают соли бензохиноновых производных с неорганическими кислотами, такие как гидрохлорид, гидробромид, сульфат и фосфат; с органическими кислотами, такие как ацетат, малеат, тартрат, метаносульфонат, бензосульфонат, толуолсульфонат, и с аминокислотами, такими как аргинин, аспарагиновая кислота и глютаминовая кислота.
Кроме того, определенные соединения изобретения существуют в форме солей металлов таких как Na, K, Са или М и эти соли металлов находятся в пределах шкалы фармакологически приемлемых солей настоящего изобретения.
Более того, как видно из, например, химической структуры, соединения изобретения имеют каждое двойную связь, так, что они могут существовать в форме стереоизомеров (цис и транс изомеров).
Соединения формулы 1 могут быть получены омылением соединения общей формулы
А СН СR1 СОR2, где значения А и R1 указаны выше, R2 означает группу ОR8, где R8 низший алкил.
В качестве примера данный способ может быть проиллюстрирован следующей схемой.
Гидрохиноновое соединение, представленное общей формулой (1) может быть получено с помощью следующего способа: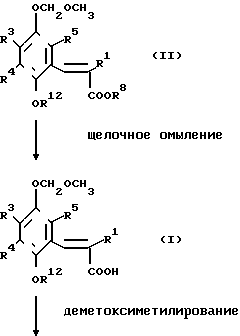
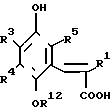 В представленных формулах, R1, R3, R4, R5 и Y определены ранее и каждый из R8 и R12 является алкильной группой.
В представленных формулах, R1, R3, R4, R5 и Y определены ранее и каждый из R8 и R12 является алкильной группой.
Соединение, представленное общей формулой (II), омыляют с помощью щелочей обычным способом, соединение, представленное общей формулой (l), при желании диметоксиметилируется для получения соединения, представленного общей формулой (l ').
Омыление проводится простым добавлением спиртового раствора каустической соды или гидроокиси калия. Диметиксиметилирование проводится в, например, ацетоне, диоксане, диметоксиэтане или в их водных растворах в присутствии, например, минеральных кислот таких как соляная или серная кислота, или органических кислот, таких как р-толуолсульфоновая или камфоросульфоновая кислота. Температура реакции желательно в пределах от 20 до 80оС.
Соединение (l '), полученное с помощью такого процесса, может быть далее окислено, для того, чтобы легко получить соединение представленное общей формулой (l'), являющееся одним из соединений по изобретению.
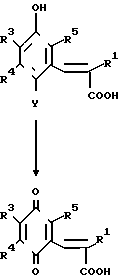

В представленных формулах R1, R3, R4 и Y определены выше.
Далее приводятся примеры осуществления заявленного способа, хотя необходимо сказать, что настоящее изобретение не ограничивается только этим.
Поскольку соединения изобретения имеют двойную связь, предполагается, что они должны существовать в формуле цис- и транс-изомеров. В следующих примерах, соединения по изобретению существуют в форме транс-изомеров, если не оговорено иначе.
Следующие символы химических структурных формул имеют следующие значения:
Ме: метильная группа; Et: этильная группа, Pr: n-пропильная группа; МОМО: метоксиметилоксильная группа.
Методический пример 1. Этил(Е)-3-/5-(6-метил-1-метоксиметилокси-2,3,4 -триметокси)фенил/-2-нонил-2-пропеноат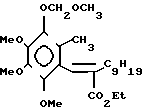 0,6 г гидрида натрия (60% маслянная суспензия) суспендировали в 5 мл диметилформамида, и добавили по каплям 8,8 г этилдиэтилфосфоно-2-ундеканоата. После того, как реакционная смесь стала гомогенной, 2,7 г 5-метоксиметилокси-6-метил-2,3,4-триметоксибензальдегида по каплям добавляли в смесь при комнатной температуре. После завершения добавления по каплям, смесь нагревали при температуре от 60 до 70оС в течение 1 ч, выливали в ледяную воду и экстрагировали этилацетатом. Органическую фазу промывали водой и сушили над безводным сульфатом магния, растворитель, отгоняли. Остаток очистили на хроматографической силикагелевой колонке (элюент; Н-гексан: этил ацетат 95:5) с получением 3,9 г целевого продукта
0,6 г гидрида натрия (60% маслянная суспензия) суспендировали в 5 мл диметилформамида, и добавили по каплям 8,8 г этилдиэтилфосфоно-2-ундеканоата. После того, как реакционная смесь стала гомогенной, 2,7 г 5-метоксиметилокси-6-метил-2,3,4-триметоксибензальдегида по каплям добавляли в смесь при комнатной температуре. После завершения добавления по каплям, смесь нагревали при температуре от 60 до 70оС в течение 1 ч, выливали в ледяную воду и экстрагировали этилацетатом. Органическую фазу промывали водой и сушили над безводным сульфатом магния, растворитель, отгоняли. Остаток очистили на хроматографической силикагелевой колонке (элюент; Н-гексан: этил ацетат 95:5) с получением 3,9 г целевого продукта
1N-ЯМР ( δ): 0,86 (m, J 6 Гц, 3Н), 1,00-1,50
(Н, 14Н), 1,36 (m, J= 7 Гц, 3Н), 2,08 (с, 3Н),
2,00-2,25 (u, 2Н), 3,58 (с, 3Н), 3,68 (с, 3Н),
3,88 (с, 6Н), 4,24 (кв, I 7 Гц, 2Н), 5,04
(с, 2Н), 7,33 (с, 1Н)
П р и м е р 1. (Е)-3-[5-(6-метил-1-метоксиметилокси-2,3,4-триметокси)фенил/-2- нонил-2-пропеоновая кислота.
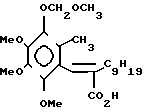 3,9 г этил (Е)-3-/5-(6-метил-1-метоксиметилокси-2,3,4-триметокси) -фенил)-2-нонил-2-пропеноата полученного в методическом примере 1 растворили в 30 мл этанола и 5 мл воды, туда добавили 1,7 г гидроокиси натрия. Смесь перемешивали 1 час при кипячении с обратным холодильником охладили и экстрагировали с n-гексаном и водную фазу подкислили 1м разбавленной соляной кислотой. Экстракцию проводили с дихлорметаном, органическую фазу промывали водой и сушили над безводным сульфатом магния. Растворитель отогнали с получением 3,6 г целевого соединения в виде бесцветного маслянистого продукта
3,9 г этил (Е)-3-/5-(6-метил-1-метоксиметилокси-2,3,4-триметокси) -фенил)-2-нонил-2-пропеноата полученного в методическом примере 1 растворили в 30 мл этанола и 5 мл воды, туда добавили 1,7 г гидроокиси натрия. Смесь перемешивали 1 час при кипячении с обратным холодильником охладили и экстрагировали с n-гексаном и водную фазу подкислили 1м разбавленной соляной кислотой. Экстракцию проводили с дихлорметаном, органическую фазу промывали водой и сушили над безводным сульфатом магния. Растворитель отогнали с получением 3,6 г целевого соединения в виде бесцветного маслянистого продукта
1Н-ЯМР ( δ): 0,86 (m, J= 6 Гц, 3Н), 1,01-1,59
(М, 14Н), 2,00-2,28 (М, 2Н), 2,10 (с, 3Н),
3,59 (с, 2Н), 3,69 (с, 3Н), 3,88 (с, 6Н), 5,04
(с, 2Н), 7,50 (с, 1Н)
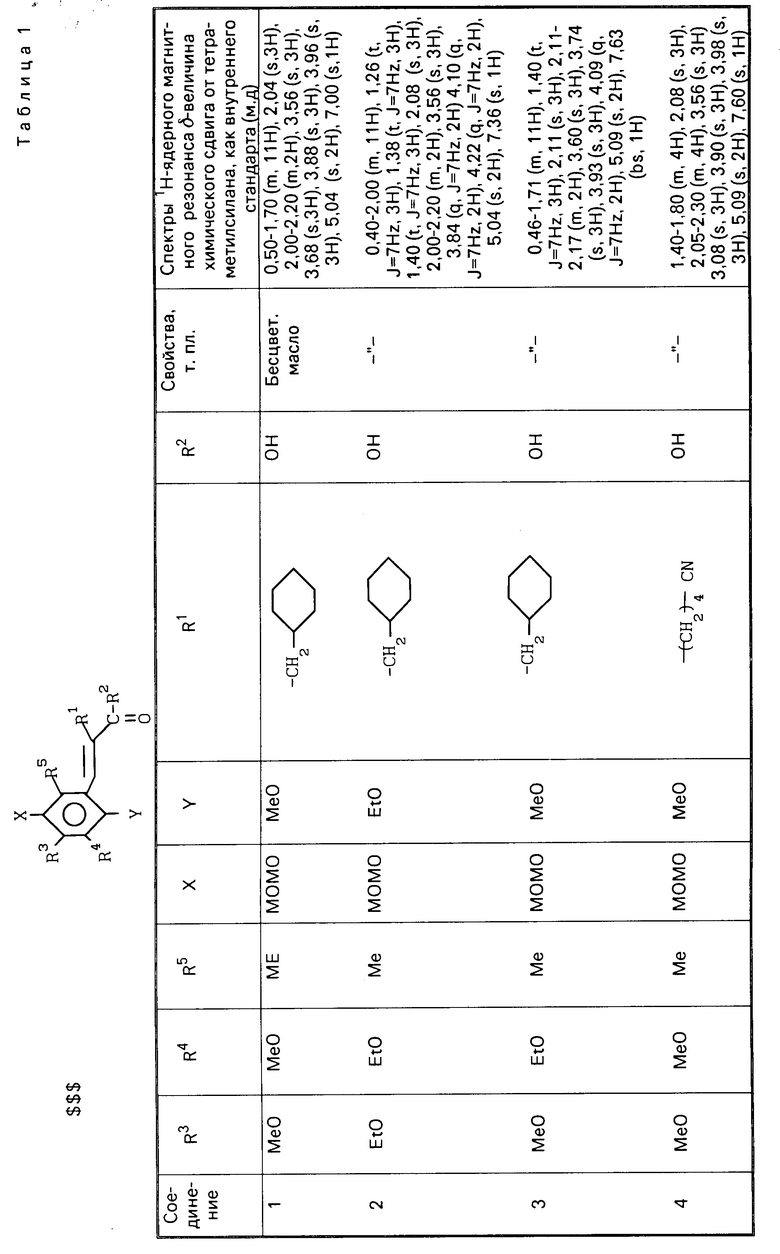
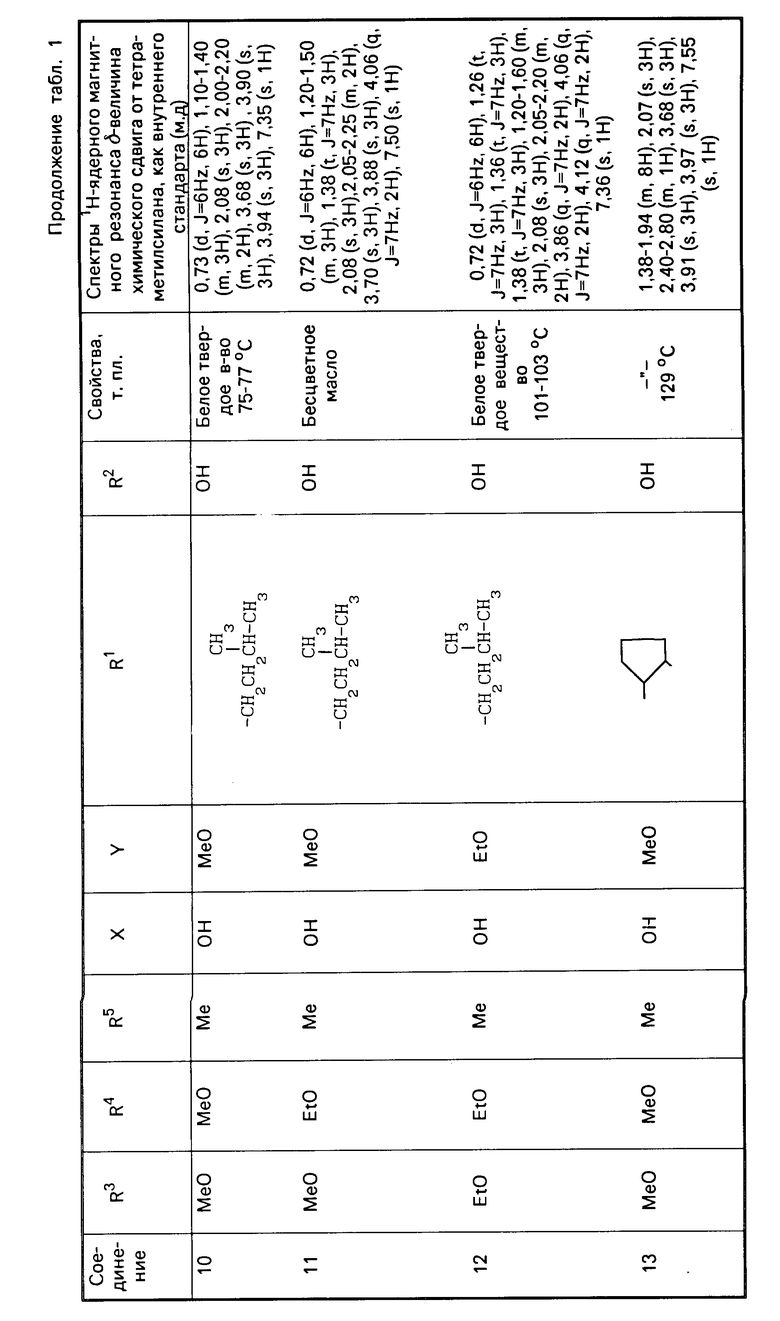
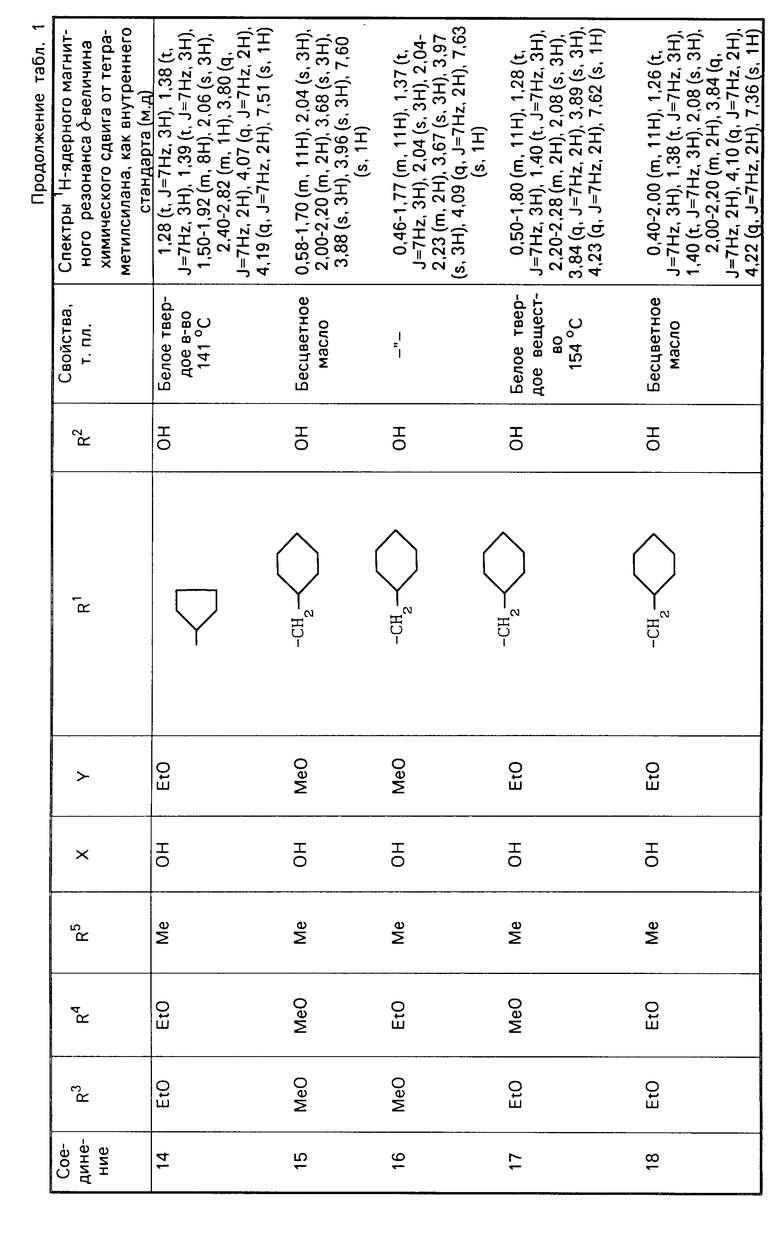
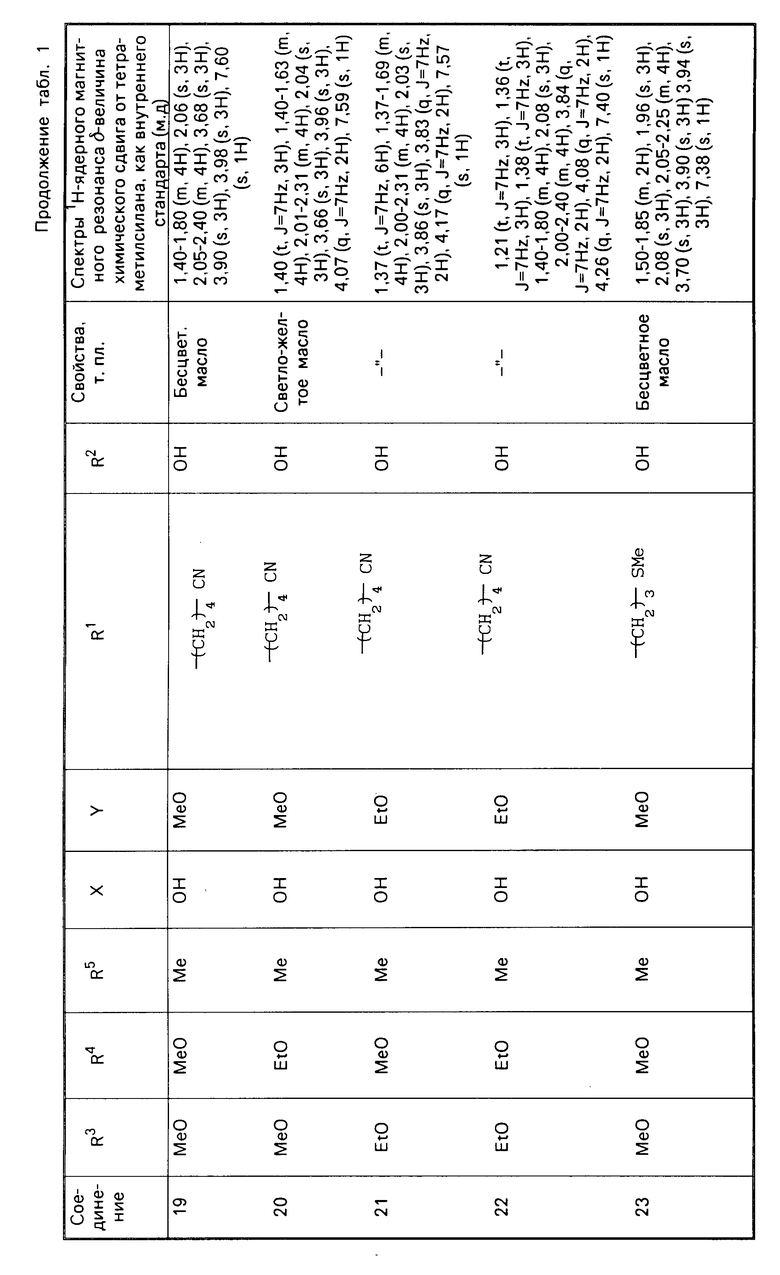
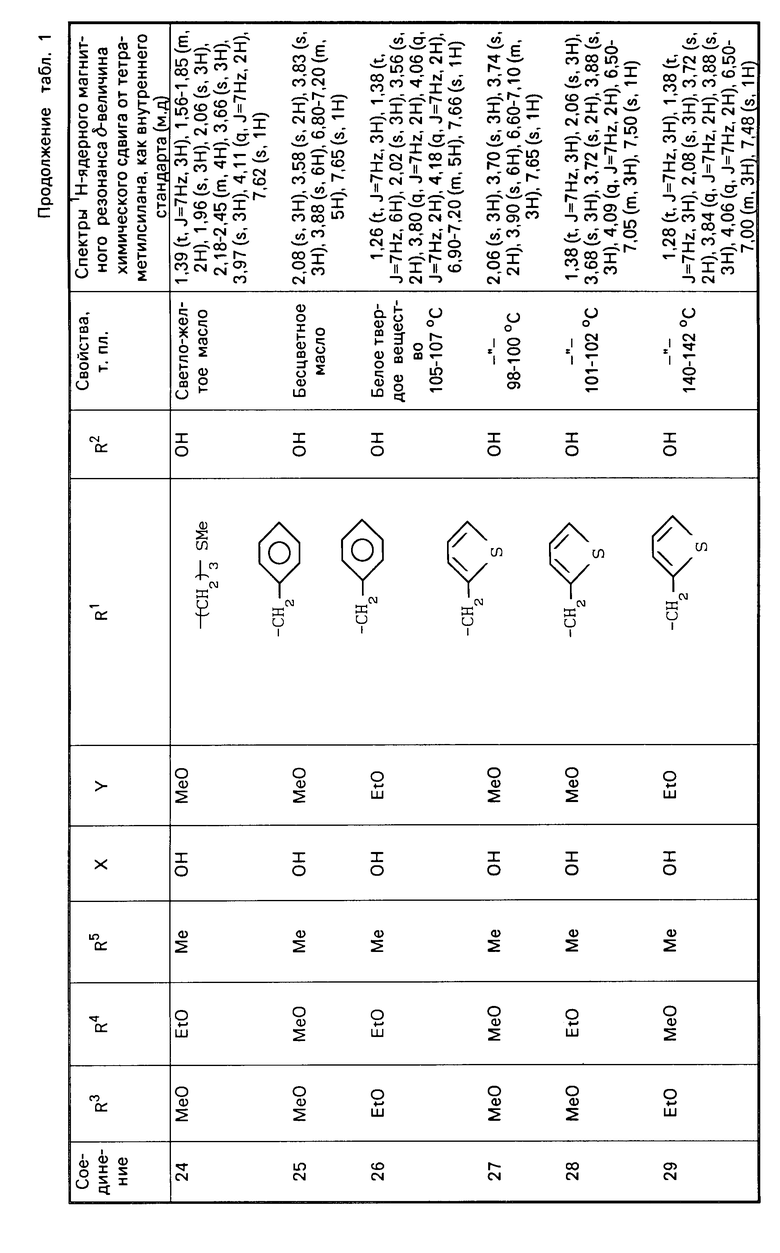
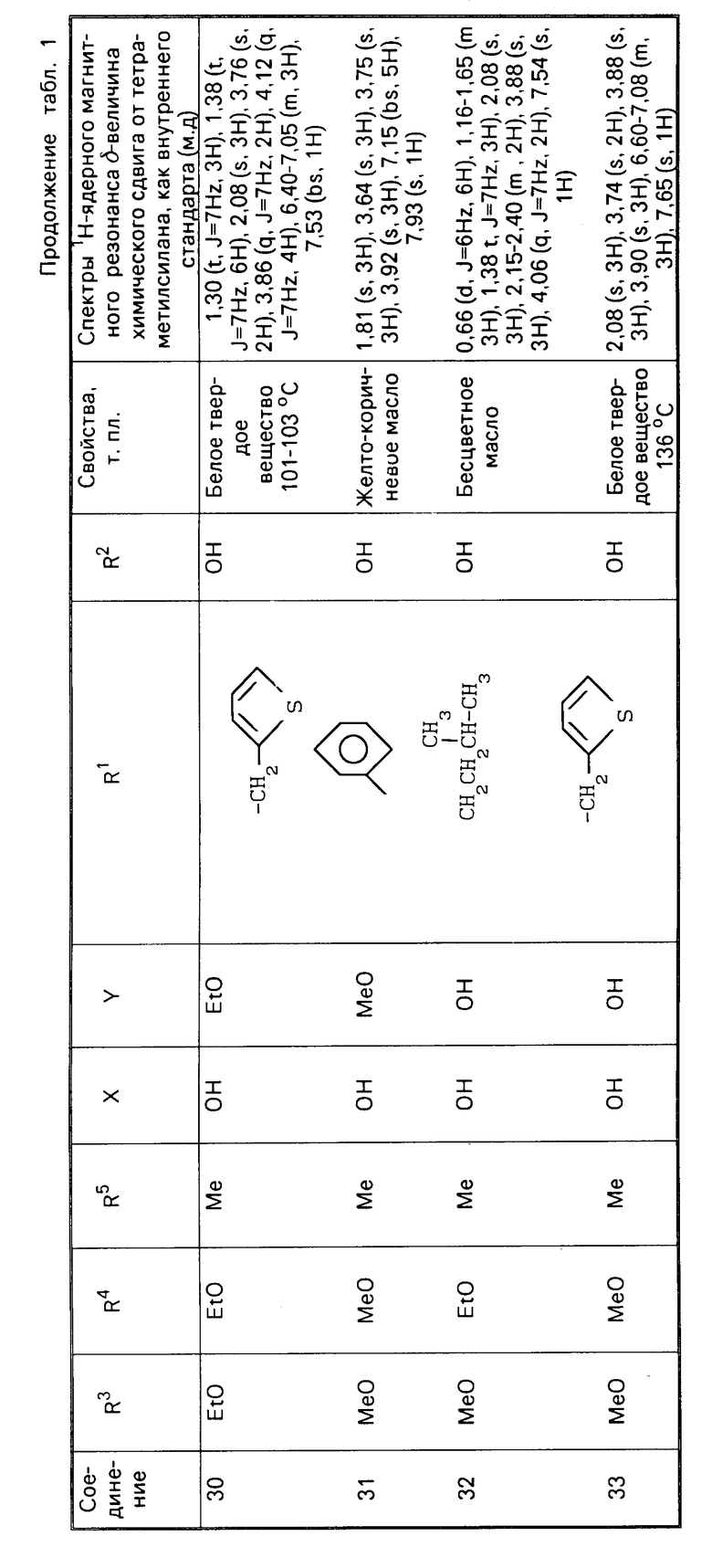
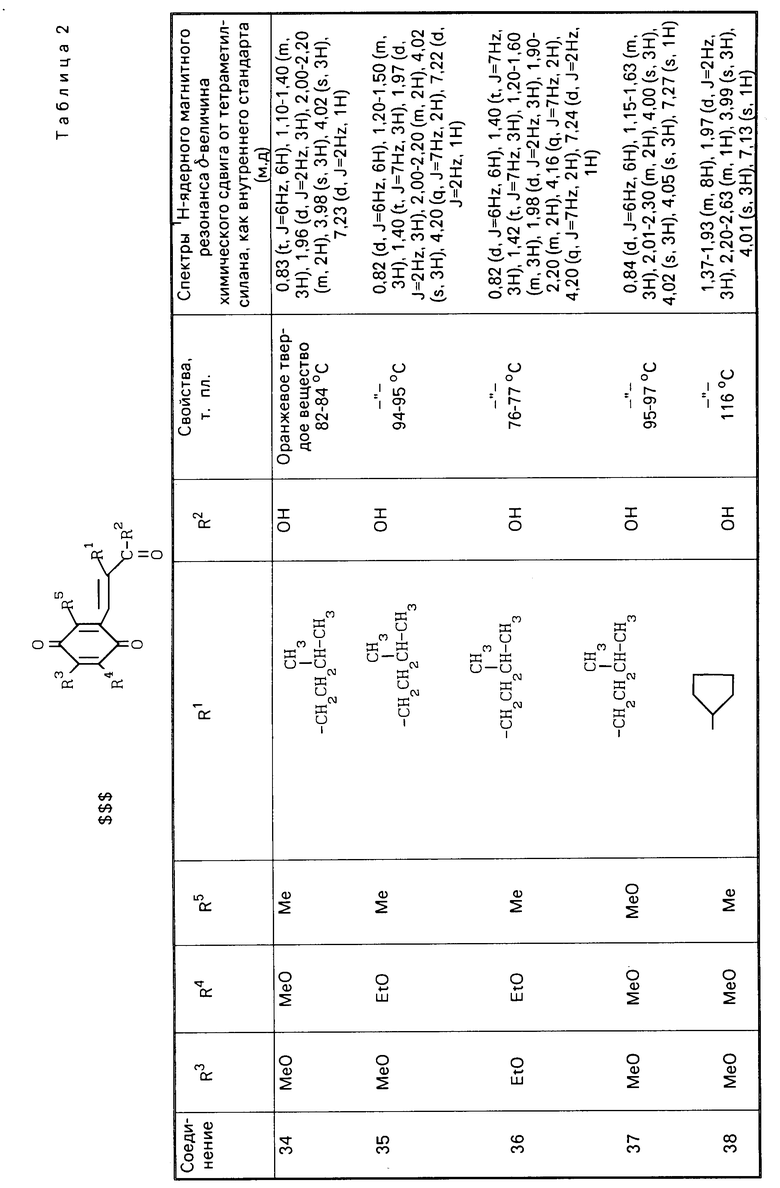
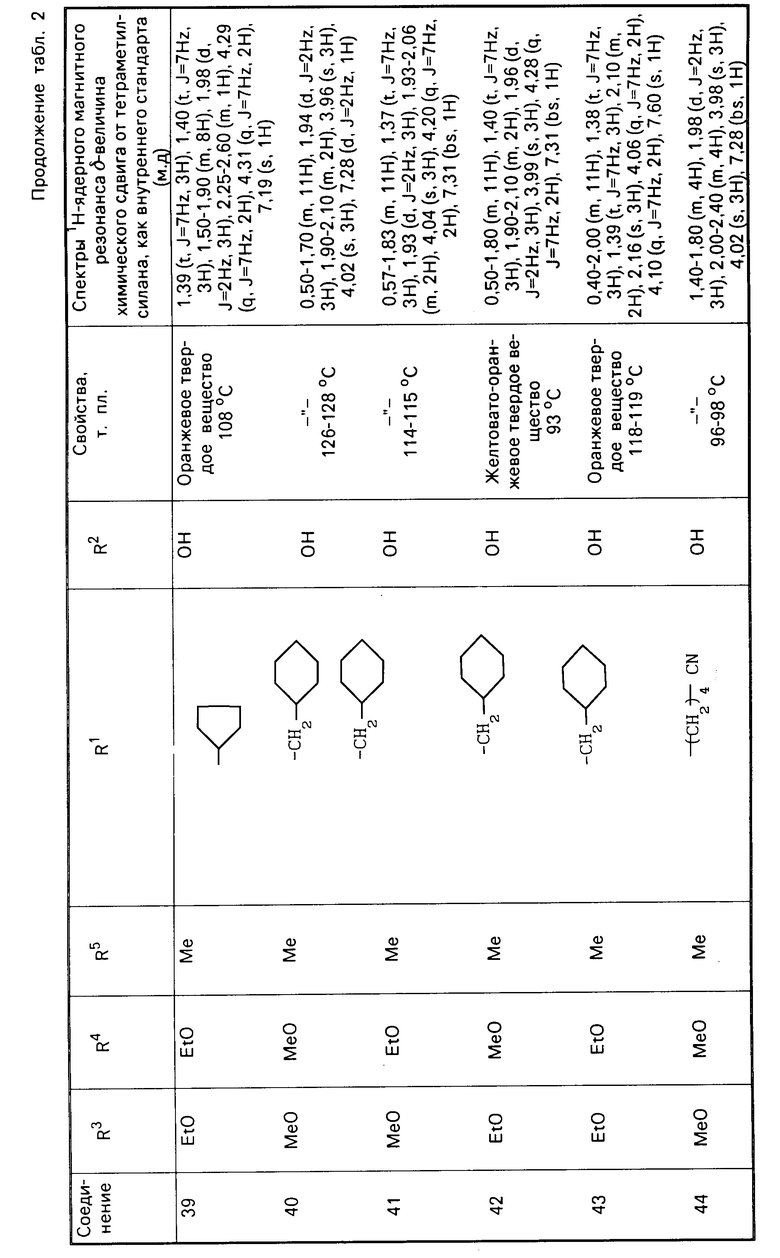
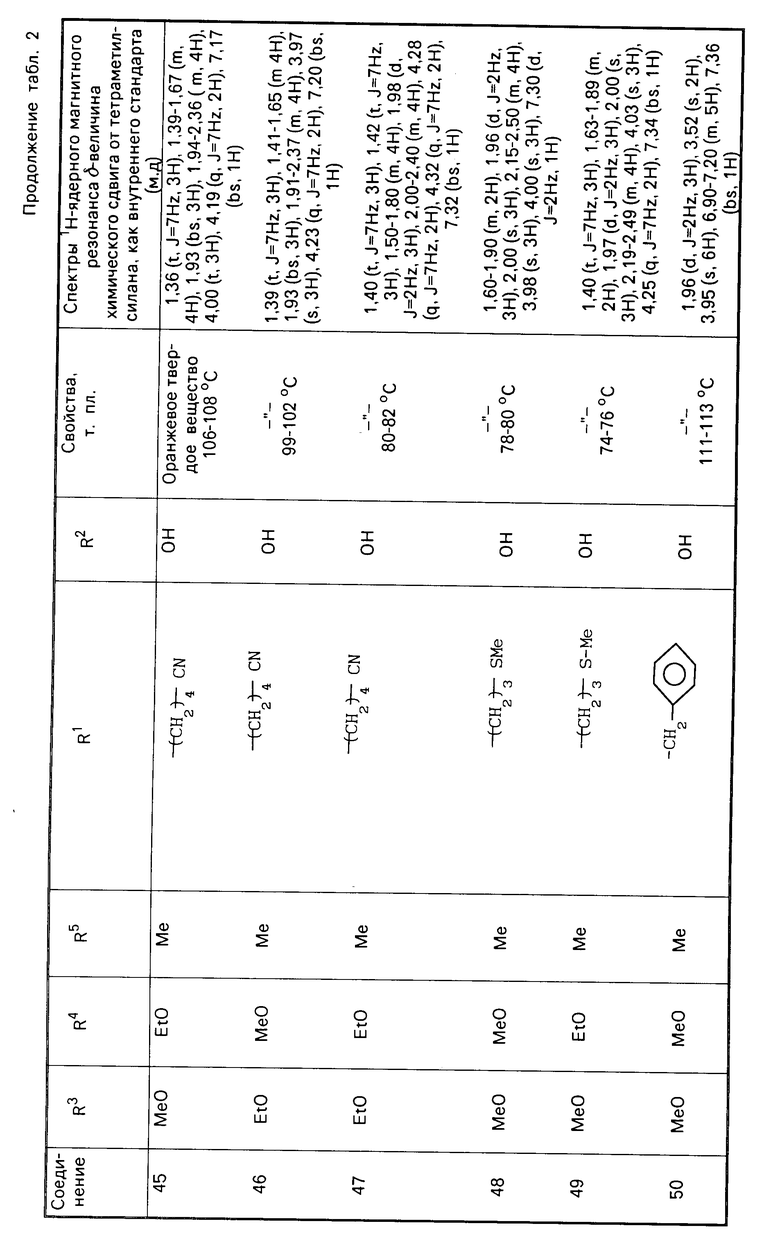
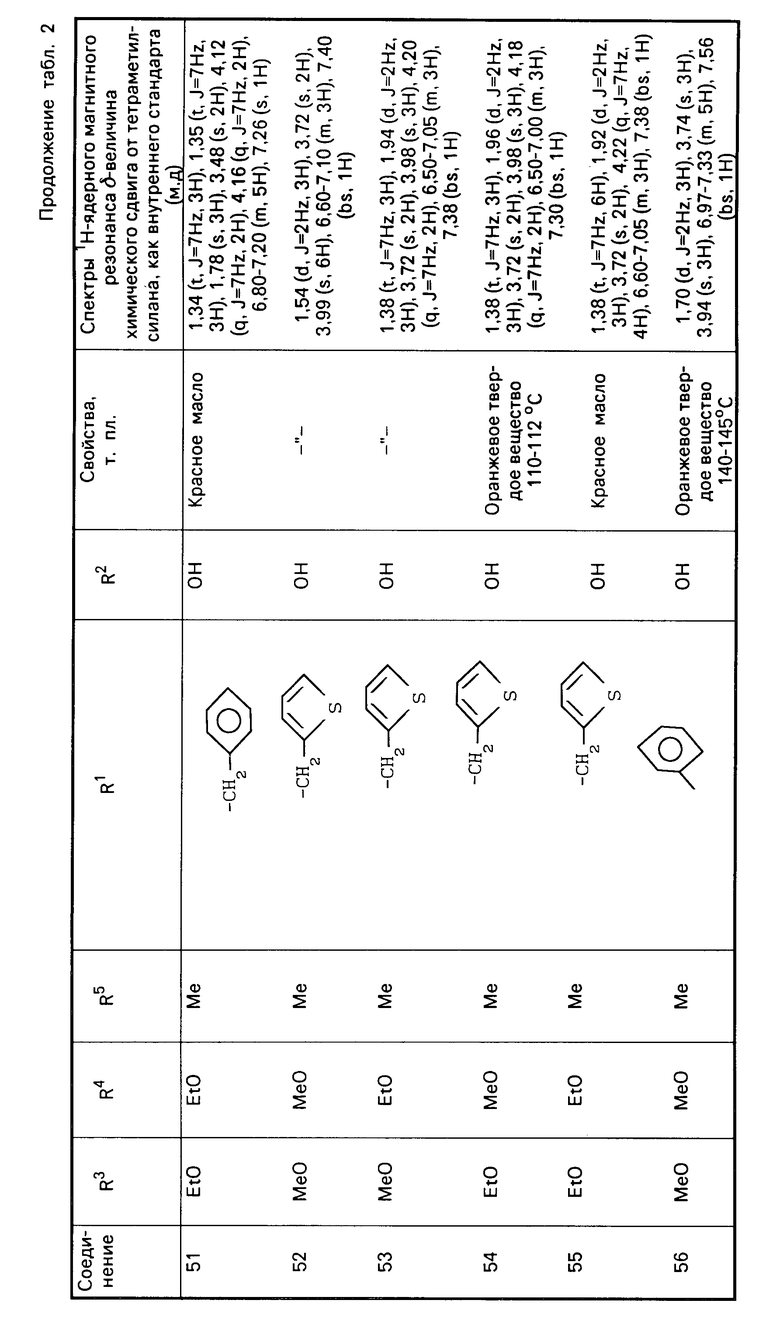
П р и м е р 2. Соединения представленные в табл. 1 и 2 получены в соответствии с методикой примера 1.
Гидрохиноновые соединения (соединения 1-32) и хиноновые соединения (соединения 34-56) представлены в табл. 1 и 2 соответственно. Фармакологические тесты.
Тест 1. Действие на крыс, модели с острым гепатитом, индуцированным α -галастосамином.
(1) Методики.
300 мг/кг GAIN было введено самцу крысы (примерно 180 г) Фишера (F 344) чтобы индуцировать острый гепатит. В каждом тесте соединение было суспензировано в 0,5% -ном водном растворе метилцеллюлозы и орально введено в дозах 100 мг/кг в час после инъекции GalN.
Кровь брали из хвоста крысы через 48 ч после введения GalN. Время свертывания крови измеряли по Гепапластиновому тесту (НРТ), и в то же время GPT-активность в плазме измеряли энзиматически.
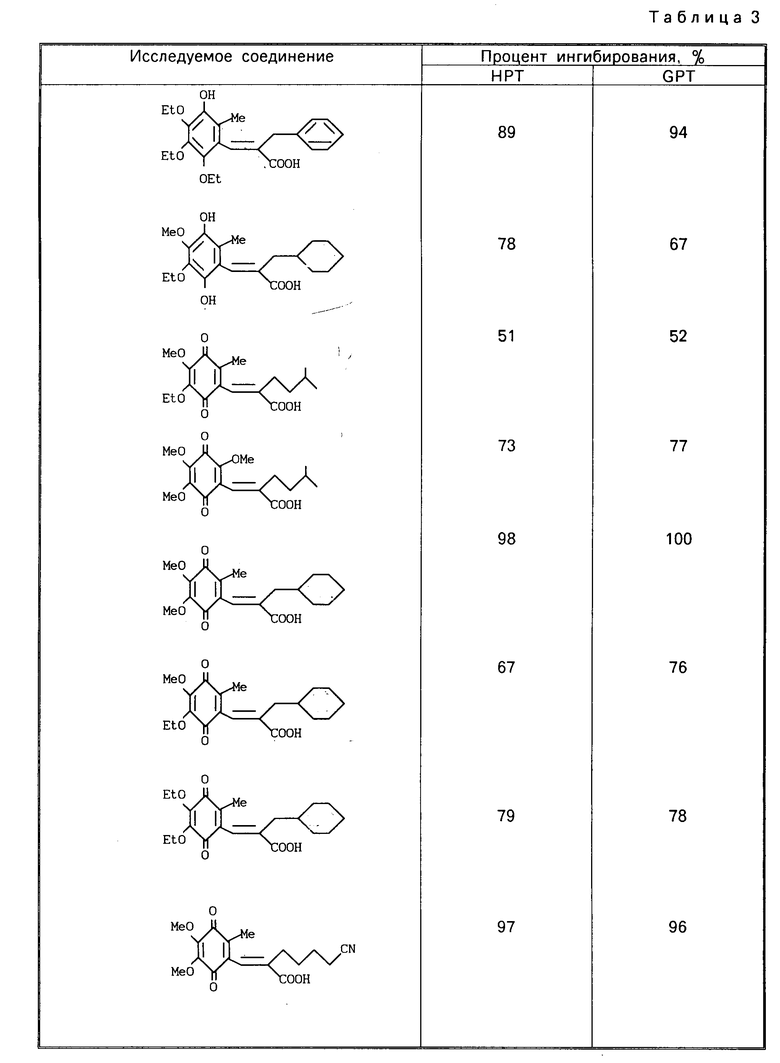
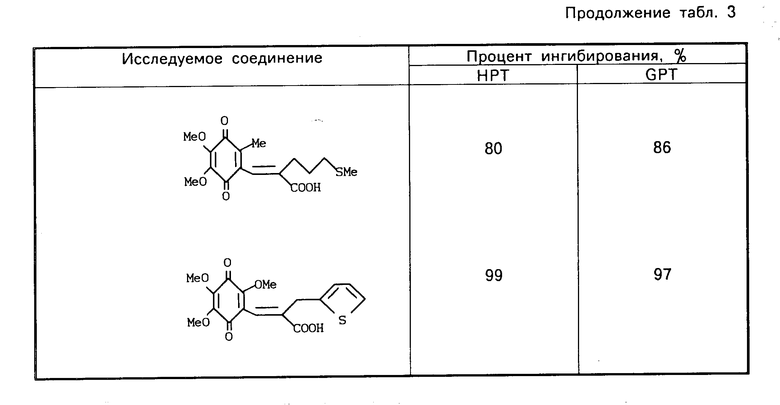
Процент снижения GalN-индуцированного гепатита при каждой проверке соединения показан в табл. 3.
(2) Результаты.
Результаты показаны в табл. 3. Соединения описаны в табл. 1 и 2.
Тест 2. Действия на мышей с propionibucterium (P, acnes)-липополисахарид (LPS)-индуцированным модельным скоротечным гепатитом.
(1) Методика.
Инактивированные нагреванием Р, acnes в количестве 1 мг/мышь были введены в пятинедельного самца BaLb/c мышей и LPS было введено внутривенно дополнительно в дозе 1 мкг/мышь через 7 дней после инъекции Р.acnes для провоцирования скоротечного гепатита. Каждое исследуемое соединение было суспензировано в 0,5% растворе метилцеллюлозы и орально давалось в дозах 100 мг/кг за 30 мин до внутривенного введения LPS.
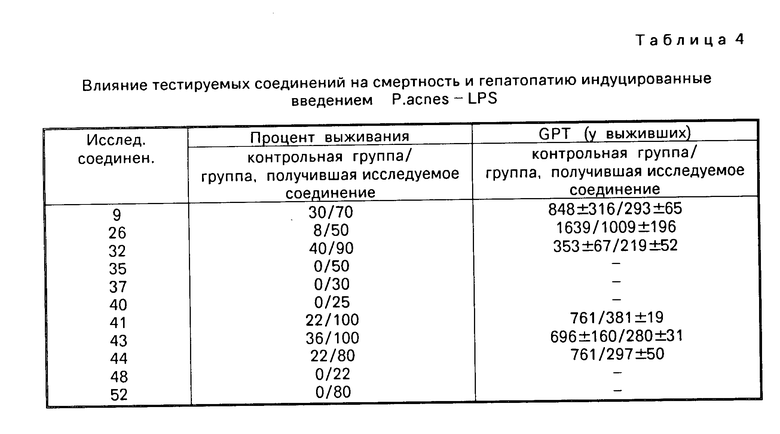
Процент выживания и GPT-активность в плазме выживших были определены через 24 ч после внутривенной инъекции LPS, эти мыши, обработанные каждым исследуемым соединением в целях предотвращения летального исхода и повреждения печени спровоцированного Р, acnes-LPS, показаны в табл. 4.
(2) Результаты.
Результаты приведены в табл. 4.
Так же как и в табл. 3, номера соединений в табл. 4 соответствуют номерам, приведенным в табл. 1 и 2.
Экспериментальный пример 3.
Тест на токсичность.
Соединение по изобретению 37 и соединение 41 как будет описано ниже были орально введены 7-недельному самцу крысе в течение 1 недели (доза 300 мг/мкг). В результате, как было установлено, ни одно соединение не привело к смерти.
Из экспериментальных тестов 1 и 2 очевидно, что соединения, представленные изобретением, высокоэффективны как терапевтические агенты для гепатических болезней.
Таким образом, соединения по изобретению являются полезными в качестве терапевтических и превентивных агентов для различных типов гепатитов животных, включая человека, и могут быть специфически использованы для лечения или предотвращения например, хронического гепатита, острого гепатита, токсической гепатопатии, алкогольного гепатита, желтухи и цирроза как последней стадии болезни.
Далее, как видно из экспериментального примера 3, соединения изобретения являются очень низко токсичными, т.е. высоко безопасными. Во многих случаях соединения представленные изобретением, должны будут приниматься в течение длительного периода времени в зависимости от природы заболевания. В этом случае изобретение представляет большую ценность.
Когда соединения по изобретению используют как терапевтические и превентивные агенты для гепатических болезней, их можно принимать в форме порошков, гранул, капсул, сиропов и капель. Доза соединений представляемых настоящим изобретением будет значительно меняться в зависимости от симптомов, давности, вида гепатической болезни и т.д. В общем соединения, представленные в изобретении, могут приниматься в дозах от 0,1 до 1,000 мг, предпочтительно от 2 до 500 мг, и еще более предпочтительно от 5 до 150 мг на взрослого человека в день от одной до нескольких порций.
Фармацевтическое приготовление осуществляется из соединений изобретения с использованием простых носителей, приемлемых для фармацевтического приготовления по обычной методике.
При получении твердого лекарства для употребления орально активный ингредиент смешивают с наполнителем и, если необходимо, с загущающим агентом, диспергатором, смазкой, красителем и т.д. далее следует приготовление таблеток, таблеток в оболочке, гранул, порошков и капсул.
Примеры наполнителей включают лактозу, кукурузный крахмал, сахарозу, глюкозу, сорбит, кристаллическую целлюлозу и диоксид кремния. Примеры загущающих агентов включают поливиниловый спирт, поливиниловый эфир, этилцеллюлозу, метилцеллюлозу, акацию, трагакант, желатин, мел, гидроксипропилцеллюлозу, гидроксипропилметил целлюлозу, цитрат кальция, декстрин и пектин.
Примеры смазок включают стеарат магния, тальк, полиэтиленгликоль, кремний, гидрированное овощное масло. Любой краситель, добавление которого в лекарства официально разрешено, может быть использован как краситель. Примеры вкусовых добавок включают какао порошок, ментол, ароматический порошок, цедру порошкообразную, борнеол, порошкообразную корицу. Покрытия из сахара и желатины и, если необходимо, пригодные другие покрытия могут применяться в таблетках и гранулах.
Когда готовят инъекции рН, модификатор, буфферный агент, стабилизатор, растворяющий агент и т.д. добавляют к активному ингредиенту, далее следует приготовление твердых лекарственных форм, внутримышечных и внутривенных инъекций в соответствии с общепринятыми методиками.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ БЕНЗОТИАЗОЛА ИЛИ ЕГО ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ | 1992 |
|
RU2041216C1 |
| ПРОИЗВОДНЫЕ БУТЕНОВОЙ ИЛИ ПРОПЕНОВОЙ КИСЛОТЫ | 1992 |
|
RU2041871C1 |
| ПРОИЗВОДНОЕ ХИНОНА ИЛИ ЕГО ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2049776C1 |
| ДИАМИНОВЫЕ СОЕДИНЕНИЯ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ | 1990 |
|
RU2045522C1 |
| СУЛЬФИРОВАННЫЕ АМИНОКИСЛОТНЫЕ ПРОИЗВОДНЫЕ И СОДЕРЖАЩИЕ ИХ ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ | 1997 |
|
RU2198656C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНА | 1992 |
|
RU2035461C1 |
| ПРОИЗВОДНОЕ БЕНЗОЛА | 1991 |
|
RU2061684C1 |
| ПРОИЗВОДНЫЕ К-252А | 1997 |
|
RU2205184C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ПРОПЕНИЛЦЕФЕМА ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1987 |
|
RU2010796C1 |
| ПРОИЗВОДНЫЕ КАРБАПЕНЕМА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2091381C1 |

Использование: в гетероциклической химии, в частности в способе получения производных хинона терапевтических агентов для лечения болезней печени. Сущность изобретения: продукт производные хинона ф-лы I: A-CH(двойная связь) CCR′-C(O)-R2 или их фармацевтически приемлемые соли, где A группа ф-лы II R3 и R4 равные или разные, метокси-или этоксигруппа: R5 метил или группа ф-лы III: 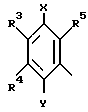 где R3 R4 R5 - см. выше, X, Y равные или разные, гидроксил или группа: -(OCH2)n-OR6 при n=0 или 1; R6 низший алкил; R′ C9H19 пентил, бензил, циклогексилметил, фенил или одна из групп
где R3 R4 R5 - см. выше, X, Y равные или разные, гидроксил или группа: -(OCH2)n-OR6 при n=0 или 1; R6 низший алкил; R′ C9H19 пентил, бензил, циклогексилметил, фенил или одна из групп 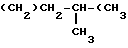 CH2-(CH2-CH2-CH2) CN или -(CH2)2-S-CH3 2-метилентиенил: R2
CH2-(CH2-CH2-CH2) CN или -(CH2)2-S-CH3 2-метилентиенил: R2
группа OR8 при R8 водород или алкил. Выход 90% Реагент 1: кетон ф-лы CR′ при R2 группа OR8 и R8 низший алкил. Реагент 2: гидроокись натрия. 4 табл.
Хиноновые производные общей формулы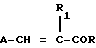
где А-группа общей формулы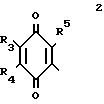
где R3 и R4, одинаковые различные и каждый метокси- или этоксигруппа;
R5 метил или группа общей формкулы;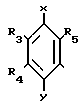
где R3 и R4 одинаковые и различные, и каждый метокси- или этоксигруппа;
R5 метил,
Х и У, одинаковые или различные и каждый гидроксильная группа или группа общей формулы
(ОСН2) ОR6,
где n 0 или 1;
R6 низшая алкильная группа;
R1 группа С9Н19 или С5Н11, или бензил или циклогексилметил, или фенил, или группа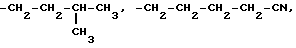
или -CH2-CH2-CH2-S-CH3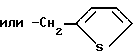
R2 группа ОR8, где R8 водород или низший алкил,
и их фармакологически приемлемые соли.
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ ЭПОКСИАМИНОПРОПИОНИТРИЛОВ | 0 |
|
SU185921A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-12-10—Публикация
1992-08-20—Подача