Изобретение относится к органическому синтезу и касается способа получения метилового эфира N-фенил-N-метоксиацетил-Д, L-аланина или его алкильных производных.
Известны представителем производных метилового эфира N-фенил-N-метоксиацетил-Д, L-аланина является метиловый эфир N-(2,6-диметилфенил)-N-метоксиацетил-Д, L-аланина (торговое название металаксил), представляющий собой систематический фунгицид, полученный фирмой ЦИБА-ГЕЙГИ в 1973 году.
По способу в соответствии с патентом ФРГ N 2515091 2,6-диметиланилин подвергают взаимодействию с метиловым эфиром ДL-α-бромпропионовой кислоты в присутствии гидрокарбоната натрия. В результате этой реакции образуется метиловый эфир N(2,6-диметилфенил)-ДL-аланина, который затем подвергают ацилированию метоксиацетилхлоридом и таким образом получают целевой продукт металаксил.
При осуществлении вышеуказанного способа реакцию ацилирования проводят после стадии алкилирования. Ацилирование стерически затрудненных вторичных аминов протекает с меньшей скоростью, чем ацилирование первичных аминов, хлорангидрид кислоты приходится брать в большом избытке, и целевой продукт получается с умеренным выходом.
Изобретение относится к способу получения производных метилового эфира N-фенил-N-метоксиацетил-ДL-аланина общей формулы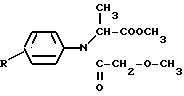 (I) где R означает водород или алкил С1-С4, исходя из соответствующего анилина с использованием реакции алкилирования метиловым эфиром галоидпропионовой кислоты при 110-140оС в присутствии конденсирующего агента, выбранного из неорганических оснований, и реакции ацилирования с использованием метоксиуксусной кислоты.
(I) где R означает водород или алкил С1-С4, исходя из соответствующего анилина с использованием реакции алкилирования метиловым эфиром галоидпропионовой кислоты при 110-140оС в присутствии конденсирующего агента, выбранного из неорганических оснований, и реакции ацилирования с использованием метоксиуксусной кислоты.
Способ по изобретению отличается тем, что соответствующий анилин подвергают вначале ацилированию смесью метоксиуксусной кислоты, которая берется в избытке 5-20% и треххлористого фосфора в среде растворителя, после чего образующееся производное N-метоксиацетиланилина общей формулы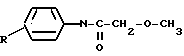 (II) в которой R имеет вышеуказанное определение, непосредственно или после выделения подвергают алкилированию 1,2-2,0-ух кратным избытком метилового эфира галоидпропионовой кислоты в присутствии щелочного металла, алкоголята, амида щелочного металла или комплексного гидрида металла.
(II) в которой R имеет вышеуказанное определение, непосредственно или после выделения подвергают алкилированию 1,2-2,0-ух кратным избытком метилового эфира галоидпропионовой кислоты в присутствии щелочного металла, алкоголята, амида щелочного металла или комплексного гидрида металла.
Предлагаемый способ основан на том факте, что ароматические амины целесообразнее сначала подвергать ацилированию и лишь затем алкилированию. В этом случае вышеописанный процесс протекает более гладко, чем при известных способах, по которым вначале проводят алкилирование, а затем ацилирование.
Ацилирование протекает легче, поскольку первичная аминогруппа может быть ацилирована легче, чем стерически затрудненный вторичный амин. Реакция алкилирования в этом случае протекает со значительно более высокой скоростью, так как механизм ее совершенно иной. Было установлено, что кислый атом водорода, связанный с атомом азота метоксиацетанилида, замещенного в 2-, 4- и/или 6-положении, может быть замещен атомом щелочного металла. Это замещение может быть осуществлено путем взаимодействия с щелочными металлами, алкоголятами, амидами щелочных металлов или комплексными гидридами металлов. Образующиеся в результате такого взаимодействия солеподобные соединения легко реагируют с алкилгалогенидами, например метиловым эфиром ДL-α-бромпропионовой кислоты.
Предлагаемый способ по сравнению с известными имеет следующие преимущества.
Ацилирование анилина, замещенного в ароматическом ядре, осуществляется с помощью смеси метоксиуксусной кислоты и треххлористого фосфора.
В этом случае метоксиацетилхлорид, реагирующий с анилином, образуется in situ, благодаря чему на одну стадию, а именно получение метоксиацетилхлорида, становится меньше. Ацилирование метоксиуксусной кислоты треххлористым фосфором осуществлено впервые. Указанное ацилирование проводят в среде растворителя. Предпочтительно используют ароматические растворители, такие как толуол, хлорбензол или ксилол. Ацилирование протекает в течение 0,5-1,0 ч.
В качестве алкилирующего агента используют алкилгалогениды, предпочтительно эфиры галогенкарбоновых кислот, например метиловый эфир ДL-α-бромпpопионовой кислоты. Температура реакции может варьироваться в пределах от 100 до 140оС, предпочтительно от 115 до 125оС. В том случае, если алкилирование проводится в присутствии алкоголята щелочного металла, выделяющийся свободный спирт можно удалять, предпочтительно непрерывно, из реакционной смеси.
При осуществлении предлагаемого способа, по которому алкилирование проводится после ацилирования, добавление реагентов требует 1 ч, на завершение реакции требуется еще 30 мин, реакция при этом протекает полностью и целевой продукт может быть получен с выходом 90% Метиловый эфир ДL-α-бромпpопионовой кислоты берется лишь с двукратным избытком.
Способ по изобретению по сравнению с известными имеет следующие преимущества.
1. Предложен новый способ синтеза производных метилового эфира N-фенил-N-метоксиацетил-ДL-аланина, например известного фунгицида "металаксила", по которому первичные ароматические амины вначале ацилируют, а затем алкилируют. Оба эти процесса протекают с более высокой скоростью и более высоким выходом, чем в том случае, когда вначале проводят алкилирование, а уже затем ацилирование. Ацилирование протекает легче, поскольку первичные амины ацилируются легче, чем вторичные. Алкилирование также протекает легче, поскольку взаимодействию с алкилгалогенидом по предлагаемому способу подвергается натриевая соль ацилированного амина.
2. Для ацилирования вместо метоксиацетилхлорида используется смесь метоксиуксусной кислоты и треххлористого фосфора, благодаря чему отпадает необходимость в получении, выделении и регенерации метоксиацетилхлорида.
3. При проведении ацилирования по предлагаемому способу ацилирующий агент берется в избытке 10% тогда как по известному уровню техники, когда используется метоксиацетилхлорид, для достижения достаточно высокого выхода, последний необходимо брать с 10-кратным избытком.
4. По известному уровню техники метиловый эфир ДL-α-бромпропионовой кислоты берется с трехкратным избытком. По предлагаемому способу алкилирующий агент берется лишь с 2-кратным избытком, а продолжительность реакции составляет 90 мин по сравнению с 18 ч в случае известного способа. При этом выход целевого продукта на 10% выше.
5. По предлагаемому способу и ацилирование, и алкилирование можно осуществлять без выделения образующихся промежуточных соединений. Более того, проведение процесса таким образом даже более предпочтительно. Этот момент также является существенным отличием предлагаемого способа, поскольку в случае известных способов промежуточные соединения должны быть выделены и очищены.
6. Предлагаемый способ является благоприятным с точки зрения охраны окружающей среды от загрязнений. При его осуществлении в качестве побочных продуктов образуются только полифосфорная кислота и бромид натрия, которые с успехом могут использоваться в других процессах, поскольку они содержат лишь очень незначительное количество примесей. Количества маточного ксилольного раствора, образующегося в конце процесса, очень незначительны, и он может быть сожжен. При осуществлении данного способа не образуется сточных вод.
П р и м е р 1. Получение N-метоксиацетил-2,6-диметиланилина. В колбу емкостью 1 дм3, снабженную мешалкой, капельной воронкой, термометром и обратным холодильником, загружают 500 см3 толуола, 121,9 г (1,0 М) 2,6-диметиланилина и 99,0 г (1,1 М) метоксиуксусной кислоты, затем в течение 1 ч при перемешивании добавляют по каплям 50,6 г (0,37 М) треххлористого фосфора, растворенного в 100 см3 толуола, и кипятят смесь в течение 90 мин с обратным холодильником, отводя из нее газообразный хлористый водород. Реакционную смесь затем охлаждают до комнатной температуры и промывают водой. Толуол отгоняют, а следы растворителя удаляют в вакууме. В качестве остатка получают желтоватый кристаллический продукт. Т.пл. 64оС. Выход 183 г (94,6%).
П р и м е р 2. Получение N-(2,6-диметилфенил)-N-(метоксиацетил)-ДL-аланина.
В колбу, снабженную мешалкой, обратным холодильником, наклонным холодильником, термометром и загрузочной воронкой, добавляют 9,66 г (0,05 М) N-метоксиацетил-2,6-диметиланилина, полученного в соответствии с примером 1, 60 см3 ксилола и 16,7 г (0,1 М) метилового эфира ДL-α-бромпропионовой кислоты. Смесь нагревают до 120оС и добавляют к ней по каплям в течение 1 ч 20 см3 30% -ного метилата натрия, отгоняя при этом непрерывно метанол. Температура смеси не должна быть ниже 110оС. Реакционную смесь затем перемешивают в течение еще 30 мин, охлаждают до комнатной температуры, смешивают с 100 см3 воды, разделяют фазы и трижды проводят экстракцию из водной фазы ксилолом, порциями по 20 см3. Ксилольные фракции объединяют, высушивают над сульфатом натрия и отгоняют ксилол. Охлажденный осадок отверждается с образованием кристаллического вещества. Т.пл. 73,5оС. Выход 12,5-13,0 г (89,5-93,0%).
П р и м е р 3. Получение метилового эфира N-(2,6-диметилфенил)-N-(метоксиацетил)-ДL-аланина из 2,6-диметиланилина, без выделения промежуточного соединения. 6,06 г (0,05 М) 2,6-диметиланилина и 4,95 г (0,055 М) метоксиуксусной кислоты растворяют в 30 см3 ксилола и к полученному раствору добавляют по каплям при перемешивании 2,6 г (0,019 М) треххлористого фосфора, растворенного в 10 см3 ксилола. По окончании добавления смесь кипятят в течение 30 мин с обратным холодильником и охлаждают до комнатной температуры. Ксилольный раствор отделяют от полифосфорной кислоты и добавляют к нему 16,7 г (0,01 М) метилового эфира ДL-α-бромпропионовой кислоты. С колбой соединяют наклонный холодильник, смонтированный вместе с обратным холодильником. Смесь нагревают до 120оС и добавляют к ней в течение 1 ч по каплям 20 см3 30%-ного (об.) раствора метилата натрия, непрерывно отгоняя из реакционной смеси метанол. Температура реакционной смеси при этом не должна быть ниже 110оС. После этого реакционную смесь перемешивают в течение еще 30 мин и затем охлаждают до комнатной температуры. Образующийся в процессе бромид натрия отфильтровывают и дважды промывают ксилолом, порциями по 10 см3. Объединенные ксилольные растворы упаривают до объема 20 см3 и охлаждают остаток до 0оС. Выпадающие кристаллы целевого продукта отфильтровывают. Т.пл. 73-74оС. Выход 13,0 г (93,0%).
Дополнительное количество продукта может быть получено из маточного раствора.
П р и м е р 4. Получение N-метоксиацетил-2,4,6-триметиланилина. Процесс проводят таким же образом, как это описано в примере 1, с той разницей, что в качестве исходного материала используют 2,4,6-триметиланилин. Т.пл. 88-89оС. Выход 188,85 г (92,0%).
П р и м е р 5. Получение метилового эфира N-(2,4,6-триметилфенил)-N-метоксиацетил-ДL-аланина. Процесс проводят таким же образом, как это описано в примере 2, с той разницей, что в качестве исходного материала используют 10,26 г N-метоксиацетил-2,4,6-триметиланилина. В качестве целевого продукта получают вязкую маслянистую жидкость. Выход 12,9 г (88,0%).
П р и м е р 6. Получение метилового эфира N-(2-этилфенил)-N-метоксиацетил-ДL-аланина. Процесс проводят таким же образом, как это описано в примере 3, с той разницей, что вместо 2,6-диметиланилина используют 2-этиланилин.
Полученный целевой продукт представляет собой вязкую маслянистую жидкость. Выход 13,3 г (94,5%).
П р и м е р 7. Получение метилового эфира N-(4-изопропилфенил)-N-метоксиацетил-ДL-аланина. Процесс проводят таким же образом, как это описано в примере 3, с той разницей, что в качестве исходного материала вместо 2,6-диметиланилина используют 4-изопропиланилин.
Полученный целевой продукт предcтавляет cобой вязкую маcляниcтую жидкоcть.
Выход 13,35 г (91,0).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ МЕТИЛ-N-АМИДООКСАМОИЛ-N-ФЕНИЛ-D, L-АЛАНИНАТЫ И ИХ СПОСОБЫ ПОЛУЧЕНИЯ | 2003 |
|
RU2247716C2 |
| Способ получения 2,6-диалкил- @ -(алкоксиметил)-2-хлорацетанилидов | 1980 |
|
SU1245258A3 |
| Фунгицидное средство | 1975 |
|
SU730268A3 |
| Способ получения 3-изопропил-бензо-2-тио-1,3-диазинон-(4)-2,2-диоксида | 1987 |
|
SU1811529A3 |
| Микробицидное средство | 1975 |
|
SU682096A3 |
| Способ получения -аминофосфоновых кислот | 1978 |
|
SU776561A3 |
| Способ получения эфира азотной кислоты N-/2-оксиэтил/-никотинамида или его солей | 1977 |
|
SU999965A3 |
| Способ получения органических содинений | 1975 |
|
SU628812A3 |
| ОПТИЧЕСКИ АКТИВНЫЙ ГЕРБИЦИДНЫЙ N-МЕТИЛ-N-2-ФТОРФЕНИЛАМИД (R)-ФЕНОКСИПРОПИОНОВОЙ КИСЛОТЫ, СПОСОБ БОРЬБЫ С КУРИНЫМ ПРОСОМ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2264392C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ N-МЕТИЛ-ПАРА-АНИЗИДИНА | 2011 |
|
RU2472774C1 |
Сущность изобретения: продукт - метиловый эфир N-фенил-N-метоксиацетил-D, L-аланин или его алкильные производные формулы RC6H4N[CH(CH3)COOCH3]C(=O)CH2OCH3. Реагент 1: анилин или его алкильное производное. Реагент 2: смесь метоксиуксусной кислоты, взятая в избытке 5-20% и треххлористого фосфора. Условия реакции: в среде растворителя, после полученное производное N-метоксиацентиланилин RC6H4NH(C=O)CH2OCH3 непосредственно в реакционной массе или после выделения из нее подвергают алкилированию при 110-140°С, используя 1,2 - 2-кратный избыток метилового эфира галоидпропионовой кислоты и органическое основание, выбранное из группы: щелочной металл, алкоголят щелочного металла, амид щелочного металла, комплексный гидрид металла.
СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА N-ФЕНИЛ-N-МЕТОКСИАЦЕТИЛ-D,L-АЛАНИНА ИЛИ ЕГО АЛКИЛЬНЫХ ПРОИЗВОДНЫХ общей формулы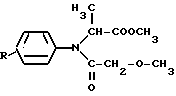
где R водород или С1 С4-алкил,
исходя из соответствующего анилина, с использованием реакции алкилирования метиловым эфиром галоидпропионовой кислоты при 110 140oС в присутствии конденсирующего агента, выбранного из неорганических оснований, и реакции ацилирования с использованием метоксиуксусной кислоты, отличающийся тем, что, с целью повышения выхода, соответствующий анилин подвергают вначале ацилированию смесью метоксиуксусной кислоты, взятой в избытке 5 20% и треххлористого фосфора в среде растворителя, после чего полученное производное N-метоксиацетиланилина общей формулы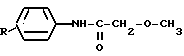
где R имеет указанные значения,
непосредственно в реакционной массе или после выделения из нее подвергают алкилированию, используя 1,2-2-кратный избыток метилового эфира галоидпропионовой кислоты и органическое основание, выбранное из группы: щелочной металл, алкоголят щелочного металла, амид щелочного металла, комплексный гидрид металла.
| СПОСОБ ПОЛУЧЕНИЯ СЫРЦОВЫХ ПРЯНИКОВ | 2013 |
|
RU2515091C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-12-27—Публикация
1990-04-19—Подача