Изобретение относится к новым биологическим активным соединениям, а именно к производным 2-меркаптобемзимидазола общей формулы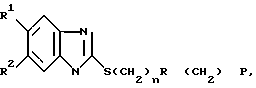
где n 0,2,5; R аллил, диалниламино или остаток моноциклического насыщенного амина, который может содержать дополнительный гетероатом R1 и R2 одинаковые или различные: Н, низшие алкилы, алкокси или их фармацевтически приемлемым солям, которые обладают селективной анксиолитической активностью.
Известно, что S производные 2-мернаптобеызимйдазолов проявляют разнообразную биологическую активность, в частности сердечно сосудистую, антигистаминовую и антиаллергическую, анальгетическую, противовоспалительную и жаропонижающую, противоязвенную, противомикробную. Имеются патентные данные об антидепрессивной активности некоторых соединений этого ряда. Гидрохлорид 5-этокси-2-этилтиобензимидазола обладает стресс-протективным и антигипоксическим действием (13). Известен также внедренный в медицинскую практику в качестве актопротектора отечественный препарат бемитил - гидрохлорид 2-этилтиобензимидазола, проявляющий также слабую транквилизирующую активность.
Этот препарат является наиболее близким аналогом заявляемым соединениям как по химической структуре, так и по фармакологическому действию.
Целью изобретения является получение производных 2-меркаптобензимидазола, обладающих высокой и селективной анксиолитической активностью при низкой токсичности.
Заявляемые соединения и их гидрохлориды синтезированы по типовым методикам путем алкилирования 2-меркаптобензимидазолов соответствующими алкилирующими агентами в водно-спиртовой среде в присутствии оснований (гидроокись натрия) и последующей обработки образующихся масло образных или кристаллических оснований в растворе абсолютного спирта или смеси абсолютного спирта и эфира спиртовым или эфирным раствором хлористого водорода.
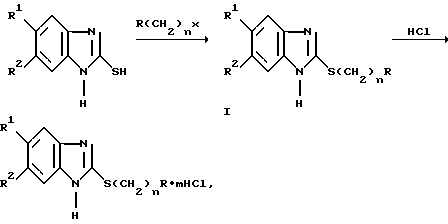 где n R, R1 и R2 имеют вышеуказанные значения,
где n R, R1 и R2 имеют вышеуказанные значения,
X хлор или бром, m=1 или 2.
Контроль за ходом реакций и чистотой полученных продуктов проводился с помощью тонкослойной хроматографии на силуфоле в системе бензол-ацетон (4: 1).
Пример 1. 5-Этокси-2-[2-(морфолино)этилтио]бензимидазол (1а) и его дигидрохлорид. К раствору 2,9 г (0,015 моля) 5-этокси-2-меркаптобензимидазола и 1,35 г (0,033 моля) гидроокиси натрия в 10 мл воды и 40 мл этанола прибавляют 3,45 г (0,018 моля) гидрохлорида 2-морфолино)этилхлорида. Реакционную смесь кипятят 2 часа до исчезновения исходного тиона (контроль по ТСХ), концентрируют до одной трети объема и разбавляют водой. Выделившееся масло экстрагируют этилацетатом. Экстракт встряхивают с 10% соляной кислотой, слои разделяют, водный слой кипятят с углем, фильтруют и подщелачивают раствором едкого кали. Вы делившееся масло экстрагируют этилацетатом, экстракт промывают водой, сушат сульфатом магния и упаривают. Получают 3,99 г (87Х) маслообразного вещества 1а. Найдено, С 58,6; Н 6,8; N 13,9; S 10,1 С15Н21N302S. Вычислено, С 58,6; Н 6,9; N 13,7; S 10,4. ПМР- спектр (СDС13), δ, м.д. 1,48 (3Н,т,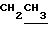 ); 4,02 (2Н,кв.
); 4,02 (2Н,кв.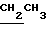 ); 2,59 (4Н, м, СН2NСН2 морфолина); 3,79 (4Н, м, СН20СН2 морфолина); 2,85 (2Н, м,СН2S); 3,24 (2Н,м,СН2N); 6,82 (1Н, д. д.6-Н) 7,00 (1H, уш.с.4-Н); 7,41 (1Н, д, 7-Н). Маслообразное основание 1а растворяют в 15 мл абсолютного спирта, обрабатывают эфирным раствором хлористого водорода и оставляют на 30 минут. Выпавший осадок отфильтровывают, промывают небольшим количеством абсолютного спирта и абсолютным эфиром. Получают 4,5 г (91% ) дигидрохлорида основания 1а, т.пл. 191-192o ( с разл. из спирта с углем). Найдено, С 47,3; Н 6,1; С1 18,6; N 11,1; S 8,4. С15Н23С12N302S. Вычислено, С 47,4; Н 6,1; Cl 18,6; N 11,0: S 8,4 ПМР-спектр (D2О), δ, м.д. 1,54 (3Н, т,
); 2,59 (4Н, м, СН2NСН2 морфолина); 3,79 (4Н, м, СН20СН2 морфолина); 2,85 (2Н, м,СН2S); 3,24 (2Н,м,СН2N); 6,82 (1Н, д. д.6-Н) 7,00 (1H, уш.с.4-Н); 7,41 (1Н, д, 7-Н). Маслообразное основание 1а растворяют в 15 мл абсолютного спирта, обрабатывают эфирным раствором хлористого водорода и оставляют на 30 минут. Выпавший осадок отфильтровывают, промывают небольшим количеством абсолютного спирта и абсолютным эфиром. Получают 4,5 г (91% ) дигидрохлорида основания 1а, т.пл. 191-192o ( с разл. из спирта с углем). Найдено, С 47,3; Н 6,1; С1 18,6; N 11,1; S 8,4. С15Н23С12N302S. Вычислено, С 47,4; Н 6,1; Cl 18,6; N 11,0: S 8,4 ПМР-спектр (D2О), δ, м.д. 1,54 (3Н, т, 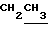 ); 4,25 (2Н, кв,
); 4,25 (2Н, кв,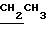 ); 3,58 (4Н, неразр.м, СН2NCH2 морфолина); 4,12 (4Н, неразр.м. СН2OCH2 морфолина); 3,74 (2Н, м, СН2S); 3,86 (2Н, м, СН2N): 7,21 (1Н,д,6-Н); 7,22 (IH, с, 4-Н); 7,41 (IH, д, 7-Н).
); 3,58 (4Н, неразр.м, СН2NCH2 морфолина); 4,12 (4Н, неразр.м. СН2OCH2 морфолина); 3,74 (2Н, м, СН2S); 3,86 (2Н, м, СН2N): 7,21 (1Н,д,6-Н); 7,22 (IH, с, 4-Н); 7,41 (IH, д, 7-Н).
Пример 2. 5-Этокси-2- аллилтиобензимидазол (1б) и его гидрохлорид. К раствору 1,95 г (0,01 моля) 5-этокси-2-меркаптобензимидазола и 0,44 г (0,011 моля) гидроокиси натрия в мл воды и 20 мл спирта прибавляют 1,32 г (0,011 моля) аллилбромида. Реакционную смесь кипятят 3 часа до исчезновения исходного тиона (контроль по ТСХ). Охлаждают и разбавляют водой. Выделившееся масло экстрагируют эфиром, экстракт сушат сульфатом магния и упаривают. Получают соединение 1б в виде масла. Маслообразный продукт растворяют в абсолютном эфире и обрабатывают эфирным раствором хлористого водорода, выпавший осадок отфильтровывают, промывают абсолютным эфиром и сушат на воздухе. Получают 2 (74%) гидрохлорида основания 1б, т.пл. 147-149o (с разл. из абсолютного спирта с эфиром). Найдено, С 53,4; Н 5,6; С1 13,1; N 10,3 S 11,9. C12H15ClN2OS. Вычислено, С 53,2; Н 5,6; С1 13,1; N 10,3; S 11,9. ПМР-спектр (D2O),δ,м.д. 1,54 (3Н, т, 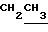 ); 4,18 (2Н, кв,
); 4,18 (2Н, кв,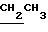 ); 4,05 (2Н, д, СН2S); 5,34 (Ив, д, CHc=CHaHв); 5,42 (На, д, CHc=CHaHв); 7,07 (1Н, уш.с, 4-Н); 7,09 (1Н, д.д. 6-Н); 7,52 (1Н, д, 7-H).
); 4,05 (2Н, д, СН2S); 5,34 (Ив, д, CHc=CHaHв); 5,42 (На, д, CHc=CHaHв); 7,07 (1Н, уш.с, 4-Н); 7,09 (1Н, д.д. 6-Н); 7,52 (1Н, д, 7-H).
Пример 3. 5,6-Диметил-2-[2-(морфолино)этилтио бензимидазол (1в) и его дигидрохлорид. К раствору 1,2 r (0,03 моля) гидроокиси натрия в 10 мл воды и 40 мл спирта прибавляют 2,67 г ( 0,015моля) 5,6-диметил-2-меркаптобензимидазола и 2,8 г (0,015 моля ) гидрохлорида 2 морфолиноэтилхлорида. Реакционную смесь кипятят в течение 6 часов до исчезновения исходного тиона (контроль по ТСХ). Охлаждают, разбавляют водой. Выпавший осадок отфильтровывают, промывают Болон и сушат на воздухе. Получают 2,95 г (69%) вещества 1в. т. пл. 147-148o (из смеси этилацетата с гексаном). Найдено, N 14,5; S 11,1. C15H21N13OS. Вычислено, N 14,5; S 11,0. ПМР-спектр (СDС13),δ м.д. 2,32 (6Н,c,2СН3); 2,62 (4Н, м, CH2NCH2 морфолина) 3,83 (4Н, м,СН2ОСН2 морфолина); 2,86 (2Н,м,СН2S); 3,21 (2Н,м,СН2N) 7,27 (2Н, с. ArH)
Основание Iв (2,5 г) растворяют в 15 мл абсолютного спирта, раствор обрабатывают эфирным раствором хлористого водорода и оставляют на 30 мин, выпавший осадок отфильтровывают, промывают абсолютным эфиром и сушат на воздухе. Получают 3,0 г (96%) дигидрохлорида основания Iв, т.пл. 250-252o(с разл. из абсолютного спирта). Найдено, С 49,4Н 6,5; Сl 19,8; N 11,6: S 8,5. C15H23CI2N30S. Вычислено, C 49,4; Н 6,4: С1 19, N 11,5; S 8,8.
Пример 4. 5,6-Диметил-2-2-(пирролидино)этилтио-]бензимидазол (Iг) и его дигидрохлорид. Синтезированы аналогично предыдущему из 2,67 г (0,015 моля) 5,6-диметил-К-меркаптобензимидазола и 2,9 г (0,17 моля) гидрохлорида 2-(пирролидино)этилхлорида в присутствии 1,36 г (0,034 моля) гидроокиси натрия (кипячение 1,5 часа). Выход соединения Iг -4,0 г (90% считая на моногидрат), т.пл. 115-116o (с разл. из водного спирта. Найдено, С 61,4; Н 7,8; N 14,5; S 10,9. C15H21N3S•H2O. Вычислено, C 61,4; Н 7,9; N 14,3: S 10,9. ПMP -спектр (СDСl3), d. м. д. 1,97 (4Н, м,b-Н пирролидина); 2,34 (6Н,с, 2CH3) 2,72 (4Н, мa-Н пирролидина); 3,02 (2Н,м,CH2S); 3,19 (2Н,м,СH2N); 7,18 (2Н, уш-с, АrН)
Дигидрохлорид основания 1г, выход колич. т.разл. 240o (из смеси абсолютного спирта с этилацетатом). Найдено, С 51,7: Н 6,5; Сl 20,4; N 11,7. C15H23CI2N3S. Вычислено, С 51,7; Н 6,7; CL 20,4; N 12,1.
Пример 5. 5,6-Диметил-2-[2- (пиперидино) этилтио] бензимидазол ( Iд ) и его дигидрохлорид. Синтезированы аналогично предыдущему из 2,67 г (0,015 моля) 5,6-диметил-2-меркаптобензимидазола и 3,13 г (0,017 моля) гидрохлорида 2- (пиперидина) этилхлорида в присутствии 1,36 г ( 0,034 моля) гидроокиси натрия. Выход соединения 1д 4,3 г (93% считая на моногидрат). т.пл. 117-119o (с разл. из водного спирта). Найдено, C 62,7; Н 8,0; N 13,6; S 10,5. C16H23N3S•H20. Вычислено, C 62,5; Н 8,2; N 13,7; S 10,4. ПМР-спектр (CDCL3), d, м. д. 1,65 (2Н, уш.м.g- H пиперидина); 1,8 (4Н,м,b -H пиперидина); 2,34 (6Н, с, 2СН3); 2,63 (4Н, уш.м.a-Н пиперидина); 2,90 (2Н,м,CH2S); 3,10 (2H,м, CH2N); 7,26 (2Н, уш.с. АrН).
Дихлоргидрат основания 1д, выход 90% т.разл. 242-245o (из смеси абсолютного спирта с этилацетатом). Найдено, С 52,3; Н 7,0: С1 19,5; N 11,2. C16H25Cl2N3S• 0,25 H2O. Вычислено, С 52,4; Н 7,0; С1 19,3; N 11,4.
Пример 6. 5,6-Диметил-2-аллилтиобензимидазол (Iе) и его гидрохлорид. Синтезированы аналогично предыдущему из 2,67 г (0,015 моля) 5,6-диметил-2-меркаптобензимидазола и 2,1 г (0,017 моля) аллилбромида в присутствии 0,7 г (0,017 моля) гидроокиси натрия. Выход соединения 1г 3 г (92%), т.пл. 119-120• ( из смеси этилацетата с гексаном). Найдено, N 12,7; S 14,7. C12H14N2S. Вычислено, N 12,8; S 14,7. ПМР-спектр (СDС13),dм.д. 2,33 (6Н, с, 2СН3); 3,89 (2H, д, CH2S); 5,10 (Нв,д, СНс-СНаНв); 5,25 (На,д, СНс=СНаНв); 5,97 (Нс. м, СНс=СНаНв); 7,30 (2Н, уш.с, АrН); 10,11 (1Н, ш.с, NH).
Гидрохлорид основания 1е, выход 93% т.пл. 204-205o (с разл. из абсолютного спирта). Найдено, С 56,8; Н 5,9; Cl 14,0; N 10,9; S 12,6. C12H15ClN2S. Вычислено, С 56,6; Н 5,9; С1 13,9; N 11,0; S 12,6.
Результаты фармакологического изучения заявляемых соединений.
Для демонстрации анксиолитического действия новых соединений был использован метод измерения двигательной активности в тесте "открытое поле", который позволяет не только оценить силу анксиолитического эффекта, но и степень его селективности [17] Сутью данного подхода является сравнительный анализ поведенческих эффектов изучаемых соединений у мышей двух инбредных линий Balb/c и С57В1/6, которые характеризуются различными генетическими детерминированными типами эмоционально-стрессовой реакции (ЭСР). О наличии анксиолитического действия судили по выявлению активирующего эффекта на двигательную активность у животных с "пассивным" типом ЭСР (линия Ва1Ь/с). Показателем седативных свойств исследуемых соединений служило выявление их ингибирующего действия на двигательную активность мышей с "активным" типом ЭСР линия С57В1/6). Селективность анксиолитического эффекта оценивали по степени совпадения диапазонов доз, оказывавших либо активирующее, либо ингибирующее действие у животных разных линий. Ранее подобный подход был с успехом применен для оценки степени селективности анксиолитического действия таких ныне известных препаратов, как феназепам [17] мексидол [18] и гидазепам [19]
В работе были использованы мыши-самцы линий Ва1Ь/с и С57В1/6 весом 20-22 г (питомник "Столбовая"). Животных содержали в условиях лабораторного вивария в клетках по 10 особей в каждой, в течение не менее двух недель до начала эксперимента, на стандартной диете, при свободном доступе к воде, при 12-ти часовом световом режиме (свет с 8.00 до 20.00). Все эксперименты проводили в период времени с 9.00 до 13.00. Все соединения вводили внутрибрюшинно в виде их водных растворов за 30 мин до начала эксперимента из расчета 0,1 мл раствора на 1О г веса животного. Через 30 минут после введения препаратов животное выдерживали в темноте в течение 1 минуты и затем помещали в один из периферических квадратов "открытого поля", которое представляет из себя белую круглую арену диаметром 1 м с белыми бортами высотой 50 см. Арена равномерно освещена 4-мя лампами по 75 Вт каждая, расположенными на высоте 1 м над поверхностью поля. Все пространство арены равномерно разделено 4-мя концентрическими окружностями, которые в свою очередь разбиты радиусами на сектора так, что периферическая окружность состоит из 16 одинаковых криволинейных квадратов. Наблюдение за животным производили в течение 3 минут, раздельно фиксировали число пересеченных квадратов на периферии, в центральных областях, число стоек и количество дефекаций. Суммарное число пересеченных квадратов вместе с числом стоек обозначали как общую активность. Статистическую обработку полученных результатов проводили используя t-критерий Стьюдента.
Испытанный в описанной экспериментальной системе наиболее близкий к заявляемым соединениям препарат бемитил продемонстрировал наличие транквилоактивирующего эффекта у мышей линии Ва1Ь/с в диапазоне доз от 0,1 мг/кг до 7,5 мг/кг. Седативное действие бемитила у мышей линии ВаlЬ/с развивалось в дозе 100 мг/кг, а у животных линии С57Вl/6 в дозе 50 мг/кг [16]
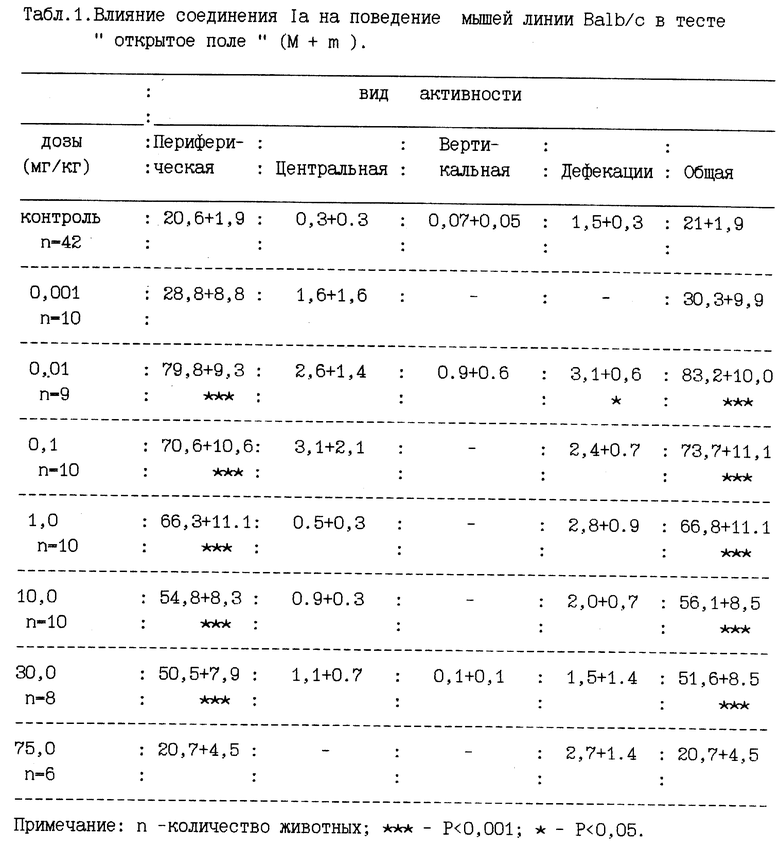
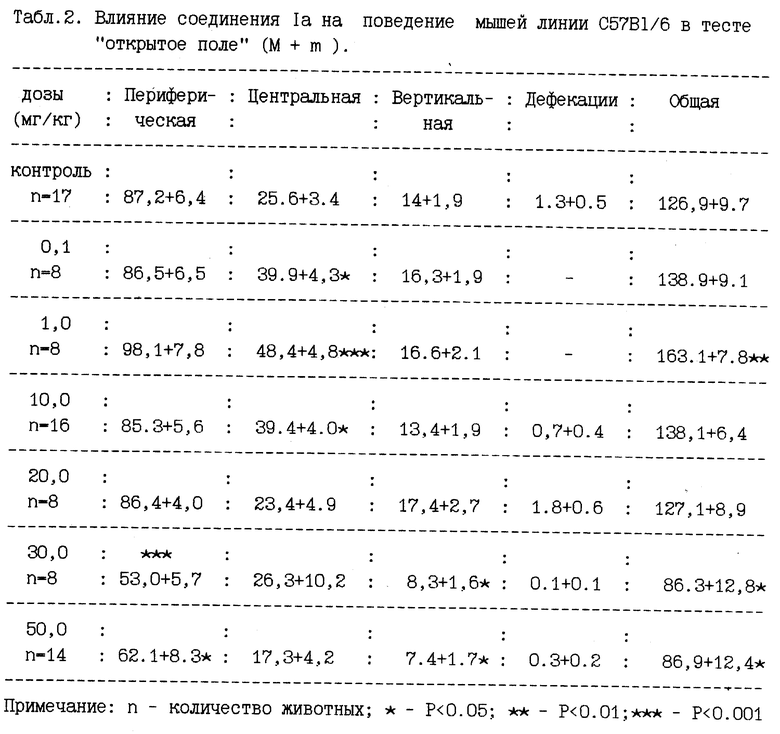
В табл. 1 представлены данные, демонстрирующие влияние соединения 1а на поведение мышей Ва1Ь/с. Показано, что в диапазоне доз от 0,01 мг/кг до 30 мг/кг это соединение повышало двигательную активность животных данной линии. В дозах 0,001 мг/кг и 75 мг/кг значения двигательной активности опытных животных не отличались от контрольных показателей. В широком диапазоне использованных доз (от 0,1 до 20,0 мг/кг) только в дозе 1,0 мг/кг выявлялась незначительная активация поведения мышей С57В1/б, тогда как в дозах 30 мг/кг и 50 мг/кг наблюдали заметное снижение двигательной активности животных этой линии (табл.2).
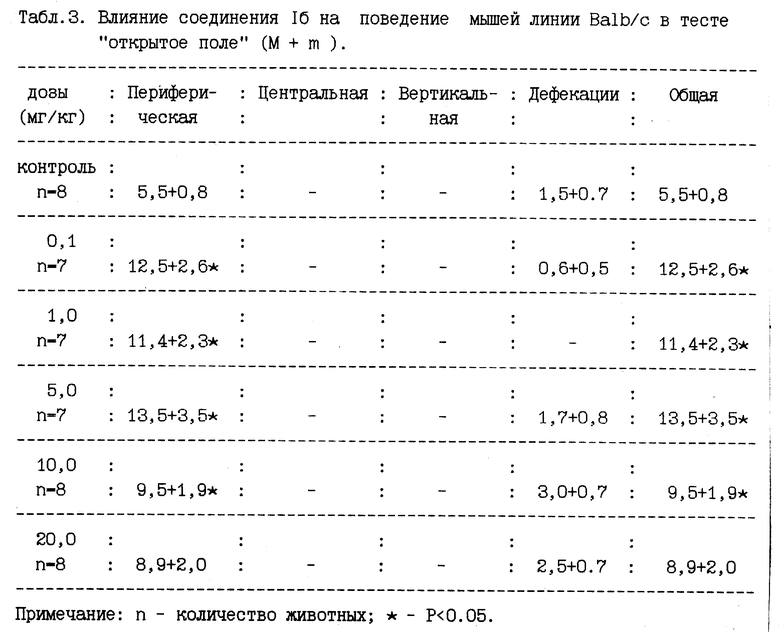
Результаты, представленные в табл.3, свидетельствуют о том, что соединение 1б в дозах 0,1, 1,0 и 5,0 мг/кг статистически достоверно повышало уровень двигательной активности мышей Bа1Ь/c в тесте "открытое поле". Поведение животных линии С57В1/6 оставалось неизменным при использовании этого соединения в дозах 1,0 и 10,О мг/кг (табл.4).
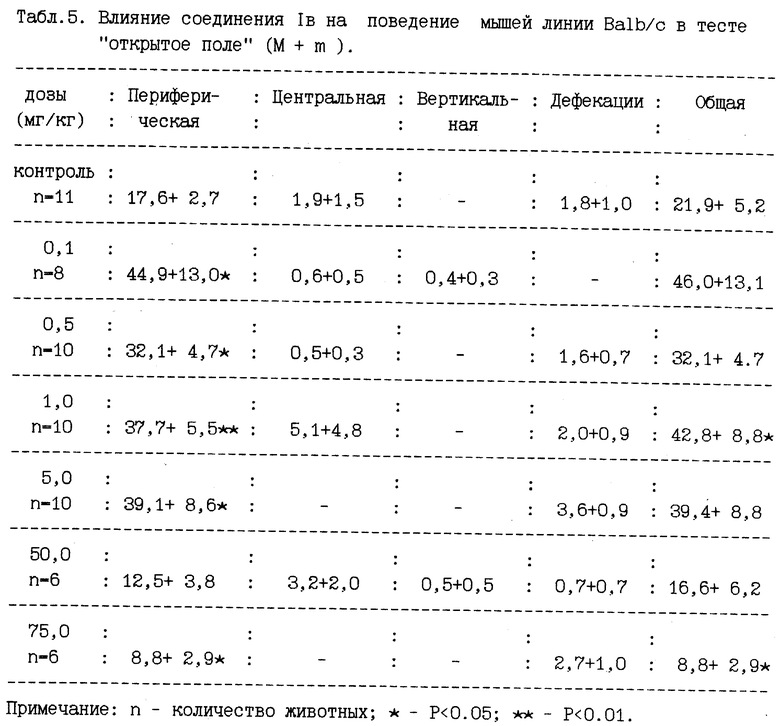
Соединение 1в, испытанное в диапазоне доз от О,1 до 75 мг/кг, в дозах 0,1, 0,5 и 5,0 мг/кг повышало периферическую двигательную активность, а в дозе 1,0 мг/кг и общую двигательную активность мышей линии Ва1Ь/с, тогда как в дозе 75.0 мг/кг наблюдался выраженный ингибирующий поведенческий эффект (табл. 5). У животных линии С57В1/6 не наблюдали изменения поведения ни в одной из использованных дозировок (1,0, 5,0 и 50,0 мг/кг) (табл.6).
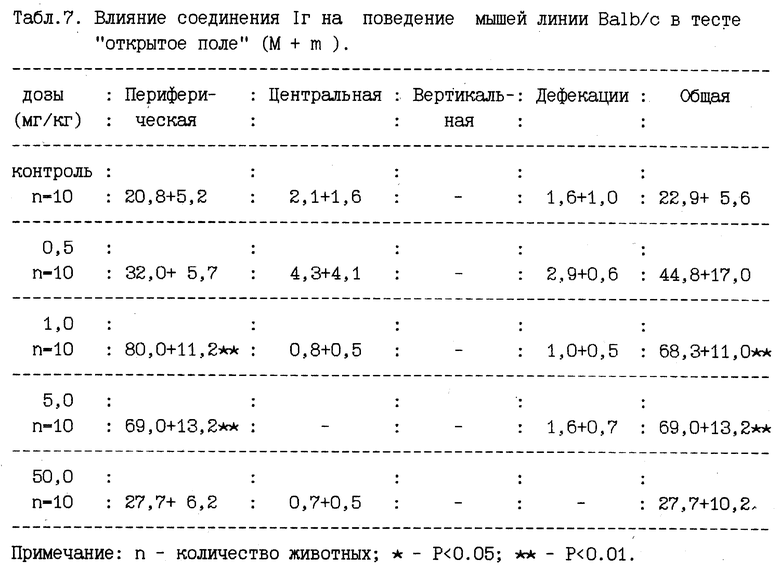
Данные, представленные в табл.7, показывают, что соединение 1 г повышает уровень двигательной активности мышей линии Ва1Ь/с лишь в дозах 1,0 и 5,0 мг/кг. Однако, ингибирующий двигательную активность эффект этого соединения у мышей линии С57В1/6 отсутствует в диапазоне доз от 1 до 50,0 мг/кг (табл. 8).
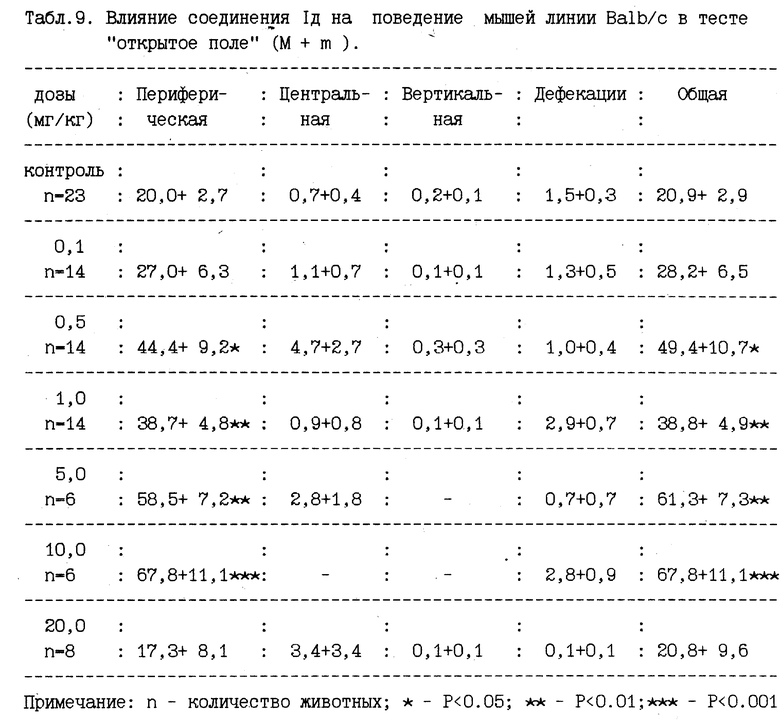
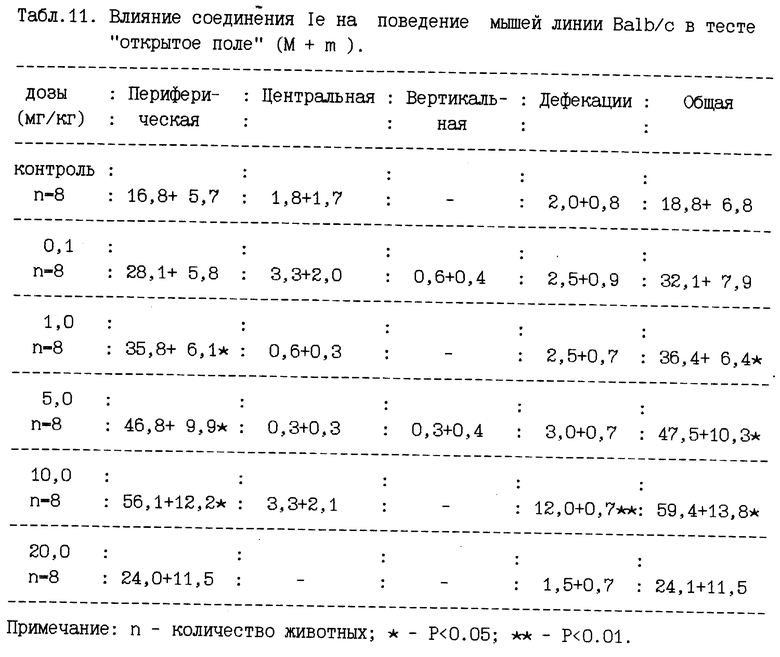
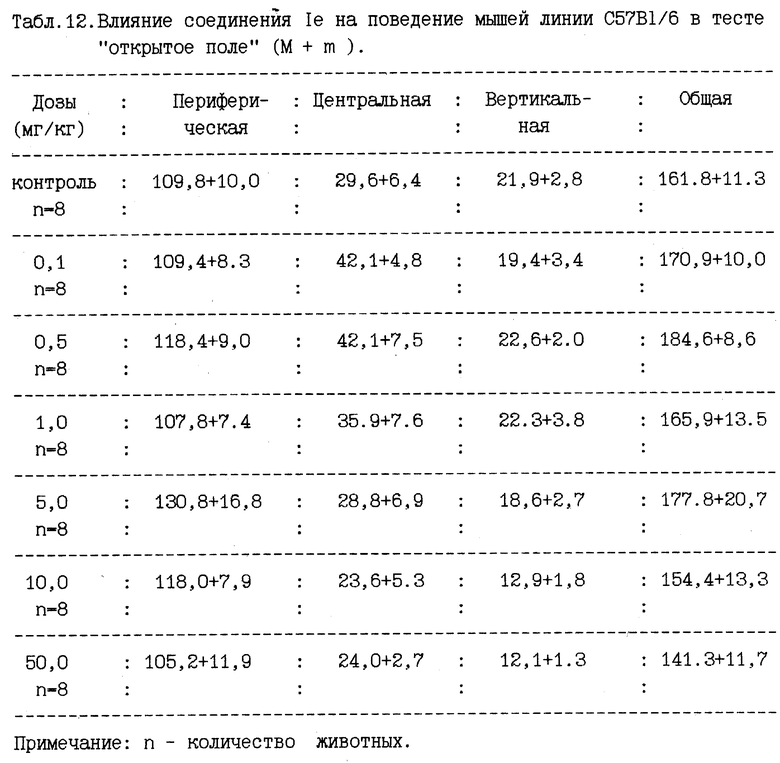
Соединение 1д, испытанное в диапазоне доз от 0,1 до 20 мг/кг, в дозах 0,5,1,0, 5,0 и 10,0 мг/кг активировало поведение мышей Ва1Ь/с (табл.9). В тоже время примененное в дозах 0,5, 5,0 и 10,0 мг/кг это соединение не изменяло поведение животных линии С57В1/6 (табл.10). Соединение 1е активировало поведение мышей линии Ва1Ь/с в дозах 1б0, 5,0 и 10,0 мг/кг, при его испытании в диапазоне доз от 0,1 до 20,0 мг/кг (табл.11). При испытании этого соединения у животных С57В1/б в диапазоне доз от 0,1 мг/кг до 50,0 мг/кг изменения поведения мышей данной линии не наблюдали (табл.12). Суммируя приведенные результаты, можно заключить, что все испытанные соединения в различных диапазонах доз оказывали оказывали выраженное анксиолитическое действие у животных с "пассивным" типом ЭСР (линия Ва1Ь/о). В тоже время все испытанные соединения либо вообще не обладали седативной активностью (линия С57В1/б), либо их седативные свойства проявлялись в дозах, значительно превышающих дозы, обладавшие анксиолитической активностью. Таким образом, можно констатировать наличие выраженного анксиоселективного действия в ряду 3-замещенных производных 2-меркаптобензимидазола.
Для дальнейшего более углубленного изучения транквилизирующего действия, а также оценки возможных побочных эффектов были отобраны 4 соединения, обладавшие наиболее выраженным анксиоселективным действием в первой серии экспериментов.
Изучение анксиолитического действия отобранных соединений проводилось в опытах на беспородных крысах-самцах весом 180-200 г в условиях общепринятой для этой цели методики столкновения питьевого и оборонительного рефлексов при действии внезапного болевого раздражителя как экстремального фактора [20] Эксперимент начинали с тренировки крыс с целью выработки у них чувства жажды и навыка взятия воды из поилки в экспериментальной камере. Для этого животных содержали на сухом корме в течение 24 часов и затем помещали в камеру, где они получали воду в течение 5 минут. Через сутки после тренировки крысе через 5 сек после начала питья наносили электрическое раздражение пропусканием тока (0,5 А) через поилку. Таким образом, столкновением двух рефлексов питьевого и оборонительного создавалась экстремальная ситуация, при которой страх получения болевого раздражения удерживал животное от взятия воды. В дальнейшем в течение 5 мин регистрировали количество взятий воды из поилки, несмотря на получение при этом каждый раз электроболевого раздражения.
Контрольные животные в создаваемой ситуации делали в среднем от 8 до 14 попыток наказуемых взятий воды из поилки (табл.13). Соединения 1а, 16, 1в и 1д в диапазоне доз от 1 до 20 мг/кг (в/бр) обладают отчетливым действием в создаваемой ситуации, устраняя чувство страха при действии болевого раздражителя, что интерпретируется как анксиолитический эффект. Это выражается в увеличении в 2-4 раза по сравнению с контролем числа наказуемых взятий воды из поилки. Таким образом, на основании проведенных экспериментов можно заключить, что соединения Iа, Iб, Iв и Iд характеризуются выраженным анксиолитическим действием в широком диапазоне доз.
Миорелаксантное действие отобранных соединений изучали на беспородных белых мышах-самцах весом 22-25 г по нарушению координации движений по общепринятому тесту вращающегося стержня [20] Мышей помещали на горизонтальный стержень диаметром 2 см при скорости его вращения 4 об/мин. Неспособность животных под влиянием введенных в/бр соединений удерживаться на стержне в течение 2-х минут рассматривали как проявление нарушения координации движений или как их миорелаксантное действие. Данные, представленные в табл.14 показывают, что соединение Iа в диапазоне доз от 0б01 до 50 мг/кг не оказывает влияния на измеряемый показатель. Отсутствие какого-либо эффекта демонстрируют также и соединения I6, Iв и Iд, испытанные в диапазоне доз от О,1 до 20 мг/кг. Таким образом, полученные в данной серии экспериментов данные показывают, что все испытанные соединения в использованных диапазонах доз не обладают миорелаксантной активностью.
Возможное снотворное действие отобранных соединений оценивали по методу потенцирования сна, вызываемого тиопенталом. Для этого белым беспородным мышам-самцам весом 20-25 г в/бр вводили тиопентал натрия в дозе 70 мг/кг и оценивали латентный период засыпания и общее время продолжительности сна. Испытуемые соединения вводили в/бр за 30 мин до введения тиопентала натрия. Данные, представленные в табл.15, демонстрируют, что все испытанные соединения не влияют на латентный период засыпания и не удлиняют продолжительность сна (табл.16). Напротив, соединение 1а в дозах 0,1 и 1,0 мг/кг достоверно укорачивают общее время сна, то есть оказывают активирующее пробуждающее действие. Сходным пробуждающим эффектом обладает и соединение Iд в дозах 1,0 мг/кг и 10,0 мг/кг (Табл.16). Кроме того, соединение Iа в дозе 1,0 мг/кг достоверно повышает латентный период засыпания животных (Табл.15).
Острая токсичность измерялась в опытах на белых беспородных мышах при пероральном введении испытуемых соединений в виде их суспензии в 1% растворе крахмала. Для соединения Iа величина LD50, рассчитанная по общепринятому методу Литчфильда-Уилкоксона, оказалась равной 1,16 г/кг (при 95% доверительном интервале 0,89 -1,48 г/кг) и близкой величине LD50 для известного препарата бемитила, который также является производным 2-меркаптобензимидазола. Таким образом можно заключить, что соединение 1а является практически нетоксичным.
На основании приведенных результатов можно заключить, что заявляемые соединения в широком диапазоне доз обладают выраженным анксиолитическим действием, которое не сопровождается побочными эффектами, свойственными широко применяемым в клинической практике транквилизаторам бензодиазепинового ряда
седативным, снотворным и миорелаксантным. ТТТ1 ТТТ2 ТТТ3 ТТТ4 ТТТ5 ТТТ6 ТТТ7 ТТТ8 ТТТ9 ТТТ10 ТТТ11 ТТТ12 ТТТ13 ТТТ14 ТТТ15 ТТТ16
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ 2-[2-(3-ОКСОМОРФОЛИН-4-ИЛ)ЭТИЛТИО]БЕНЗИМИДАЗОЛЫ, ОБЛАДАЮЩИЕ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2373202C2 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ПРОТИВОФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2136667C1 |
| СОЛИ 2-[2-(ДИЭТИЛАМИНО)ЭТИЛТИО] -5,6-ДИМЕТИЛБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИГИПОКСИЧЕСКОЙ И АНТИАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ И 2-[2-(ДИЭТИЛАМИНО)ЭТИЛТИО] -5,6-ДИМЕТИЛБЕНЗИМИДАЗОЛ В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА ДЛЯ СИНТЕЗА СОЛЕЙ 2-[2-(ДИЭТИЛАМИНО)ЭТИЛТИО] -5,6-ДИМЕТИЛБЕНЗИМИДАЗОЛА | 1991 |
|
RU2027709C1 |
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО | 1999 |
|
RU2175229C2 |
| ПРОИЗВОДНЫЕ 1,4-БЕНЗОДИАЗЕПИНА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2133248C1 |
| ПРОИЗВОДНЫЕ 4,6-ДИМЕТИЛ-2,3-ДИГИДРО-1Н-ПИРАЗОЛО[4,3-c]ПИРИДИН-3-ОНОВ И ЭФИРЫ 2,6-ДИМЕТИЛ-4-ФЕНИЛ-ГИДРАЗИНОНИКОТИНОВЫХ КИСЛОТ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ ДЛЯ ИХ СИНТЕЗА, ОБЛАДАЮЩИЕ АНТИДЕПРЕССАНТНОЙ И АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2394034C2 |
| АНКСИОЛИТИЧЕСКОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНКСИОЛИТИЧЕСКОГО ДЕЙСТВИЯ | 1999 |
|
RU2155065C1 |
| ПРОИЗВОДНЫЕ 1-(4-ФЕНИЛАЗОФЕНОКСИ)-3-АМИНОПРОПАНОЛА-2, ОБЛАДАЮЩИЕ ПОТЕНЦИАЛЬНОЙ СТРЕСС-ПРОТЕКТИВНОЙ АКТИВНОСТЬЮ | 1982 |
|
RU1031137C |
| Производные 2-аминометил-4,4-диметил-4 @ -1,3-бензтиазина в свободном виде или в виде кислотно-аддитивной соли,обладающие антидепрессивной активностью | 1979 |
|
SU770029A1 |
| ДИЦИКЛОГЕКСИЛАМИДЫ N-ЗАМЕЩЕННЫХ α-АМИНОКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ И АНТИФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2114821C1 |








Использование в качестве соединений, обладающих селективной анксиолитической активностью. Производные 2-меркаптобензимидазола, обладающие селективной анксиолитической активностью ф-лы, где n=0 2,3 R-аллил, диалкиламино или остаток моноциклического насыщенного амина, который может содержать дополнительный генератор R1 и R2 -H низший алкил алкокси или их фармацевтически приемлемые соли, получаемые алкилированием 2-меркаптобензимидазолов соответствующими алкилирующими агентами в водно-спиртовой среде в присутствии оснований. Структура соединения ф-лы 1: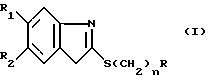
Производные 2-меркаптобензимидазола общей формулы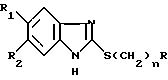
где n 0, 2, 3;
R аллил, диалкиламино или остаток моноциклического насыщенного амина, который может содержать дополнительный гетероатом;
R1 и R2 одинаковые или различные и означают водород, низший алкил, алкокси или их фармацевтически приемлемые соли,
обладающие селективной анксиолитической активностью.
| Машковский М.Д | |||
| Лекарственные средства.- М.: Медицина, 1993. |
Авторы
Даты
1996-06-10—Публикация
1994-06-10—Подача