Изобретение направлено на решение задачи усиления фотодинамического повреждения клеток-мишеней, относится к биотехнологии, может быть использовано в клеточной и молекулярной биологии, представляет интерес для разработки методов, которые могут быть использованы в экспериментальной медицине и фармакологии.
Основная схема применения фотодинамической терапии (ФДТ) состоит из введения в организм фотосенсибилизатора (ФС), который поглощается практически всеми клетками; затем вследствие различий в микроциркуляции, распределении, интенсивности обмена и т.п. ФС дольше задерживается в клетках-мишенях, например, в раковых клетках, нежели в нормальных тканях. Если в это время клетки-мишени и находящиеся в них молекулы ФС осветить, то свет вызовет фотохимические реакции, в результате которых клетки-мишени погибнут.
Основной побочный эффект ФДТ состоит в повышенной чувствительности кожи и глаз к свету: пациенты должны тщательно оберегаться от солнечного света в течение 6 недель и более. Другой побочный эффект состоит в тошноте и рвоте, вызываемыми у пациентов введением ФС в высоких дозах.
Очевидно, что оба этих побочных эффекта вызываны сочетанием двух причин: недостаточной селективностью ФС по отношению к клеткам-мишеням и избыточной концентрацией их в тканях пациента. Повышение специфичности ФДП может быть достигнуто за счет использования ФС в составе композиций.
В части изобретения, относящегося к объекту композиция, аналогом может служить композиция на основе микросфер (Dachor, R. Shea, C.R. and Hasan, T. Photosensitized destruction of human bkadder carcinoma cells treated with chlorin e -conjugated microspheres. Proc. Natl. Acad. Sci. USA, 88, 1580-1584, 1991 аналог композиции). Использование композиций фотосенсибилизатора с микросферами приводит к усилению фотодинамического повреждения (ФДП) клеток. Такие композиции неспецифически поступают в клетку путем фагоцитоза и могут попадать в лизосомы. Недостаток композиций с микросферами состоит в том, что фотодинамическое действие этих композиций не является специфичным по отношению к типу клеток.
Другим аналогом композиции может служить композиция хлорина е с моноклональными антителами [1] К недостаткам такой композиции можно отнести то, что она способна действовать только на поверхность клетки-мишени, и вызываемое ею ФДП не затрагивает наиболее чувствительные к ФДП компартменты клеток-мишеней.
Этого недостатка лишена композиция из фотосенсибилизатора, компонента-носителя фотосенсибилизатора, а также компонента для узнавания клеток-мишеней и транспорта фотосенсибилизатора внутрь клеток-мишеней путем специфического рецептор-опосредуемого эндоцитоза, которая является прототипом изобретения [3] Композиция инсулин-БСА-хлорин, описанная в [3] после связывания со специфическими рецепторами на поверхности клеток-мишеней способна к рецепторопосредуемому эндоцитозу и, соответственно. к транспорту внутрь клеток, где и происходит после облучения клеток процесс генерации активных форм кислорода, которые являются действующим началом при ФДП клеток. Прототип обладает преимуществом по сравнению с композицией с моноклональными антителами или композицией с микросферами. Композиция при наличии специфического связывания с поверхностными клеточными рецепторами, присущими для данного типа клеток, способна к интернализации путем рецептор-опосредуемого эндоцитоза, вследствие чего образование активных продуктов фотоокисления происходит внутри клетки вблизи от чувствительных к повреждению компартментов клеток. Недостатком композиции является отсутствие какого-либо специального компонента для направленного транспорта внутри клеток-мишеней, например, для транспорта ФС в наиболее чувствительные к фотоповреждению компартменты клеток или для транспорта из менее чувствительных компартментов. В результате не происходит эффективного транспорта в эти компартменты и ФДП оказывается не таким сильным, как могло бы быть при наличии компонента для направленного транспорта внутри клеток.
Технический результат, достигаемый изобретением, состоит в создании композиций, которые способны производить ФДП клеток-мишеней в низких концентрациях, за счет того, что в составе композиции помимо ФС, носителя фотосенсибилизатора и компонента для узнавания клеток-мишеней и рецептор-опосредуемого эндоцитоза, имеется также компонент, обладающий способностью направленного транспорта ФС внутри клеток-мишеней, что благодаря доставке ФС в наиболее чувствительные к ФДП компартменты приводит к усилению ФДП.
Предлагаемые композиции имеют в своем составе ФС,компонент-носитель фотосенсибилизатора, компонент для узнавания клеток-мишеней и рецептор-опосредуемого эндоцитоза в них и компонент для направленного транспорта ФС внутри клеток-мишеней, например, для транспорта в наиболее чувствительные к ФДП компартменты этих клеток. Для достижения указанного технического результата в составе композиции имеется ФС-компонент, повреждающий клетки при фотоактивации, носитель ФС-компонент, необходимый для прикрепления ФС и других компонентов, компонент для узнавания и связывания композиций с поверхностью клеток-мишеней и доставки композиций внутрь клеток-мишеней путем рецептор-опосредуемого эндоцитоза, компонент для направленного транспорта ФС внутри клеток-мишеней. Отдельные компоненты, составляющие композиции, могут быть объединены между собой ковалентно и/или находиться в механической смеси. В качестве компонентов направленного внутриклеточного транспорта могут быть использованы вещества, способные транспортировать композицию или ее компоненты в ядро. Из компонентов, обладающих способностью для транспорта в ядро, могут быть использованы гормоны, белки и пептиды, имеющие аминокислотную последовательность ядерной локализации (кариофильную последовательность), а также эндосомолитические компоненты, которые способны высвобождать композиции и ФС из эндосом например, некоторые вирусы эндосомолитические амфипатические пептиды), что делает возможным более эффективный транспорт в один из наиболее чувствительных к ФДП компартментов клетки ядро. Другим чувствительным компартментом объектом для направленного транспорта внутри клетки-мишени могут служить, например, лизосомы. В качестве компонентов-носителей ФС могут быть использованы различные полимеры, например, белки, в том числе рекомбинантные полипептиды. Как компоненты для узнавания клеток-мишеней (связывания с ними) и транспорта ФС внутрь леток путем рецептор-опосредуемого эндоцитоза могут быть использованы эндоцитируемые лиганды,в частности пептидные гормоны (инсулин, сопатотропин, пролактин и т. д.), лектины (конканавалин А, рицин, лектин из проростков пшеницы и т.д.), другие белковые (трансферрин, ферритин), и небелковые (сахара, низкомолекулярные гормоны) компоненты. В качестве ФС могут быть использованы различные молекулы, способные при облучении светом генерировать активные формы кислорода (порфирины, фталоцианины и т.д.).
Существует ряд возможных типов конструкций, укладывающихся в изложенную выше схему. Для направленной доставки ФС в ядра эукариотических клеток была использована композиция, состоящая из следующих компонентов: ФС хлорина е6, компонента-носителя бычьего сывороточного альбумина, компонента для узнавания клеток мишеней и транспорта ФС путем рецептор-опосредуемого эндоцитоза эндоцитируемого лиганда пептидного гормона инсулина и компонента обладающего способностью направленного транспорта внутри клеток-мишеней - кариофильной последовательности большого Т-антигена вируса SV-40, обеспечивающей направленный внутриклеточный транспорт композиции в ядро. Данная композиция имеет следующую структуру: на белок-носитель БСА были последовательно ковалентно присоединены хлорин е6, кариофильная последовательность и инсулин.
В состав данной композиции входит синтезированная химическим путем кариофильная последовательность большого Т-антигена вируса SV-40 (пептид РI 101). Пептид РI 101 включает в себя кариофильную последовательность: NH2-Tyr-Gly-Val-Lys-Arg-Lys-Lys7-Lys-Pro-Pro-Ala-Ala-His- Gln-Ala-Asp-Ala-Ala-Ala-Glu-Asp-Asp-Ser-Gly-Pro-Gly-Cys.
Следующая композиция имеет сходный состав, но роль белка-носителя здесь выполняет β-галактозидаза из E. coli. Данная композиция была приготовлена следующим образом: был получен химерный белок Р10, в котором белок-носитель ((β-галактозидаза) слит с компонентом, обладающим способностью к направленному транспорту в ядро, а именно с кариофильной последовательностью большого Т-антигена вируса SV-40; галактозидазная часть белка Р10 выполняет роль носителя и обеспечивает внутриклеточный транспорт композиции в ядра клеток-мишеней; к этому рекомбинантному белку были ковалентно присоединены ФС хлорин е 6 и инсулин. Для данной композиции было показано, что присутствие в ее составе кариофильной последовательности приводит к существенному усилению ФДП клеток-мишеней. Но даже такая композиция не способна полностью транспортироваться в ядра клеток, т.к. в ее составе находится инсулин и поэтому такая композиция после интернализации в клетку-мишень путем рецептор-опосредуемого эндоцитоза оказывается заключенной в эндосомы. Для выхода композиции из эндосомных везикул необходимо включить в ее состав еще один компонент направленного транспорта ФС внутри клеток-мишеней, а именно компонент, обеспечивающий выход композиции из эндосом.
В результате исследований последних лет была доказана обнаруженная более 10 лет назад возможность разрушения эндоцитозных везикул (например, эндосом) с помощью аденовирусов. В состав следующей композиции введен эндосомолитический компонент нереплицирующийся мутантный тип вируса, который обеспечивает выход композиций из эндосом (аденовирус человека, серотип 5, штамм dl-312). Последующий внутриклеточный транспорт ФС в ядра осуществляется за счет того, что в составе композиции находится кариофильная последовательность (находящаяся в составе белка Р10).
В части изобретения, относящейся к объекту "способ фотодинамического повреждения" известен ряд аналогов способа ФДП клеток-мишеней.
Усиление ФДП клеток-мишеней при снижении действующей концентрации ФС возможно путем использования производных ФС, имеющих другие места локализации в клетке, более чувствительные к фотодинамическому действию. Известен, например, способ ФДП путем использования производных ФС, проникающих в клетку при помощи неспецифического эндоцитоза и обнаруживаемых в мембранных компонентах и лизосомах [2] К усилению ФДП приводит использование конъюгатов ФС с микросферами, которые неспецифически поступают в клетку путем фагоцитоза и также проникают в лизосомы. Оба эти способа имеют один и тот же недостаток: ФС и их производные могут накапливаться как в клетках-мишенях, так и в нормальных клетках, т.е. являются неспецифичными по отношению к типу клеток.
Повышение специфичности ФДТ может быть достигнуто путем конъюгации ФС с лигандом, имеющим специфические рецепторы на поверхности клеток-мишеней. Для этой цели были предложены композиции ФС с моноклональными антителами к этим клеткам. Такой подход позволяет увеличить селективность и эффективность ФДТ за счет специфического узнавания клеток-мишеней и связывания композиций с их поверхностью.
Еще одним аналогом способа ФДП клеток-мишеней является способ усиления ФДП клеток-мишеней при помощи использования композиций ФС хлорина е6 с моноклональными антителами [1]
В указанном аналоге композицию, содержащую ФС, добавляют к клеткам-мишеням, выдерживают с ними, и затем облучают светом. В результате за счет свойств композиции ФС направленно доставляют к клеткам в составе композиции, которая связывается со специфическими клеточными рецепторами. При таком способе основной мишенью ФС являются плазматические мембраны клеток. Последнее не является оптимальным, поскольку ФДП не распространяется на значительно более чувствительные внутриклеточные мишени ядро или лизосомы.
Такого недостатка лишен способ ФДП предлагаемый в [3] Данный способ обладает тем недостатком, что после поглощения ФС клеткам он за счет свойств применяемой композиции следует тем путем, который предопределен свойствами лиганда компонента для узнавания и рецептор-опосредуемого эндоцитоза клеток. При этом он не обязательно попадает (или попадает в незначительной мере) в другие чувствительные к ФДП части клетки.
Технический результат, достигаемый изобретением в части объекта "способ", состоит в повышении безопасности и экономичности способа, в усилении ФДП клеток-мишеней за счет использования композиции, способной направленно переносить ФС внутри клеток-мишеней.
Предлагаемый способ усиления ФДП включает в себя внесение ФС к клеткам в составе композиции, способной направленно переносить ФС внутри клеток-мишеней, выдерживание их при температуре нормальной жизнедеятельности клеток с последующим их облучением светом.
В результате такого применения композиции происходит направленная доставка ФС к клеткам-мишеням,его связывание со специфическими рецепторами на клетках-мишенях, затем перенос ФС внутрь клеток-мишеней посредством рецептор-опосредуемого эндоцитоза, транспорт ФС в наиболее чувствительные к ФДП компартменты клеток, после чего фотоактивация ФС наиболее эффективна. В качестве чувствительных компартментов используют ядра. Для достижения указанного технического результата в способе ФДП клеток-мишеней используют такие композиции, в составе которых есть ФС, компонент-носитель ФС, компонент для узнавания клеток-мишеней и транспорта внутрь клетки-мишени путем рецептор-опосредуемого эндоцитоза и компонент, обладающий способностью направленного транспорта внутри клеток-мишеней. В способе фотодинамического повреждения клеток-мишеней используются композиции, обладающие способностью направленного транспорта в ядро клетки и композиции обладающие также способностью высвобождаться ФС из эндоцитозных компартментов.
Изобретение решает задачу усиления ФДП клеток-мишеней. При решении этой задачи учитывается, что фотодинамический эффект подавляющего большинства ФС (порфиринов, фталоцианинов) обусловлен генерацией активных форм кислорода (синглетного кислорода, некоторых кислородных свободных радикалов и т.д.), которые и являются собственно токсическими агентами. Средний пробег активных форм кислорода в клетке не превышает сотых долей микрона, вследствие этого основной мишенью для ФС становятся клеточные мембраны, где, как показано и локализуется ФС. Усиление ФДП при снижении действующей концентрации достигается использованием ФС в составе композиции, в которой имеются компоненты, обеспечивающие направленный транспорт ФС в наиболее чувствительные к ФДП компартменты клеток-мишеней, повреждение которых критично для клетки. Доставка ФС в чувствительные к ФДП компартменты клеток-мишеней осуществляется после того, как ФС в составе композиции будет связан с клеткой-мишенью и затем поглощен ею. Для получения композиций, которые бы могли связываться со специфическими рецепторами клеток-мишеней и затем путем рецептор-опосредуемого эндоцитоза доставляться в клетки-мишени, проведена конъюгация ФС с лигандом, имеющим такие рецепторы на поверхности клеток-мишеней. Такие лиганды, как, например, инсулин, соматотропин и многие другие, после связывания со своими рецепторами на поверхности клеток проникают внутрь клеток путем рецептор-опосредуемого эндоцитоза, после чего можно осуществить направленный внутриклеточный транспорт комплекса композиция-рецептор в наиболее чувствительные компартменты клеток. Если к лиганду, который проникает в клетку путем рецептор-опосредуемого эндоцитоза, присоединить компонент для направленного транспорта, то можно за счет направленной доставки заменить внутриклеточную локализацию ФС, доставить ФС в более чувствительные компартменты клеток, что позволяет снизить действующую концентрацию ФС. Использование композиций позволяет также объединить несколько молекул ФС вместе, что может усиливать локальное действие вещества в местах поражения после направленной внутриклеточной доставки.
Способ фотодинамического повреждения клеток-мишеней с использованием композиций для усиления фотодинамического повреждения клеток-мишеней осуществляется следующим образом. Синтезируют компоненты композиции, приготовляют композицию применительно к избранному типу клеток-мишеней, вносят композицию к объекту, содержащему клетки-мишени для ФДП, выдерживают при температуре нормальной жизнедеятельности клеток, и активируют ФС светом.
Ниже приведен перечень иллюстраций к способу ФДП клеток-мишеней путем направленной внутриклеточной доставки ФС и композиции для ФДП клеток-мишеней путем направленной внутриклеточной доставки ФС.
Фиг. 1. Зависимость выживаемости клеток гепатомы человека PLC/PRF/5 от концентраций композиций (Р10)-инсулин(хлорин е6), (β-галактозидаза)-инсулин-(хлорин е6), и хлорина е6 при дозе облучения 12,3 кДж/м2. А (Р10)-инсулин-(хлорин е6); В - (β-галактозидаза)-инсулин-(хлорин е6); С хлорин е6.
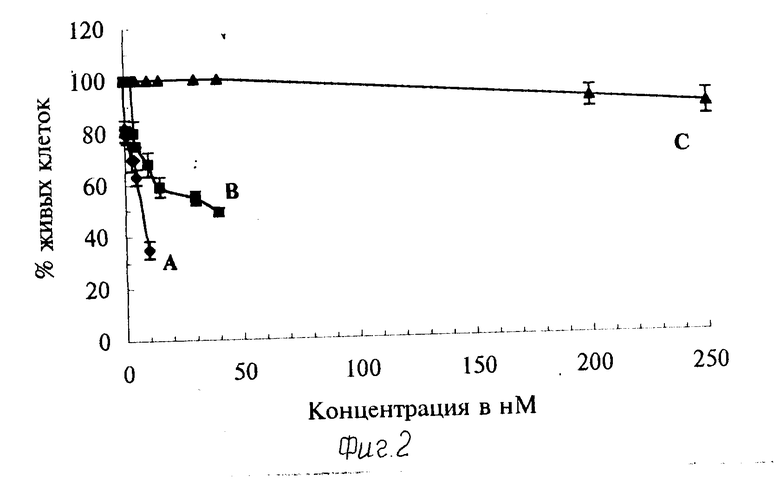
Фиг. 2. Зависимость выживаемости клеток гепатомы человека PLC/PRF/5 от концентраций композиций (Р10)-инсулин(хлорин е6), (β-галактозидаза)-инсулин-(хлорин е6), и хлорина е при дозе облучения 96 кДж/м6. А (Р10)-инсулин-(хлорин е6); В (β- галактозидаза)-инсулин-(хлорин e6); С-хлорин е6.
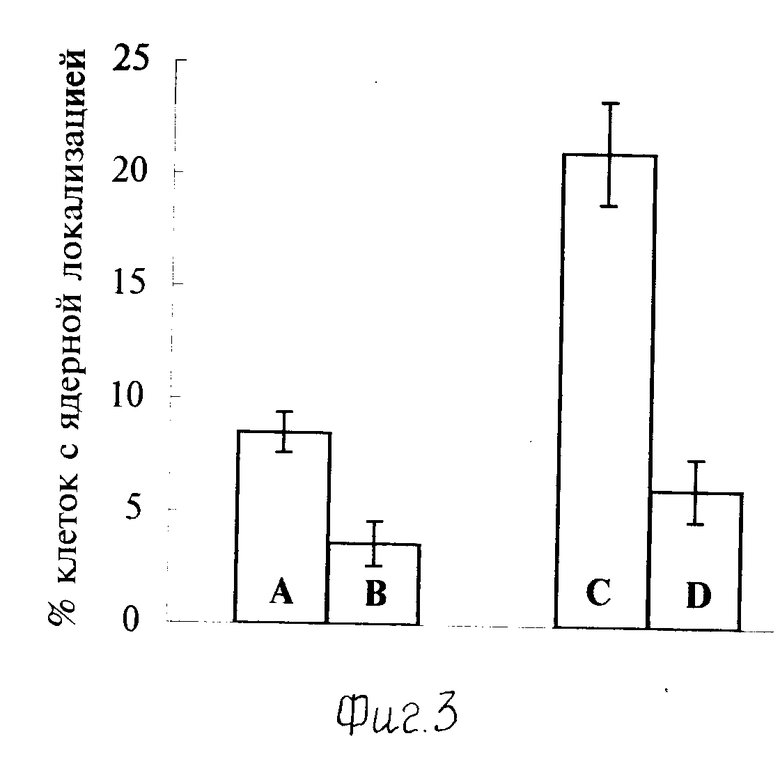
Фиг.3. Сравнение локализации активных форм кислорода после фотоактивации композиций в клетках гепатомы человека PLC/PRF/5. А (Р10)-инсулин-(хлорин е ), В (β-галактозидаза)-инсулин-(хлорин е6). С - (Р10)-инсулин-(хлорин е6)+ (аденовирус человека серотипа 5, штамм dl-312), D (βгалактозидаза)-инсулин-(хлорин-е6) + (аденовирус человека серотипа к, штамм dl-312). Локализацию определяли по образованию 2',7'-дихлорфлуоресцеина. Возможность осуществления способа фотодинамического повреждения клеток-мишеней с использованием композиции для фотодинамического повреждения клеток-мишеней фотосенсибилизатора подтверждается следующими примерами.
Пример 1. Синтез композиции (БСА)-(хлорин е6)- (РI 101)-инсулин.
Стадия 1. Получение хлорина е6.
Хлорин е6 получали из листьев крапивы (Urtica dioica L.) по стандартному методу Фишера с модификациями.
Стадия 2. Синтез конъюгата (БСА)-(хлорин е6).
Конъюгацию БСА с хлорином е6 проводили в Na-фосфатном буфере (10 мМ, рН 7,5) с помощью циклогексил-3(2- морфолиноэтил)карбодиимид мето-4-толуенсульфоната (КДИ) (Serva). Соотношение (БСА):(хлорин е6):(КДИ) было равно 1: 30: 300. Реакция проходила при 4oС в течение 18 ч. После этого проводили диализ против того же буфера.
Стадия 3. Активирование конъюгата (БСА)-(хлорин е6) 3-малеимидобензоилгидроксисукцинимидным эфиром (МБС).
Для активирования NH -групп БСА для дальнейшей конъюгации проводили реакцию с МБС (Sigma). Реакцию проводили в том же Na-фосфатном буфере при соотношении (БСА): (МСБ) равном 1:100. МБС разводили в диметилформамиде и добавляли к конъюгату (БСА)-(хлорин е6). Смесь оставляли на 1 ч при комнатной температуре и затем избыток МБС удаляли диализом против Na-фосфатного буфера (10 мМ, рН 7,5; 0,5 мМ ЭДТА).
Стадия 4. Синтез композиции (БСА)-(хлорин е6)-(РI 101).
Пептид РI 101 содержит на С-конце цистеин, через SH- группу которого можно проводить конъюгацию пептида с активированными МБС аминогруппами БСА. При смешивании пептида с активированным МБС конъюгатом (БСА)-)-(хлорин е6) в анаэробных условиях (соотношение (БСА)-(хлорин е6) и пептид равно 1:30), происходит ковалентное присоединение пептида к БСА. Реакцию проводили 3 ч при комнатной температуре, после чего избыток пептида удаляли диализом против Na-фосфатного буфера (10 мМ, рН 7,5; 0,5 мМ ЭДТА).
Стадия 5. Активирование инсулина с помощью сульфосукцинимидил 4-(малеимидометил)циклогексан-1-карбоксилата (сульфо-СМЦК).
Инсулин и сульфо-СМЦК (Pirce) разводили в Na-фосфатном буфере (10 мМ, рН 7,5) и смешивали в соотношении 1:1,5. Реакция проходила при 37oС в течение 30 мин. Затем проводили диализ против Na-фосфатного буфера (10 мМ, рН 7,5; 0,5 мМ ЭДТА).
Стадия 6. Восстановление SH-групп БСА с помощью дитиотреитола (ДТТ).
К конъюгату (БСА)-(хлорин е6)-(РI 101) добавляли ДТТ (Sigma) до конечной концентрации 50 мМ и инкубировали при 37 С 30 мин, затем диализовали против Na-фосфатного буфера (10 мМ, рН 7,5; 0,5 мМ ЭДТА).
Стадия 7. Получение композиции (БСА)-(хлорин е6) РI 101)-инсулин.
Полученные после стадий 4 и 5 соответственно инсулин и (БСА)-(хлорин е6) (РI 101) смешивали в анаэробных условиях в соотношениях 15:1. Инкубацию проводили в течение 18 ч при 4oС. Затем композицию очищали колоночной хроматографией на сефакриле S-300, элюцию проводили в 25 мМ Hepes, рН 7,5; 50 мМ NaCl.
После всех стадий конъюгации проводили электрофорез в полиакриламидном геле по методу Лэммли для определения молекулярных масс полученной композиции.
Пример 2. Определение локализации композиции (БСА)-(хлорин е6)-(РI 101)-инсулин в клетках гепатому человека PLC/PRF/5.
Для выявления локализации композиции (БСА)-(хлорин е6)-(РI 101)-инсулин в клетках использовали 2',7'-дихлорфлуоресциндиацетат. При инкубации этого вещества с клетками при 37oС оно проникает внутрь клеток и там дезацетилируется внутриклеточными эстеразами. Если в месте нахождения образовавшегося 2', 7'-дихлорфлуоресцина происходит образование активных форм кислорода, то 2', 7'-дихлорфлуоресцин, взаимодействуя с ними, превращается во флуоресцирующий 2',7'-дихлорфлуоресцеин. Поскольку известно,что пробег активных форм кислорода очень мал, то места локализации композиции совпадают с местами генерируемых ей активных форм кислорода после облучения клеток и, таким образом, в присутствии 2',7'-дихлорфлуоресциндиацетата можно выявлять как место нахождения композиции в клетке, так и место генерации именно тех токсических продуктов, которыми и обусловливается ФДП, вызываемое ФС. Клетки гепатомы человека PLC/PRF/5 инкубировали со 100 нМ композицией (БСА)-(хлорин е6)-(РI 101-инсулин в течение 18 ч при 37oС в среде RPMI-1640, содержащей 2 мг/мл БСА, 25 мМ Hepes, рН 7,5. После окончания инкубации клетки промывали той же средой, инкубировали 5 мин с 2,5 мкМ 2',7'-дихлорфлуоресциндиацетата, отмывали от него и освещали слайд-проектором, распределение флуоресценции в клетках фиксировали с помощью видеокамеры АТ-200 (Photometrics) c охлаждаемой ПЗС-матрицей. Как видно из фиг.1 композиция (БСА)-(хлорин е6)-(РI 101)-инсулин значительно более эффективно проникает в клетку и в ядра клеток, чем композиция (БСА)-(хлорин е6)-(РI 101Т)-инсулин (пептид РI 101Т отличается от пептида РI 101 тем, что Lys7 был заменен на Thr7), причем доставка композиций в клетку осуществляется через инсулиновые рецепторы, что доказывается отсутствием флуоресценции в клетках при одновременной инкубации их с композицией и со 100-кратным избытком свободного инсулина.
Пример 3. Синтез композиции (Р10)-инсулин-(хлорин е6).
В качестве белка-носителя для создания данной композиции был использован рекомбинантный белок Р10. Белок Р10 представляет собой продукт химерного гена, в котором к последовательности, кодирующей бактериальный белок b-галактозидазу из E.coli, была присоединена кариофильная последовательность большого Т-антигена вируса SV40. В качестве контроля использовалась бактериальная β-галактозидаза.
Стадия 1. Выделение белков Р10 и β-галактозидазы.
Для получения химерного белка Р10 и β-галактозидазы использовали соответственно плазмиды рDJ87 и pDJ148, экспрессирующиеся в клетках Е.coli.
Для каждого белка соответствующую культуру E.coli наращивали в LB-бульоне (Sigma) с Na-ампициллином и изопропил-β-тиогалактозидом (СибЭнзим) в качестве индуктора экспрессии белка. После центрифугирования бактериальной массы и лизиса ультразвуком суспензию вновь центрифугировали и супернатант наносили на аффинную колонку, где в качестве сорбента использовался р-аминобензил 1-тио-β-D-галактопиранозид (Sigma). После промывки колонки буфером с 20 мМ трис-НСL, рН 7,4; 10 Мм МgCl2, 1,6 М NaCl (Sigma), 10 мМ 2-меркаптоэтанола (для удаления примесей других белков), выделяемый белок элюировали боратным буфером (0,1 М, рН 10,05; 10 мМ 2-меркаптоэтанол). Присутствие белка во фракциях определяли по цветной реакции с о-нитрофенил-β-D-галактопиранозидом (Sigma). После диализа в фосфатном буфере (10 мМ, рН 7,0; 10 мМ 2-меркаптоэтанол) белок концентрировали ультрафильтрацией. Концентрацию белка определяли по поглощению при 280 нм.
Стадия 2. Получение хлорина е6.
Хлорин е6 получали как в примере 1.
Стадия 3. Получение аминохлорина.
К хлорину е6 добавляли КДИ и диаминогексан (Sigma) в 5 мМ Na-фосфатном буфере, рН 7,5. Соотношение концентраций (хлорин е6) (КДИ) диаминогексан в реакционной смеси составляло 1:100:100. Реакция проходила при 4oС в течение ночи. затем избыток КДИ и диаминогексана удаляли диализом в Na-фосфатном буфере (10 мМ, рН 7,0).
Стадия 4. Получение цитраконированного инсулина.
Для получения конъюгатов с лигандом, имеющим специфические интернализуемые рецепторы, использовали инсулин, модифицированный цитракониевым ангидридом. Взаимодействие инсулина с цитракониевым ангидридом приводит к защите концевых аминогрупп инсулина, которые участвуют во взаимодействии с рецепторами, поэтому при дальнейшей модификации инсулина после цитраконирования участвуют аминогруппы лизинов, находящиеся в середине полипептидной цепи. Модификацию инсулина цитракониевым ангидридом проводили по методу Шектера [2]
Стадия 5. Синтез конъюгатов (Р10)-(хлорин е6) и (β-галактозидаза)-(хлорин е6).
Для конъюгации белков с аминохлорином е также использовали КДИ. Реакцию проводили в Na-фосфатном буфере (10 мМ, рН 7,0) при концентрационном соотношении белок: (аминохлорин е6):(КДИ) равном 1:30:300. Конъюгаты очищали от несвязавшегося аминохлорина е6 и избытка КДИ диализом.
Стадия 6. Синтез композиций (Р10)-инсулин-(хлорин е6) и (β-галактозидаза)-инсулин-(хлорин е6).
Модифицированный цитраконильными группами инсулин был ковалентно присоединен к конъюгатам (Р10)-(хлорин е6) и (β-галактозидаза)-(хлорин е6) с помощью бифункционального сшивающего реагента сукцинимидил 3-(2-пиридилдитио)пропионата (СПДП) (Sigma) по схеме Юнга. Инсулин был взят в концентрации, в 15 раз превышающей концентрацию конъюгата по белку. После инкубации и диализа в Na-фосфатном буфере (10 мМ, рН 7,0) цитраконильные группы снимали закислением и последующим защелачиванием композиций. Затем композиции очищали диализом в Na-фосфатном буфере (10 мМ. рН 7,0).
Для определения числа присоединившихся молекул инсулина на молекулу композиции проводили электрофорез композиций в 5% ПААГ по методу Лэммли. Полученное соотношение белок:(хлорин е6): инсулин в композициях было равно 1: 5:8.
Пример 4. ФДП клеток гепатомы человека PLC/PRF/5 композицией (Р10)-инсулин-(хлорин е6).
Использование композиции на клетках гепатомы человека показало, что наличие в составе композиции последовательности, обеспечивающий транспорт композиции в ядро, значительно усиливало фотодинамическое действие хлорина е6, входящего в состав этой композиции. При дозе облучения 12,3 кДж/м2 для композиции (Р10)-инсулин-(хлорин е6) концентрация полумаксимального эффекта ЕС50 была равна 17 нМ, для контрольной композиции (β-галактозидаза)-инсулин-(хлорин е6) ЕС50 была равна 319 нМ и для свободного хлорина е6 ЕС50 была равна 11500 нМ. При дозе облучения 96 кДж/м2 для композиции (Р10)-инсулин-(хлорин е6) ЕС50 была равна 7,2 нМ6 Для композиции (β--галактозидаза)- инсулин-(хлорин е6) ЕС50 была равна 38 нМ, для хлорина е6 ЕС50 была равна 350 нМ. Зависимость выживаемости клеток гепатомы человека PLC/PRF/5 концентрации композиций и хлорина е6 представлены на фиг. 2 и 3.
Пример 5. Способ получения композиции (Р10)- инсулин-(хлорин е6) + эндосомолитический компонент (аденовирус) и композиции (β-галактозидаза)-инсулин-(хлорин е6) + эндосомолитический компонент (аденовирус).
Для освобождения композиций из внутриклеточных эндосом и выхода в цитозоль мы использовали аденовирус человека Аd5 dl-312. Для этого клетки инкубировали с композицией (Р10)-инсулин-(хлорин е6) или (β-галактозидаза)-инсулин-(хлорин е6) совместно с аденовирусом. На вторые сутки после посева клетки отмывали средой RPMI-1640, содержащей 2 мг/мл БСА, 25 мМ Нереs, рН 7,5 и инкубировали с композициями или с композициями в присутствии вируса. Концентрация композиций в среде инкубации составляла 20 нМ, аденовируса 3,66 х 1010 вир.ч./мл (0,0366 опт.ед. при 260 нМ). В экспериментах с аденовирусом проводили предварительную инкубацию при 4oС в течение 1 ч для обеспечения эффективного связывания вируса и композиций со своими рецепторами и последующего одновременного начала цикла интернализации рецепторов инсулина и аденовируса после перенесения клеток на 37oС. После 18-часовой инкубации при 37oС клетки отмывали той же средой.
Пример 6. Локализация композиций (Р10)-инсулин(хлорин е6) + эндосомолитический компонент (аденовирус) и (β-галактозидаза)-инсулин-(хлорин е6) + эндосомолитический компонент (аденовирус) в клетках гепатомы человека PLC/PRF/5. При инкубации клеток гепатомы человека PLC/PRF/5 с композицией (Р10)-инсулин-(хлорин е6) в присутствии аденовируса Аd5 dl-312 количество клеток с преимущественной локализацией композиции в ядре увеличивалось на 148% что было в 3,5 раза больше, чем для композиции (β-галактозидаза)-инсулин-(хлорин е6) (Фиг.4).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ЖИВОТНЫХ | 1996 |
|
RU2108714C1 |
| СПОСОБ НАПРАВЛЕННОЙ ГЕНЕТИЧЕСКОЙ ТРАНСФОРМАЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ ЖИВОТНОГО И УСТРОЙСТВО ДЛЯ ВВЕДЕНИЯ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА В МОЛОЧНЫЙ ПРОТОК МОЛОЧНОЙ ЖЕЛЕЗЫ ЖИВОТНОГО | 1993 |
|
RU2025487C1 |
| ЦИТОТОКСИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПОВРЕЖДЕНИЯ КЛЕТОК-МИШЕНЕЙ | 2002 |
|
RU2218938C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, ЭКСПРЕССИРУЮЩАЯ МОДУЛЬНЫЙ ПОЛИПЕПТИД ДЛЯ ДОСТАВКИ ФОТОСЕНСИБИЛИЗАТОРА, И ШТАММ ESCHERICHIA COLI ВКПМ В-8356 - ПРОДУЦЕНТ МОДУЛЬНОГО ПОЛИПЕПТИДА | 2004 |
|
RU2265055C2 |
| Монокатионный хлориновый фотосенсибилизатор для фотодинамической инактивации опухолевых клеток | 2022 |
|
RU2792003C1 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2016 |
|
RU2646834C1 |
| КОМПОЗИЦИЯ ДЛЯ ВИЗУАЛИЗАЦИИ И ПОВРЕЖДЕНИЯ КЛЕТОК-МИШЕНЕЙ | 2015 |
|
RU2611653C1 |
| Гель-фотосенсибилизатор для фотодинамической терапии | 2015 |
|
RU2606834C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОГО ЛЕЧЕНИЯ ОСТРОГО И ХРОНИЧЕСКОГО ГНОЙНОГО ГАЙМОРИТА | 2002 |
|
RU2228775C1 |
| Радиолюминесцентный препарат на основе аддукта хлорина Е6 и европия для фотодинамической терапии глубоких опухолей | 2024 |
|
RU2838226C1 |
Использование: биотехнология, клеточная и молекулярная биология, фотодинамическое повреждение клеток-мишеней. Сущность изобретения: композиция для фотодинамического повреждения клеток-мишеней состоит из фотосенсибилизатора, компонента-носителя фотосенсибилизатора, компонента для узнавания клеток-мишеней и транспорта фотосенсибилизатора внутрь клетки-мишени путем специфического рецептор-опосредуемого эндоцитоза и компонента, обладающего способностью направленного транспорта фотосенсибилизатора внутри клеток-мишеней. Способ фотодинамического повреждения клеток заключается в добавлении предлагаемой композиции к клеткам и выдерживании их при температуре, нормальной для жизнедеятельности клеток. При облучении клеток светом происходит фотохимическая реакция, в результате которой клетки-мишени гибнут. 2 с. и 19 з.п.ф-лы, 3 ил.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Rpkestraw S.L., Tompkins r.d., and Jarmush M.l | |||
| Antibodytargeted photolysis: In vitro studies with Sn (IV) chlorin e iovalenty bound tomonoclonal antibodies using a modified dextran carrier | |||
| Proc | |||
| Natl | |||
| Acad | |||
| Sci | |||
| U.S.A., 1990, V | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
| Визирное зеркало | 1925 |
|
SU4217A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Kessel D | |||
| Dexerminants of photosensitiration by monohaspartyl chlorin e | |||
| photochem | |||
| Photobiol., 1989, v | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| КОПИРОВАЛЬНЫЙ СТАНОК ДЛЯ ДЕРЕВА | 1921 |
|
SU447A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Aehlynina T.V., Rosenkran Z.A.A., jans D.A., Sobolev A.S.Insalinmediated intrasellular tprgeting enhances the photodynamic activity of ohlorin e | |||
| Canvnr Rns, 1995, v | |||
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
| СПОСОБ ПРИМЕНЕНИЯ КОГЕРЕРА В ТЕЛЕФОНАХ С ФОНИЧЕСКИМ ВЫЗОВОМ | 1923 |
|
SU1014A1 |
Авторы
Даты
1996-09-20—Публикация
1996-02-12—Подача