Изобретение относится к медицине, в частности борьбе с заболеваниями, вызываемыми патогенными микроорганизмами: грамположительными кокками, грамотрицательными бактериями и патогенными грибами.
Известно применение бактерицидных и фунгицидных препаратов для обработки раневой поверхности с целью предотвращения развития гнойно-воспалительного процесса.
Недостатком известных препаратов является высокий порог токсичности, совмещенный с низкой бактерицидной активностью и ограниченным спектром действия на различных представителей патогенных микроорганизмов, обсеменяющих раны.
Гексахлорофен препарат с относительно низкой токсичностью, обладает бактерицидными свойствами по отношению к грамположительным микроорганизмам [1] Это свойство гексахлорофена обусловило его широкое применение в хирургической практике. Недостатком гексахлорофена является относительно низкий уровень его бактерицидной активности к грамположительным микроорганизмам и отсутствие таковой к клеткам грамотрицательных бактерий, а также отсутствие фунгицидного действия.
С целью снижения токсичности препарата и придания ему бактерицидной активности к грамотрицательным микроорганизмам, повышения фунгицидного действия используют судамат натрия.
Поставленная цель достигается за счет применения 1,1-диоксотиолан-3-ил дитиокарбамата натрия.
Анализ литературных источников не позволил выявить сведения об использовании судамата натрия для подавления микробного обсеменения ран различного происхождения. Также не известно снижение токсичности дитиокарбаматов за счет замены катиона в его молекуле. Поэтому предложенное решение отвечает требованию критерия "новизна". Поскольку снижение токсичности и повышение эффективности действия судаматов при замене катионов калия натрием нельзя было предвидеть заранее, предложенное решение отвечает также требованиям критерия "существенные отличия".
Для получения судамата использовали известную методику синтеза дитиокарбаматов: к 0,1 моль соответствующего амина прибавляют 6,0 г (0,15 моль) гидроксида натрия, растворенного в минимальном количестве воды. При охлаждении реакционной смеси прибавляют по каплям 7,0 мл (0,11 моль) сероуглерода. Далее раствор для удаления большей части воды нагревают над вакуумом. Остаток растворяют в ацетоне, охлаждают дитиокарбамат эфиром и фильтруют [3] В отдельных случаях для предупреждения побочных реакций рекомендуют получать вещества в среде водного ацетона или диоксана [4] Исходя из этого использовали для получения судамата синтез по методике [3] использовав вместо минимального количества воды такое же количество водно-диоксановой смеси (1:1, мас.). Синтез исходного амина хорошо изученный процесс и для получения этого реагента была использована известная методика [5] Структурная формула судамата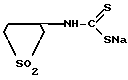
Пример 1. Цитотоксичность препарата проверяли на суточных культурах клеток Hep-2, которые выращивали на питательной среде известного состава [6] Однослойную культуру клеток дважды отмывали от остатков сыворотки крупного рогатого скота в среде роста. Препарат вносили на культуру клеток в среде Игла в указанных в табл. 1 концентрациях, клетки выдерживали в термостате при 37oC на протяжении 24 ч. Результаты даны в табл. 1.
Пример 2. На освобожденной от волосяного покрова боковой поверхности туловища морской свинки вызывали инфицированную патогенными грибами поверхностную рану путем втирания смеси культуру грибов с пылью абразивного материала до появления капель крови. Развитие микоза подтверждали микологическими исследованиями: микроскопией и посевом на питательные среды. Препарат наносили на поверхность раны с помощью марлевой салфетки, пропитанной водным раствором в субтоксических концентрациях. Эффективность действия гексахлорофена, калиевой и натриевой форм судамата в 1,0 концентрации приведена в табл. 2.
Из данных табл. 1, 2 следует, что судамат натрия имеет относительно низкую цитотоксочность и более высокую эффективность
Пример 3. У белых крыс-самцов в верхней трети задней конечности выбривали участки 2 х 2 см, через сутки дозированно наносили поверхностные резанные раны с помощью шести параллельно закрепленных ножей с выступающей кромкой 2 мм. Длина разреза 1 см. Опытных животных разбили на группы: первой группе животных раны не инфицировали и никаких видов лечения не применяли; животным из остальных групп через 0,5 1,0 ч после нанесения раны втирали суточные культуры микроорганизмов. Препараты растворяли в физиологическом растворе, пропитывали ими шестислойные салфетки и наносили на инфицированные раны. Полученные результаты даны в табл. 3.
Из данных табл. 3 следует, что заживление ран, инфицированных золотистым стафилококком и подвергнутых лечению судаматом-натрия, протекало в сроки, близкие по значению к срокам заживления ран у животных с необсемененной золотистым стафилококком раневой поверхностью. Гексахлорофен обладает более низкой активностью к золотистому стафилококку.
Заживление ран, инфицированных клебсиеллой пневмонии, под действием судамата натрия протекало в более сжатые сроки по сравнению с заживлением у животных, не получивших лечение. Однако эти сроки были значительно более длительными, чем у животных, раны которых не были инфицированы. Применение гексахлорофена было не эффективным.
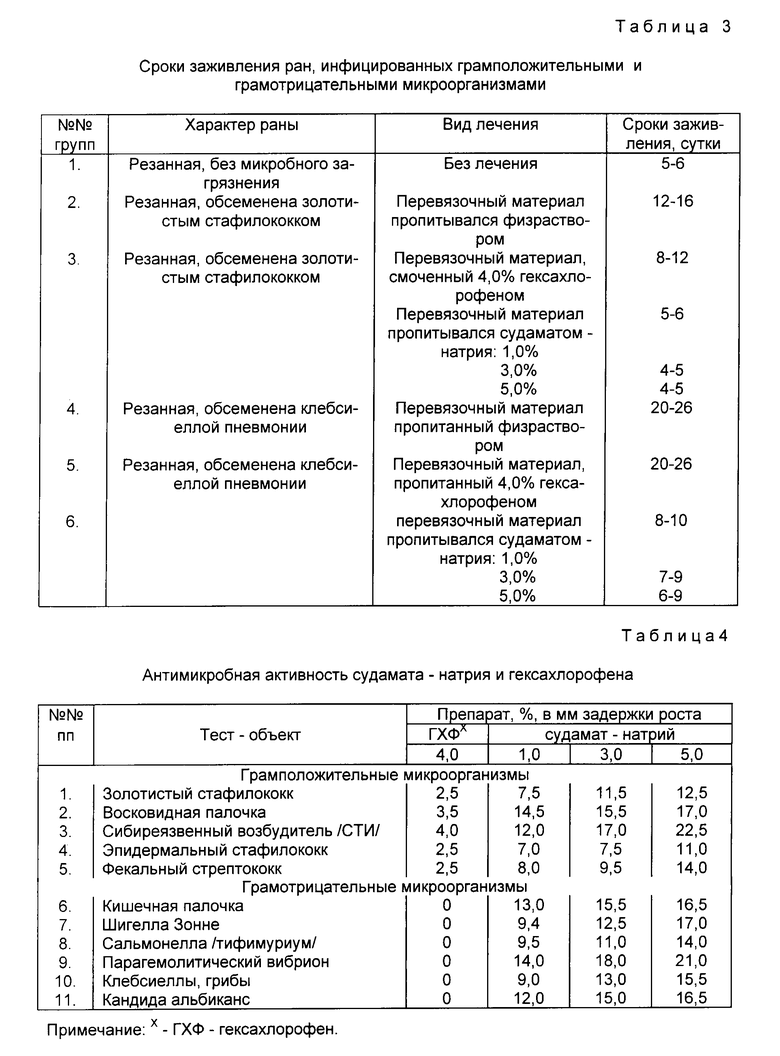
Пример 4. Результаты бактерицидной и фунгицидной активности судамата натрия (предлагаемый) и гексахлорофена (прототип) даны в табл. 4.
Из данных табл. 4 следует, что судамат натрия обладает бактерицидными свойствами по отношению к грамположительным микроорганизмам в более выраженной степени, чем гексахлорофен. Отсутствие активности у гексахлорофена к грамотрицательным микробам и грибам наряду с высокой активностью для судамата натрия подтверждает преимущество последнего.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭНТЕРОСОРБЦИИ | 1991 |
|
RU2016574C1 |
| СОСТАВ СО СТАБИЛИЗИРОВАННЫМ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫМ ПОТЕНЦИАЛОМ | 2012 |
|
RU2499600C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ДЕЗИНФИЦИРУЮЩИМИ, СПОРОЦИДНЫМИ И РАНОЗАЖИВЛЯЮЩИМИ СВОЙСТВАМИ | 2002 |
|
RU2203035C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ НАГНОЕНИЙ КОЖИ | 1992 |
|
RU2022566C1 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе диоксидина | 2016 |
|
RU2667974C2 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе бактериолитического и протеолитического комплекса ферментов | 2016 |
|
RU2655808C2 |
| Комбинированная композиция для лечения инфицированных ран различного генеза | 2018 |
|
RU2691144C1 |
| ПОРОШКООБРАЗНЫЙ ПРЕПАРАТ С АНТИБАКТЕРИАЛЬНЫМ И РЕГЕНЕРИРУЮЩИМ ЭФФЕКТАМИ | 2016 |
|
RU2629596C1 |
| МНОГОСЛОЙНЫЙ МАТЕРИАЛ С ХИТОЗАНОВЫМ СЛОЕМ ИЗ НАНО- И УЛЬТРАТОНКИХ ВОЛОКОН С АНТИБИОТИКОМ | 2015 |
|
RU2604410C2 |
| СПОСОБ ПОВЫШЕНИЯ ЧУВСТВИТЕЛЬНОСТИ БАКТЕРИЙ К БИОДЕСТРУКТИВНОМУ ДЕЙСТВИЮ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ В СОЧЕТАНИИ С ФОТОСЕНСИБИЛИЗАТОРОМ | 1999 |
|
RU2151601C1 |
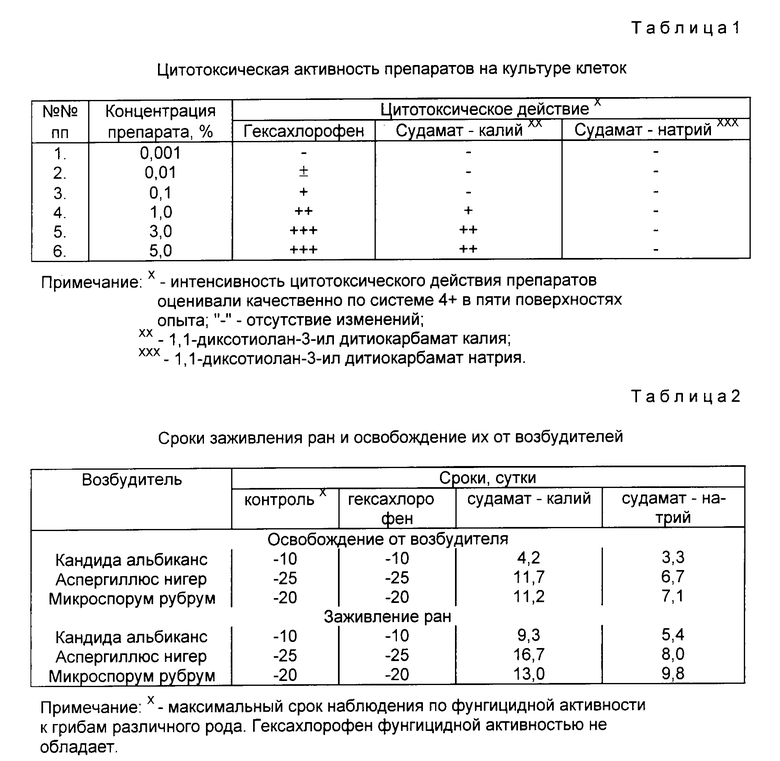
Изобретение относится к медицине и касается антимикробного средства для борьбы с заболеваниями, вызываемыми патогенными микроорганизмами. Цель - снижение токсичности и придание средству бактерицидной активности к грамотрицательным микроорганизмам. Сущность изобретения: применяют в качестве антимикробного средства 1,1-диоксотиолан-3-илдитиокарбамат натрия. Использование антимикробного средства обеспечивает быстрое заживление ран, инфицированных клебсиеллой пневмонии. 4 табл.
Применение 1,1-диоксотиолан-3-ил-дитиокарбамата натрия в качестве антимикробного средства.
| Бырко В.М | |||
| Дитиокарбаматы | |||
| - М.: Наука, 1984, с | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
Авторы
Даты
1997-12-10—Публикация
1993-10-28—Подача