Изобретение относится к области медицинской микробиологии и может быть использовано в лабораториях НИИ, системе противотуберкулезных учреждений, а также ветеринарии.
Характеристика аналога. Известны среды для определения лекарственной устойчивости к пиразанамиду. Наиболее часто с целью определения лекарственной резистентности используются среды Миддлбрука 7H10 и Левенштейна-Йенсена, содержащие пиразанамид. Однако аналогов заявляемого предложения (как комплекса) нет. В научной и информационно-патентной литературе, а также в практике фтизиобактериологии не известны субстрат и способ, одинаково пригодный как для определения лекарственной резистентности к пиразанамиду, так и для идентификации микробактерий.
Критика прототипа. В связи с тем, что резистентность к пиразинамиду выявляется в строго определенном диапазоне pH (5,0 5,5), вышеназванные среды необходимо подкислять до указанных значений pH. Однако при подкислении ухудшаются ростовые свойства сред. Так при субкультировании взвеси, содержащей стандартный инокулят, на плотной среде Левенштейна-Иенсена с нейтральным pH (6,8 7,2) результат читают на 14-й день. Рост на подкисленной до 5,0 5,5 среде замедляется, и результат можно прочесть лишь на 4-й 6-й неделе. Кроме того, недостатком прототипа является сложный состав, включающий дорогостоящий и дефицитные импортные ингредиенты. Дополнительными недостатками среды Левенштейна-Иенсена с низким pH являются разрывы скошенной поверхности среды, наступающие в процессе коагуляции, и чрезвычайно поздние сроки получения результатов исследования устойчивости к пиразинамиду (до 6 недель) применительно к отдельным клиническим случаям с хроническим течением туберкулеза (4). Дополнительным недостатком среды является необходимость выращивания микобактерий в газовой среде, содержащей углекислоту.
Сущность настоящего предложения. Целью заявляемого объекта является: а) создание нового субстрата с пиразинамидом на основании отечественных доступных химиопрепаратов и препаратов; б) исключение дополнительного технологического этапа подкисления среды; в) обеспечение роста испытываемых культур микобактерий в короткие сроки; г) удешевление анализа.
Решение поставленных задач обеспечивается специально сконструированным субстратом, в который входят следующие компоненты, г на 1 л готовой среды:
Калий фосфорнокислый однозамещенный 4,0 9,0
Магний сернокислый 0,2 0,6
Натрий лимоннокислый 0,3 0,9
Железо-аммоний (III) сернокислое 0,01 0,04
Железо-аммоний (II) сернокислое 0,01 0,04
Аминоуксусная кислота 0,5 1,3
α-аминоянтарная кислота 0,3 0,9
Янтарная кислота 0,8 1,6
Аммоний янтарнокислый 1,2 2,4
Натрий фосфорнокислый однозамещенный 1,3 2,4
Бриллиантовый зеленый 0,01 0,04
Глицерин, мл 7,0 17,0
Гидролизин, мл 15,0 50,0
Гомогенизированная яичная масса, мл 200 500
Пенициллин 100000 300000
Вода Остальное
Конечная pH среды 5,4 5,6
Перед коагуляцией в среду вводят пиразинамид для обеспечения концентрации 25-50-75-100-200-400 мкг/мл.
Как видно из компонентного состава, предлагаемый субстрат состоит из доступных отечественных препаратов, а достигаемая без подтитровки pH обеспечивает те уникальные условия, при которых наиболее эффективно действует пиразинамид. Кроме того, специально подобранные новые химические соединения несут двойную функцию: способствуют формированию низкой pH и одновременно являются стимуляторами роста измененных микобактерий. Особый режим уплотнения и коагуляции сред обеспечивает требуемую консистенцию и способствует быстрому росту микобактерий. Кроме того, предлагаемый способ позволяет инкубировать микобактерии в обычных условиях, без применения CO2-инкубатора.
Исследование резистентности к пиразанамиду у микобактерий, выделенных от больных, показало, что предлагаемая методика позволяет выдать в клинику результат на 10-й 14-й день.
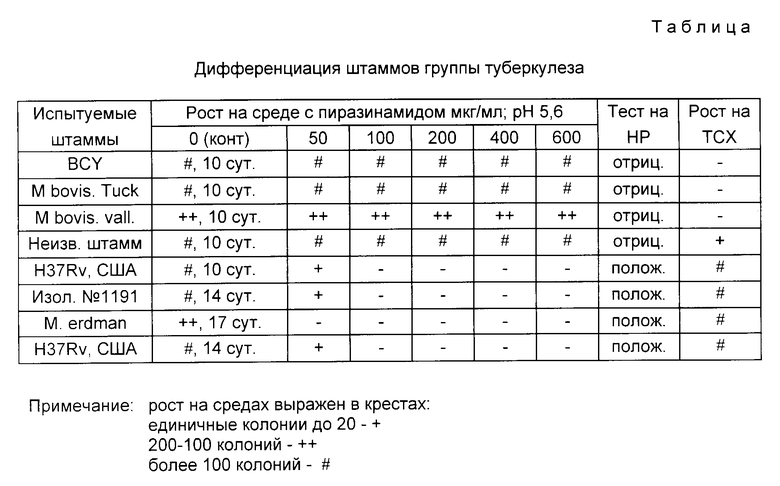
Минимально-ингибирующая концентрация пиразинамида для большинства лабораторных штаммов: Академия, H37RV, Erdman составляет 25 мкг/мл. Чувствительными штаммами следует считать те, которые не растут на предлагаемой среде с 50 100 мкг/мл пиразинамида. Помимо определения резистентности к пиразинамиду предлагаемый способ позволяет установить тип микобактерий (человеческий либо бычий). Дифференцирующая способность сред с пиразинамидом отражена в таблице 1.
Пример 1. В подогретой до 80 90oC дистиллированной воде последовательно растворяют, г: калий фосфорнокислый однозамещенный 4,0; магний сернокислый 0,2; натрий лимоннокислый 0,3; железо-аммоний (II) сернокислое 0,01; железо- аммоний (Ш) сернокислое 0,01; аминоуксуная кислота 0,5; a-аминоянтарная кислота 0,3; янтарная кислота 0,8; аммоний янтарнокислый 1,2; натрий фосфорнокислый однозамещенный 1,2; бриллиантовый зеленый 0,01; глицерин 7 мл; гидролизин 15 мл; гомогенизированная яичная масса 200 мл, дистиллированная вода остальное. Солевые компоненты растворяют в указанном растворе, автоклавируют при 1 атм (121oC) в течение 25 мин, охлаждают до комнатной температуры, добавляют гомогенизированную яичную массу, раствор бриллиантового зеленого, 100000 ед. пенициллина, пиразинамид для получения рабочих концентраций 25-50-75-100-200-400 мкг/мл. Часть среды без пиразинамида используют как контроль. Коагулируют при 78oC в течение 30 мин. Стерильность сред с пиразинамидом и без него испытывается термостатированием при 37oC в течение 48 ч. Засев взвести плотностью 10 млн. микробных тел в 1 мл производится по 0,2 мл на каждую опытную пробирку и контроль. Индикация роста производится визуально, начиная с 8-го дня ежедневно.
Пример 2. В подогретой до 80 90oC дистиллированной воде последовательно растворяют, г: калий фосфорнокислый однозамещенный 9,0, магний сернокислый 0,6; натрий лимоннокислый 0,9; железо-аммоний (II) сернокислое 0,04; железо- аммоний (III) сернокислое 0,04; аминоуксусная кислота 1,3; a-аминоянтарная кислота 0,9; янтарная кислота 1,6; аммоний янтарнокислый 2,4; натрий фосфорнокислый однозамещенный 2,4; бриллиантовый зеленый 0,04; глицерин 17 мл; гидролизин 50 мл; гомогенизированная яичная масса 500 мл; пенициллин 300000 ед. дистилированная вода остальное. Солевые компоненты растворяют в указанном порядке, автоклавируют при 1 атм (121oC) в течение 25 мин, охлаждают до комнатной температуры, добавляют гомогенизированную яичную массу, раствор бриллиантового зеленого, 300000 ед. пенициллина, пиразинамид для получения рабочих концентраций 25-50-75-100-200-400 мкг/мл. Далее, как в примере 1.
Пример 3. В подогретой до 80 90oC дистиллированной воде последовательно растворяют, г: калий фосфорнокислый однозамещенный 6,5; магний сернокислый 0,4; натрий лимоннокислый 0,6; железо-амомний (II) сернокислое 0,025; железо-аммоний (III) сернокислое 0,025; аминоуксусная кислота 0,9; a-аминоянтарная кислота 0,6; янтарная кислота 1,2; аммоний янтарнокислый 1,8; натрий фосфорнокислый однозамещенный 1,8; бриллиантовый зеленый 0,025; глицерин 12 мл; гидролизин 32 мл; гомогенизированная яичная масса 350 мл; пенициллин 200000 ед. Перед коагуляцией в среду вводят пиразинамид для обеспечения концентраций 25-50-75-100-200-400 мкг/мл. Далее, как в примере 1.
Технико-экономическая или иная эффективность. Предлагаемая среда состоит из доступных недефицитных ингредиентов отечественного производства. По источнику аминного азота предлагаемая среда дешевле среды Левенштейна-Иенсена в 75 раз. Предлагаемая среда имеет полуплотную консистенцию, в связи с чем расход уплотнителя (диэтические яйца) на единицу объема в 2 раза меньше, чем в среде Левенштейна-Иенсена. В целом 1 т предлагаемой среды дешевле 1 т среды Левенштейна-Иенсена приблизительно на 1000 руб.
Кроме того, существенная экономия затрат рабочего времени обеспечивается одноэтапной технологией приготовления среды. Использование предлагаемой среды не требует специальных условий (CO2-инкубатор), обеспечивает быстрый рост испытуемых штампов в "кислом" диапазоне pH (5,4 5,6), служит надежным тестом для типирования микобактерий.
Источники информации
1. Z.N. Kantos, I.E. Amadio, E.A. Catalini, M. D.C. Zonardo, Z. Dominguez, D. Cuffo, A. Zaslo, O. Zatini, I. Poggio, H. Reyes Iutierres, M.T. Vacenzuela. Pyrasinamidase activity and susceptibility to pyrazinamide in clinical isolates of Mycobacterium tuberculosis. Pyrazinamide suseptibility of M. tuberculosis.
2. Slottmeier K.D. Blat R.F. and Kubica I.P. Pyrazinamide suseptibility and amidase activity of tubercle bacilli, American Review of Respiratory Desease 1967, 97, 1072.
3. Mycobacterial culture collection US Goverment Printing Office 1980.
4. Авт. св. СССР N 1666530, C 12 N 1/20, C 12 Q 1/04, 1991.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения чувствительности культур Mycobacterium tuberculosis к пиразинамиду | 2022 |
|
RU2792782C1 |
| КОМБИНИРОВАННАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ДИФФЕРЕНЦИАЦИИ MYCOBACTERIUM TUBERCULOSIS И MYCOBACTERIUM BOVIS | 1993 |
|
RU2102483C1 |
| Питательная среда для выращивания микробактерий туберкулеза | 1978 |
|
SU839254A1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ МИКОБАКТЕРИЙ | 2005 |
|
RU2300571C2 |
| ПЛОТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ, ВЫДЕЛЕННЫХ ИЗ ЛЕПРОМ БОЛЬНЫХ ЛЕПРОЙ | 2009 |
|
RU2413764C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ИНДИКАЦИИ И ДИФФЕРЕНЦИАЦИИ ВОЗБУДИТЕЛЕЙ ТУБЕРКУЛЕЗА | 1995 |
|
RU2086257C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ И НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ | 2006 |
|
RU2322495C2 |
| Способ дифференциации МYсовастеRIUм аVIUм от МYсовастеRIUм INтRасеLLULаRе | 1989 |
|
SU1666530A1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДЫ ДЛЯ ВЫРАЩИВАНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2005 |
|
RU2295561C2 |
| Питательная среда для культивирования микобактерий туберкулеза | 1988 |
|
SU1555358A1 |
Использование: медицинская микробиология. Сущность изобретения: питательная среда с пиразинамидом для определения лекарственной устойчивости возбудителей туберкулеза и их идентификации включает следующие компоненты, г: калий фосфорнокислый однозамещенный 4,0 - 9,0; магний сернокислый 0,2 - 0,6; натрий лимоннокислый 0,3 - 0,9; железо (III) сернокислое аммиачное 0,01 - 0,04; железо (II) сернокислое аммиачное 0,01 - 0,04; аминоуксуcная кислота 0,5 - 1,3; α-аминоянтарная кислота 0,3 - 0,9; янтарная кислота 0,8 - 1,6; аммоний янтарнокислый 1,2 - 2,4; натрий фосфорнокислый однозамещанный 1,3 - 2,4; бриллиантовый зеленый 0,01 - 0,04; глицерин, мл 7,0 - 17,0; гидролизин, мл 15,0 - 50,0; гомогенизированная яичная масса, мл 200 - 500; пенициллин, ед./мкл 100000 - 300000; пиразинамид, мкг/мл 50 - 200; вода до 1 л. 1 табл.
Питательная среда с пиразинамидом для определения лекарственной устойчивости возбудителей туберкулеза и их идентификации, содержащая калий фосфорнокислый однозамещенный, магний сернокислый, бриллиантовый зеленый, глицерин, гомогенизированную яичную массу и воду, отличающаяся тем, что она дополнительно содержит натрий лимоннокислый, железо (III) сернокислое аммиачное, железо (II) сернокислое аммиачное, аминоуксусную кислоту, α-аминоянтарную кислоту, янтарную кислоту, аммоний янтарнокислый, натрий фосфорнокислый однозамещенный, гидролизин, пенициллин, пиразинамид при следующем количественном соотношении компонентов:
Калий фосфорнокислый однозамещенный, г 4,0 9,0
Магний сернокислый, г 0,2 0,6
Натрий лимоннокислый, г 0,3 0,9
Железо (III) сернокислое аммиачное, г 0,01 0,04
Железо (II) сернокислое аммиачное, г 0,01 0,04
Аминоуксусная кислота 0,5 1,3 г
α-аминоянтарная кислота, г 0,3 0,9
Янтарная кислота, г 0,8 1,6
Аммоний янтарнокислый, г 1,2 2,4
Натрий фосфорнокислый однозамещенный, г 1,3 2,4
Бриллиантовый зеленый, г 0,01 0,04
Глицерин, мл 7,0 17,0
Гидролизин, мл 15,0 50,0
Гомогенизированная яичная масса, мл 200 500
Пиразинамид, мкг/мл 50 200
Пенициллин, ед/мкл 100000 300000
Вода, л До 1о
| SU, авторское свидетельство, N 1666530, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1997-12-20—Публикация
1993-01-06—Подача