Данное изобретение относится к медицине и ветеринарии, а именно к лабораторным методам диагностики туберкулеза.
Известные культуральные исследования диагностического материала традиционно осуществляются на плотных яичных средах. Существует большое количество плотных питательных сред и разные лаборатории используют различные среды. В настоящее время наиболее часто применяемой средой является питательная среда Финн-2 (приказ МЗ РФ №109 от 21. 03.03, стр.269).
Состав среды Финн-2 (в г/л):
1. Минеральные соли:
Первичное культивирование микобактерий туберкулеза из диагностического материала затруднено тем, что существует ряд факторов, ограничивающих широкое применение культурального метода, в частности известные ограничения, связанные с медленным размножением микобактерий туберкулеза и их избирательное отношение к составу питательных сред. В связи с широким применением специфических противотуберкулезных препаратов наблюдаются изменения биологических свойств возбудителя, влияющее на способность микобактерий расти на питательных средах, что также снижает информативность культурального метода и диктует необходимость широкого поиска более совершенных питательных сред, которые позволили бы ускорить получение результатов и повысить эффективность и чувствительность метода. По данным микробиологической лаборатории ЯНИИТ, в 3,0-4,0% случаев из-за скудного роста культур МБТ не происходит накопления достаточной бактериальной массы для дальнейшей работы с выделенной культурой, возникает необходимость получения субкультур и, таким образом, удлиняются сроки выдачи результатов идентификации и определения чувствительности к противотуберкулезным препаратам.
С учетом вышеперечисленного предложена питательная среда на основе яичной среды Финн-2, минеральные солевые компоненты последней растворяются в растворе гумата натрия, а не в дистиллированной воде.
Состав предложенной питательной среды (в г/л):
1. Минеральные соли:
Приготовление питательной среды.
1. Приготовление 0,1% раствора гумата натрия.
Исходный раствор гумата натрия, полученный из сапропеля по общеизвестной методике, разводится стерильной дистиллированной водой в соотношении 1:10 для получения 0,1% раствора. Необходимое количество раствора на 1 л яичной массы до 1000,0 мл рН не коррегируют. Срок хранения 3-4 недели при комнатной температуре.
2. Приготовление солевой основы питательной среды. При слабом подогревании (не доводя до кипения) на водяной бане в приготовленном 0,1% - 1000,0 мл растворе гумата натрия растворяют минеральные соли и глицерин по росписи среды Финн-2, в указанной последовательности. Автоклавируют при 1 атм. 30 мин рН не коррегируют. Срок хранения 3-4 недели при комнатной температуре.
3. Приготовление яичной массы.
Свежие диетические куриные яйца со сроком не более 7 суток, без трещин и дефектов скорлупы моют в теплой проточной воде с помощью ручных щеток и мыла, оставляют на 30 мин в мыльном растворе. Тщательно промывают в проточной воде и погружают в 70% этиловый спирт на 30 мин. Затем в стерильном боксе яйца разбивают стерильным ножом в стерильную посуду, доводя общий объем яичной массы до 1 л. Для этого требуется 20-25 яиц в зависимости от их величины. Тщательно взбивают стерильным венчиком.
4. Приготовление 2,0% малахитового зеленого. Раствор малахитового зеленого:
Малахитовый зеленый - 2,0 г;
Стерильная дистиллированная вода- 100,0 мл.
Растворить в стерильной дистиллированной воде малахитовый зеленый, поместив раствор в термостат на 1-2 часа. Стерилизовать при 1 атм. 30 мин.
5. Приготовление среды.
В большую стерильную емкость, соблюдая правила стерильности, помещают растворы:
Раствор минеральных солей в 0,1% гумате натрия - 1000,0
Яичная масса - 1000,0
Тщательно перемешивают, фильтруют через 4-слойный марлевый фильтр.
Добавляют 30,0 мл 2,0% раствора малахитового зеленого, тщательно перемешивают в течение не более 15 мин, разливают в стерильные пробирки по 5,0.
6. Свертывание среды.
Свертывание среды проводят в специальных аппаратах при 85°С в течение 45 мин.
7. Питательные среды хранят в холодильнике, при температуре +4°С, в течение месяца.
Питательная среда, полученная предложенным способом, апробирована на музейных штаммах МБТ «Академия», «БЦЖ» и штаммах МБТ, выделенных от больных различными форами туберкулеза. Контролем служила стандартная питательная среда Финн-2 (Ф-2). Посев на пробирки со средами осуществляли путем внесения суспензии музейных культур, приготовленной по оптическому стандарту мутности - 500 млн. кл/мл в количестве 0,2 мл в каждую пробирку. Посевы клинических штаммов культур МБТ производили в разведении 50 млн. кл/мл в количестве 0,2 мл в каждую пробирку. Регистрировали: появление начального роста в сутках и массивность роста на 21 сутки наблюдения: до 20 колоний, от 20 до 50 колоний, от 50 до 100 колоний и более 100 колоний.
Способ иллюстрируется фиг.1-6.
Начальный рост МБТ «шт. Академия» на контрольной среде Ф-2 зарегистрирован на 10,6±0,5 сутки. В опытной среде на 8,1±0,4 сутки наблюдения (разница статистически достоверна р<0,005) (диаграмма 1).
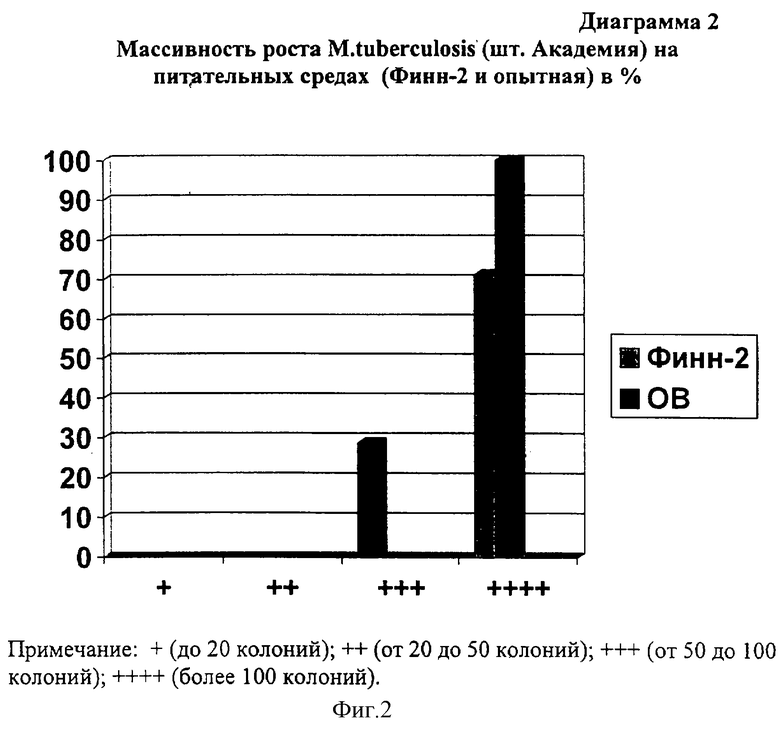
Массивность роста учитывалась по количеству выросших колоний МБТ на 21 сутки наблюдения: от 50 до 100 колоний и более 100 колоний. На контрольной среде Ф-2 в 28,6% случаев дали рост от 50 до 100 колоний и 71,4% случаев более 100 колоний. В опытной среде регистрировалось следующее: рост от 50 до 100 колоний - не зарегистрирован; более 100 колоний - в 100% случаев (диаграмма 2).
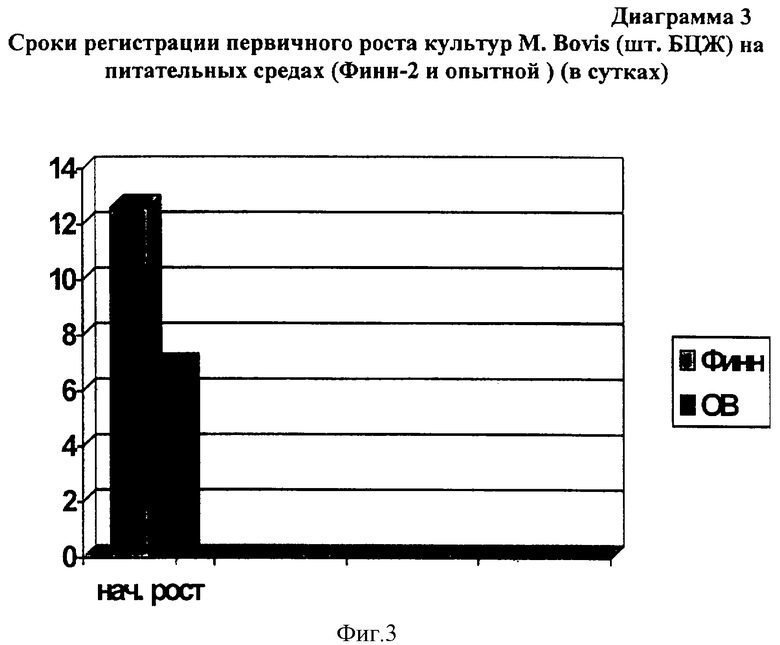
Начальный рост МБТ «шт. БЦЖ» в контрольной среде Финн-2 зарегистрирован на 12,6±0,8 сутки, а в опытной среде на 6,9±0,5 сутки наблюдения (разница статистически достоверна р<0,001) (диаграмма 3).
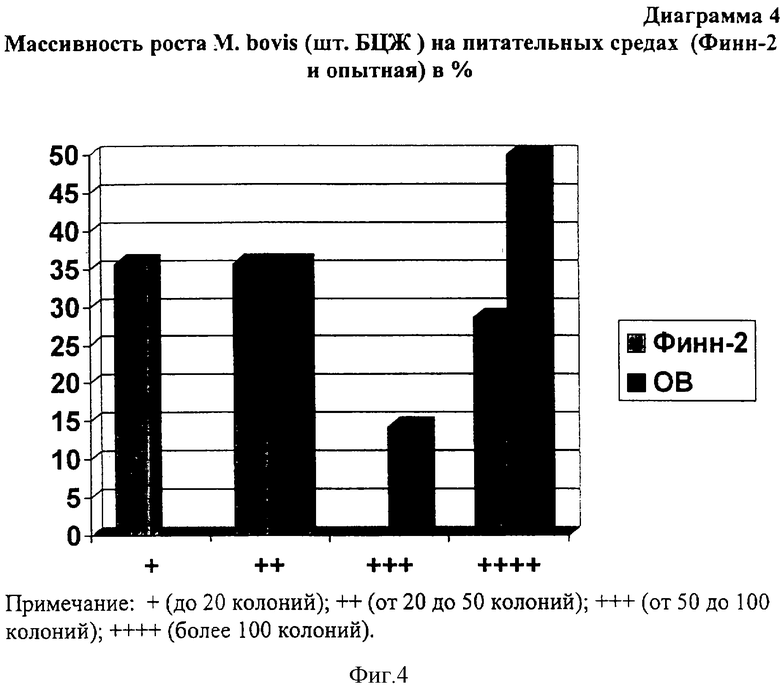
Учитывалась массивность роста или накопление биомассы МБТ (шт. БЦЖ) на 21 сутки наблюдения: до 20 колоний, от 20 до 50, от 50 до 100 и более 100 колоний. Как видно из диаграммы 4, в контрольной среде Финн-2 в 35,7% массивность роста достигала до 20 колоний, в 35,7% рост от 20 до 50 колоний, в 28,6% массивность роста составляла более 100 колоний. В опытных средах в 35,7% рост от 20 до 50 колоний, в 14,3% от 50 до 100 колоний и в 50% случаях более 100 колоний (диаграмма 4).
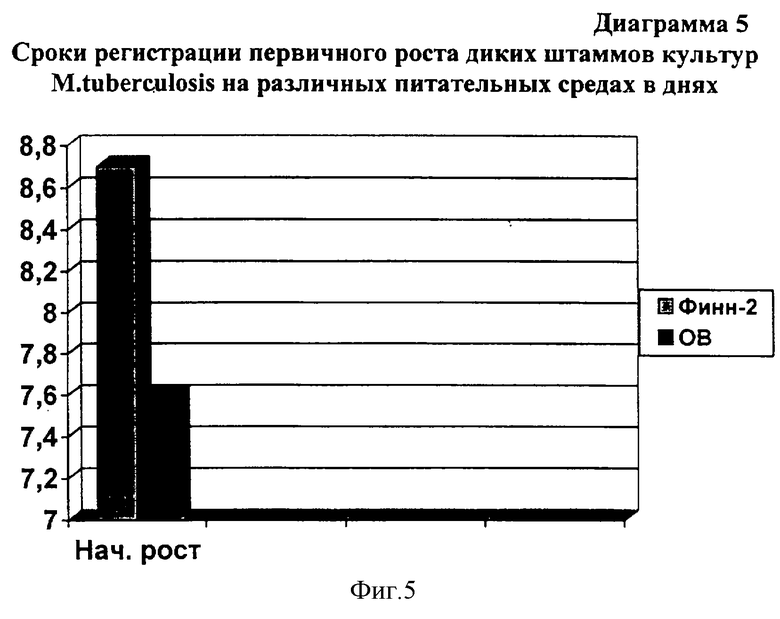
Начальный рост штаммов МБТ, выделенных от больных различными формами туберкулеза, зарегистрирован на контрольной среде Ф-2 на 8,7±0,2 сутки наблюдения. В опытной среде начальный рост на 7,6±0,2 сутки наблюдения (диаграмма 5).
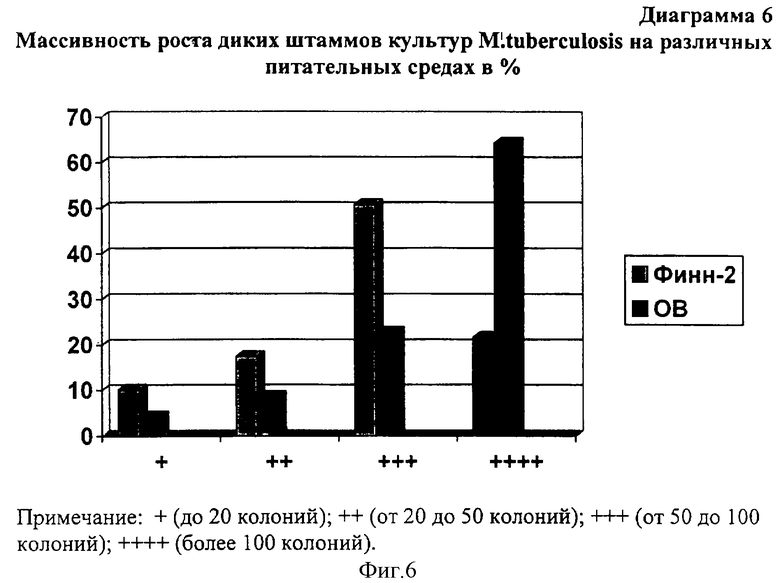
Массивность роста МБТ: на среде Ф-2 - до 20 колоний -10,6%; от 20 до 50 колоний - 56,1%; от 50 до 100 колоний-24,2%; более 100 колоний - 9,1%. В опытной среде до 20 колоний - 4,3%; от 20 до 50 колоний - 8,6%; от 50 до 100 колоний - 22,8% и более 100 колоний - 64,3% (диаграмма 6).
На основании проведенных исследований питательная среда, приготовленная предложенным способом, имеет ряд преимуществ:
1. Более выраженные питательно-ростовые свойства, что позволяет в 2,6 раза чаще получать массивный рост МБТ при малом числе микробных тел в посевном материале;
2. Длительное сохранение в пробирке конденсационной жидкости, что предохраняет среду от преждевременного засыхания;
3. Не содержит дорогостоящих компонентов.
Применение питательной среды, приготовленной предложенным способом:
1. Для культивирования возбудителя туберкулеза из диагностического материала человека и животных.
2. Для сохранения и выращивания лабораторных штаммов и выделенных культур микобактерий туберкулеза.
Описание гумата натрия
Гумат натрия - это водорастворимая форма ГВ, выделенных из озерных сапропелевых отложений. Обобщенная формула ГВ сапропеля может быть представлена как (C39H68O26N3)n, где n - количество фрагментов. В составе гуминовых веществ в результате жесткого кислотного гидролиза обнаружены 16 аминокислот, главным образом, аспарагановая, глутаминовая кислоты, глицин, аланин, ряд углеводов, макро- и микроэлементы (азот, фосфор, калий, марганец, цинк и др.) (Мярикянов и др., 1991, Сазонов, 2000). Стандартность препарата достигается использованием сырья одного месторождения, постоянством цикла выделения. Применяемый для приготовления питательных сред исходный раствор гумата натрия (1%) представляет собой темнокоричневую вязкую жидкость, со специфическим запахом. Гумат натрия обладает способностью стимулировать биологические процессы в живых организмах и транспортировать к клеткам микроэлементы и другие ценные соединения. С учетом указанных характеристик предлагается использовать указанные биологически активные свойства гумата натрия при приготовлении питательных сред для выращивания микобактерий туберкулеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ МИКОБАКТЕРИЙ ПРИ БАКТЕРИОЛОГИЧЕСКОЙ ДИАГНОСТИКЕ ТУБЕРКУЛЕЗА | 2008 |
|
RU2366700C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ИНДИКАЦИИ И ДИФФЕРЕНЦИАЦИИ ВОЗБУДИТЕЛЕЙ ТУБЕРКУЛЕЗА | 1995 |
|
RU2086257C1 |
| ПЛОТНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ, ВЫДЕЛЕННЫХ ИЗ ЛЕПРОМ БОЛЬНЫХ ЛЕПРОЙ | 2009 |
|
RU2413764C1 |
| СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2000 |
|
RU2192472C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПИТАТЕЛЬНОЙ СРЕДЫ ДЛЯ ВЫРАЩИВАНИЯ МИКОБАКТЕРИЙ | 2008 |
|
RU2403281C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ МИКОБАКТЕРИЙ | 1995 |
|
RU2121000C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ И НОКАРДИОФОРМНЫХ АКТИНОМИЦЕТОВ | 2006 |
|
RU2322495C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ МИКОБАКТЕРИЙ | 2005 |
|
RU2300571C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ УСКОРЕННОГО ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЯ ТУБЕРКУЛЕЗА ИЗ ОЧАГОВ ВНЕЛЕГОЧНОЙ ЛОКАЛИЗАЦИИ НА ОСНОВЕ СРЕДЫ ФИННА-II | 1993 |
|
RU2117046C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ ИЗ БИОЛОГИЧЕСКОГО МАТЕРИАЛА И КУЛЬТИВИРОВАНИЯ МИКОБАКТЕРИЙ | 2006 |
|
RU2315812C1 |
Изобретение относится к области биотехнологии. Способ включает смешивание солевой основы, состоящей из минеральных солей, с глицерином, растворение смеси солевой основы и глицерина, приготовление раствора малахитового зеленого, приготовление яичной массы и смешивание полученных растворов с яичной массой. При этом растворение смеси солевой основы и глицерина осуществляют в 0,1%-ном растворе гумата натрия, а компоненты берут в следующем количестве: магний сернокислый (MgSO4×7Н2О) 0,5 г, натрий лимоннокислый (C6H5O7Na3×5,5Н2O) 0,1 г, квасцы железоаммонийные (Fe(NH4)(SO4)2×12Н2О) 0,05 г, калий однозамещенный фосфорнокислый (КН2PO4) 20,0 г, аммоний лимоннокислый однозамещенный (С6Н11О7Н) 5,0 г, натрий глутаминовокислый однозамещенный (C5H8NaO4×Н2О) 10,0 г, глицерин (С3Н8O3) 20,0 мл, 0,1% раствор гумата натрия (C39H68O26N3)n до 1000,0 мл. В результате использования среды, приготовленной предложенным способом, достигается получение первой генерации культур МБТ на три дня раньше и увеличение биомассы в 2,1 раза по сравнению с контролем. 6 ил.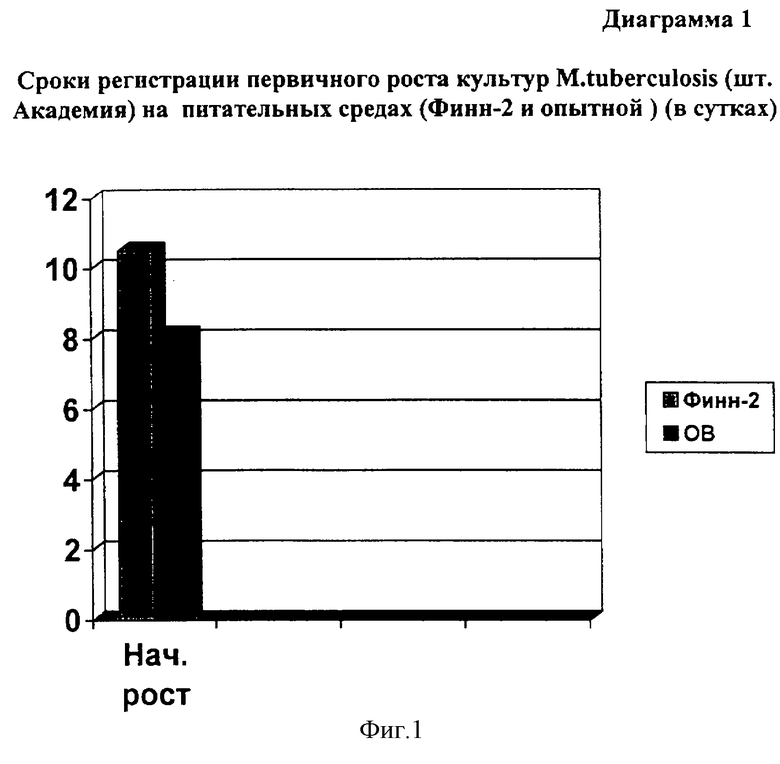
Способ получения среды для выращивания микобактерий туберкулеза, включающий смешивание солевой основы, состоящей из минеральных солей, с глицерином, растворение смеси солевой основы и глицерина, приготовление раствора малахитового зеленого, приготовление яичной массы и смешивание полученных растворов с яичной массой, отличающийся тем, что растворение смеси солевой основы и глицерина осуществляют в 0,1%-ном растворе гумата натрия, а компоненты берут в следующем количестве,:
| ЛИОТЕКД I | 0 |
|
SU325879A1 |
| RU 2059715 C1, 10.05.1996 | |||
| ЛАБИНСКАЯ А.С., Микробиология с техникой микробиологических исследований, М., Медицина, 1978, с.288 | |||
| Туберкулез сельскохозяйственных животных, под ред | |||
| ШИШКОВА В.П., УРБАНА В.П., М., Агропромиздат, 1991, с.120-121. | |||
Авторы
Даты
2007-03-20—Публикация
2005-02-15—Подача