Изобретение относится к области неорганической химии, в частности, к катализаторам и способам их приготовления, и может быть использовано в газоперерабатывающей промышленности на установках Клауса.
Процесс Клауса предназначен для получения элементарной серы путем окисления сероводорода диоксидом серы по реакции:
2H2S + SO2 A 3/n + H2O (1).
В газах, поступающих на установки Клауса, наряду с сероводородом и диоксидом серы обычно содержится до 2 об.% одноуглеродных сероорганических соединений CS2 и COS. Одним из наиболее важных требований, предъявляемых к катализаторам процесса Клауса, является активность в реакциях гидролиза указанных соединений:
CS2 + 2 H2O F CO2 + 2 H2S (2),
COS + H2O A CO2 + H2S ( 3).
В результате протекания реакций (2) и (3) образуется сероводород, который окисляется диоксидом серы по реакции (1), что приводит к повышению выхода целевого продукта - элементарной серы. При низкой активности катализатора в реакциях гидролиза CS2 и COS проходят через каталитические конвертеры и поступают с хвостовыми газами установки Клауса в термическую печь, где сжигаются с образованием SO2. Таким образом, высокая активность катализатора процесса Клауса в реакции гидролиза CS2 и COS позволяет повысить выход элементарной серы и одновременно сократить выбросы SO2 в атмосферу.
Известен способ получения катализатора для процесса Клауса путем термического гидролиза аммоний - титанил сульфата при pH 0,8-1,2 и pH 1,8 - 2,2, отделения полученных осадков фильтрацией, их промывки и смешения в массовом отношении 7,5-9,0 : 2,5-1,0 [1].
Полученный катализатор проявляет достаточно высокую активность в реакции окисления сероводорода диоксидом серы, но не обладает активностью в реакциях гидролиза сероорганических соединений.
Известен титаноксидный катализатор процесса Клауса, полученный из орто- и метатитановых кислот или оксигидроксида титана. Недостатком известного катализатора является низкая активность в реакциях гидролиза сероорганических соединений. Так, степень превращения CS2 и COS при 300oC и времени контакта 4 с не превышает 28% [2].
Известен катализатор для процесса Клауса, содержащий смесь оксидов титана, циркония и церия в соотношении 62,3 : 23,2 : 14,5. Катализатор получают раздельным осаждением оксигидроксидов титана, циркония и церия путем взаимодействия основных сульфатов титана, циркония и нитрата церия с щелочным агентом, их смешением и обработкой влажной катализаторной массы азотной кислотой при соотношении (оксигидроксиды металлов) : (H2O) : (HNO3 = 69 : 23 : 8 с последующими стадиями формовки, сушки и прокаливания.
Полученный катализатор обеспечивает выходы серы по реакции (1), близкие к термодинамически равновесным. Конверсия CS2 при температуре 340oC и времени контакта 0,5 и 1,0 с составляет 63 и 95% соответственно [3].
Недостатком известного катализатора является относительно невысокая активность в реакциях гидролиза сероорганических соединений при малых временах контакта.
Недостатками способа приготовления катализатора являются:
раздельное получение трех осадков оксигидроксидов титана, циркония и церия, приводящее к осложнению технологии;
введение в катализаторную массу азотной кислоты, в связи с чем требуется наличие дорогостоящей коррозионностойкой аппаратуры;
выбросы в атмосферу значительных количеств оксидов азота, образующихся в результате разложения азотной кислоты при прокаливании катализатора.
Наиболее близким по технической сущности и достигаемому эффекту к предлагаемому техническому решению является катализатор, содержащий 65-98,5 мас. % диоксида титана (оксидный компонент) и 1,5-35 мас.% сульфата кальция, стронция или бария (соединение щелочноземельного элемента).
Способ его приготовления заключается в получении оксигидроксида титана обработкой тетрахлорида титана водным раствором щелочного агента, отделении осадка, промывке водой (или без промывки), сушке при 110oC в течение 24 ч, перемешивании полученного порошка в течение 30 мин с водой и карбоксиметилцеллюлозой, экструзии этой смеси, сушке экструдата при 110oC в течение 8 ч, прокаливании при 450-500oC в течение 2-7 ч, пропитке продукта раствором сульфата аммония или серной кислоты, сушке в течение 4 ч при 110oC, последующей пропитке нитратом щелочноземельного элемента, сушке при 110oC в течение 4-12 ч и прокаливании при 450oC в течение 1-2 ч.
Полученный катализатор обеспечивает выходы серы по реакции (1), близкие к термодинамически равновесным. Конверсия CS2 при температуре 260oC и времени контакта 1 с составляет 72%, при температуре 340oC и времени контакта 3 с - 99% [4] (прототип).
Недостатком известного катализатора является относительно невысокая активность в реакциях гидролиза сероорганических соединений при низких температурах и малых временах контакта.
Недостатками способа приготовления катализатора являются:
многостадийность и сложность технологии;
большие затраты энергии на многократные стадии сушки и прокаливания катализаторной массы;
наличие выбросов в атмосферу оксидов азота (около 100 кг на 1 т катализатора).
Сравнение данных по активности в реакциях окисления сероводорода диоксидом серы и гидролиза сероорганических соединений показывает, что катализаторы, полученные по патентам [3] и [4], практически одинаковы. Выбор в качестве прототипа катализатора по патенту [4] обусловлен тем, что предлагаемый катализатор также, как и прототип содержит оксидный компонент и соединение щелочноземельного элемента. Кроме того, производство катализатора по прототипу освоено в промышленности (катализатор CRS-31, Фирма Рон-Пуленк), что позволяет использовать его для сравнения каталитической активности прототипа и предлагаемого катализатора в одних и тех же экспериментальных условиях.
Технической задачей изобретения является создание катализатора для получения серы по процессу Клауса, обладающего повышенной активностью в реакциях гидролиза сероорганических соединений, а также способа его приготовления, позволяющего упростить технологию производства катализатора и устранить образование и выбросы в атмосферу оксидов азота.
Техническая задача решается заявляемым катализатором, содержащим оксидный компонент и соединение щелочноземельного элемента, отличающийся тем, что в качестве оксидного компонента катализатор содержит твердый раствор оксидов титана и редкоземельных элементов (РЗЭ), имеющий состав Ti(РЗЭx)O(2+1,5x), где 0,174≥x≥ 0,027, а в качестве соединения щелочноземельного элемента - карбонат кальция при следующем содержании компонентов, мас.%:
Карбонат кальция - 1 - 10
Твердый раствор оксидов титана и РЗЭ, соответствующий составу Ti(РЗЭx)O(2+1,5x), где 0,174 ≥x≥ - 0,027 Остальное.
Техническая задача решается также способом его приготовления, включающим получение оксигидроксида титана обработкой тетрахлорида титана водным раствором щелочного агента, формование, сушку и прокаливание, отличающимся тем, что одновременно с получением оксигидроксида титана получают оксигидроксиды редкоземельных элементов (РЗЭ) путем совместной обработки тетрахлорида титана и хлоридов РЗЭ водным раствором или суспензией щелочного агента, в которые вводится карбонат кальция, взятый из расчета, чтобы его содержание в готовом катализаторе составляло 1-10 мас.%, количества тетрахлорида титана и хлоридов РЗЭ берут из расчета, чтобы соотношение оксидов титана и РЗЭ в твердом растворе было в пределах (73,7-94,7) : (5,3-26,3) и процесс ведут при соотношении компонентов, обеспечивающем содержание в катализаторе, мас. %:
Карбонат кальция - 1 - 10
Твердый раствор оксидов титана и РЗЭ, соответствующий составу Ti(РЗЭx)О(2+1,5x), где 0,174≥ x ≥ 0,027 - Остальное.
Сущность изобретения заключается в том, что катализатор для получения серы по процессу Клауса содержит карбонат кальция и твердый раствор оксидов титана и РЗЭ, имеющий состав Ti(РЗЭx)О(2+1,5x), где 0,174≥x≥ 0,027, при следующем соотношении компонентов, мас. %: карбонат кальция 1-10, твердый раствор оксидов титана и РЗЭ остальное.
Отличительными признаками способа приготовления катализатора являются :
одновременное получение оксигидроксидов титана и РЗЭ путем совместной обработки тетрахлорида титана и хлоридов РЗЭ водным раствором или суспензией щелочного агента;
предварительное введение соединения кальция (карбонат кальция) в водный раствор или суспензию щелочного агента.
Указанные отличительные признаки позволяют получить катализаторную массу в одну стадию.
Получение катализаторов осуществляют следующим образом.
В реактор заливают определенное количество водного раствора или суспензии щелочного агента, в который добавляют карбонат кальция из расчета, чтобы в готовом катализаторе содержалось 1-10 мас.% CaCO3, и при перемешивании в суспензию вводят рассчитанные количества хлоридов РЗЭ и тетрахлорида титана, обеспечивающие нейтрализацию щелочного агента. В качестве хлоридов РЗЭ может быть использована, например, смесь, содержащая хлориды церия, лантана, неодима, празеодима, самария или любой из хлоридов РЗЭ в отдельности.
При взаимодействии хлоридов РЗЭ и тетрахлорида титана со щелочным агентом образуется смесь оксигидроксидов РЗЭ и титана, выпадающих в осадок, и хлорид кальция, растворяющийся в маточнике. Количества TiCl4 и хлоридов РЗЭ берут из расчета, чтобы соотношение (TiO2): (оксиды РЗЭ) в твердом растворе было в пределах (73,7- 94,7) : (5,3 - 26,3).
Полученный осадок, содержащий карбонат кальция, оксигидроксиды титана и РЗЭ, отделяют фильтрацией и промывают водой для удаления хлорида кальция, затем катализаторную массу отделяют фильтрацией, добавляют раствор карбоксиметилцеллюлозы (КМЦ) из расчета 0,5-1,0 мас.% КМЦ на прокаленный катализатор, подсушивают и формуют в виде экструдатов, которые сушат при 110-120oC в течение 2 ч и прокаливают при 450oC в течение 4 ч, или полученную катализаторную массу после фильтрации сушат и прокаливают в тех же условиях, а затем таблетируют.
При совместном осаждении оксигидроксидов титана и РЗЭ по описанному способу происходит равномерное распределение оксигидроксидов РЗЭ в оксигидроксиде титана. Последующие стадии сушки и прокаливания приводят к формированию твердого раствора оксидов титана и РЗЭ, обладающего повышенной активностью в реакциях гидролиза сероорганических соединений. Наличие в составе катализатора 1-10 мас. % карбоната кальция усиливает основные свойства последнего, что также повышает активность в реакциях гидролиза сероорганических соединений. Таблетирование позволяет повысить механическую прочность гранул катализатора по сравнению с экструдатами.
Активность синтезированных образцов катализатора определяют в реакции гидролиза сероуглерода и в реакции Клауса (окисление сероводорода диоксидом серы) на микроимпульсной установке с хроматографическим анализом продуктов реакции. Для проведения опытов навеску катализатора (0,05-0,1 г) с размером зерна 0,25-0,50 мм помещают в стальной микрореактор длиной 70 мм и диаметром 3 мм и прогревают в токе гелия в течение 1 ч.
При определении активности катализаторов в реакции гидролиза сероорганических соединений в реактор микрошприцем вводят смесь жидкостей CS2 : H2O = 1 : 2.
При определении активности катализаторов в реакции Клауса в реактор вводят смесь газов H2O : SO2 = 2 : 1.
Время контакта реагентов с катализатором составляет 0,05-0,25 с, температура в зоне реакции 300oC и 220oC соответственно для реакций гидролиза сероуглерода и окисления сероводорода диоксидом серы. Активность катализаторов выражают в виде константы скорости реакции, рассчитанной по уравнению Хебгуда и Бассета (J. Phys. Chem. 1960, v. 64, p.769). Значение константы скорости реакции рассчитывают как среднее из пяти измерений.
Изобретение иллюстрируется следующими примерами.
Пример 1. В реактор загружают 1710 мл 10 %-ной суспензии гидроксида кальция, в которую добавляют 1 г карбоната кальция, и при перемешивании вводят 7,9 г смеси хлоридов РЗЭ, содержащей, мас.%: церия 55,4, лантана 26,8, неодима 12,2, празеодима 4,8 и самария 0,8, а затем 222,8 г тетрахлорида титана. Полученный осадок отделяют фильтрацией, промывают водой для удаления хлорида кальция, полученную катализаторную массу отделяют фильтрацией, смешивают с 10 мл 10%-ного раствора КМЦ, подсушивают до содержания влаги 40-60 мас.%, формуют в виде экструдатов, сушат при 110-120oC в течение 2 ч и прокаливают при 450oC в течение 4 ч, или осадок отделяют фильтрацией, сушат и прокаливают в условиях, аналогичных описанным выше, а затем таблетируют.
Получают катализатор, содержащий мас. %: 1,0 CaCO3 и 99,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,027)O2,04 при соотношении оксидов титана и РЗЭ, равном 94,7: 5,3.
Пример 2. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1760 мл 10%-ной суспензии гидроксида кальция, в которую добавляют 2 г карбоната кальция, и при перемешивании вводят 29,1 г хлорида церия и 209,1 г тетрахлорида титана.
Получают катализатор, содержащий мас. % : 2,0 CaCO3 и 98,0 твердого раствора оксидов металлов состава Ti(Ce0,054)O2,10 при соотношении оксидов титана и церия равном 89,6 : 10,4.
Пример 3. Катализатор готовят аналогично описанному в примере 2 с той разницей, что в реактор загружают 1445 мл 10%-ного раствора гидроксида аммония и при перемешивании вводят 22,9 г хлорида лантана и 196,4 г тетрахлорида титана.
Получают катализатор, содержащий маc. %: 2,0 CaCO3 и 98,0 твердого раствора оксидов металлов состава Ti(La0,091)O2,14 при соотношении оксидов титана и лантана, равном 84,4 : 15,6.
Пример 4. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1355 мл 10%-ного раствора гидроксида аммония, в который добавляют 3 г карбоната кальция, и при перемешивании вводят 30,2 г смеси хлоридов РЗЭ и 182,4 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 3,0 CaCO3 и 97,0 твердого раствора оксидов металлов состава Тi (РЗЭ0,127O2,19 при соотношении оксидов титана и РЗЭ, равном 79,2 : 20,8.
Пример 5. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1500 мл 10%-ной суспензии гидроксида кальция, в которую добавляют 5 г карбоната кальция, и при перемешивании вводят 23,7 г смеси хлоридов РЗЭ и 179,5 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 5,0 CaCO3 и 95,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,102)O2,15 при соотношении оксидов титана и РЗЭ, равном 79,4 : 16,6.
Пример 6. Катализатор готовят аналогично описанному в примере 2 с той разницей, что в реактор загружают 1588 мл 10%-ной суспензии гидроксида кальция, в которую добавляют 7,5 г карбоната кальция, и при перемешивании вводят 20,6 г хлорида церия, 10,8 г хлорида лантана и 185,5 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 7,5 CaCO3 и 92,5 твердого раствора оксидов металлов состава Ti(РЗЭ0,090)O2,14 при соотношении оксидов титана и РЗЭ, равном 84,4 : 15,6.
Пример 7. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1500 мл 10%-ной суспензии гидроксида кальция, в которую добавляют 10 г карбоната кальция, и при перемешивании вводят 21,0 г смеси хлоридов РЗЭ и 180,5 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 10,0 CaCO3 и 90,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,090)O2,14 при соотношении оксидов титана и РЗЭ, равном 84,4 : 15,6.
Пример 8. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1530 мл 10%-ной суспензии гидроксида кальция и при перемешивании вводят 39,7 г смеси хлоридов РЗЭ и 173,3 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 10,0 CaCO3 и 99,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,173)O2,26 при соотношении оксидов титана и РЗЭ, равном 73,7 : 26,3.
Пример 9. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1520 мл 10%-ной суспензии гидроксида кальция и водят 40 г смеси хлоридов РЗЭ и 172,2 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 1,0 CaCO3 и 99,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,180)O2,27 при соотношении оксидов титана и РЗЭ, равном 73,0 : 27,0.
Пример 10. Катализатор готовят аналогично описанному в примере 4 с той разницей, что в реактор загружают 1744 мл 10%-ной суспензии гидроксида кальция и при перемешивании вводят 7,35, г смеси хлоридов РЗЭ и 219,4 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 3,0 CaCO3 и 97,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,026)O2,38 при соотношении оксидов титана и РЗЭ, равном 95,0 : 5,0.
Пример 11. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1460 мл 10%-ной суспензии гидроксида кальция, в которую добавляют 12,5 г карбоната кальция, и при перемешивании вводят 20,5 г хлоридов РЗЭ и 175,5 г тетрахлорида титана.
Получают катализатор, содержащий мас. %: 12,5 CaCO3 и 87,5 твердого раствора оксидов металлов состава Ti(РЗЭ0,090)O2,13 при соотношении оксидов титана и РЗЭ, равном 84,4 : 15,6.
Пример 12. Катализатор готовят аналогично описанному в примере 1 с той разницей, что в реактор загружают 1665 мл 10%-ной суспензии гидроксида кальция, в которую не добавляют карбонат кальция, и при перемешивании вводят 200 г тетрахлорида титана.
Получают катализатор, содержащий мас.%: 100,0 твердого раствора оксидов металлов состава Ti(РЗЭ0,09)O2,14 при соотношении оксидов титана и РЗЭ, равном 84,4 : 15,6.
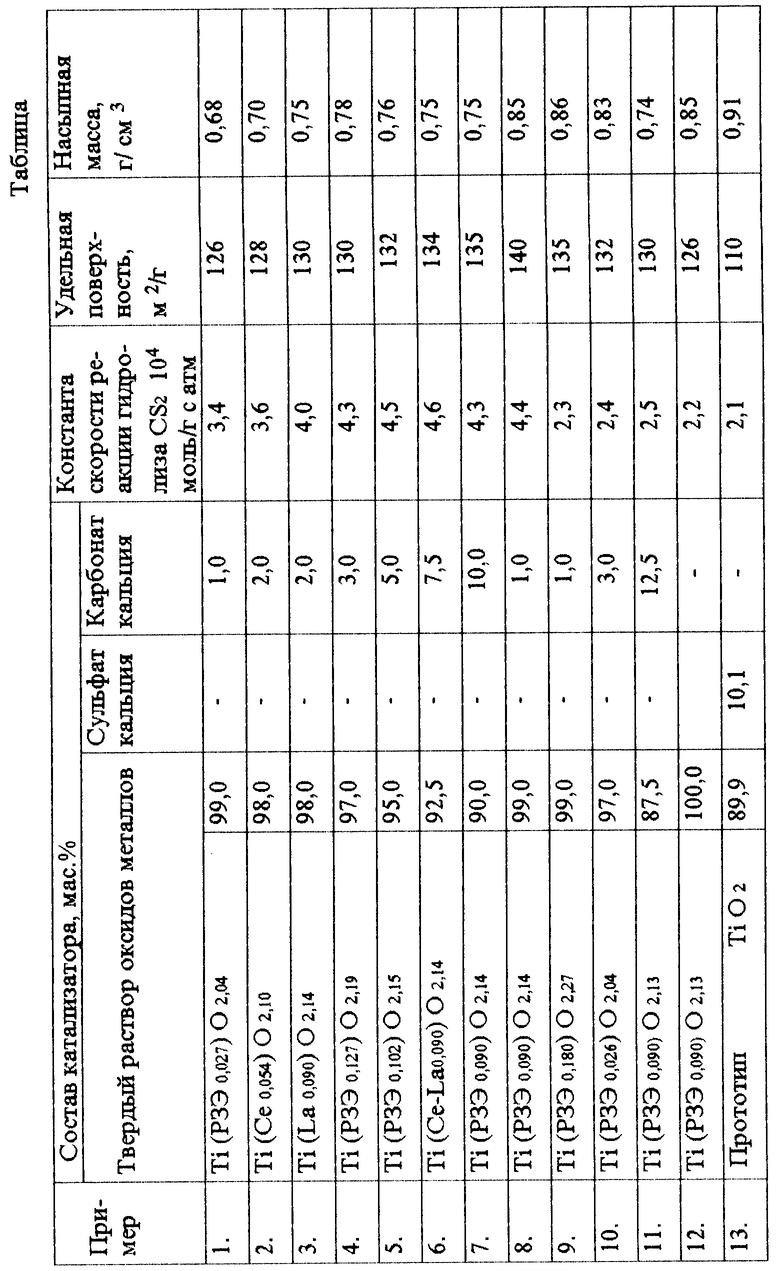
Приведенные в таблице данные по каталитической активности и физико-химическим свойствам катализаторов, приготовленных по описанному способу и прототипу (титаноксидный катализатор марки CRS-31 фирмы Рон-Пуленк, Франция) показывают, что образцы катализатора, полученные по предлагаемому способу, обладают значительно более высокой активностью в реакции гидролиза сероуглерода по сравнению с прототипом. Так, константа скорости реакции гидролиза сероуглерода на предлагаемом катализаторе в 1,6-2,2 раза выше (опыты 1-8) по сравнению с известным катализатором (превращение сероуглерода при температуре 300oC и времени контакта 0,25 с в опытах 1-8 на предлагаемом катализаторе составляет 72-78 %, на катализаторе по прототипу - 48%). В опытах 9-11 активность катализаторов в реакции гидролиза сероуглерода несколько ниже, в связи с тем, что в катализаторах, полученных в опытах 9 и 10, соотношение компонентов в твердом растворе (оксиды титана и РЗЭ) выходит за границы оптимума, а в катализаторе, полученном в опыте 11, содержание CaCO3 выходит за границы оптимума.
Все образцы катализатора, приготовленные описанным способом, обладают более развитой поверхностью по сравнению с прототипом, что способствует повышению их активности в реакции Клауса), обеспечивая термодинамически равновесные выходы целевого продукта, а также высокой термостабильностью (после прокаливания катализаторов при температуре 800oC в течение 8 ч активность практически не снижается).
Приготовленные по описанному способу образцы катализаторной пасты обладают высокой пластичностью, поэтому при формовании катализатора по варианту экструзии получаются гладкие экструдаты, которые после сушки и прокаливания обладают достаточной механической прочностью при относительно низкой насыпной массе (0,68-0,85 кг/л). Механическая прочность катализатора может быть увеличена при использовании варианта формования таблетированием путем подбора оптимального давления прессования, обеспечивающего достаточно высокую прочность и необходимые текстурные характеристики таблеток.
Предлагаемый способ приготовления катализатора по сравнению с прототипом позволяет упростить технологию промышленного производства, снизить стоимость катализатора за счет резкого сокращения количества технологических операций, в частности, сокращения числа и продолжительности стадий сушки и прокаливания, связанных с большими затратами энергии, а также исключить образование и выбросы оксидов азота в окружающую среду в связи с тем, что для приготовления катализатора не используются нитраты.
Использование предлагаемого катализатора в газоперерабатывающей промышленности позволит за счет высокой активности в реакции гидролиза CS2 и COS увеличить выход газовой серы и сократить выбросы диоксида серы в окружающую среду, поскольку не подвергшиеся реакции гидролиза CS2 и COS поступают с хвостовыми газами установки Клауса в термическую печь, где сжигаются с образованием диоксида серы, который выбрасывается в атмосферу.
Изложенное выше, обуславливает получение технического результата, включающего создание катализатора и способа его приготовления.
Технический результат изобретения заключается в более высокой активности предлагаемого катализатора в реакции гидролиза сероорганических соединений по сравнению с прототипом, упрощении способа приготовления катализатора за счет резкого сокращения количества технологических операций и исключении выбросов в окружающую среду оксидов азота.
Литература.
Авторское свидетельство СССР N 1558457, кл. B 01 J 21/06, 1990.
Патент Франции N 2481145, кл. B 01 J 21/06, 1981.
Авторское свидетельство СССР N 2598094, кл. B 01 J 53/36, 1987.
Патент СССР N 1213976, кл. B 01 J 21/06, 1986.5
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ СЕРЫ ПО ПРОЦЕССУ КЛАУСА И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 1995 |
|
RU2076776C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ СЕРЫ ПО ПРОЦЕССУ КЛАУСА И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2000 |
|
RU2176156C2 |
| Каталитическая композиция на основе оксидных соединений титана и алюминия и ее применение | 2021 |
|
RU2775472C1 |
| Катализатор, способ его получения, применение и способ извлечения серы | 2017 |
|
RU2670606C9 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ДИОКСИДА ТИТАНА И ОКСИДА АЛЮМИНИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2015 |
|
RU2574599C1 |
| КАТАЛИЗАТОР ДЛЯ ОБРАБОТКИ ГАЗОВ, СОДЕРЖАЩИХ СЕРНИСТЫЕ СОЕДИНЕНИЯ, И СПОСОБ ОБРАБОТКИ УКАЗАННЫХ ГАЗОВ | 1995 |
|
RU2112595C1 |
| КАТАЛИЗАТОР ДЛЯ УДАЛЕНИЯ СОЕДИНЕНИЙ СЕРЫ ИЗ ПРОМЫШЛЕННЫХ ГАЗОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2280505C1 |
| КАТАЛИЗАТОР ДЛЯ ОБРАБОТКИ ГАЗОВ, СОДЕРЖАЩИХ СОЕДИНЕНИЯ СЕРЫ, И СПОСОБ ОБРАБОТКИ ГАЗА, СОДЕРЖАЩЕГО СОЕДИНЕНИЯ СЕРЫ | 1995 |
|
RU2103058C1 |
| СПОСОБ ОЧИСТКИ ГАЗОВ ОТ МОНООКСИДА УГЛЕРОДА И ОРГАНИЧЕСКИХ ВЕЩЕСТВ | 1991 |
|
RU2080910C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ФОРМОВАННОГО ВАНАДИЙ-ТИТАНОВОГО КАТАЛИЗАТОРА ДЛЯ ОЧИСТКИ ГАЗОВ | 1990 |
|
RU2050194C1 |
Предлагаемое изобретение относится к катализаторам для получения серы по процессу Клауса и способам его приготовления. Катализатор содержит в своем составе, мас.%:CaCO3 и 90-99 твердого раствора оксидов титана и редкоземельных элементов (РЗЭ), имеющий состав Ti(РЗЭx)O(2+1,5х), где 0,174<$E>= >x<$E>=>0,027. Катализатор получают путем одновременной обработки тетрахлорида титана и смеси хлоридов РЗЭ водным раствором или суспензией щелочного агента, в который вводят карбонат кальция, взятый в определенном количестве, с последующими стадиями отделения осадка, его промывки от хлорида кальция, отделения катализаторной массы фильтрацией, формования, сушки и прокаливания, или сушки, прокаливания и таблетирования. Технический результат изобретения заключается в более высокой активности предлагаемого катализатора в гидролизе сероорганических соединений по сравнению с прототипом, упрощении способа приготовления катализатора за счет резкого сокращения количества технологических операций и исключении выбросов в окружающую среду оксидов азота. 2 с.п. ф-лы, 1 табл.
Карбонат кальция 1 10
Твердый раствор оксидов титана и РЗЭ, соответствующий составу Ti(РЗЭх)О2+1,5х, где 0,174 ≥ x ≥ 0,027 Остальное
2. Способ приготовления катализатора для получения серы по процессу Клауса, включающий получение оксигидроксида титана обработкой тетрахлорида титана водным раствором щелочного агента, формование, сушку и прокаливание, отличающийся тем, что одновременно с получением оксигидроксида титана получают оксигидроксиды редкоземельных элементов (РЗЭ) путем совместной обработки тетрахлорида титана и хлоридов РЗЭ водным раствором или суспензией щелочного агента, в которые вводят карбонат кальция, взятый из расчета, чтобы его содержание в готовом катализаторе составляло 1 10 мас. количества тетрахлорида титана и хлоридов РЗЭ берут из расчета, чтобы соотношение оксидов титана и РЗЭ в твердом растворе было в пределах 73,7 94,7 5,3 26,3, и процесс ведут при соотношении компонентов, обеспечивающих следующее содержание в катализаторе, мас.
Карбонат кальция 1 10
Твердый раствор оксидов титана и РЗЭ, соответствующий составу Ti(РЗЭх)О2+1,5x, где 0,174 ≥ x ≥ 0,027 Остальноеа
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| SU, авторское свидетельство, 1558457, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| FR, патент, 2481145, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| FR, патент, 2598094, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| SU, патент, 1213976, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1998-01-27—Публикация
1996-07-08—Подача