2-Алкокси-2-тио-5-(N-фенилкарбамоил)-6-Метил-1,4,2 -оксатиафосфорины
Изобретение относится к химии фосфорорганических соединений, в частности к новым фосфорсодержащим гетероциклическим соединениям 2-алкокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиафосфоринам общей формулы
где
R CH3 (I), C2H5 (II), i-C3H7 (III)
Соединения I III обладают биологической активностью и могут быть использованы в сельском хозяйстве, преимущественно в качестве протравителей семян.
Указанные соединения могут быть получены из легко доступного дитиадифосфетидина в результате ряда последовательных превращений: алкоголиза, алкилирования промежуточно образующейся триэтиламинной соли хлорметил-0-этилдитиофосфоновой кислоты анилидом α -хлорацетоуксусной кислоты и последующей циклизации под действием основания полученного анилида a -(0-этил-хлорметилтиофосфонилтио)ацетоуксусной кислоты, сопровождающейся 1,4- S, O миграцией фосфорильной группы. Перечисленная последовательность превращений представлена на следующей схеме: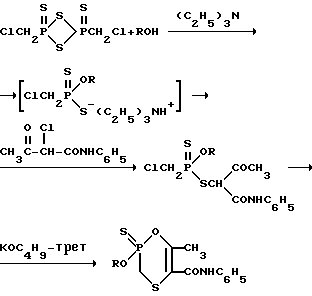
R имеет вышеуказанные значения.
Строение полученных соединений подтверждено элементным анализом и данными ПМР- и ЯМР-спектров.
Биологическая активность оценивалась в полевых условиях опытах на примере соединения II, условно названного "фоскарбоксин". Испытания показали, что фоскарбоксин, кроме фунгицидного действия на патогенов, оказывает положительное влияние на развитие корневой системы и рост надземной части проростка. Молодые растения более интенсивно формировали корневую систему. Длина главного корешка на ячмене в варианте с фоскарбоксином на 25 30% больше, чем в варианте с этанолом. Это способствовало лучшему поглощению питательных веществ. Длина проростков при испытаниях на ячмене была на 50% выше по сравнению с эталоном. Обнаружено также, что препарат оказывает благоприятное действие на факторы роста, обуславливающие урожай, например формирование боковых побегов и густоту стояния растений. Густота стояния растений в варианте с фоскарбоксином был на 24 50% выше, чем в контроле (без обработки семян) и на 9 40% выше, чем в вариантах с эталонами. Коэффициент кущения в посевах ячменя был в 2 раза больше, чем в контроле и в 1,5 раза больше, чем в вариантах с эталонами.
Фоскарбоксин в норме расхода 1,0 и 1,5 кг действующего вещества на тонну семян превосходил эталоны по активности против пыльной головни на 20 23% против корневых гнилей на 30 40% и по прибавкам урожайности на 4 5 ц/га.
Соединения I III являются малотоксичными для теплокровных животных: LD50 при испытании на мышах > 2000 мг/кг.
Ассортимент фосфорорганических пестицидов, в том числе производных тиофосфорной и тиофосфоновой кислот, обладающих разнообразными видами активности, чрезвычайно велик. В этом смысле уместно сослаться на один из обзоров, например, В. К. Промоненкова и др. опубликованных в сборнике "Итоги науки и техники", серия Органическая химия, т. 8 под ред. М.И. Кабачника. - М. ВИНИТИ, 1989, с. 3, а также на монографию Мельникова Н.Н. Пестициды. -М. Химия, 1987, с. 400.
Что касается гетероциклических фосфорсодержащих соединений, то среди них также известно достаточно много соединений с пестицидной активностью, например инсектицид салитион 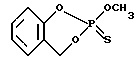 [1]
[1]
Известны фосфорсодержащие гетероциклические соединения, в том числе замещенные 1,3,2-оксатиафосфоринаны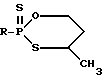
где
R CH3 и C2H5 и другие,
обладающие активностью против членистоногих и нематод [2]
В [3] описан замещенный 1,3,2-оксазафосфоринан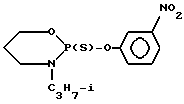
проявляющий активность против галловых нематод.
Наиболее близкие структурные аналоги, а именно оксатиафосфорины, имеющие формулу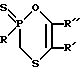
где
R C2H5O, R'-H, R''-трет-C4H9;
R-(C2H5)2N, R'-H, R''-2,4,5-Cl3C6H2;
R-C2H5O, R'-COOC2H5, R''-CH3,
и другие описаны в [4]
Проведенные биологические испытания не выявили, однако, среди них перспективных для дальнейшей разработки препаратов.
Другим структурным и одновременно функциональным аналогом соединений, обозначенных как объект настоящего изобретения является широко известный 2,3-дигидро-6-метил-5-фенил-1,4-оксатинин(карбоксин) действующее вещество препарата витавакс (Uniroyal) и ряда других препаратов.
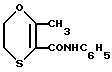
содержащий в цикле вместо фосфорорганического фрагмента углеводородный [1, с. 251]
По биологической активности соединения I III оказались близкими именно к карбоксину. Поэтому препараты на его основе были взяты в качестве эталонов. Как показали испытания, вновь синтезированные соединения имеют определенные преимущества по сравнению с известными, о чем уже было упомянуто выше.
Пример 1. 2-Хлорметилэтокситиофосфонилтиоацетоацетанилид.
К суспензии 2,89 г (0,01 моль) бис-хлорметилдитиодифосфетидина в 10 мл абсолютного бензола добавили раствор 2,02 г (0,02 моль) триэтиламина, 5 мл этилового спирта в 10 мл абсолютного бензола. Смесь перемешивали в течение 30 мин при 20oC, а затем добавили 4,23 г (0,02 моль) 2-хлорацетоацетанилида, реакционную массу оставили на ночь, осадок солянокислого триэтиламина отфильтровали, растворитель удалили в вакууме. Остаток очищали методом колоночной хроматографии на силикагеле, растворитель-петролейный эфир-этилацетат, 8: 1. Получили 4,2 г 2-хлорметилэтокситиофосфонилтиоацетоацетанилида. Выход 58% Tпл 70oC.
Найдено, N 3,54; S 17,23;
C13H17ClNO3O3PS2.
Вычислено, N 3,83; S 17,53.
Пример 2. 2-Этокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиафосфорин (II).
К суспензии 1,24 г (0,011 моль) трет-бутилата калия в ТГФ по каплям добавили 4,05 г (0,011 моль) 2-хлорметилэтокситиофосфонилтиоацетоацетанилида в ТГФ при 5oC и перемешивали 5 ч. при 20oC, осадок отфильтровали, растворитель удалили в вакууме. Остаток кристаллизовали из гексана с этилацетатом.
Получили 2,7 г 2-этокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиофосфорина. Выход 75% Tпл 110 112oC.
Найдено, C 47,13; H 4,86; N 3,78; P 9,76.
C13H16NO3PS2
Вычислено, C 47,40; H 4,00; N 4,25; P 9,40.
Аналогично получены соединения I и III.
2-Метокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиафосфорин (I). Выход 20% Tпл 119 120oC.
Найдено, C 45,46; H 4,19; P 9,70; S 20,32.
C12H14NO3PS2.
Вычислено, C 45,70; H 4,47; P 9,82, S 20,33.
2-Изопропокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиафосфорин (III). Выход 80% Tпл 82 84oC.
Найдено, N 3,85; P 9,35; S 19,17.
C14H18NO3PS2.
Вычислено N 4,08; P 9,02; S 18,67.
В спектрах ПМР соединений I III, наряду с сигналами протонов алкоксильных групп у атома фосфора, наблюдались сигналы протонов метильной группы в области 2,15 м.д. в области 9,4 м.д. имелись сигналы NH-протонов, а в области 7,1 7,7 м.д. ароматические протоны. Неэквивалентные метиленовые протоны гетерокольца проявлялись в области 3,30 3,53 м.д. в виде ABX системы (JHH 14,8; JPH 11,0; JPH 2,2 Гц). В спектрах ЯМР 31P в области 83,0 м.д. характерной для эфиров тиофосфоновых кислот, наблюдался синглетный сигнал, в то время как для исходных дитиофосфонатов был расположен в более слабом поле ( δp 95 м.д.).
Пример 3. Биологическая и хозяйственная эффективность фоскарбоксина в качестве протравителя семян зерновых культур.
Методика проведения испытаний.
Полевые опыты проводились в Московской области на яровом ячмене сорта Московский-3 против пыльной головни (Ustilago nuda, U. nigra) и корневых гнилей, вызываемых грибами рода Helminthosporium (H. Sativum, H. teres) и Fusarium spp. Опыты проводились по общепринятой методике НИИХСЗР (методическое руководство по проведению теплично-полевых испытаний протравителей семян, фунгицидов и бактерицидов, Черкассы, 1996).
Фоскарбоксин испытывался в норме расхода 1,0 и 1,5 кг/т семян по действующему веществу (д.в.)
В качестве этанола были взяты витавакс (карбоксин) и фенокс (карбоксин) в норме расхода 1,5 кг/т семян по д.в. витатиурам (карбоксин + тирам) 1,6 кг/т семян по д.в.
Урожай убирали методом пробного снопа. В каждом варианте для анализа урожайности использовали 5 снопов с площади 0,5 м2.
Перед протравлением семена анализировали на зараженность возбудителями семенной инфекции по общепринятой методике. В результате выявлен следующий состав патогенного комплекса,
Bipolaris spp. 14
Fusarium spp. 14
Penicillium spp. 5
Бактериозы 3.
Результаты испытаний приведены в табл. 1 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФУНГИЦИДНЫЙ СОСТАВ | 1992 |
|
RU2032344C1 |
| ФУНГИЦИДНЫЙ СИНЕРГИТИЧЕСКИЙ СОСТАВ | 1992 |
|
RU2030153C1 |
| N-( α -АЛКОКСИАЛКИЛ)КАПРОЛАКТАМЫ, ОБЛАДАЮЩИЕ ИНСЕКТОРЕПЕЛЛЕНТНОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2017731C1 |
| ГИДРОХЛОРИД ЕНОЛА 2-ПИНАКОЛИЛТИО-4(5)-МЕТИЛИМИДАЗОЛИНА-2, ОБЛАДАЮЩИЙ РОСТРЕГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2010793C1 |
| 2-ДИМЕТИЛАМИНО-1,3-БИС-(ДИАЛКОКСИДИТИОФОСФОРИЛТИО)ПРОПАНЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ АКТИВНОСТЬЮ | 1988 |
|
SU1612550A1 |
| ДИЭТИЛЭТАНОЛАММОНИЕВАЯ СОЛЬ 2-МЕТОКСИКАРБОНИЛ -N-[(4-МЕТОКСИ -6-ФТОР- 1,3- ПИРИМИДИН-2-ИЛ) АМИНОКАРБОНИЛ] -БЕНЗОЛСУЛЬФАМИДА, ОБЛАДАЮЩАЯ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ, И ГЕРБИЦИДНЫЙ СОСТАВ НА ЕЕ ОСНОВЕ | 1992 |
|
RU2043345C1 |
| ПРОИЗВОДНЫЕ N-[4-(1-ГИДРОКСИ-1-ТРИФТОРМЕТИЛ-2,2,2-ТРИФТОРЭТИЛ)ФЕНИЛ]МОЧЕВИНЫ, ОБЛАДАЮЩИЕ АНТИДОТНОЙ АКТИВНОСТЬЮ К 2-ХЛОР-N-[(4-МЕТОКСИ-6-МЕТИЛ-1,3,5-ТРИАЗИН-2-ИЛ)АМИНОКАРБОНИЛ] БЕНЗОЛСУЛЬФАМИДУ В ПОСЕВАХ ЛЬНА | 1991 |
|
SU1825496A3 |
| ТРАНС-4,5-ДИАЗИДОИМИДАЗОЛИДИН-2-ОН, ПРОЯВЛЯЮЩИЙ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 1993 |
|
RU2034838C1 |
| N-[4-2'-ГИДРОКСИГЕКСАФТОРИЗОПРОПИЛ)ФЕНИЛ] -N-ЭТИЛ-N'-ФЕНИЛМОЧЕВИНА, ОБЛАДАЮЩАЯ РОСТРЕГУЛИРУЮЩИМ И АНТИДОТНЫМ ДЕЙСТВИЕМ | 1990 |
|
RU1743153C |
| 1-(2,4-Дихлорфенокси)-2-формамидо-3,3-диметилбутан, обладающий фунгицидной активностью | 1988 |
|
SU1775395A1 |



Использование: в сельском хозяйстве в качестве протравителей семян. Сущность изобретения: продукты 2-алкокси-2 тио-5- (N-фенилкарбамоил)-6 метил-1,4,2-оксатиафосфорины ф-лы
где R - CH3, C2H5, изо-C3H7, 4 табл.
2-Алкокси-2-тио-5-(N-фенилкарбамоил)-6-метил-1,4,2-оксатиафосфорины общей формулы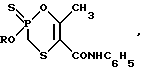
где R CH3 (I); C2H5 (II); i C3H7 (III).
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Мельников Н.Н | |||
| и др | |||
| Справочник | |||
| Пестициды и регуляторы роста растений | |||
| -М.: Химия, 1995, с.251, 368 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US, патент, 4695563, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RU, патент, 2053235, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
1998-02-27—Публикация
1996-09-11—Подача