Изобретение относится к биотехнологии, а именно к производству лекарственных препаратов из животного сырья, и может найти применение в производстве препаратов иммуностимулирующего и радиопротективного действия.
В настоящее время в лечебной практике используются иммуностимуляторы бактериальной природы (продигиозан, сальмозан и т.д.) [1], и широкий спектр препаратов из тимуса (тимозин, тимоген, T-активин и т.д.) [2 - 4].
Недостатком таких препаратов является многостадийность и сложность производства, использование импортных реактивов и оборудования, использование токсичных и огнеопасных реактивов. К тому же иммуностимуляторы бактериальной природы имеют широкий спектр противопоказаний и побочных действий (развитие аллергических реакций, болезненность и отеки в месте введения и т.д.).
Одним из источников получения препаратов иммуностимулирующего и радиопротективного действия могут служить эмбрионы птиц. В этом случае положительным моментом является доступность, дешевизна и экологическая чистота сырьевых ресурсов.
Известны способы получения субстанций, обладающих иммунологической активностью, из эмбриональных тканей животных и птиц [5 - 8]. Однако во всех этих работах были использованы неочищенные тканевые экстракты и говорить о применении результатов данных работ в практике не приходится.
Анализ литературы показал, что способ получения из эмбрионов птиц биологически активных веществ, а именно нуклеопротеидных комплексов, обладающих иммунотропной и радиопротективной активностью, ранее не описан.
Технический задачей изобретения является разработка способа получения нуклеотидных комплексов из эмбрионов птиц, обладающих иммунотропной и радиопротективной активностью.
Способ осуществляется следующим образом. Эмбрионы птиц извлекают из оболочки и отмывают в 0,15 М NaCl от следов крови. К отмытым эмбрионам приливают равный объем 0,15 M NaCl и гомогенизируют в размельчителе тканей в течение 1 мин при скорости ножей 8000 об/мин.Гомогенат центрифугируют на холоду при 4000g в течение 15-20 мин.Супернатант пропускают через полые волокна из полиамида с верхним пределом селективности 50 kDa. Ультрафильтрат собирают и пропускают через полые волокна из полиамида с верхним пределом селективности 5 kDa. Концентрат, представляющий собой целевую фракцию, центрифугируют для отделения денатурировавших белков, и лиофильно высушивают. Из 100 эмбрионов получают 350 доз препарата.
В биологическом плане целевой продукт обладает широким комплексом свойств, проявляющихся уже в дозе 0,01 мг/кг веса; стимулирует фагоцитоз и гуморальный иммунитет; способствует восстановлению иммунитета, подавленного химическим путем, а также восстановлению иммунореактивности подопытных животных, подвергнутых рентгеновскому облучению.
Способ иллюстрируется следующими примерами.
Пример 1. Введение нуклеопротеидных комплексов.
100 яиц с эмбрионами птиц (куры, перепела и т.д.), полученные из инкубатора, протирают спиртом, извлекают эмбрионы и трижды промывают 250 мл 0,15 М NaCl. К отмытым эмбрионам приливают равный объем 0,15 М NaCl (обычно 60 - 65 мл) и гомогенизируют в размельчителе тканей в течение 1 мин при скорости ножей 8000 об/мин. Гомогенат центрифугируют на холоду при 4000g в течение 15 - 20 мин. Супернатант объемом 120 - 130 мл пропускают через полые волокна из полиамида с верхним пределом селективности 50 kDa. Для этого используют установку УПЛ-0,1 производства г. Кириши или аналогичную. Давление и скорость потока устанавливают согласно паспортным данным установки. Ультрафильтрат в объеме 100 - 110 мл собирают и пропускают через полые волокна из полиамида с верхним пределом селективности 5 kDa. Концентрат, представляющий собой целевую фракцию в объеме 25 мл, центрифугируют для отделения денатурировавших белков, и лиофильно высушивают. Для получения лекарственной формы препарат подвергают стерилизующей фильтрации, розливу согласно дозе,и высушиванию стандартными методами, предусмотренными для лекарственных препаратов.Из 100 эмбрионов получают 350 доз препарата иммуностимулирующего радиопротективного и противоопухолевого действия.
Специфическая активность целевой фракции иллюстрируется следующими примерами.
Иммуностимулирующая активность.
Пример 2.Исследование фагоцитозстимулирующей активности.
Эксперименты проводят на белых беспородных мышах линии С 57 В 1/6 (самцы массой 20-24 г). Целевую фракцию вводят внутрибрюшинно в различных дозах.В разные сроки после введения проводят исследования состояния фагоцитарного зве на неспецифической защиты.С этой целью определяют фагоцитарную активность и фагоцитарный индекс.
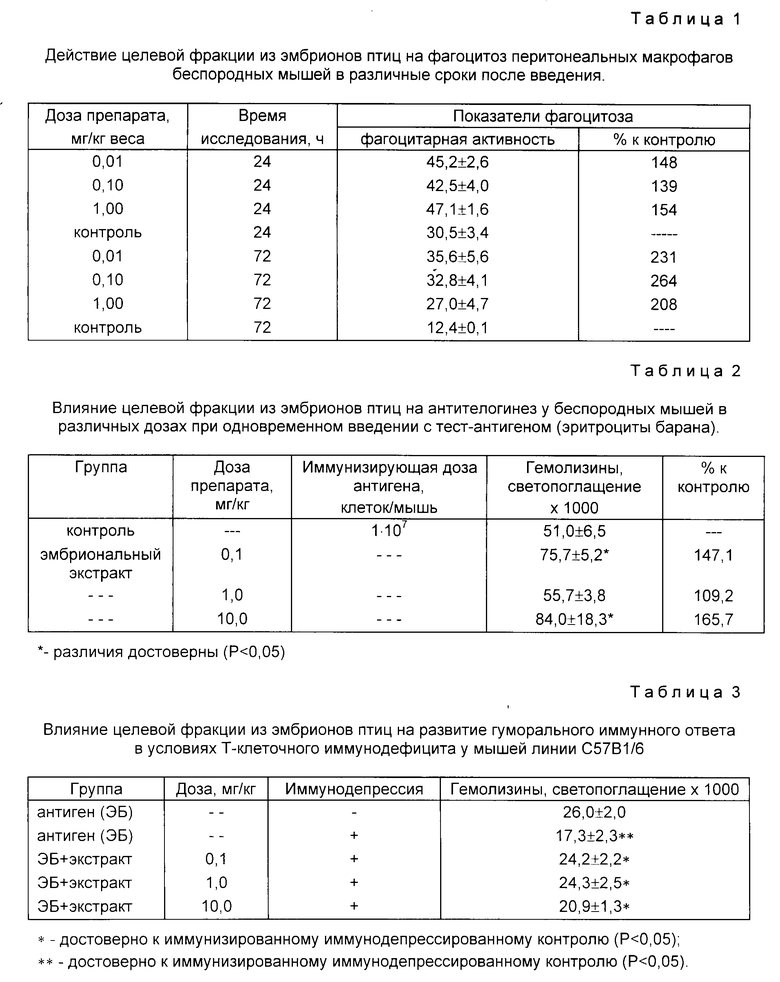
Данные по фагоцитозстимулирующей активности приведены в табл.1.
Из данных табл.1 видно, что целевая фракция оказывает стимулирующие действие на фагоцитоз перитонеальных макрофагов в дозе 0,01 - 1,0 мг/кг веса, сохраняющееся в течение 72 ч после введения.
Пример 3. Исследование антителогенезстимулирующей активности препарата.
Влияние целевой фракции на гуморальный иммунный ответ оценивают при одновременном внутрибрюшинном введении препарата и тест-антигена (эритроциты барана) в дозе 1 • 107 клеток/мышь белым беспородным мышкам массой 20 - 25 г.
Показано стимулирующее действие целевой фракции в дозах 0,10 - 10 кг общего белка на 1 кг массы тела (табл. 2).
Пример 4. Исследование антителогенезстимулирующей активности препарата в условиях T-клеточного иммунодефицита.
Влияние целевой фракции на гуморальный иммунный ответ в условиях T-клеточного иммунодефицита оценивают при одновременном внутрибрюшинном введении препарата и тест-антигена (эритроциты барана) в дозе 1 • 107 клеток/мышь белым беспородным мышам массой 20 - 25 г на фоне предварительного введения гидрокортизона.
Показано, что введение целевой фракции способствует восстановлению подавленного иммунитета при введении его в дозах 0,1 - 10 мг/кг (табл. 3).
Пример 5. Исследование радиопротективной активности.
Влияние целевой фракции на гуморальный иммунный ответ у иммунодепрессированных рентгеновским излучением в дозе 4 Гр подопытных животных оценивают при одновременном внутрибрюшинном введении препарата и тест-антигена (эритроциты барана) в дозе 1 • 107 клеток/мышь белым беспородным мышам массой 20 - 25 г.
Показано, что введение целевой фракции в дозе 1 мг/кг способствует восстановлению иммунореактивности иммунодепрессированных рентгеновским излучением подопытных животных (табл.4).
Из описания видно, что предлагаемый способ позволяет получать целевой продукт, обладающий широким спектром биологических свойств, проявляющихся уже в дозе 0,01 мг/кг веса:
- стимулирует фагоцитоз;
- стимулирует гуморальный иммунитет;
- способствует восстановлению подавленного химическим путем иммунитета;
- способствует восстановлению иммунореактивности иммунодепрессированных рентгеновским излучением подопытных животных.
Приведенные данные наглядно свидетельствуют о иммунокоррегирующей активности полученного препарата, что позволяет предполагать вероятные области его применения. Во-первых, в терапии врожденных и приобретенных иммунодепрессий и иммунодефицитов. Во-вторых, в терапии инфекционных заболеваний человека и животных, сопровождающихся нарушением иммунного статуса. В-третьих, в качестве адъюванта при вакцинировании.
Список литературы:
1. Растунова Г.А., Щербакова Э.Г., Круглова И.С. Продигиозан как активатор перитонеальных макрофагов. Антибиотики, 1981, N 6, с. 524 - 544.
2. Klein J.J., Goldstein A.L., White A. Proc. Nat. Acad. Sci., 1965, N 53, p. 812 - 817.
3. Low T.L.K., Goldstein A.L. Sprinder Semin. Immunopathol., 1979, N 2, p. 169 - 186.
4. Thurman G.B., Ahmed A., Strong D.M. et al. Transplant. Proc., 1975, N 7, p. 299 - 312
5. Полежаев Л.П. Утрата и восстановление регенерационной способности органов и тканей у животных. - М.: 1968, с. 275.
6. Донецкий Д. Современные вопросы частной хирургии. - М.: 1986, с. 173 - 174.
7. Глухенький Б. Врачебное дело. 1984, N 6, с. 93 - 94.
8. Топор Б. Возможности активации репаративного остеогенеза у онкологических больных. В кн.: VIII Республиканская конференция онкологов Молдавии. Кишинев, 1989, с. 222 - 223.

Способ получения нуклеопротеидных комплексов из эмбрионов птиц, обладающих иммунотропной и радиопротективной активностью, включает отмывание и гомогенизацию эмбрионов птиц в 0,15 М NaCl, центрифугирование на холоду и очистку на полиамидных полых волокнах с верхними пределами селективности 50 и 5 kDa. 4 табл.
Способ получения нуклеопротеидных комплексов из эмбрионов птиц, обладающих иммунотропной и радиопротективной активностью, заключающийся в том, что отмывание и гомогенизацию эмбрионов проводят в 0,15 М NaCl, гомогенат центрифугируют на холоду в течение 15 - 20 мин, полученный супернатант пропускают последовательно через полиамидные полые волокна с верхними пределами селективности 50 KDa и 5KDa, а концентрат, представляющий собой целевую фракцию, центрифугируют и лиофильно высушивают.
Авторы
Даты
1998-05-10—Публикация
1995-06-30—Подача