Изобретение относится к медицине, точнее к гемостазиологии и фармакологии, а именно к способам получения биологически активных препаратов, способных найти применение в клинической и экспериментальной областях медицины в качестве тромболитического препарата.
В настоящее время известно значительное число биологически активных веществ, обладающих фибринолитической, тромболитической активностью, полученных из различных природных источников (US, N 4873222, 1989; PCT N 870050, 1987; US, N 3743722; US, N 3819605, 1974) или синтетическим путем (US, N 4861865). Действие одних из них направлено на активацию плазминогена в плазмин, другие обладают собственной фибринолитической активностью. К последним принадлежит препарат гементин, выделяемый из слюнных желез пиявки Haementeria ghilianii (US, N 4390630, 1983; ЕП N 0346894, 1989).
В последние годы обнаружен принципиально новый механизм фибринолиза и тромболизиса, который обеспечивает растворение твердого стабилизированного фибрина. Этот механизм предполагает гидролиз ε-(γ-Glu)-Lys-изопептидных связей, образующих поперечные сшивки или cross-links между отдельными полипептидными цепями в стабилизированном фибрине. Этот механизм стимулируется ферментом дестабилазой - эндо-ε-(γ-Glu)-Lys-изопептидазой из медицинской пиявки Hirudo medicinalis (Baskova I. P., Nikonov G.I. Biokchimyia, 1985, p. 424).
На сегодняшний день известны еще два препарата из пиявки Hirudo medicinalis, обладающие изопептидазной функцией:
а). Фибрин-изопептидаза с мол.м. 15000 ± 1000 Дальтон (решение о выдаче патента по заявке 5000191/13 от 5.07.93). Выделение фермента из медицинской пиявки включает фракционирование сульфатом аммония, очистку методами анионообменной (носитель DEAE-Toyopearl) и катионообменной (носитель - CM-Toyopearl) хроматографии и гель-фильтрации.
б). Фермент, растворяющий кровяные сгустки с мол. м. 57000 Дальтон (патент PCT 091/08233, 1991, DE, 3939801, 1991).
Выделение фермента из секрета слюнных желез медицинской пиявки Hirudo medicinalis включает поэтапную хроматографическую очистку с использованием катионообменника в присутствии детергента твин 80, аффинную хроматографию на конканавалине-A, очистку с помощью хелата меди и HPLC-катионообменную хроматографию на моно-S.
Однако ни для одного из этих препаратов не описана тромболитическая активность, хотя один из известных препаратов называется "ферментом, растворяющим кровяные сгустки" (патент PCT 091/08233, 1991).
Задачей предлагаемого изобретения является разработка эффективного способа получения фермента дестабилазы, обладающего не только амидолитической, экзо- и эндоизопептидазной активностями, но также выраженными тромболитическими свойствами и отличающегося по молекулярной массе и аминокислотной последовательности.
Поставленная задача получения фермента дестабилазы осуществляется следующим образом.
Экстракт из пиявки семейства Hirudinidae подвергают аффинной хроматографии, которую проводят на колонке с иммобилизованными на сефарозе-4B антителами к дестабилазе. Колонку уравновешивают 0,02 М трис-HCl буферным раствором, pH 7,4; буферным раствором отмывают несвязавшийся белок и элюируют дестабилазу тем же буферным раствором, содержащим 0,3 M NaCl. Полученный препарат вновь хроматографируют на колонке с KM-трисакриловом сорбентом, уравновешенной 0,02 M трис-HCl буферным раствором, pH 7,4. Элюируют целевой продукт 0,05 - 0,20 M NaCl, растворенном в том же 0,02 M трис-HCl буферном растворе. Фракции, содержащие конечный продукт, собирают, обессоливают гель-фильтрацией на суперозе-12 и лиофилизируют. В результате полученный препарат содержит 100% активного вещества. Степень чистоты подтверждена электрофоретически.
Способ получения фермента дестабилазы иллюстрируется следующими конкретными примерами его выполнения.
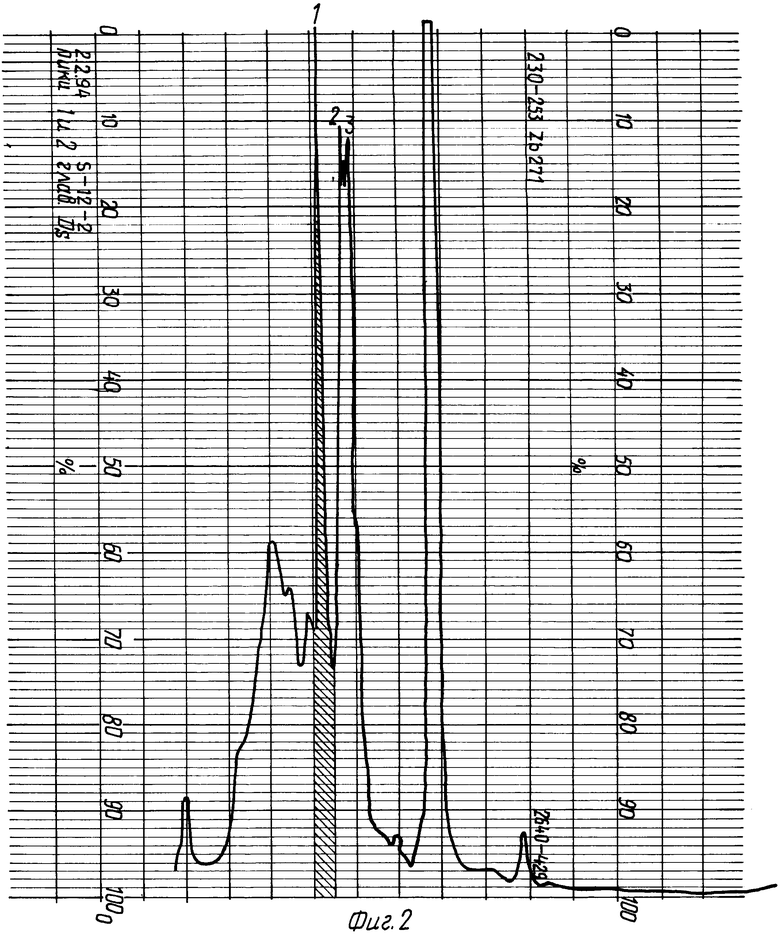
Пример 1. Медицинскую пиявку, голодавшую не менее трех месяцев, пропускают через мясорубку и экстрагируют физиологическим раствором. Экстракт наносят на колонку с сефарозой-4B с иммобилизованными на ней антителами к дестабилазе, уравновешенную 0,02 M трис-HCl буферным раствором pH 7,4. Фермент элюируют 0,3 M NaCl, растворенным в 0,02 M трис-HCl буферном растворе pH 7,4, фракции объединяют; полученный раствор (8 мл, концентрация белка 0,5 мг/мл) наносят на колонку с KM-трис-акриловым сорбентом, уравновешенную 0,02 М трис-HCl буферным раствором, pH 7,4. Фермент дестабилаза элюировалась при градиенте NaCl 0,05 - 0,20 М (фиг. 1). Обессоливание проводят гель-фильтрацией на суперозе-12. О месте расположения пика, соответствующего дестабилазе, судят по амидолитической активности фракций (субстрат L-γ-Glu-pNA), которая соответствует 3•10 kat/mg (фиг. 2). На фиг. 1, 2 штриховка - активность дестабилазы.
Способ позволяет очистить фермент в 2400 раз. Выход белка составляет 0,1% от исходно взятой белковой смеси. Гомогенность препарата подтверждена методом электрофореза в геле полиакриламида.
Пример 2. Пиявок из семейства Hirudinidae, голодавших не менее четырех месяцев, измельчают и экстрагируют физиологическим раствором. Экстракт наносят на колонку с агарозой-6B иммобилизованными на ней антителами к дестабилазе, уравновешенной 0,02 М трис-HCl буферным раствором pH 7,2. Дестабилазу элюируют 0,2 М NaCl, растворенном в 0,02 М трис-HCl буферном растворе pH 7,2. Фракции, обладающие ферментативной активностью, объединяют и пропускают через колонку с DEAE-сефадексом A-50, уравновешенную 0,02 М трис-HCl буферным раствором pH 7,2. Полученные фракции наносят на колонку с KM-целлюлозой и элюируют буферным раствором 0,02 М трис-HCl pH 6,5 в градиент NaCl от 0,1 до 0,3 М.
Фракции, обладающие ферментативной активностью, объединяют, обессоливают гель-фильтрацией через сефадекс Г-25.
В результате очистка достигается в 2500 раз. Конечная амидолитическая активность дестабилазы (субстрат L-γ-Glu-pNA) составляет 7 • 10 - 9 kat/mg.
Выход белка - 0,12% от исходного содержания белковой смеси. Гомогенность фермента подтверждена методом электрофореза в геле полиакриламида.
В результате изучения первичной структуры, физико-химических, кинетических свойств нового фермента-дестабилазы получены следующие характеристики, позволяющие его идентифицировать.
УФ-спектр - характерный максимум поглощения при λ = 278 нм.
Молекулярная масса - мол.м. мономера - дестабилазы 12600 ± 300 Дальтон. Определена методом высокоэффективной гель-фильтрации на колонке супероза-12 (0,02 М трис-HCl, pH 7,0) и градиентного электрофореза в 4 - 16% ПААГ с 1% SDS.
Изопептидазная активность. Изопептидазную активность определяют по способности фермента гидролизовать изопептидные связи в природном субстрате - продукте ограниченного протеолиза стабилизированного фибрина, димере его D-фрагмента (D-димер), в котором сохранены изопептидные связи между γ-γ-цепями фибрина (Завалова Л.Л. и др. Биохимия. т. 56, 1991, с. 115-124). С этой целью 0,1 - 2,0 мкг фермента инкубируют с 50 мкг D-димера в 0,02 М трис-HCl буферном растворе, pH 8,0 в течение 10-70 ч. Общий объем инкубационной смеси - 100 мкл. В результате реакции наблюдают гидролиз изопептидной связи в D-димере и образование D--мономеров, за накоплением которых следят с помощью метода электрофореза в ПААГ. Установлено, что новый белок вызывает растворение сгустков стабилизированного фибрина, гидролизует γ-Glu-ε-Lys-изопептидные связи в димере фрагмента D и в диизопептиде γ-Glu-ε-Lys.
Амидолитическая активность. Амидолитическую активность фермента определяют по его способности гидролизовать амидную связь в γ-Glu-pNA с образованием p-нитроанилина по методу Басковой И.П. и др. (Биохимия, 1990, т. 55, с. 674 - 679). Для этого 10-100 мкл раствора фермента прибавляют к пробе, содержащей 0,02 М трис-HCl буферного раствора, pH 8,0 и 0,05 мг/мл γ-Glu-pNA в общем объеме 0,5 мл и инкубируют 5-30 мин при 25oC. За развитием реакции следят спектрофотометрически при длине волны 405 нм.
Установлено, что новый фермент гидролизует амидные связи в γ-Glu-данзилкадаверине и в низкомолекулярных субстратах трипсина и химотрипсина, содержащих в положении P1 основную или гидрофобную аминокислоту.
Термостабильность. Фермент сохраняет активность при 22 - 37oC в течение 80 ч, при 7oC - в течение 15 дней, при 75oC - в течение 15 мин.
Диапазон pH-стабильности. Сохраняет активность в диапазоне pH 4,5 - 8,5 (при 37oC в течение 7 дней, субстрат γ-Glu-pNA).
Первичная структура. Для идентификации первичной структуры фермент хроматографируют на обращенно-фазовой колонке с Agmapoke RP-300 (4,6 • 100) в градиенте ацетонитрила от 0 до 60% за 1 мин. Определяют N-концевую аминокислотную последовательность дестабилазы. Идентифицирован 41 аминокислотный остаток. В качестве N-концевой аминокислоты определен треонин. Затем проводят CNBr-гидролиз дестабилазы и полученную смесь вновь хроматографируют на той же колонке в тех же условиях. В результате получены четыре пептидных фрагмента со следующими частичными аминокислотными кислотными последовательностями:
1. Thr Val-Ser-XLeu--Ile--Val-GluX---Ile Gly--Gly-.
2. -Ala Gly Ser Leu--Gly---Ile----Ile-Gly--Gly Gly-Gln.
3. ---Ala--X-Gly Gly--Pro Thr X---Ala-Ile---.
4. Gly Pro-Gly X-Ser Leu--.
В результате гидролиза фермента глутаминовой протеазой выделен фрагмент: Ile Gly--Gly--Ala Gly Ser-.
Тромболитическая активность. Тромболитическую активность фермента дестабилазы анализируют в экспериментах на животных (крысы с массой тела 200 г). У животных стимулируют тромбообразование в яремной вене посредством введения активированной стеклом сыворотки крови с последующим стазированием участка яремной вены (метод Wessller, 1975). Образовавшийся тромб фиксируют наложением лигатуры на соответствующий участок вены. Контрольные животные получают внутривенные инъекции 0,2 мл физиологического раствора, а экспериментальные - такой же объем раствора дестабилазы, содержащего 0,72 мг белка. Тромболизис наблюдается на 85% спустя 67 ч после введения препарата, и на 100% - через 137 ч после введения. У группы контрольных животных наблюдают спонтанный тромболизис на 17% спустя 67 ч после введения физиологического раствора и на 23% спустя 137 ч после введения.
Полученное вещество отличается от известных эндо- и экзо-ε-(γ-Glu)-Lys-изопептидаз по удельной активности, наличием тромболитической активности, по молекулярной массе и аминокислотной последовательности.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФИБРИН-ИЗОПЕПТИДАЗА | 1991 |
|
RU2049819C1 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИСТРЕССОРНЫМ, ПРОТИВОСУДОРОЖНЫМ И НЕЙРОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1997 |
|
RU2115660C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pET15/N-Dest+ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, ШТАММ Escherichia coli BL21(DE3)Gold, ТРАНСФОРМИРОВАННЫЙ РЕКОМБИНАНТНОЙ ДНК pET15/N-Dest+, И СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО БИФУНКЦИОНАЛЬНОГО ФЕРМЕНТА - ДЕСТАБИЛАЗЫ МЕДИЦИНСКОЙ ПИЯВКИ | 2015 |
|
RU2658429C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ИНСУЛИНА ИЛИ ЕГО БИОТЕХНОЛОГИЧЕСКИХ ПРЕДШЕСТВЕННИКОВ | 1994 |
|
RU2081122C1 |
| ФУЛЛЕРЕНОВОЕ ПРОИЗВОДНОЕ ГЛИКОПЕПТИДА, ОБЛАДАЮЩЕЕ АДЪЮВАНТНОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2124022C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОГО МАКРОПОРИСТОГО КРЕМНЕЗЕМА ДЛЯ ХРОМАТОГРАФИИ БИОПОЛИМЕРОВ | 1988 |
|
RU2080905C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВТОРИЧНЫХ АМИНОВ | 1998 |
|
RU2148055C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА δ СНА | 1995 |
|
RU2111972C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИНСУЛИНА ЧЕЛОВЕКА | 1991 |
|
RU2045535C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИНТЕРЛЕЙКИНА-3 ЧЕЛОВЕКА, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК P3PTEIL3, КОДИРУЮЩАЯ РЕКОМБИНАНТНЫЙ ИНТЕРЛЕЙКИН-3 ЧЕЛОВЕКА, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI - ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ИНТЕРЛЕЙКИНА-3 ЧЕЛОВЕКА | 1995 |
|
RU2099421C1 |
Изобретение относится к медицине, точнее к способам получения биологически активных веществ из животного сырья, и может найти применение в терапии тромбозов и в экспериментальных областях медицины. Изобретение позволяет повысить новый тромболитический фермент, дестабилазу, эндо-ε(γ-Glu)-Lys-изопептидазу, обладающую экзо-ε(γ-Glu)-Lys-изопептидазной и амидолитической активностью. Установлена частичная аминокислотная последовательность фермента. Для этого из пиявки семейства Hirudinidae получают экстракт, подвергают его аффинной хроматографии, дополнительно очищают на анионо- или катионообменнике, собирают целевой продукт, затем обессоливают гель-фильтрацией, собирают белок с мол.м. 126000±300 Дальтон. 2 ил.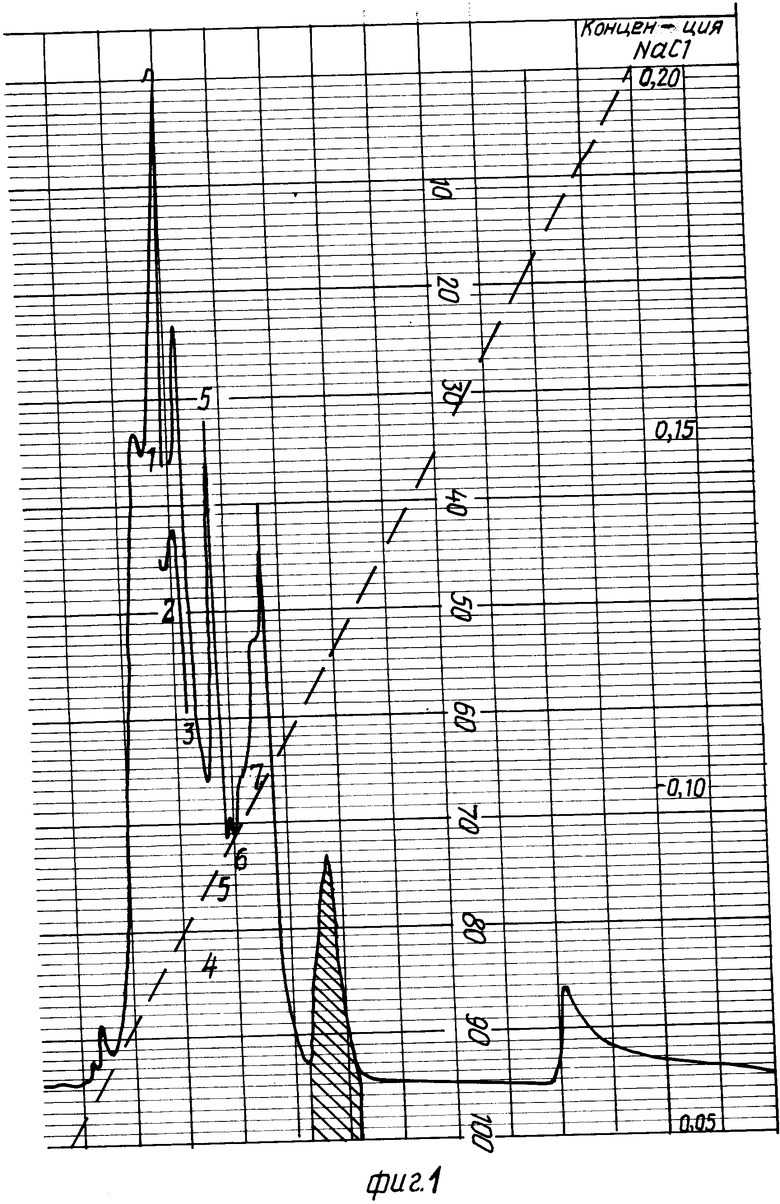
Способ получения фермента дестабилазы, обладающего фибринолитической, тромболитической, эндо- и экзо-ε-(γ-Gly)-Lys-изопептидазной и амидолитической активностью и характеризующегося следующими частичными аминокислотными последовательностями:
1. Thr Val-Ser-X Leu--Ile--Val-Gly X---IleGly--Gly-,
2. -AlaGlySerLeu--Gly---Ile----Ile---Gly--GlyGly---Gln,
3. ---Ala--X- GlyGly--ProThr X---Ala-Ile---,
4. GlyPro-Gly X-SerLeu--,
заключающийся в том, что экстракт из пиявок семейства Hirudinidae хроматографируют на сорбенте с иммобилизованными антителами к ферменту дестабилазе, фракции, обладающие ферментативной активностью, объединяют, вновь хроматографируют на анионо- или катионообменнике, собирают целевой продукт, дополнительно очищают гель-фильтрацией и лиофилизуют.
Авторы
Даты
1998-06-10—Публикация
1994-12-23—Подача