Изобретение относится к медицине и может быть использовано для создания лекарств.
Новое направление, родившееся около десяти лет назад и получившее активный практический выход в последнее время, посвящено созданию лекарственных средств нового поколения, смысл которого заключается в непосредственной доставке лекарства в клетку. В основе такого направления лежит особенность высокоаффинного взаимодействия комплекса лиганд-рецептор, участниками которого являются, с одной стороны, разнообразные лиганды, являющиеся своеобразным "адресом" для посадки на рецепторы, а с другой - специфический спектр рецепторных белков цитоплазматической мембраны клетки, имеющие соответствующие "узнающие" участки. Использование таких естественных возможностей организмов дало предпосылки для разработки и создания ряда лекарственных средств белковой природы, т.н. fusion-белков, имеющих специфические адресные части. Изменив адресную часть, можно "заставить" нужный рецептор клетки "узнать" лиганд, содержащий новую адресную часть, используя т.н. феномен "адресной доставки".
Наибольшее предпочтение в этом смысле отдано бактериальным токсинам, способным повреждать клетку хозяина, тем или иным способом вызывая ее гибель. Настоящее изобретение касается иммунотоксина на основе белка, токсическая часть которого представлена каталитической и трансмембранной частями дифтерийного токсина (DT), а адресная часть - человеческим интерлейкином-2 (IL-2).
Данный белок обладает как цитотоксическим действием по отношению к клеткам-продуцентам рецептора IL-2, так и иммуносупрессивным действием. Следовательно, он может быть применен для лечения таких патологий, как T-клеточный лейкоз, лимфогрануломатоз, различные аутоиммунные заболевания, в т.ч. диабет 1 типа, ревматоидный артрит и т.п., а также при трансплантации органов и тканей.
Наиболее исследованным объектом, несущим сильное токсическое начало, является дифтерийный токсин (DT) из Corynebacterium diphtheriae. Он имеет три структурно-обособленных домена, обладающих различными функциями [2]. На фиг. 1 представлена пространственная трехмерная структура DT, выполненная с использованием программы визуализатора WebLab Viewer [7]. Координаты атомов взяты из Брукхевенского банка данных [8]. В частности, каталитический домен ответственен за ADP-рибозилирование фактора элонгации 2, которое приводит к нарушению работы белок-синтезирующего аппарата клетки и, в дальнейшем, к ее гибели. Трансмембранный домен несет гидрофобные, мембранно-ассоциированные участки, проникающие через мембрану; он необходим для транслокации каталитической части токсина в цитозоль клетки. Рецепторный домен служит для узнавания токсина клеткой через соответствующие поверхностные рецепторы, проникая в клетку в ответ на снижение pH в эндосоме [1,3]. В норме таким рецептором является гепарин-связывающий эпидермальный фактор роста (HB-EGF-like) [4] . Последовательное расположение всех доменов представлено на фиг. 2, а именно: трехдоменная организация дифтерийного токсина: C - каталитический, T - трансмембранный, R - рецепторный домены соответственно; числа указывают номера аминокислот, соответствующие доменам. Нумерация аминокислотных остатков соответствует зрелому белку, не имеющему сигнальной последовательности (первые 25 остатков не участвуют в нумерации).
К настоящему моменту в мире накоплен довольно обширный материал, касающийся как структурных, так и функциональных особенностей рекомбинантных иммунотоксинов, в том числе созданных и на основе дифтерийного токсина. Разнообразие генетических форм химерных токсинов обусловлено поиском наиболее оптимальной конструкции как с точки зрения ее токсичности, так и высокой аффинности взаимодействия с рецептором. В связи с этим существующие рекомбинантные токсины отличаются, во-первых, адресной частью, во-вторых, качеством точечных аминокислотных замен, направленных на повышение активности вновь синтезированного белка, и, в-третьих, длиной линкера, соединяющего ферментно-трансмембранную часть токсина с "новым" адресом.
Известны иммунотоксины на основе DT, в которых N-терминальный фрагмент токсической части представлен двумя первыми доменами и характеризуется, в основном, двумя вариантами последовательностей, длиной 389 и 486 аминокислотных остатков. Кроме адресных частей, они отличаются длиной линкера, соединяющего трансмембранный домен DT и вновь присоединенную последовательность адреса [5].
Наиболее близким по технической сущности и достигаемому результату к предложенному изобретению является рекомбинантный иммунотоксин на основе DT и IL-2, в котором токсическая (каталитическо-трансмембранная) часть (DT) имеет длину 389 аминокислот, и способ его получения, заключающийся в конструировании плазмиды рДТИ23, и клонирование фрагмента последовательности интерлейкина-2 [6].
В вышеуказанном техническом решении для экспрессии и наработки слитого белка использовался штамм продуцент на базе E.coli. Однако, это может повлечь за собой ряд проблем. Во-первых, использование телец включения для экспрессии создает чисто технологические трудности, касающиеся выделения, очистки и стабильности химерного белка. Во-вторых, будучи грамм-отрицательной бактерией, оболочка E.coli содержит токсические липополисахариды, которыми может загрязняться препарат. Кроме того, система протеолиза в E.coli настроена на распознавание "свой - чужой", поэтому существует высокая вероятность протеолитического расщепления гибридного белка, что влечет за собой сегрегационную и структурную неустойчивость и, как следствие, снижение продуктивности рекомбинантной популяции.
Задачей настоящего изобретения является создание слитого белка DT-IL2 и разработка способа его получения, позволяющего обеспечить высокую токсичность и способность секретироваться во внеклеточное пространство. Поставленная задача решается описываемым рекомбинантным иммунотоксином, содержащим каталитическую и трансмембранную части дифтерийного токсина длиной 482 аминокислоты и адресную часть, представленную человеческим интерлейкином-2, и имеющим аминокислотную последовательность, представленную в конце текста описания.
Поставленная задача решается также описываемым способом получения рекомбинантного иммунотоксина DT-IL2, включающим конструирование гибридной плазмиды на основе вектора pBR322 по сайтам рестрикции EcoRI-Hindlll, точечный мутагенез для получения ApaLI сайта в районе 482 аминокислотного остатка DT путем замены последнего тимина в сайте gtgcat на цитозин, модификацию белок-синтезирующего аппарата штамма-продуцента PW8 введением необходимой тРНК, связывающей образующуюся тРНК с лейциновым кодоном cta IL2, клонирование фрагмента последовательности IL2 по сайтам ApaLI-ApaLI с последующим введением полученного фрагмента в ApaLI-сайт вектора pSUL17M, сортировку, клонирование и отбор канонических клонов, содержащих искомый рекомбинантный иммунотоксин DT-IL2.
Создание изобретения основано на изучении длины линкера иммунотоксина, которое позволило сделать вывод, что он не должен быть слишком большим, так как несколько изменившаяся трехмерная структура иммунотоксина в результате присоединения "чужого" домена может способствовать усилению протеолитической деградации иммунотоксина. Для двух известных вариантов рекомбинантных токсинов длина такого линкера составляет 2 и 99 аминокислот, соответственно. При конструировании также необходимо было учесть, что линкерный участок не должен содержать сайт, ответственный за связывание с рецептором к нативному дифтерийному токсину (дикому типу). Такой участок начинается в районе 482 остатка. Таким образом, предлагаемая конструкция, названая DT482-IL2, содержит более короткий линкер, что способствует, с одной стороны, большей устойчивости к протеазам, а с другой - позволяет адресной части быть более гибкой, что способствует повышению аффинности взаимодействия с рецептором. Более того, предложенная конструкция, в отличие от известной, позволяет сохранить каталитически важные аминокислотные остатки, Ser466 и Arg458, являющиеся неотъемлемой частью активного центра.
Выбор штамма-продуцента Corynebacterium diphtheriae диктуется существованием регламента на продукцию DT и его производных. Согласно принятым промышленным регламентам, в Российской Федерации таким штаммом является PW8.
Таким образом, предлагаемое изобретение имеет следующие преимущества перед существующими аналогами, в том числе прототипом. Во-первых, линкер характеризуется сохранением всех аминокислотных остатков, необходимых для выполнения каталитической функции активного центра. Во-вторых, продуцент, выбранный нами для наработки слитого белка, является предпочтительнее, чем E. coli. В частности, синтезируемый иммунотоксин секретируется во внеклеточное пространство, что технологически более эффективно. И кроме того, используемый штамм PW8 разрешен для промышленного применения.
Способ конструирования слитого белка DT482-IL2 включает следующие стадии.
1. Получение гибридной плазмиды pSUL17.
После индукции бактериофага β налидиксовой кислотой было проведено выделение ДНК этого бактериофага, содержащего полную последовательность дифтерийного токсина. После обработки полученной ДНК рестриктазами EcoRI-HindUI проводят выделение фрагмента, кодирующего DT. На следующем этапе проводят включение выделенного фрагмента ДНК DT в плазмиду pBR322 по указанным сайтам рестрикции для получения гибридной плазмиды pSUL17.
2. Точечный мутагенез для получения ApaLI сайта.
С целью создания слитого белка DT-IL-2 и учета структурно-функциональных особенностей обоих белков используют ApaLI сайт в качестве "стыковочного узла" между каталитическо-трансмембранной частью DT и IL-2. Последний имеет данный уникальный сайт на 5'-конце. Что касается последовательности DT, то в районе 482 остатка имеется участок gtgcat (VaI482His483), в котором замена одного нуклеотида также приведет к получению ApaLI сайта, gtgcac.
3. Модификация белок-синтезирующего аппарата штамма PW8.
Поскольку в качестве штамма-продуцента используют PW8 Corynebacterium diphtheriae, то необходимо учесть особенности белок-синтезирующего аппарата данного продуцента с целью дальнейшего безошибочного синтеза слитого белка, содержащего интерлейкин-2 человека. Было выяснено, что пул лейциновых кодонов cta IL-2 является минорным для Corynebacterium diphtheriae. В связи с этим необходимо видоизменить белок-синтезирующий аппарат, для чего вводят в хромосому штамма-продуцента ген необходимой тРНК так, чтобы образующаяся тРНК была способна связываться с вышеуказанным кодоном.
4. Клонирование кодирующего фрагмента последовательности IL-2.
После выделения тотальной мРНК IL-2 из культуры тимоцитов человека проводят полимеразную цепную реакцию, сопряженную с обратной транскрипцией (праймеры 5'GTGCACCTACTTCAAGT3' и 3'GGGGTGCACTTAATTATCAAGTTAGTG 5' AMV-ревертаза, PFU-1-полимераза для ПЦР). Полученные ампликоны обрабатывают рестриктазой ApaLI. После выделения необходимого фрагмента ДНК проводят введение ApaLI - ApaLI фрагмента в ApaLI-сайт pSUL17M. Полученные таким образом гибридные плазмиды, отличающиеся направлением встроенного фрагмента, подвергают сортировке и клонированию для отбора канонических клонов, содержащие искомый слитый белок (pSUL178).
5. Проведение трансформации клеток тройного лизогена PW8 по бактериофагу β плазмидой pSUL178.
Осуществление селекции стабильных клонов, секретирующих искомый белок DT482-IL2.
В результате осуществления способа получен целевой продукт, имеющий аминокислотную последовательность, представленную на фиг. 3 (первичная последовательность рекомбинантного белка; сигнальная последовательность выделена курсивом, интерлейкиновая часть - мелким шрифтом).
Таким образом, предлагаемая генно-инженерная конструкция позволяет получать слитый белок наиболее эффективным способом, который может быть легко адаптирован к существующим промышленным технологиям. Препарат DT482-IL2 обладает как противоопухолевой активностью, уничтожая малигнизированные T-клетки, так и иммунносупрессивной активностью, что может быть использовано при лечении аутоиммунных заболеваний и трансплантации органов и тканей.
Литература
1. Bell, C.E., Eisenberg, D. Crystal structure of diphtheria toxin bound to nicotinamide adenine dinucleotide. Biochemistry 35, 1996, 1137-1149.
2. Bennett, M. J., Choe, S. Eisenberg, D. Refined structure of dimeric diphtheria toxin at 2.0 A resolution, Protein Sci 3, 1994, 1444-1463.
3. London, E. How bacterial protein toxins enter cells: the role of partial unfolding in membrane translocation, Mol. Microb. 22, 1992, 3277-3282.
4. Mitamura, T., Higashiyama, S., Taniguchi, N., Klagsbrun, M., Mekada, E. Diphtheria toxin binds to the epidermal growth factor (EGF) - like domain of human heparin-binding EGF-like growth factor/diphtheria toxin receptor and inhibits specifically its mitogenic activity. J. Biol. Chem. 270, 1995, 1015-1019.
5. Shaw, J.P., Akiyoshi, D.E., Arrigo, D., A., Rhoad, A.E., Sullivan, B. , Thomas, J., Genbauffe, F.S., Bacha, P., Nichols, J.C. Cytotoxic properties of DAB486EGF and DAB389EGF, epidermal growth factor (EGF) receptor-targered fusion toxins. J. Biol Chem. 266, 1991, 21118-21124.
6. Заявка RU 93055180, БИ N23, 1996.
7. WebLab Viewer: http://www.msi.com.
8. Bernstein, F. C. , Koetzie, T.F., Williams, G.J.B., Meyer Jr.E.F., Brice, M.D., Rodgers, J.R., Kennard, O., Shimanouchi, T. and Tasumi, M. The Protein Data Bank: A computer-based archival file for macromolecular structures. J. Mol. Biol. 112, 1977, 535-542.


Изобретение относится к медицине. Разработан рекомбинантный иммунотоксин на основе дифтерийного токсина и интерлейкина-2, в котором каталитическо-трансмембранная часть дифтерийного токсина имеет длину 482 аминокислоты. Предложен также способ получения рекомбинантного иммунотоксина DT482-IL2. Новый иммунотоксин может быть использован для создания лекарственных средств для лечения опухолевых и аутоиммунных заболеваний. Способ обеспечивает высокую токсичность белка и способность секретироваться во внеклеточное пространство, в отличие от известных способов. 2 с.п. ф-лы, 3 ил.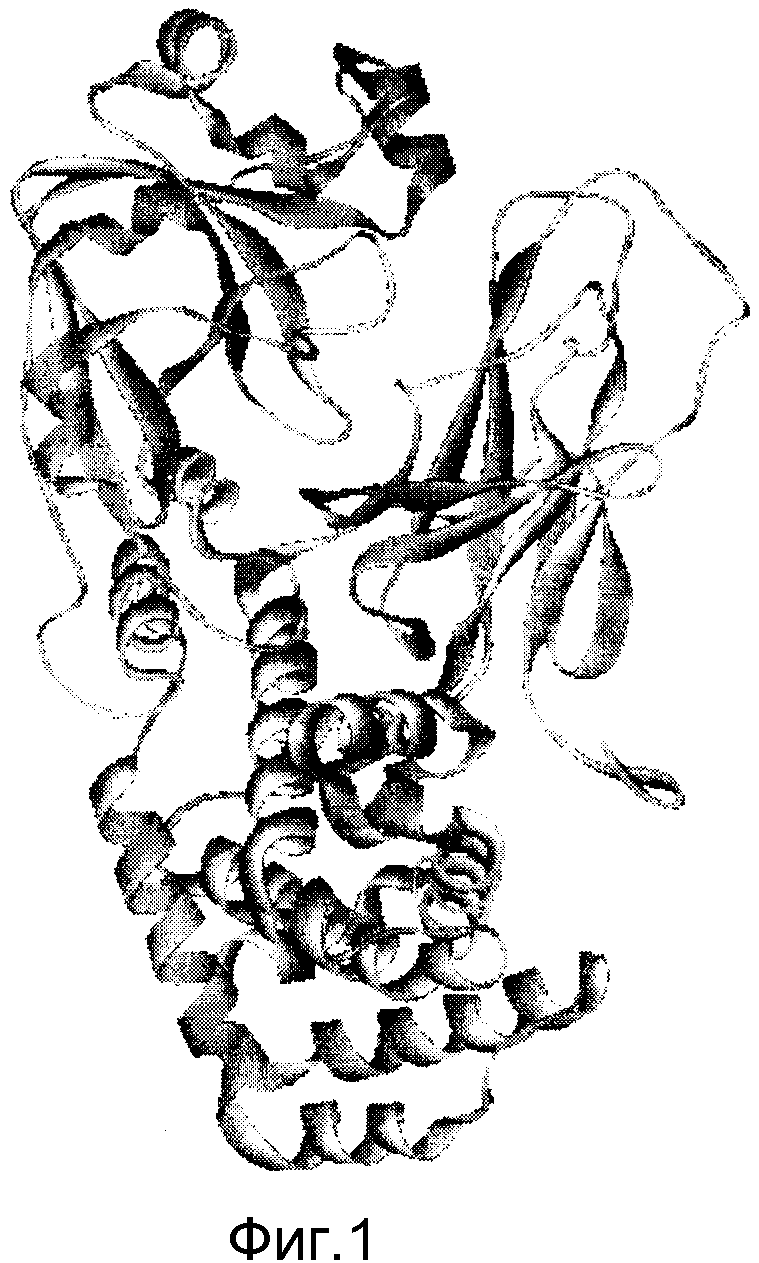
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РДТИ 23, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОЙ ПЛАЗМИДНОЙ ДНК РДТИ 23 И ШТАММ БАКТЕРИЙ ESCHERICHIA COLI, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДНУЮ ДНК РДТИ 23 - ПРОДУЦЕНТ СЛИТОГО БЕЛКА ДТИЛ 2 | 1993 |
|
RU2077585C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ОХЛАЖДАЮЩЕЕ УСТРОЙСТВО ДЛЯ ЭЛЕКТРИЧЕСКОГО УСТРОЙСТВА И ЭЛЕКТРИЧЕСКОЕ УСТРОЙСТВО, В ЧАСТНОСТИ АВТОМАТИЧЕСКИЙ ВЫКЛЮЧАТЕЛЬ, СОДЕРЖАЩИЙ ТАКОЕ ОХЛАЖДАЮЩЕЕ УСТРОЙСТВО | 2013 |
|
RU2650183C2 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 5061692, 29.10.91 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Автоматический огнетушитель | 0 |
|
SU92A1 |
Авторы
Даты
1998-07-20—Публикация
1997-07-22—Подача