Изобретение относится к пирометаллургии, в частности к восстановлению твердым углеродом металлов из смеси их оксидов, растворенных в расплаве галогенидов щелочных и/или щелочноземельных металлов.
При обогащении руд и переработке концентратов во многих случаях получают полупродукты, представляющие собой смесь оксидов нескольких металлов. Разделение или очистка черного металла, полученного в результате восстановления такого полупродукта, осуществляется с использованием сложных передельных металлургических процессов. Актуальной является задача разделения металлов на стадии их восстановления из смеси оксидов.
Известен способ восстановления железа из рудно-флюсовых расплавов углеродом, в котором твердый углеродистый восстановитель (полукокс) взаимодействует в ванне расплава с окислами железа и восстанавливает их с выделением окиси углерода [1].
Недостатком известного способа является то, что выделяющаяся в процессе реакции окись углерода вследствие повышения вязкости расплава из-за поглощения тепла в зоне реакции вспенивает расплав в ванне печи, прерывая процесс.
Известен способ получения железа, включающий жидкофазное восстановление окислов железа твердым углеродистым восстановителем, в котором в ванну печи со вспененным расплавом окислов вводят сверху смесь руды с известью и уголь, а снизу подают дутье природного газа и кислорода [2].
К недостаткам способа относится сложность технического исполнения, низкая производительность и технологическая неустойчивость процесса.
Известен способ, принятый за прототип, получения металлов и сплавов, включающий растворение окислов в расплаве галогенидов щелочных и/или щелочноземельных металлов и жидкофазное восстановление окислов из раствора их в расплаве-растворителе, отличающийся тем, что восстановление окислов осуществляют твердым углеродом при температуре, соответствующей энергии их образования, причем после восстановления окислов расплав-растворитель отделяют от металла и повторно используют для растворения исходного продукта [3].
Недостатком способа, принятого за прототип, является невозможность при заданной температуре расплава избирательного отделения от расплава-растворителя металла, восстановленного из менее энергоемкого оксида, при условии, что при этой температуре термодинамически возможно восстановление сразу нескольких оксидов. Например, при использовании в качестве расплава-растворителя фтористого кальция CaF2, содержащегося в плавиковом шпате, при температуре расплава выше температуры плавления указанного растворителя (1418oC), возможно восстановление и извлечение в сплав сразу нескольких металлов, для оксидов которых изменен термодинамический потенциал реакции восстановления ΔG
Задачей изобретения является избирательное восстановление твердым углеродом металлов из смеси их оксидов, растворенных в расплаве галогенидов щелочных и/или щелочноземельных металлов.
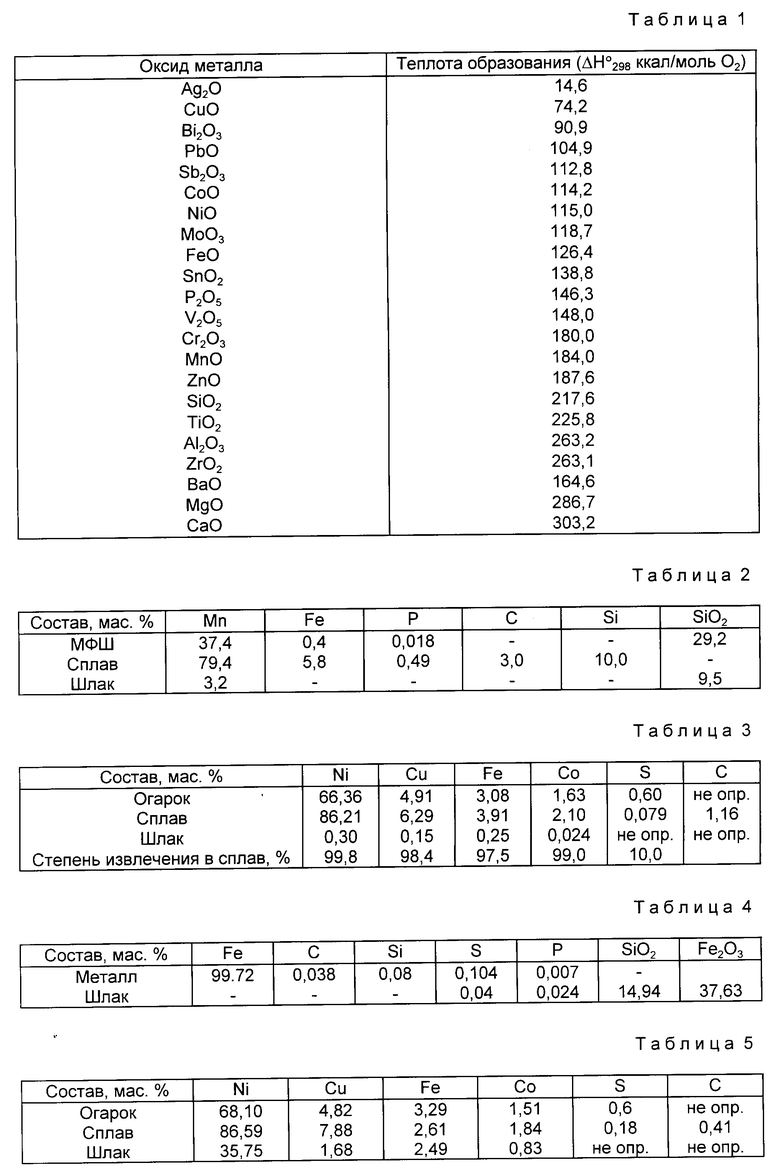
Решение задачи обусловлено тем, что все оксиды элементов по степени своего сродства к кислороду или по прочности связи с кислородом, или по величине теплоты образования ΔH
Ag2O - 14,6
CuO - 74,2
Bi2O3 - 90,0
PbO - 104,9
Sb2O3 - 112,8
CoO - 114,2
NiO - 115,0
MoO3 - 118,7
FeO - 126,4
SnO2 - 138,8
P2O5 - 146,3
V2O5 - 148,0
Cr2O3 - 180,0
MnO - 184,0
ZnO - 187,6
SiO2 - 217,6
TiO2 - 225,8
Al2O3 - 253,2
ZrO2 - 263,1
BaO - 264,6
MgO - 286,7
CaO - 303,2
Каждый последующий металл в представленном ряду является восстановителем для всех оксидов предыдущих металлов (такие реакции протекают практически при всех процессах, где существуют металлическая и оксидная фазы). Следовательно, ни один последующий оксид металла в представленном энергетическом ряду не может быть полностью восстановлен, пока не восстановлены все предыдущие оксиды металлов. Степень восстановления твердым углеродом из раствора смеси оксидов каждого последующего оксида металла в представленном энергетическом ряду зависит от степени восстановления всех предыдущих оксидов и от численной разницы величин прочностной характеристики восстанавливаемых оксидов.
При восстановлении металлов из раствора смеси их оксидов первым будет восстанавливаться металл, оксид которого имеет наименьшее значение ΔH
Указанный технический результат достигается тем, что в способе избирательного восстановления металлов из смеси их оксидов, включающем растворение оксидов в расплаве галогенидов щелочных и/или щелочноземельных металлов, жидкофазное восстановление оксидов твердым углеродом при заданной температуре, непрерывное отделение восстановленного металла от расплава-растворителя, который повторно используют для растворения исходного продукта, согласно изобретению, восстановление менее прочного оксида ведут, поддерживая в расплаве-растворителе его концентрацию выше концентрации более прочного оксида, путем непрерывной загрузки исходного продукта, причем при достижении концентрации более прочного оксида уровня концентрации менее прочного оксида растворение исходного продукта в расплаве-растворителе прекращают и восстанавливают смесь оксидов, отделяя полученных сплав от расплава-растворителя изолированно от металла, восстановленного из мене прочного оксида.
Эффект избирательного восстановления металлов из смеси их оксидов достигается тем, что при поддержании в растворе оксидов в расплаве-растворителе избыточной концентрации менее прочного оксида металла, более прочный оксид металла не восстанавливается до тех пор, пока концентрация его оксида не достигнет уровня концентрации менее прочного оксида, после чего загрузку исходного продукта в расплав-растворитель прекращают и все растворенные оксиды восстанавливают совместно, а полученный сплав удаляют из раствора отдельно от металла, восстановленного из менее прочного оксида.
Способ осуществляется следующим образом.
В ванну дуговой электропечи, футерованную углеродистой массой, либо оборудованную водяным охлаждением с целью образования гарнисажа, загружают плавиковый шпат, расплавляют его в дуговом режиме и в рудно-термическом режиме доводят до жидкоподвижного состояния. Затем в ванну печи непрерывно загружают шихту, состоящую из смеси оксидов металлов и углеродистого восстановителя (коксика). При этом оксид металла с меньшей величиной ΔH
Примеры осуществления способа.
Пример 1 (по прототипу). В опыте использовалась дуговая электропечь мощностью 100 кВА, позволяющая загружать до 100 кг шихтовых материалов. В ванну печи с углеродистой футеровкой загружался плавиаковый шпат в количестве 50 кг, который плавился в дуговом режиме и доводился в рудно-термическом режиме до жидкоподвижного состояния в течение 25 - 30 мин. Затем в ванну печи загружался передельный малофосфористый марганцевый шлак (МФШ) в количестве 40 кг и металлургический кокс в количестве 8 кг. Продолжительность опыта с момента загрузки шихты составила 45 мин.
Химический анализ исходного малофосфористого шлака и полученных продуктов приведен в табл. 2.
Из приведенных данных химического анализа следует, что оксиды железа и фосфора, как наименее прочные, первыми восстановились полностью из их раствора в расплаве. Оксид марганца восстанавливался единолично, пока его концентрация в растворе не сравнялась с концентрацией оксида кремния, после чего активно восстанавливался кремний, содержание которого в сплаве достигло 10%.
Пример 2 (по прототипу). В дуговую электропечь мощностью 40 кВА, позволяющую загружать до 100 кг шихтовых материалов, снабженную углеродистой футеровкой, загружался плавиковый шпат в количестве 15 кг, который плавился и доводился до жидкоподвижного состояния в течение 25 - 30 мин. Затем в ванну печи загружался никелевый огарок в количестве 31,5 кг и металлургический кокс в количестве 8 кг, содержащий C - 69,7%, золы - 23,4%. Продолжительность восстановительной плавки составила 0,5 ч, ее окончание фиксировалось по отсутствию пламени горящей окиси углерода над ванной печи. В результате плавки получен слиток металла массой 24,2 кг и шлак в количестве 13,6 кг.
Химический анализ исходного огарка, а также полученных металла и шлака приведен в табл. 3.
Из химического анализа полученных продуктов видно, что все оксиды металлов, содержащиеся в огарке, восстановились практически полностью.
Пример 3 (по предлагаемому способу).
В опыте использовалась трехфазная дуговая электропечь мощностью 4000 кВА. В ванну печи, работающую на гарнисаже, загрузили 1100 кг плавикового шпата, расплавили его в дуговом режиме и в рудно-термическом режиме довели до жидкотекучего состояния. В расплав в течение трех часов непрерывно загружалась железная руда в количестве 1800 кг, класса - 30 мм, следующего состава, %: Fe - 56,28; FeO - 2,78; CaO - 0,54; MgO - 0,17; SiO2 - 12,85; S - 0,155; P - 0,01; п.п.п. - 4,08; и металлургический кокс в количестве 400 кг, класса - 10 мм, химического состава,%: зольность - 36,31; Sобщ - 0,545; Pзолы - 0,056.
Сразу по окончании загрузки плавку заморозили.
В результате восстановительной плавки получено 635 кг металла.
Химический анализ полученных металла и шлака приведен в табл. 4.
Из химического анализа видно, что при поддержании в расплаве-растворителе концентрации оксидов железа, превышающей концентрацию оксида кремния в 2,5 раза, кремний практически не восстанавливается и в металл не переходит. Это дает возможность получать железо высокой степени чистоты непосредственно из железных руд и концентратов.
Пример 4 (по предлагаемому способу).
В дуговую электропечь мощностью 40 кВА, позволяющую загружать до 100 кг шихтовых материалов, снабженную углеродистой футеровкой, загружался плавиковый шпат в количестве 10 кг, который плавился и доводился до жидкоподвижного состояния в течение 25 - 30 мин. Затем в ванну печи непрерывно в течение 15 мин загружался никелевый огарок в количестве 20 кг и металлургический кокс в количестве 2 кг, содержащий C - 67,3%, золы - 25,0%. Сразу по окончании загрузки плавку заморозили. В результате плавки получен слиток металла массой 8,5 кг и шлак в количестве 17,5 кг.
Химический анализ исходного огарка, а также полученных металла и шлака приведен в табл. 5.
Из приведенных данных химического анализа видно, что при поддержании в расплаве-растворителе концентрации оксида никеля, превышающей концентрацию оксида железа в 15 раз, часть железа исходного огарка (33%) все же переходит в металлическую фазу. В то же время значительная часть железа (67%) остается в шлаке. Это дает возможность частично рафинировать никель от железа в процессе восстановления агарка и получать никелевый сплав с пониженным содержанием железа.
Следует отметить, что чем выше разница величин теплот образования оксидов металлов, тем лучше эти металлы разделяются в процессе восстановления по предлагаемому способу.
При разнице теплот образования оксидов железа и кремния, равной 91,2 ккал/моль O2, можно оставлять почти весь оксид кремния в расплаве-растворителе, получая практически чистое по кремнию железо (пример 3). При разнице теплот образования оксидов никеля и железа, равной 11,4 ккал/моль O2, то есть существенно меньшей, чем у оксидов железа и кремния, железо частично восстанавливается вместе с никелем и переходит в сплав (пример 4). В этом случае можно говорить только о понижении содержания железа в никелевом сплаве.
Таким образом, по предлагаемому способу можно осуществлять избирательное восстановление твердым углеродом металлов из смеси их оксидов, растворенных в расплаве галогенидов щелочных и/или щелочноземельных металлов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ АККУМУЛЯТОРНОГО СВИНЦОВОГО ЛОМА | 1997 |
|
RU2119540C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОВ И СПЛАВОВ | 1991 |
|
RU2037543C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОУГЛЕРОДИСТЫХ МЕТАЛЛОВ И СПЛАВОВ | 2000 |
|
RU2164543C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОВ И СПЛАВОВ | 1998 |
|
RU2130500C1 |
| УСТРОЙСТВО ДЛЯ ВОССТАНОВЛЕНИЯ ОКСИДОВ МЕТАЛЛОВ | 1998 |
|
RU2133291C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИОБИЯ ИЗ ЕГО ОКСИДА | 2003 |
|
RU2241774C1 |
| СПОСОБ ПЕРЕРАБОТКИ АЛЮМИНИЕВЫХ ШЛАКОВ | 1998 |
|
RU2148664C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРРОХРОМА | 1998 |
|
RU2148672C1 |
| СПОСОБ ОБЖИГА КЕРАМИЧЕСКИХ ИЗДЕЛИЙ | 1995 |
|
RU2096382C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЯ ИЗ ЕГО ОКСИДА | 2000 |
|
RU2165989C1 |
Изобретение относится к пирометаллургии, в частности, к восстановлению твердым углеродом металлов из смеси их оксидов, растворенных в расплаве галогенидов щелочных и/или щелочноземельных металлов. Способ включает растворение оксидов в расплаве галогенидов щелочных и/или щелочноземельных металлов, жидкофазное восстановление оксидов твердым углеродом при заданной температуре, непрерывное отделение восстановленного металла от расплава-растворителя (р.р). Последний повторно используют для растворения исходного продукта. Восстановление менее прочного оксида ведут постоянно поддерживая в р.р. его концентрацию выше концентрации более прочного оксида. Для этого непрерывно загружают исходный продукт. При достижении концентрации более прочного оксида уровня концентрации менее прочного оксида растворение исходного продукта в р. р. прекращают и восстанавливают смесь оксидов, отделяя полученный сплав от р. р. изолированно от металла, восстановленного из менее прочного оксида. Изобретение позволяет осуществить избирательное восстановление твердым углеродом металлов из смеси их оксидов, растворенных в расплаве галогенидов щелочных и/или щелочноземельных металлов. 5 табл.
Способ восстановления металлов из смеси их оксидов, включающий растворение оксидов в расплаве галогенидов щелочных и/или щелочноземельных металлов, жидкофазное восстановление оксидов твердым углеродом при заданной температуре, отделение восстановленного металла от расплава-растворителя, который повторно используют для растворения исходного продукта, отличающийся тем, что восстановление менее прочного оксида ведут, постоянно поддерживая в расплаве-растворителе его концентрацию выше концентрации более прочного оксида путем непрерывной загрузки исходного продукта, причем по достижении концентрации более прочного оксида уровня концентрации менее прочного оксида растворения исходного продукта в расплаве-растворителе прекращают и восстанавливают смесь оксидов, отделяя полученный сплав от расплава-растворителя изолированно от металла, восстановленного из менее прочного оксида.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| SU, авторское свидетельство, 88996, кл | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Химия и жизнь | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RU, патент, 2037543, кл | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Кубашевский О | |||
| Олкокк С.Б | |||
| Металлургическая термохимия | |||
| - М.: Металлургия, 1982, с.208-261. | |||
Авторы
Даты
1998-07-20—Публикация
1997-09-08—Подача