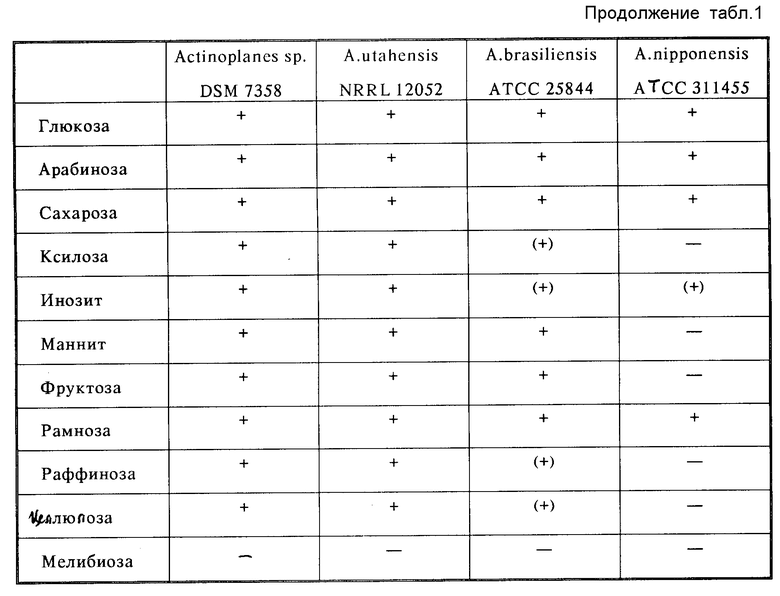
Для характеристики штамма Actinoplanes sp. DSM 7358 проводят сравнение близко родственных штаммов по методу ISP, разработанному Ширлингом и Готлибом (Int. J. of Sys. Bacteriol. 16, 3 (1966), стр. 313 - 340). Результаты сравнений, приведенные в таблице 1, показывают, что штамм Actinoplanes sp. DSM 7358 по своим морфологическим и физиологическим признакам отличается от других штаммов.
3a) Получение липопептида A 1437 B и D.
Ферментер на 500 л запускают в работу при следующих условиях:
Питательная среда: 11 г/л сахарозы, 6 г/л мясного экстракта, 0,3 г/л экстракта дрожжей, 0,6 г/л сульфата магния, 0,1 г/л KH2PO4, 10 мкм FeCl3•6H2O, 0,6 г/л L-валина, pH 7,3 (перед стерилизацией)
Продолжительность инкубации: 120 часов
Температура при инкубации: 30oC
Скорость при перемешивании: 50 об/мин,
Аэрационные условия: 150 л мин-1
Путем повторного добавления этанольного раствора полиоли удается подавить процесс пенообразования. Производство штамма достигает максимума через 96 - 120 часов.
После окончания ферментации Actinoplanes sp. DSM 7358 культуральный бульон фильтруют при добавлении около 2% фильтрующего средства (например, целита®), культуральный фильтрат охлаждают до 4oC и pH устанавливают на уровне 1,5. Через 4 часа продукт обрабатывают на центрифуге при 10000 об.(g) и образующий осадок повторно суспендируют в дистиллированной воде. Путем нейтрализации суспензии указанное вещество переходит в раствор. Последний вымораживают и лиофилизируют. Выход составляет около 1,5 г/л сырого продукта (= 750 г).
3b) Разделение сырого продукта методом йонной хроматографии (с получением B + D).
Хроматографическую колонку емкостью 3,2 л (10 см внутренний диаметр х 40 см высота) загружают DEAE-сефарозой Фаст-Флау и эквилибрируют 10 ммолями калийфосфатного буфера, pH 7,0 в 40% метанола (буфер A). Затем в колонке растворяют 25 г A 1437 B сырого продукта (полученного от аналогии с примером 3a) в 3,5 л воды, вводят в колонку и промывают 1 л воды, а затем 6 л буфера A. В прогоне и промывных водах остаются примеси сырого продукта. Затем вводят 10 - 100 ммолей фосфата калия, pH 7,0-градиента в 40% метаноле, 25 - 35 ммолями фосфата калия элюируют A 1437 D-пептид и с 40 - 55 ммолями выделяют антибиотик А 1437 B.
Соответствующие фракции очищают от метанола под вакуумом. Для очистки от солей используют проникающую дианионовую колонку HP-20, производства фирмы Мицубиси, Япония, емкостью 1 л, 9 л фракций, содержащих чистый B-пептид, подают в колонку, после чего промывают 3 л очищенной от солей воды. Элюируют смесью воды-изопропанола по градиентному методу (0 - 50% спиртовых компонентов). Путем промывания 15 - 25% изопропанола чистый A 1437 B очищают от носителя. Этот продукт из колонки специально собирают, концентрируют в вакууме и подвергают криогенной сушке. Получают 4,8 г A 1437 B 97%-ной чистоты. После соответствующего обессоливания A 1437 D-содержащих фракций получают 3,1 г антибиотика. Чистота составляет 98%.
4a) Получение липопептидов A 1437 A и C.
Процесс получения аналогичен описанному в п. 3a с той лишь разницей, что L-валин в питательной среде заменяют на 4 г/л лейцина и ферментацию проводят в 50 л биореакторе. Выход составляет 1,3 г/л сырого пептида (= 65 г).
4b) Выделение липопептидов A 1437 A и C.
10 г сырого продукта растворяют в 100 мл дистиллированной воды и обрабатывают в соответствии с представленной ниже схемой.
Схема обработки сырого продукта: 10 г сырого пептида в 100 мл дистиллированной воды.
↓
Адсорбация на Q-сефарозе в быстром потоке (фирма Фармазия) (5 х 20 см колонка)
↓
Элюирование со следующими градиентами: буфер A: NaH2PO4 1 ммоль в 50% метаноле, pH 5,9; буфер B: NaH2PO4 100 ммолей в 50% метаноле, pH 5,3; 20 мин.: буфер A 60 мин при 25% в буфере B, затем 30 минут при 25% в буфере B,
↓
Лиофилизация A 1437 A или C-фракций и растворение в элюенте.
↓
Удаление солей на биогеле P2 (100 - 200 меш) фирмы Биорад (колонка 7 х 20 см)
↓
1,6 г липопептида A 1437 A (80%-ный) 1,2 г липопептида A 1437 C (80%-ный)
↓
RP-хроматография на нуклеозиле ®C18 (7 мкм) (колонка 20 х 250 мм, 200 мг загрузка)
Элюирование со следующими градиентами: буфер A: дистиллированная вода, 0,1% ТФА; буфер B: ацетонитрил; 10 мин: буфер B 60 мин - 90% буфер B при скорости потока 10 мл/мин.
↓
Лиофилизация A 1437 A или C-фракций
↓
150 мг A 1437 A (чистота более 95%)
5a) Получение липопептидов A 1437 E, F, G, и H.
Получение проводят, как описано в примере 3a, с той лишь разницей, что в среде получения вместо L-валина используют 1,5 г/л L-изолейцина и ферментацию проводят в 50 л биореакторе. Выход составляет 1,4 г/л сырого пептида (70 г).
5b) Разделение сырого продукта методом йонной хроматографии.
На колонке, описанной в примере 3a, и по методике, приведенной в примере 3a, проводят разделение 25 г сырого липопептида, выделенного в соответствии с примером 5 a; с 14 - 19 ммолями буфера элюируют липопептид A 1437 F (выход: 1,8 г); 18 - 25 ммолями буфера элюируют A 1437 E (выход: 1,3 г); 35 - 50 ммолями - соответственно A 1437 H (выход: 2,7 г) и 64 - 82 ммолями буфера элюируют A 1437 G (выход 1,9 г).
Соответствующие фракции соединяют и освобождают от метанола в вакууме.
5c) Очистка компонентов из примера 5b на реверсивной фазе RP-18.
Проникающую препаративную колонку для хроматографического анализа методом высокоэффективной жидкостной хроматографии (HPLC) при высоком давлении емкостью 500 мл (5,1 см (внутренний диаметр) х 25 см высота) заполняют ликросорбом (Li Chrosorb) G RP-18,10 мкм и вводят солесосодержащий раствор a 1437 G с 1,9 г антибиотика. Элюируют способом линейного градиента с 5% ацетонитрила в 10 ммолях калийфосфатного буфера pH 7,0 и 36% ацетонитрила в 10 ммолях калийфосфатного буфера, pH 7,0. При использовании 24 - 26% ацетонитрила выделяют липопептид A 1437 G. После концентрирования в вакууме, удаления солей на 100 мл поглощающей смолы® дианион HP - 20 в смеси вода / 50% изопропанол после проведения криогенной сушки получают 1,1 г липопептида A 1437 G с чистотой 99%.
Соответствующую дополнительную очистку A 1437 H-раствора, полученного в соответствии с примером 5b, проводят с помощью градиента растворителя 10 - 50% ацетонитрила в 10 ммолях калийфосфатного буфера, pH 7,0. Элюирование антибиотика осуществляют с 37 - 39% частями растворителя. После концентрирования соответствующих фракций и обессоливания на ®дианионе HP - 20, а также последующей криогенной сушки получают 2,2 г липопептида A 1437 H чистотой более 98%.
5d) Очистка липопептидных антибиотиков A 1437 E и F из примера 5b на MCl-геле.
Полученный в соответствии с примером 5b солесодержащий A 1437 F-раствор с 1,8 г антибиотика подают в 1 л MCl-геля CHP 20P (производства Мицубиси Кэзей Корпорейшн). Колонка имеет следующие размеры: внутренний диаметр 6 см, высота 35 см. Поле загрузки носителя с подлежащим разделению продуктом промывают буфером A (5 ммолей калийфосфатного буфера pH 7,0 с 20% ацетонитрила) и элюируют по градиентному методу против буфера B (5 ммолей калийфосфатного буфера, pH 7,0 с 70% ацетонитрила). 34 - 35%-частей растворителя ведет к элюированию чистого антибиотика. После концентрирования в вакууме и обессоливания на ®дианионе PH-20 получают 1,4 г липопептида с чистотой более 98%. Аналогичная обработка сырого продукта A 1437 E из примера 5a дает 1 г липопептида A 1437 с чистотой более 98%.
6a) Получение липопептида A 1437 K.
Получение проводят, как описано в примере 4a, с той лишь разницей, что в среде получения вместо L-валина в питательном растворе используют 500 мг/л L- α -аминомасляной кислоты (или 1 г/л рацемата) и процесс ферментации проводят в биореакторе емкостью 10 л. Выход составляет 1,1 г/л сырого пептида (= 10 г).
6b) Выделение липопептида A 1437 K.
10 г сырого продукта растворяют в 100 мл дистиллированной воды и обрабатывают по приведенной ниже схеме.
Схема обработки (А 1437 К): 10 г сырого пептида в 100 мл дистиллированной воды, поглощение на Q-сефарозе в быстром потоке (3,5 х 17 см колонка); элюирование со следующими градиентами: буфер A: NaH2PO4 1 ммоль в 50% метаноле, pH 5,9; буфер B: NaH2PO4 100 ммолей в 50% метаноле, pH 5,3; 20 мин; буфер A - - -> 45 мин на 25% буфере, последующие 45 мин - при 25%-ном буфере B; лиофилизация A 1437 K-фракций.
Обессоливание на биогеле P2 (100 - 200 меш) (7 х 20 см колонка),
700 мг A 1437 K (60%-ный),
RP-хроматография (обращенно-фазовая хроматография) на нуклезиле
C18 7 мкм (20 х 250 мм колонка).
Загрузка: 50 мг предварительно очищенного продукта
Элюирование со следующим градиентом
буфер A: дважды дистиллированная вода, 0,1% ТФА,
буфер B: ацетонитрил
10 мин: буфер A /5% буфер B - -> через 60 мин - 70% буфер B при 10 мл/мин скорости потока
лиофилизация A 1437 K-фракций
5,6 мг A 1437 (>95%)
7a) Получение липопептидов A 1437 L и M.
Получение проводят по аналогии с примером 4a, но вместо L-валина в получаемую смесь вводят 500 мл/г L-норвалина (или 1 г/л рацемата) и ферментацию проводят в биореакторе емкостью 10 л. Выход составляет 1,2 г/л сырого пептида (= 12 г).
7b) Выделение липопептидов A 1437 L и M.
10 г сырого продукта растворяют в 100 мл дистиллированной воды и обрабатывают в соответствии с приведенной ниже схемой:
Схема обработки: 10 г сырого пептида в 100 мл дистиллированной воды; поглощение на Q-сефарозе в быстром потоке, (3,5 х 17 см колонка).
Элюирование со следующим градиентом:
Буфер A: NaH2PO4 1 ммоль в 50% метаноле, pH 5,9,
Буфер B: NaH2PO4 100 ммолей в 50% метаноле, pH 5,3,
20 мин: буфер A - - -> 45 мин 25% буфер B, последующие 45 мин - в 25% буфере B,
лиофилизация A 1437 L и M-фракций,
очищение от солей на биогеле P2 (100 - 200 меш) (7 х 20 см колонка)
900 мг A 1437 L и M (около 60%)
RP-(-обращенно-фазовая) хроматография на нуклезиле C18 7 мкм (20 х 250 мм колонка)
Загрузка: 50 мг предварительно очищенного продукта
элюирование со следующим градиентом: буфер A: дважды дистиллированная вода, 0,1% ТФА
буфер B: ацетонитрил
10 мин: буфер A/5% буфера B - - - через 60 мин на 70% буфере B при скорости потока 10 мл/мин,
лиофилизация A 1437 L и M-фракций 5,8 мг A 1437 (>95%-ный) 6,7 A 1437 M(>95%-ный)
8) HPLC-система (использование метода высокоэффективной жидкостной хроматографии при высоком давлении) для определения A 1437 липопептидов.
Приведенная ниже система дает возможность разделять и количественно дифференцировать липопептиды в смеси сырья или в культуральном фильтрате.
Время удерживания составляет от 11,5 минут (A 1437 E) до около 15,9 минут (A 1437 H).
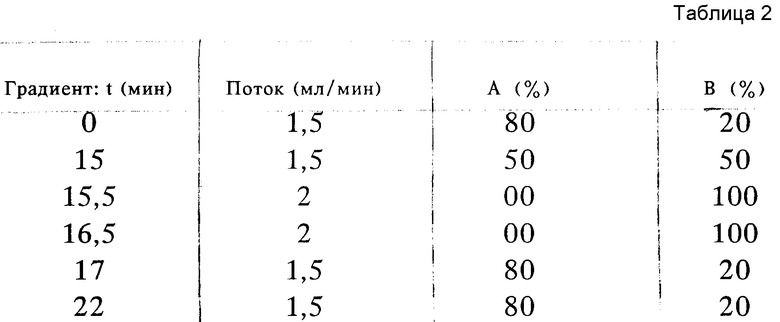
Растворитель: A калий-фосфатный буфер, pH 7,0 10 ммолей, B ацетонитрил (см. табл. 2)
Колонка: Шандон ODS, гиперсил RP-18 (обращенно-фазовая хроматография) (120 х 4,6 мм с 20 х 4,6 мм предварительной колонкой) или
Нуклеозил 120 RP-18 обращенно-фазовая хроматография (120 х 4,6 мм с 20 х 4,6 предварительной колонкой),
Скорость потока: 1,5 мл/мин
Обнаружение: 210 нм,
Введение: 10 мкм
7) Сравнение между Actinoplanes nipponensis ATCC 31145 и Actinoplanes spec. DSM 7358.
По описанному в примере 1b методу от обоих штаммов отбирают предварительную культуру, которую в дальнейшем используют для прививания производящей среды следующего состава:
Среда 1: как описано в примере 3a
Среда 2: как среда 1, но, однако, без L-валина
Среда 3: глюкоза 30 г/л, соевая мука 20 г/л, Fe2(SO4)3 0,3 г/л, MnCl2•4H2O 0,3 г/л и CoCl2•6H2O pH 7,3 соответственно по 100 мл среды в колбе Эрленмейера на 300 мл.
Инкубацию проводят при 30oC во вращающейся встряхивающей машине. Через 48, 96 и 144 часа определяют концентрацию A 1437 липопептидов в фильтрате культуры методом HPLC высокоэффективной жидкостной хроматографии при высоком давлении (см. пример 6). В средах 2 и 3 при штамме Actinoplanes nipponensis ATCC 31145 липопептидов не обнаруживают. В среде 1 через 144 часа удается определить очень незначительные количества некоторых липопептидов. Если в качестве основы использовать специфическую идентичную экстинкцию этих соединений в сравнении с A 1437 пептидами, то образующееся количество составит по меньшей мере в 100 раз (более 1 мг/л) низкую концентрацию A 1437 B, которую удалось получить при синтезе из штамма Actinoplanes spec. DSM 7358 в среде 1 за тот же период времени.
8) Активность A 1437 липопептидов.
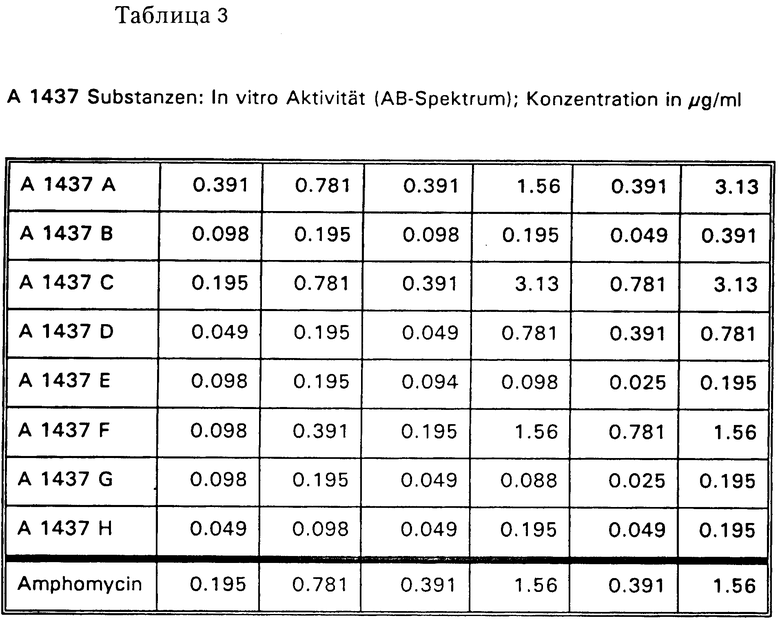
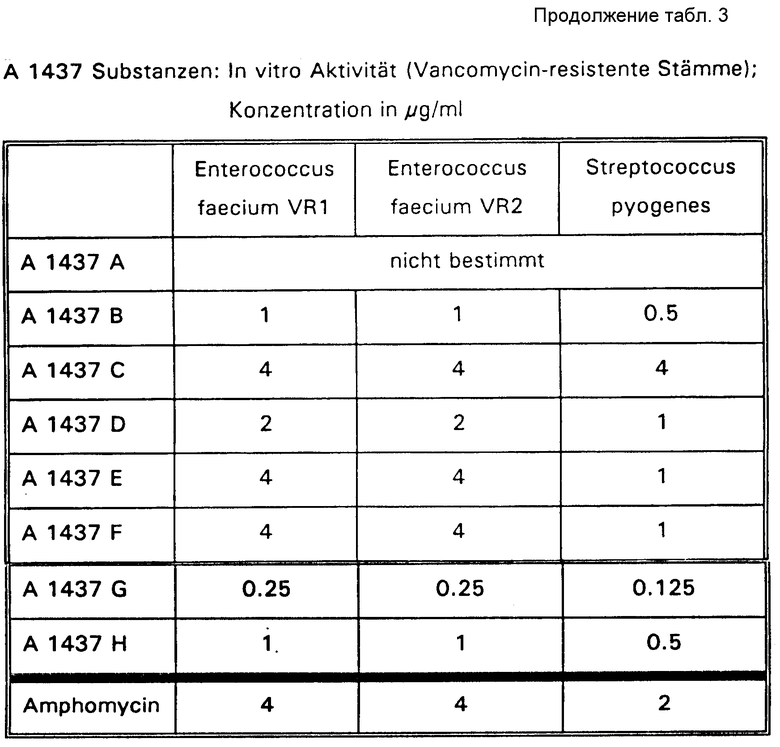
Чувствительность относящихся микроорганизмов к A 1437 липопептидам определяют с помощью Агар - разбавление - теста. В качестве агара используют агар Бюллера-Хинтона с добавлением к нему в случае с S.pyogenes и Enterococcen 10% крови лошади. Содержащие антибиотик пластины прививают с помощью многоканального шприцевого устройства (5•104 единиц/место стационарной культурой соответствующего штамма). Минимальную ингибирующую концентрацию МНК определяют при 37oC. Минимальная ингибирующая концентрация представляет собой концентрацию антибиотика, при которой после 24-часовой инкубации не отмечается видимого роста микроорганизмов.
Результаты приведены в таблице 3. Используемый в качестве контрольного вещества амфомицин получают с фирмы Берингер Маннгейм (Германия).
Амфомицин производят на фирме в виде тонкого химиката
Соединения K, L M обладают активностью in vitro, сравнимой с активностью соединений A - H.
9a) Характеристика A 1437 D.
Липопептид A 1437 D выделяют в виде твердого аморфного вещества.
Данные оптического вращения: +35o (с = 0,1 метанол).
HPLC: Высокоэффективная жидкостная хроматография при высоком давлении:
время удерживания: 15,1 минут.
Аминокислоты: 2 аспарагиновые кислоты, 1 аспарагин, 1 β -метиласпартат, 2 глицина, 2 2,3-диаминомасляные кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин
FAB-MS: m/e = 1303, 6952 /(M+H)+/
Молярная масса: 1302, 6884 (C59H94N14O19)
CID-MS: m/z = 356, 491, 517, 520, 741, 761, 938, 982
ИК/KBr/:v = 3420 (шир.), см-1, 2930, 1660, 1530, 1450, 1400.
9b) Характеристика A 1437 B
Липопептид A 1437 B выделяют в виде твердого аморфного продукта.
Значение оптического вращения: +27o (с = 0,1, метанол)
HPLC: Высокоэффективная жидкостная хроматография при высоком давлении:
время удерживания: 12,8 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицин, 2 2,3-диаминомасляные кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
FAB-MS: m/e = /(M+H)+/
Молярная масса: 1303 (C59H93N13O20)
CID-MS: m/z = 356, 407, 518, 521, 741, 762, 938, 982
ИК (KBr): δ = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9c) Характеристика A 1437 C
Липопептид A 1437 C выделяют в виде твердого аморфного вещества.
Значение оптического вращения: +30o /с = 0,1, метанол/
HPLC: Высокоэффективная жидкостная хроматография при высоком давлении:
время удерживания: 14,1 минут.
Аминокислоты: 2 аспарагиновые кислоты, 1 аспарагин, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
Молярная масса 1288 (С58H92N14O19).
CID-MS: m/z = 356, 392, 503, 503, 741, 747, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2930, 1660, 1530, 1450, 1400.
9d) Характеристика A 1437 A.
Липопептид A 1437 A выделяют в виде твердого аморфного вещества.
Оптическое вращение: +30o /с = 0,1, метанол/
HPLC: Высокоэффективная жидкостная хроматография при высоком давлении:
время удерживания: 11,8 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
молярная масса: 1289 (C58H91N13O20)
CID-MS: m/z = 356, 478, 504, 507, 741, 748, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9e) Характеристика A 1437 F.
Липопептид A 1437 F выделяют в виде твердого аморфного вещества.
Значение оптического вращения: +31o /с = 0,1, метанол/,
HPLC: Высокоэффективная жидкостная хроматография при высоком давлении:
время удерживания: 13,8 минут.
Аминокислоты: 2 аспарагиновые кислоты, 1 аспарагин, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
молярная масса: 1288 (C58H92N14O19)
CID-MS: m/z = 356, 392, 503, 506, 741, 747, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2930, 1660, 1530, 1450, 1400.
9f) Характеристика A 1437 E.
Липопептид A 1437 E выделяют в виде твердого аморфного вещества.
Высокоэффективная жидкостная хроматография:
время удерживания: 11,5 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
молярная масса: 1289 (C58H91N13O20)
CID-MS: m/z = 356, 393, 504, 507, 741, 748, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9g) Характеристика A 1437 H.
Липопептид A 1437 H выделяют в виде твердого аморфного вещества.
Значение оптического вращения: +32o /с = 0,1, метанол/
HPLC: Высокоэффективная жидкостная хроматография:
время удерживания: 15,9 минут.
Аминокислоты: 2 аспарагиновые кислоты, 1 аспарагин, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
молярная масса: 1316 (C60H96N14O19)
CID-MS: m/z = 356, 420, 531, 534, 741, 775, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2930, 1660, 1530, 1450, 1400.
9h) Характеристика A 1437 G.
Липопептид A 1437 G выделяют в виде твердого аморфного вещества.
Значение оптического вращения: +34o /с = 0,1, метанол/
HPLC: Высокоэффективная жидкостная хроматография
время удерживания: 13,6 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколиновая кислота, 1 валин.
молярная масса: 1317 (C60H95N13O20)
CID-MS: m/z = 356, 421, 532, 535, 741, 776, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9i) Характеристика A 1437 K.
Липопептид A 1437 K выделяют в виде твердого аморфного вещества.
HPLC: Высокоэффективная жидкостная хроматография:
время удерживания: 12,5 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколин, 1 валин.
FAB-MS: m/z = /(M + H)+/
молярная масса: 1299 (C58H91N13O20).
CID-MS: m/z = 393, 504, 507, 741, 748, 938, 981
IK (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9j) Характеристика A 1437 L.
Липопептид A 1437 L выделяют в виде твердого аморфного вещества.
HPLC: Высокоэффективная жидкостная хроматография:
время удерживания: 13,0 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколин, 1 валин.
FAB = = MS: m/e = /(M + H)+/
молярная масса: 1289 (C59H93N13O20).
CID-MS: m/z = 407, 518, 741, 761, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
9k) Характеристика A 1437 M.
Липопептид A 1437 M выделяют в виде твердого аморфного вещества.
HPLC: Высокоэффективная жидкостная хроматография:
время удерживания: 9,8 минут.
Аминокислоты: 3 аспарагиновые кислоты, 1 β - метиласпартат, 2 глицина, 2 2,3-диаминомасляных кислоты, 1 пролин, 1 пипеколин, 1 валин.
FAB-MS: m/e = /(M + H)+/
молярная масса: 1275 (C57H89N13O20).
CID-MS: m/z = 379, 490, 493, 724, 741, 938, 981
ИК (KBr): v = 3420 (шир.), см-1, 2925, 1650, 1535, 1450, 1400.
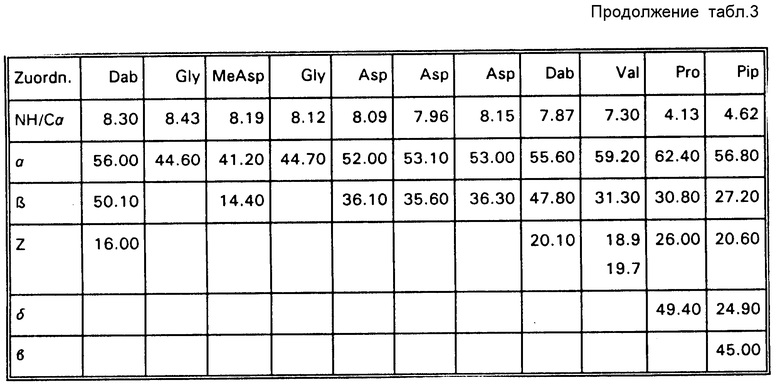
10) C13-химические сдвиги.
В таблице 4 представлены C-13-химические сдвиги CH-сигналов A 1437 B.
Для сравнения с 1H-данными, NH-химические соединения NH-сигналов соответственно для Pip и Pro даются с указанием CaP-сдвигов соответствующих спиновых систем.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ЛИПОПЕПТИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2141970C1 |
| Способ получения фунгистатических липопептидов | 2023 |
|
RU2825156C1 |
| ГЛИКОПЕПТИДЫ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ, ОБЛАДАЮЩИЙ АНТИБИОЦИДНЫМ ДЕЙСТВИЕМ | 1992 |
|
RU2099349C1 |
| СПОСОБ ОЧИСТКИ ЛИПОПЕПТИДА (ВАРИАНТЫ), АНТИБИОТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ОЧИЩЕННОГО ЛИПОПЕПТИДА (ВАРИАНТЫ) | 2001 |
|
RU2311460C9 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛА ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ СОВМЕСТИМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СРЕДСТВО ДЛЯ СНИЖЕНИЯ ВЫСОКОГО ДАВЛЕНИЯ КРОВИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ СНИЖЕНИЯ КРОВЯНОГО ДАВЛЕНИЯ | 1993 |
|
RU2116300C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПЕПТИДАМИДОВ ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ СОВМЕСТИМЫХ АЦЕТАТОВ ИЛИ ГИДРОХЛОРИДОВ | 1991 |
|
RU2036200C1 |
| ИМИДАЗО-АННЕЛИРОВАННЫЕ ИЗО- И ГЕТЕРОЦИКЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2076105C1 |
| ЗАМЕЩЕННЫЕ ОСНОВАНИЕМ БЕНЗОИЛГУАНИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ИНГИБИРОВАНИЯ КЛЕТОЧНОГО NA/H-АНТИПОРТЕРА | 1996 |
|
RU2161604C2 |
| ЗАМЕЩЕННЫЕ АЗОЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2047604C1 |
| 3' И/ИЛИ 2'-АМИНО- ИЛИ ТИОЛМОДИФИЦИРОВАННЫЕ НУКЛЕОЗИДЫ, НУКЛЕОТИДЫ ИЛИ ОЛИГОНУКЛЕОТИДЫ, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ | 1991 |
|
RU2073682C1 |

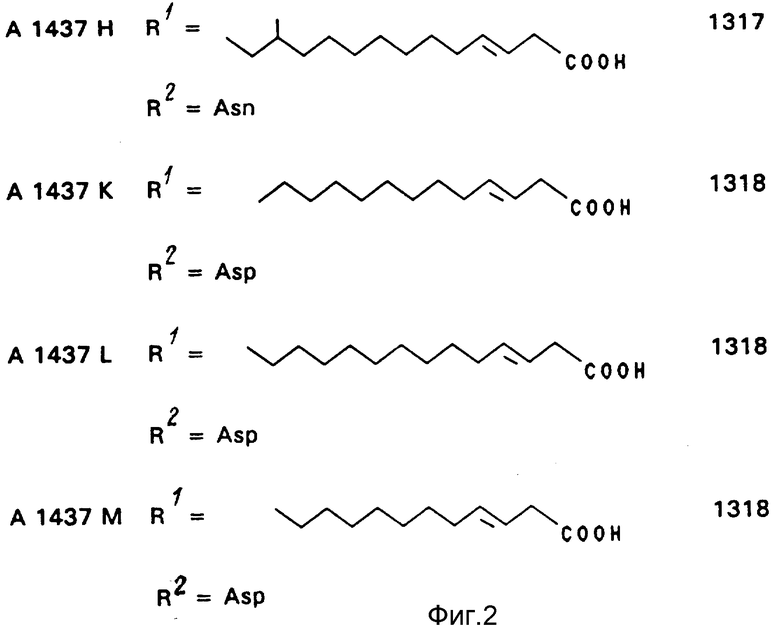
Использование: в медицине. Сущность изобретения: липопептиды формулы I: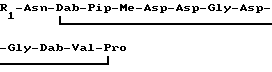 ,
,
где R1 = 3,4-ненасыщенная или насыщенная или независимо от этого разветвленная или неразветвленная жирная кислота с длиной цепи от 12 до 15 включительно атомов углерода; способ их получения заключается в том, что культивируют Actinoplanes sp. DSM-7358 в питательной среде, содержащей источники углерода, азота и минерального вещества в аэробных условиях с последующим выделением посредством осаждения при pH 0,5 - 4,0 и очисткой на ионообменных смолах или хроматографии на гидрофобной матрице, причем обе хроматографии можно проводить альтернативно или последовательно в любой последовательности, лекарственное средство, обладающее антибиотической активностью против граммположительных бактерий, в особенности против бактерий, устойчивых к гликопептидам на основе активнодействующего вещества и соответствующего фармацевтического носителя, содержащее в качестве активного вещества липопептиды формулы I в эффективном количестве; штамм Actinoplanes sp. DSM-7358 в качестве продуцента липопептидов I. 4 с. и 9 з.п. ф-лы, 2 ил. , 4 табл.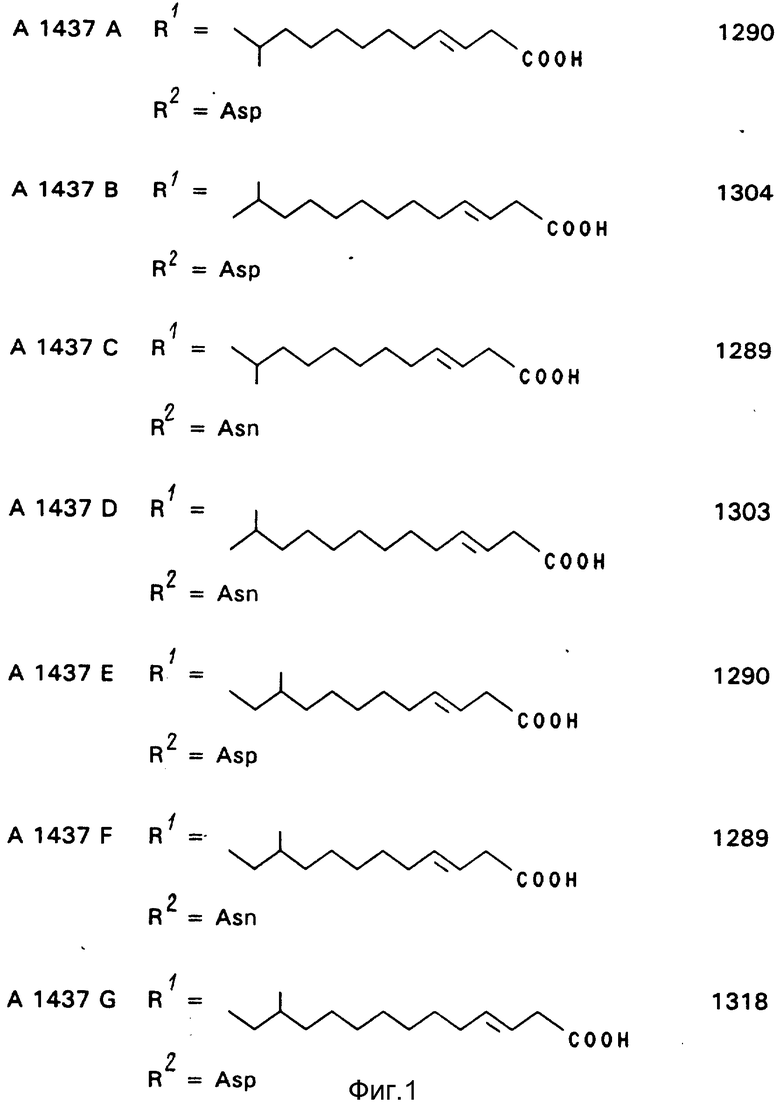
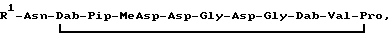
где R1 - 3,4-ненасыщенная, или насыщенная, или независимо от этого разветвленная или неразветвленная жирная кислота с длиной цепи 12 - 15 атомов углерода.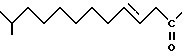
6. Липопептид по п.4, отличающийся тем, что R1 означает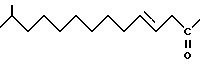
7. Липопептид по п.4, отличающийся тем, что R1 означает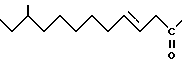
8. Липопептид по п.4, отличающийся тем, что R1 означает
9. Способ получения липопептидов по пп.1 - 8, заключающийся в том, что культивируют Actinoplanes sp. DSM 7358 в питательной среде, содержащей источники углерода, азота и минеральные вещества в аэробных условиях с последующим выделением целевого продукта и его очисткой.
| Neu H.C | |||
| Science | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Bodasnzky Miklos, Sigler Gerald F.et.al | |||
| Journal amer | |||
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Strong Robert C., Bodanszky Agnes et al | |||
| Antimicrobial Agents and chemotherapy | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| US, патент, 4001397, A 61 K 35/74, 1972 | |||
| EP, заявка, 0448343, C 07 K 7/06, 1991. | |||
Авторы
Даты
1998-08-20—Публикация
1994-06-07—Подача