Область техники
Настоящее изобретение относится к новым производным диметилфуранкарбоксианилида, проявляющих превосходное противомикробное действие, к антисептику для древесины, содержащему производное диметилфуранкарбоксианилида в качестве активного компонента, и к защитной композиции для древесины, в которой производное диметилфуранкарбоксианилида в качестве одного из активных компонентов, объединено с каким-либо коммерчески отступным антисептиком древесины, действие которого уже подтверждено.
Предшествующий уровень техники
Чтобы предохранить лесоматериалы от гниения, происходящего из-за разнообразных грибков, вызывающих гниение древесины, ранее использовались различные виды неорганических и органических соединений. Однако у этих препаратов имеются недостатки, такие как воздействие на организм человека вследствие их высокой токсичности, видимое загрязнение окружающей среды, необходимость их высокой концентрации при применении и дороговизна.
Что касается соединений, относящихся к производным диметилфуранкарбоксианилида по настоящему изобретению, соединения, представленные ниже формулой, были описаны в заявке Japanese Patent Kokai Applicаtion Sho 50-10376 в качестве химических препаратов, предотвращающих повреждение растений; в которых, однако, радикал R ограничен фенилом, нитрозамещенным фенилом, карбоксизамещенным фенилом, фенилзамещенным фенилом, метилзамещенным фенилом, галогензамещенным фенилом или метоксизамещенным фенилом. К тому же этот патент умалчивает о других производных, и не описана активность этих соединений в отношении разрушающих древесину грибков.

Сущность изобретения
Целью настоящего изобретения является создание нового антисептика для древесины, который более безопасен и который может быть более эффективно использован в низких концентрациях и/или при этом стоимость его должна быть невысокой.
Учитывая подобную ситуацию, упомянутую выше, авторы настоящего изобретения рассмотрели производные фуранкарбоксианилида и интенсивно их исследовали. Результатом исследований заявителей явилось то, что новые производные диметилфуранкарбоксианилида, представленные нижеследующей формулой I, очень полезны в качестве антисептиков для древесины, и более того, если производное диметилфуранкарбоксианилида в качестве активного компонентf комбинируется с любым другим коммерчески доступным антисептиком для древесины, может наблюдаться эффект усиления действия, и может быть изготовлен защитный состав для древесины.
Соединениями по настоящему изобретению являются производные диметилфуранкарбоксианилида, представленные общей формулой
В этой формуле R1 и R2 одинаковы или различны и каждый представляет собой атом водорода; алкильную группу, содержащую от 2 до 6 атомов углерода; циклоалкильную группу, содержащую от 3 до 6 атомов углерода; алкенильную группу, содержащую от 3 до 6 атомов углерода; алкинильную группу, содержащую от 2 до 6 атомов углерода; галогеналкильную группу, содержащую от 1 до 3 атомов углерода; алкоксигруппу, содержащую от 2 до 6 атомов углерода; алкоксиалкиленовую группу, содержащую от 1 до 6 атомов углерода в алкоксисоставляющей части и содержащую от 1 до 6 атомов углерода в алкиленовой составляющей части; цианогруппу; замещенную амидную группу; алкоксикарбонильную группу, содержащую от 1 до 6 атомов углерода в алкокси части; бензоильную группу, которая может, необязательно, содержать от 1 до 2 заместителей; бензоиламиногруппу, которая может, необязательно, содержать от 1 до 2 заместителей; алканоил-аминогруппу, содержащую от 2 до 6 атомов углерода; циклоалкилкарбониламиногруппу, содержащую от 3 до 6 атомов углерода в циклоалкильной части; бензильную группу, которая может, необязательно, содержать от 1 до 2 заместителей; фенильную группу, которая может, необязательно, содержать от 1 до 2 заместителей; или алкоксикарбонилалкениленовую группу, содержащую от 1 до 6 атомов углерода в алкокси части и содержащую от 2 до 5 атомов углерода в алкениленовой части; причем R1 и R2 одновременно не являются атомами водорода.
Настоящее изобретение относится к вышеуказанным соединениям, антисептику для древесины и антисептической композиции для древесины, содержащей производное диметилфуранкарбоксианилида в качестве активного компонента.
Краткое описание чертежей
На фиг. 1 (a) - (e) показаны минимальные ингибирующие концентрации (в миллионных долях - млн-1) соединения по примеру 1 в сочетании с различными антисептиками для древесины. На фиг. 2 (a) - (e) показаны минимальные ингибирующие концентрации (млн-1) соединения по примеру 2 в сочетании с различными антисептиками для древесины.
Наилучший способ использования изобретения
В указанной общей формуле I в качестве алкильной группы, содержащей от 2 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана алкильная группа с линейной или разветвленной цепью, такая как этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, гексил, изогексил или втор-гексил; особенно предпочтительно, алкильная группа, содержащая от 2 до 6 атомов углерода.
В указанной общей формуле I в качестве циклоалкильной группы, содержащей от 3 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана циклоалкильная группа, такая как циклопропил, циклобутил, циклопентил или циклогексил; предпочтительно, циклоалкильная группа, содержащая от 3 до 6 атомов углерода; и, более предпочтительно, циклоалкильная группа, содержащая от 5 до 6 атомов углерода.
В указанной общей формуле I в качестве алкенильной группы, содержащей от 3 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана алкенильная группа, такая как аллил, изопропенил, металлил, 2-бутенил, 3-бутенил, 1,3-бутандиенил, 2-пентенил или 2-гексенил; предпочтительно, алкенильная группа, содержащая от 3 до 4 атомов углерода; и, более предпочтительно, изопропенил.
В указанной общей формуле I в качестве алкинильной группы, содержащей от 2 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана алкинильная группа, такая как этинил, пропаргил, 2-бутинил, 4-пентинил или 2-гексинил; предпочтительно, алкинильная группа, содержащая от 2 до 4 атомов углерода; и, более предпочтительно, этинил.
В указанной общей формуле I в качестве галогеналкильной группы, содержащей от 1 до 3 атомов углерода, которая включена в определения для R1 и R2, может быть указана галогеналкильная группа, такая как трифторметил, трихлорметил, пентафторэтил, 2,2,2-трихлорэтил, или 2,4-дихлорпропил; предпочтительно, галогеналкильная группа, содержащая от 1 до 2 атомов углерода; и, более предпочтительно, трифторметил.
В указанной общей формуле I в качестве алкоксигруппы, содержащей от 2 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана алкоксигруппа с линейной или разветвленной цепью, такая как этокси, пропокси, изопропокси, бутокси, пентокси или гексилокси; предпочтительно, алкоксигруппа, содержащая от 2 до 4 атомов углерода; и, более предпочтительно, алкоксигруппа, содержащая от 2 до 3 атомов углерода.
В указанной общей формуле I в качестве содержащей от 1 до 6 атомов углерода алкоксигруппы, входящей в состав алкоксиалкильной группы, содержащей от 1 до 6 атомов углерода в алкокси части и содержащей от 1 до 6 атомов углерода в алкильной части, которая включена в определения для R1 и R2, может быть указана алкоксигруппа с линейной или разветвленной цепью, такая как метокси, этокси, пропокси, изопропокси, бутокси, пентокси, неопентокси или гексилокси; предпочтительно, алкоксигруппа, содержащая от 1 до 5 атомов углерода; и, более предпочтительно, алкоксигруппа, содержащая от 1 до 3 атомов углерода или содержащая 5 атомов углерода.
В указанной общей формуле I в качестве алкиленовой группы, входящей в состав алкоксиалкиленовой группы, содержащей от 1 до 6 атомов углерода в алкокси части и от 1 до 6 атомов углерода в алкиленовой части, которая включена в определения для R1 и R2, может быть указана алкиленовая группа с линейной или разветвленной цепью, такая как метилен, этилен, пропилен, триметилен, тетраметилен, пентаметилен или гексаметилен; предпочтительно, алкиленовая группа, содержащая от 1 до 2 атомов углерода; и, более предпочтительно, метилен.
В указанной общей формуле I в качестве замещенной амидной группы, которая включена в определения для R1 и R2, может быть указана моноалкиламидная группа, такая как метиламид, этиламид, изопропиламид, бутиламид, втор-бутиламид; диалкиламидная группа, такая как диметиламид, диэтиламид, диизопропиламид, дибутиламид, ди-втор-бутиламид, метилэтиламид, метилизопропиламид, метилбутиламид, метил-втор-бутиламид, этилизопропиламид, изопропилбутиламид, пирролидиламид или пиперидиламид; необязательно замещенный фениламид, такая как фениламид, 2-хлорфениламид, 2,4-дихлорфениламид, 2-метилфениламид, 2-этилфениламид или 4-метоксифениламид; предпочтительно, метиламид, пиперидиламид или фениламид.
В указанной общей формуле I в качестве алкоксикарбонильной группы, содержащей от 1 до 6 атомов углерода в алкокси части, которая включена в определения для R1 и R2, может быть указана группа, которая образована вышеупомянутой алкоксигруппой, содержащей от 1 до 6 атомов углерода, входящей в состав алкоксиалкильной группы, содержащей от 1 до 6 атомов углерода в алкокси части и содержащей от 1 до 6 атомов углерода в алкильной части, и карбонильной группой, такая как группа метоксикарбонил, этоксикарбонил, изопропоксикарбонил, бутоксикарбонил, вторбутоксикарбонил, трет-бутокси-карбонил, пентилоксикарбонил, или гексилоксикарбонил; предпочтительно, алкоксикарбонильная группа, содержащая от 1 до 3 атомов углерода в алкокси части.
В указанной общей формуле I в качестве бензильной группы, которая может, необязательно, содержать от 1 до 2 заместителей, которая включена в определения для R1 и R2, может быть указана необязательно замещенная бензоильная группа, такая как бензоил, 2-хлорбензоил, 2,4-дихлорбензоил, 2-метилбензоил, 2,4-диметилбензоил 4-этилбензоил или 4-метоксибензоил; предпочтительно, бензоил.
В указанной общей формуле I в качестве бензоиламиногруппы, которая может, необязательно, содержать от 1 до 2 заместителей, которая включена в определения для R1 и R2, может быть указана необязательно замещенная бензоиламиногруппа, которая образована замещением в аминогруппе (группах) вышеуказанной бензольной группой, которая может, необязательно, содержать от 1 до 2 заместителей, такая как бензоиламино, 2-хлорбензоиламино, 2,4-дихлорбензоиламино, 2,4-диметилбензоиламино, 4-метилбензоиламино, 4-этилбензоиламино или 4-метоксибензоиламино; предпочтительно бензоиламино.
В указанной общей формуле I в качестве алканоиламиногруппы, содержащей от 2 до 6 атомов углерода, которая включена в определения для R1 и R2, может быть указана ацетиламиногруппа, пропиониламиногруппа, бутириламиногруппа, изобутириламиногруппа, валериламиногруппа, изовалериламиногруппа, капроиламиногруппа или изокапроиламиногруппа; предпочтительно ацетиламиногруппа.
В указанной общей формуле I в качестве циклоалкилкарбониламиногруппы, содержащей от 3 до 6 атомов углерода в циклоалкильной части, которая включена в определения для R1 и R2, может быть указана группа циклопропилкарбониламино, циклобутилкарбониламино, циклопентилкарбониламино или циклогексилкарбониламино; предпочтительно циклогексилкарбониламино.
В указанной общей формуле I в качестве бензильной группы, которая может, необязательно, содержать от 1 до 2 заместителей, которая включена в определения для R1 и R2, может быть упомянут бензил, 2-метилбензил, 2,4- диметилбензил, 2-хлорбензил, 4-метоксибензил или 4-этоксибензил; предпочтительно бензил.
В указанной общей формуле I в качестве алкоксикарбонилалкениленовой группы, содержащей от 1 до 6 атомов углерода в алкокси части и содержащей от 2 до 5 атомов углерода в алкениленовой части, которая включена в определения для R1 и R2, может быть упомянут метоксикарбонилвинилен, этоксикарбонил-2-пропенилен, метоксикарбонил-2-бутенилен или этоксикарбонил-2-пентенилен; предпочтительно, метоксикарбонилвинилен.
Предпочтительные соединения, соответствующие указанной формуле I, включают соединения, в которых R1 и R2 одинаковы или различны, каждый из них представляет собой атом водорода; алкильную группу, содержащую от 2 до 6 атомов углерода; алкенильную группу, содержащую от 3 до 4 атомов углерода; алкинильную группу, содержащую от 2 до 4 атомов углерода; циклоалкильную группу, содержащую от 3 до 6 атомов углерода; алкоксикарбонильную группу, содержащую от 1 до 6 атомов углерода в алкокси части; алкоксиалкиленовую группу, содержащую от 1 до 6 атомов углерода в алкокси части и содержащую от 1 до 2 атомов углерода в алкиленовой части; циклоалкилкарбониламиногруппу, содержащую от 3 до 6 атомов углерода в циклоалкильной части; алкоксигруппу, содержащую от 2 до 4 атомов углерода; бензоильную группу, которая может, необязательно, содержать от 1 до 2 заместителей; бензильную группу, которая может, необязательно, содержать от 1 до 2 заместителей; или алкоксикарбонилалкениленовую группу, содержащую от 1 до 6 атомов углерода в алкокси части и содержащую от 2 до 5 атомов углерода в алкениленовой части; причем R1 и R2 одновременно не представляют атомы водорода. Более предпочтительные, указанные соединения включают такие, в которых: (2) R1 и R2 одинаковы или различны и, каждый, из них представляет собой атом водорода; алкильную группу, содержащую от 2 до 6 атомов углерода; алкенильную группу, содержащую от 3 до 4 атомов углерода; циклоалкильную группу, содержащую от 5 до 6 атомов углерода; алкоксикарбонильную группу, содержащую от 1 до 3 атомов углерода в алкокси части; алкоксиметиленовую группу, содержащую от 1 до 6 атомов углерода в алкокси части; циклоалкилкарбониламиногруппу, содержащую от 4 до 6 атомов углерода в циклоалкильной части; бензоильную группу; бензильную группу, которая может, необязательно, содержать 1 заместитель; или алкоксикарбонилалкениленовую группу, содержащую от 1 до 3 атомов углерода в алкокси части и содержащую от 2 до 4 атомов углерода в алкениленовой части; причем R1 и R2 одновременно не представляют атомы водорода. Особенно предпочтительные указанные соединения включают такие, в которых:
(3) R1 представляет 3-алкильную группу, содержащую от 2 до 6 атомов углерода; 3-алкоксикарбонильную группу, содержащую от 1 до 3 атомов углерода в алкокси части; 3-алкоксиметиленовую группу, содержащую от 1 до 3 атомов углерода в алкокси части; циклоалкилкарбониламиногруппу, содержащую от 4 до 6 атомов углерода в циклоалкильной части; бензильную группу, которая может быть замещена метоксигруппой; бензоильную группу; или алкоксикарбонилалкениленовую группу, содержащую от 1 до 3 атомов углерода в алкокси части и содержащую от 2 до 3 атомов углерода в алкениленовой части; и
(4) R2 представляет атом водорода.
Примеры новых производных диметилфуранкарбоксианилида, которые могут использоваться в качестве активного компонента антисептика для древесины по настоящему изобретению, представлены в следующей таблице.
В табл. 1 использованы следующие сокращения:
Bz - бензил
Bu - бутил
Et - этил
Hx - гексил
Me - метил
Ph - фенил
Pip - пиперидил
Pn - пентил
Pr - пропил
Среди приведенных выше соединений к предпочтительным относятся соединения N 3, 4, 5, 6, 7, 8, 10, 11, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 31, 33, 35, 36, 38, 40, 42, 43, 44, 45, 46, 48, 49, 50, 51, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 64, 69, 70, 71, 72, 75, 80, 81, 82, 83, и 85; а к наиболее предпочтительным относятся соединения NN 3, 6, 10, 19, 22, 24, 26, 27, 33, 35, 36, 38, 40, 42, 44, 45, 46, 48, 53, 55, 60, 61, 69, 70, 81, 83 и 85.
Соединения согласно указанной общей формуле I могут быть получены по способу, представленному либо следующим способом A, или способом B.
Способ A
Способ B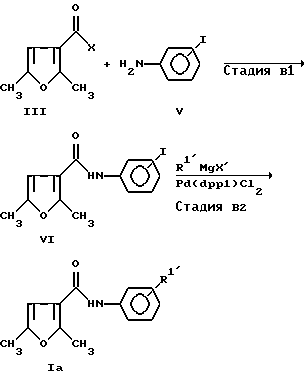
В приведенных формулах R1 и R2 определены как указано выше. R1 представляет собой C1-C6 алкильную группу, C3-C6 циклоалкильную группу или бензильную группу, которая может, необязательно, содержать 1 или 2 заместителя. Соединение формулы Ia представляет собой соединение общей формулы I, в котором R2 представляет собой R1, а R1 обозначает атом водорода. Соединение формулы V является иодзамещенным анилином. X обозначает атом галогена, такой как хлор, бром или йод, предпочтительно хлор. X обозначает атом галогена, такой как хлор, бром или йод, предпочтительно, бром или йод.
Соединения по настоящему изобретению могут быть получены хорошо известными способами.
Стадия A1 включает получение соединения общей формулы I путем взаимодействия соединения общей формулы III с соединением общей формулы IV в инертном растворителе в присутствии дегидрогалогенизирующего агента.
Соединение формулы III, используемое в качестве исходного продукта на этой стадии, может быть получено путем гидролиза 2,5-диметилфуран-3-карбоксилата, который может быть получен путем конденсации хлорацетона с ацетоацетатом и последующим галогенированием.
Соединение формулы IV, используемое в качестве исходного продукта на этой стадии, является производным анилина, которое является коммерчески доступным или может быть получено при помощи хорошо известных способов.
Примеры используемых инертных растворителей включают, например, простые эфиры, такие как эфир, изопропиловый эфир, тетрагидрофуран или диоксан; ароматические углеводороды, такие как бензол, толуол или ксилол; галоидированные углеводороды, такие как дихлорметан, хлороформ или четыреххлористый углерод; и смеси двух или более из этих растворителей; предпочтительно, ароматические углеводороды (особенно толуол).
Примеры используемых дегидрогалоидирующих агентов включают, например, третичные амины, такие как триэтиламин, N,N-диметиламинопиридин или им подобные, и пиридины. Эту реакцию можно проводить в присутствии или в отсутствие растворителя. Для того, чтобы плавно провести реакцию с использованием растворителя, реакцию проводят при температуре от 0oC до температуры кипения используемого растворителя, предпочтительно от комнатной температуры до 100oC. Время, требуемое для проведения реакции, составляет, в целом, от 30 минут до 5 часов, предпочтительно, от 30 минут до 2 часов.
Стадия B1 включает получения соединения, имеющего общую формулу (VI), путем взаимодействия соединения, имеющего общую формулу III, с соединением, имеющим общую формулу V, в инертном растворителе в присутствии дегидрогалоидирующего агента.
Соединение формулы V, используемое в качестве исходного продукта на этой стадии, является производным анилина, которое промышленно выпускается или может быть получено при помощи хорошо известных способов.
Условия проведения реакции, применяемые на этой стадии, подобны условиям, применяемым на стадии A1.
Стадия B2 включает получения соединения, имеющего общую формулу Ia, путем взаимодействия соединения, имеющего общую формулу VI, с реактивом Гриньяра, имеющим общую формулу:
R1′MgX′,
в инертном растворителе в присутствии катализатора.
Примеры предпочтительных используемых инертных растворителей включают, например, простые эфиры, такие как диэтиловый эфир изопропиловый эфир, тетрагидрофуран или диоксан; в особенности предпочтительно, диэтиловый эфир.
В качестве особенно предпочтительного катализатора может быть использован хлорид [1,1'-бис(дифенилфосфино)-ферроцен]палладия (II) (Pd(dppf)Cl2).
Реактивы Гриньяра, используемые в этом процессе, являются коммерческими доступными или могут быть получены путем взаимодействия магния с алкилгалогенидом, представленным формулой 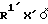 (где R1′ и X' определены как указано выше) в соответствии с хорошо известными способами.
(где R1′ и X' определены как указано выше) в соответствии с хорошо известными способами.
Реакцию обычно проводят при температуре от 0oC до 50oC, предпочтительно, при комнатной температуре. Хотя время, требуемое для этой реакции, изменяется в зависимости от природы растворителя и реагента, которые используются, обычно реакция полностью завершается за время в пределах от 10 часов до 10 дней.
Соединения, имеющие указанную общую формулу I в соответствии с настоящим изобретением, обладают сильной антисептической активностью в отношении древесины при низкой концентрации, по сравнению с активностью, проявляемой существующими антисептиками для древесины. Композиция, состоящая из комбинации вышеупомянутого соединения I с известным антисептиком для древесины, дает синергетический эффект, и требуются более низкие концентрации, чем можно было бы ожидать на основании активности, проявляемой каждым компонентом по отдельности, так что у композиции проявляется эффективная антисептическая активность в отношении древесины при низкой концентрации. Следовательно, новые производные диметилфуранкарбоксианилида являются крайне эффективными в качестве антисептиков для древесины в низкой концентрации, чем решается одна из проблем улучшения качества жизни.
Следующие примеры иллюстрируют получение соединений по настоящему изобретению и приготовление составов на их основе более подробно. Эти примеры не могут истолковываться как ограничивающие объем настоящего изобретения.
Пример 1
3'-Ацетиламино-2,5-диметилфуран-3-карбоксианилид
К раствору 0,50 г 2,5 диметилфуран-3-карбонилхлорида в 10 мл дихлорметана добавляли 0,44 мл триэтиламина и 0,47 г 3-ацетиламиноанилина при охлаждении льдом, и получившуюся смесь перемешивали при комнатной температуре в течение 2,5 часов, после чего нагревали с обратным холодильником в течение 4,5 часов. После того, как реакционная смесь охлаждалась, ее разбавляли путем добавления 10 мл дихлорметана. Разбавленную смесь последовательно промывали 1 н. гидроксидом натрия, 1 н. соляной кислотой и насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия, после чего отгоняли растворитель. Остаток очищали при помощи колоночной хроматографии на силикагеле и желательные фракции перекристаллизовывали из этилацетата с получением 0,51 г желаемого соединения в виде белых кристаллов с выходом 59,4%.
Т.пл.: 172,0 - 172,5oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 8,4 (1H, ушир.), 7,95 (1H, ушир.), 7,88 (1H, м), 7,4 (1H, м), 7,32 (1H, м), 7,25 (1H, т, J=8 Гц), 6,25 (1H, с), 3,55 (3H, с), 2,25 (3H, с), 2,15 (3H, с).
ИК (KBr) см-1: 3306, 1672, 1651, 1086, 781.
Элементный анализ (%): Вычислено для C15H16N2O3: C, 66,16; H, 5,92; N, 10,29. Найдено: C, 66,30; H, 5,98; N, 10,32.
Следуя методике, подобной описанной выше, но используя подходящее производное анилина вместо 3-ацетиламиноанилина, получали следующие соединения.
Пример 2
3'-(N-метилкарбамоил)-2,5-диметилфуран-3-карбоксианилид
Выход: 42,0%
T. пл.: 212,0 - 213,0oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 8,5 (1H, ушир.), 8,05 (1H, м), 7,88 (1H, м), 7,52 (1H, м), 7,38 (1H, т, J=8 Гц), 6,8 (1H, ушир.), 6,35 (1H, с), 2,95 (3H, д, J=1,4 Гц), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3293, 1638, 1581, 1074, 689.
Элементный анализ (%): Вычислено для C15H16N2O3: C, 66,16; H, 5,92; N, 10,29. Найдено: C, 66,08; H, 6,20; N, 10,28.
Пример 3
3'-(1-Пиперидилкарбонил)-2,5-диметилфуран-3-карбоксианилид
Выход: 50,0% T.пл.: 183,0 - 185,0oC
1H ЯМР (CDCl3) δ млн-1: 7,68 (1H, м), 7,55 (2H, м), 7,35 (1H, т, J=8 Гц), 7,1 (1H, м), 6,15 (1H, с), 3,7 (2H, ушир.), 3,35 (2H, ушир.), 2,55 (3H, с), 2,25 (3H, с), 2,75 - 1,4 (6H, м).
ИК (KBr) см-1: 3302, 1663, 1615, 1065, 808.
Элементный анализ (%): Вычислено для C19H22N2O3: C, 69,92; H, 6,79; N, 8,58. Найдено: C, 69,52; H, 6,88; N, 8,48.
Пример 4
3'-(N-фенилкарбамоил)-2,5-диметилфуран-3-карбоксианилид
Выход: 53,5%
T.пл.: 182,5 - 184,0oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 8,48 (1H, ушир.), 8,2 (1H, ушир.), 8,1 (1H, с), 7,95 (1H, м), 7,7 (2H, д, J = 8 Гц), 7,65 (1H, д, J=8 Гц), 7,45 (1H, т, J=8 Гц), 7,35 (2H, т, J=8 Гц), 7,15 (1H, т, J=8 Гц), 6,28 (1H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3282, 1646, 1080, 755, 691
Элементный анализ (%): Вычислено для C20H18N2O3: C, 71,84; H, 5,43; N, 8,38. Найдено: C, 71,87; H, 5,64; N, 8,34.
Пример 5
3'-Трет-бутоксикарбонил-2,5-диметилфуран-3-карбоксианилид
Выход: 92,0%
T. пл.: 117,0 - 118,0oC
1H ЯМР (CDCl3) δ млн-1: 8,05 (1H, м), 7,88 (1H, м), 7,75 (1H, м), 7,4 (1H, т, J=8 Гц), 7,35 (1H, ушир.), 6,1 (1H, с), 2,55 (3H, с), 2,25 (3H, с), 1,65 (9H, с).
ИК (KBr) см-1: 3362, 1687, 1672, 1067, 757.
Элементный анализ (%): Вычислено для C18H21HO4: C, 68,55; H, 6,71; N, 4,44. Найдено: C, 68,04; H, 7,00; N, 4,40.
Пример 6
3'Метоксикарбонил-2,5-диметилфуран-3-карбоксианилид
Выход: 77,1%
T. пл. 104,0 - 106,0oC
1H ЯМР (CDCl3) δ млн-1: 8,05 (1H, м), 7,98 (1H, м), 7,8 (1H, м), 7,42 (1H, т, J=8 Гц), 7,38 (1H, ушир.), 6,1 (1H, с), 3,92 (3H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3437, 1704, 1675, 1070, 759.
Элементный анализ (%): Вычислено для C15H15NO4: C, 65,92; H, 5,53; N, 5,13. Найдено: C, 66,02; H, 5,60; N, 5,08.
Пример 7
3'-Бензоил-2,5-диметилфуран-3-карбоксианилид
Выход: 69,1%
T.пл.: 137,0 - 139,0oC
1H ЯМР (CDCl3) δ млн-1: 8,05 (1H, м), 7,85 - 7,7 (3H, м), 7,6 (1H, м), 7,55 - 7,35 (5H, м), 6,1 (1H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3386, 1672, 1647, 1069, 707.
Элементный анализ (%): Вычислено для C20H17NO3: C, 75,22; H, 5,37; N, 4,39. Найдено: C, 75,38; H, 5,43; N, 4,38.
Пример 8
3'-Бензоиламино-2,5-диметилфуран-3-карбоксианилид
Выход:46,0%
T. пл.: 194,5 - 195,0oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 8,7 (1H, ушир.), 8,1 (1H, м), 7,95 (1H, ушир. ), 7,9 (2H, м), 7,6 - 7,4 (5H, м), 7,3 (1H, т, J=8 Гц), 6,25 (1H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3283, 1642, 1074, 791, 705
Элементный анализ (%) : Вычислено для C20H18N1O3: C, 71,84; H, 5,43; N, 8,38. Найдено: C, 71,96; H, 5,53; N, 8,28.
Пример 9
3'-Валериламино-2,5-диметилфуран-3-карбоксианилид
Выход: 70,3%
T. пл.: 104,0 - 105,0oC
1H ЯМР (CDCl3) δ млн-1: 7,9 (1H, ушир.), 7,45 - 7,1 (5H, м), 6,1 (1H, с), 2,55 (3H, с), 2,35 (2H, т, J=7 Гц), 2,25 (3H, с), 1,7 (2H, м), 1,4 (2H, м), 0,95 (1H, т, J=7 Гц).
ИК (KBr) см-1 : 3250, 1660, 1644, 1074, 781
Элементный анализ (%): Вычислено для C18H22N2O3: C, 68,77; H, 7,05; N, 8,91. Найдено: C, 68,73; H, 7,17; N, 8,90.
Пример 10
3'-Циклогексилкарбониламино-2,5-диметилфуран-3-карбоксианилид
Выход: 45,1%
Т. пл.: 212,5 - 213,0oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 7,92 (1H, ушир.), 7,88 (1H, ушир.), 7,45 - 7,35 (2H, м), 7,25 (1H, т, J = 8 Гц), 6,22 (1H, с), 2,55 (3H, с), 2,25 (3H, с), 2,25 - 2,2 (1H, м) , 2,0 - 1,2 (10H, м).
ИК (KBr) см-1: 3238, 1651, 1639, 1076, 781.
Элементный анализ (%): Вычислено для C20H24N2O3: C, 70,57; H, 7,11; N, 8,23. Найдено: C, 70,56; H, 7,26; N, 8,16.
Пример 11
2,5-Диметилфуран-3-карбокси(3-метоксиметиланилид)
Выход: 73,3%
Т. пл.: 102,5 - 103,5oC
1H ЯМР (CDCl3) δ млн-1: 7,55 (1H, м), 7,52 (1H, д, J = 8 Гц), 7,32 (1H, т, J = 8 Гц), 7,32 (1H, ушир.), 6,9 (1H, д, J = 8 Гц), 6,1 (1H, с), 4,45 (2H, с), 3,4 (3H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3278, 1645, 1237, 1107, 784.
Элементный анализ (%): Вычислено для C15H17NO3: C, 69,48; H, 6,61; N, 5,40. Найдено: C, 69,22; H, 7,02; N, 5,37.
Пример 12
3'-Этоксиметил-2,5-диметилфуран-3-карбоксианилид
Выход: 64,4%
Т. пл.: 85,0 - 85,5oC
1H ЯМР (CDCl3) δ млн-1: 7,65 - 7,55 (2H, м), 7,38 (1H, т, J = 8 Гц), 7,35 (1H, ушир.), 7,15 (1H, д, J = 8 Гц), 6,15 (1H, с), 4,55 (2H, с), 3,58 (2H, кв, J = 8 Гц), 2,55 (3H, с), 2,25 (3H, с), 1,3 (3H, т, J = 8 Гц).
ИК (KBr) см-1: 3279, 1646, 1115, 785.
Элементный анализ (%): Вычислено для C16H19NO3: C, 70,31; H, 7,01; N, 5,12. Найдено: C, 70,14; H, 7,27; N, 5,06.
Пример 13
3'-Изопропилоксиметил-2,5-диметилфуран-3-карбоксианилид
Выход: 92,7%
Т. пл.: 68,0 - 69,5oC
1H ЯМР (CDCl3) δ млн-1: 7,55 (1H, д, J = 8 Гц), 7,5 (1H, м), 7,3 (1H, т, J = 8 Гц), 7,3 (1H, ушир.), 7,12 (1H, д, J = 8 Гц), 6,1 (1H, с), 4,5 (2H, с), 3,7 (1H, м), 2,55 (3H, с), 2,25 (3H, с), 1,25 (6H, д, J = 7 Гц).
ИК (пленка жидкости) см-1: 3321, 1651, 1072, 785.
Элементный анализ (%): Вычислено для C17H21NO3: C, 71,06; H, 7,37; N, 4,87. Найдено: C, 70,35; H, 7,14; N, 4,91.
Пример 14
3'-(4-Метоксибензил)-2,5-диметилфуран-3-карбоксианилид
Выход: 86,8%
Т. пл.: 100,0 - 102,5oC
1H ЯМР (CDCl3) δ млн-1: 7,45 (1H, м), 7,35 (1H, м), 7,25 (1H, т, J = 8 Гц), 7,25 (1H, ушир.), 7,1 (2H, д, J = 8 Гц), 6,92 (1H, д, J = 8 Гц), 6,88 - 6,75 (1H, м), 6,82 (2H, д, J = 8 Гц), 6,05 (1H, с), 3,9 (2H, с), 3,75 (3H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3345, 1656, 1246, 1074, 694.
Элементный анализ (%): Вычислено для C21H21NO3: C, 75,20; H, 6,31; N, 4,18. Найдено: C, 75,28; H, 6,32; N, 4,21.
Пример 15
3'-(2-Метоксикарбонилвинил)-2,5-диметилфуран-3-карбоксианилид
Выход: 63,3%
Т. пл.: 159,5 - 161,5oC
1H ЯМР (CDCl3) δ млн-1: 7,82 (1H, м), 7,7 (1H, д, J = 15 Гц), 7,58 (1H, м), 7,38 (1H, ушир.), 7,35 (1H, т, J = 8 Гц), 7,28 (1H, м), 6,48 (1H, д, J = 15 Гц), 6,12 (1H, с), 3,82 (3H, с), 2,55 (3H, с), 2,25 (3H, с)
ИК (KBr) см-1: 3387, 1685, 1670, 1068, 800.
Элементный анализ (%): Вычислено для C17H17NO4: C, 68,22; H, 5,72; N, 4,68. Найдено: C 67,55; H, 5,64; N, 4,62.
Пример 16
3'-Фенил-2,5-диметилфуран-3-карбоксианилид
Выход: 50,0%
Т. пл.: 90,0 - 92,0oC
1H ЯМР (CDCl3) δ млн-1: 7,82 (1H, с), 7,6 (2H, д, J = 8 Гц), 7,55 (1H, д, J = 8 Гц), 6,48 - 6,3 (6H, м), 6,12 (1H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3367, 1646, 1074, 755.
Элементный анализ (%): Вычислено для C19H17NO2: C, 78,33; H, 5,88; N, 4,81. Найдено: C, 78,17; H, 6,00; N, 4,72.
Пример 17
3'-Неопентилоксиметил-2,5-диметилфуран-3-карбоксианилид
Выход: 50,0%
Т. пл.: 95,5 - 97,0oC
1H ЯМР (CDCl3) δ млн-1: 7,48 (2H, м), 7,32 (1H, т, J = 8 Гц), 7,3 (1H, ушир. ), 7,12 (1H, д, J = 8 Гц), 4,52 (2H, с), 3,12 (2H, с), 2,55 (3H, с), 2,25 (3H, с), 0,95 (9H, с).
ИК (KBr) см-1: 3324, 1646, 1091, 700.
Элементный анализ (%): Вычислено для C19H25NO3: C, 72,35; H, 7,99; N, 4,44. Найдено: C, 72,38; H, 8,03; N, 4,20.
Пример 18
3'-Изопропенил-2,5-диметилфуран-3-карбоксианилид
Выход: 50,0%
Т. пл.: 71,0 - 72,0oC
1H ЯМР (CDCL3) δ млн-1: 7,65 (1H, м), 7,5 (1H, м), 7,3 (1H, ушир.), 7,3 (1H, т, J=8 Гц), 7,22 (1H, м), 6,12 (1H, с), 5,4 (1H, с), 5,1 (1H, с), 2,6 (3H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3275, 1641, 1580, 1078, 790.
Элементный анализ (%): Вычислено для C16H17NO2: C, 75,27; H, 6,71; N, 5,49. Найдено: C, 75,29; H, 6,88; N, 5,48.
Пример 19
3'-Этинил-2,5-диметилфуран-3-карбоксианилид
Выход: 50,0%
Т.пл.: 83,0 - 84,0oC
1H ЯМР (CDCl3) δ млн-1: 7,7 (1H, м), 7,6 (1H, м), 7,32 - 7,2 (3H, м), 6,1 (1H, с), 3,05 (1H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3245, 1644, 1079, 796.
Элементный анализ (%): Вычислено для C15H13NO: C, 75,30; H, 5,48; N, 5,85. Найдено: C, 75,50; H, 5,46; N, 5,96.
Пример 20
3'-Этил-2,5-диметилфуран-3-карбоксианилид
Выход: 91,0%
Т.пл.: 113,0 - 115,0oC
Масс-спектрометрия (m/z): 243 (M+), 123,94
1H ЯМР (CDCL3) δ млн-1: 7,47 - 6,95 (4H, м), 6,1 (1H, с), 2,66 (3H, кв), 2,60 (3H, с), 2,29 (3H, С), 1,25 (3H, т).
Пример 21
3'-Изопропил-2,5-диметилфуран-3-карбоксианилид
Выход: 84,0%
Т.пл.: 79 - 80oC
Масс-спектрометрия (m/z): 257 (M+), 149,135
1H ЯМР (CDCl3) δ млн-1: 7,47 - 6,98 (4H, м), 6,11 (1H, с), 2,91 (H, кв, кв), 2,60 (3H, с), 2,29 (3H, с), 1,26 (д, 6H).
Пример 22
2'-6'-Диэтил-2,5-диметилфуран-3-карбоксианилид
Выход: 85,2%
Т.пл.: 128,0 - 131,0oC
Масс-спектрометрия (m/z): 271 (M+), 242,228
1H ЯМР (CDCl3) δ млн-1: 7,28 - 7,12 (3H, м), 6,82 (1H, ушир.), 6,16 (1H, с), 2,63 (4H, кв), 2,58 (3H, с), 2,31 (3H, с), 1,20 (6H, т).
Пример 23
3'-Гексил-2,5-диметилфуран-3-карбоксианилид
(Стадия 1) К раствору 3,95 г 2,5-диметилфуран-3-карбонилхлорида в 60 мл хлорметана добавляли 3,45 мл триэтиламина и 2,99 мл м-йоданилина при охлаждении льдом и получившуюся смесь перемешивали при комнатной температуре.
(Стадия 1) К раствору 3,95 г 2,5-диметилфуран-3-карбонилхлорида в 60 мл хлорметана добавляли 3,45 мл триэтиламина и 2,99 мл м-йоданилина при охлаждении льдом, и получившуюся смесь перемешивали при комнатной температуре в течение 6,5 часов. После того, как реакционная смесь охлаждалась, ее разбавляли путем добавления 50 мл дихлорметана. Разбавленную смесь последовательно промывали 1 н. гидроксидом натрия, 1 н. соляной кислотой и насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия, после чего отгоняли растворитель. Остаток подвергали очистке при помощи колоночной хроматографии на силикагеле с получением 7,64 г 2,5-диметилфуран-3-карбокси(3-йоданилида) в виде бледно-желтых кристаллов, что соответствует выходу 89,9%.
(Стадия 2) К раствору 0,68 кристаллов, полученных на стадии 1, в 8 мл диэтилового эфира добавляли 29,3 мг хлорида [1,1'-бис(дифенилфосфино)ферроцен] палладия II и 11 мл 1 M гексилмагнийбромида, полученного из гексилбромида и магния, разделенные на 6 равных частей, и получившуюся смесь перемешивали при комнатной температуре в течение 47 часов. После добавления 2 н. соляной кислоты к реакционной смеси катализатор отфильтровывали и фильтрат экстрагировали диэтиловым эфиром. Экстракт последовательно промывали водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия. После отгонки растворителя остаток очищали при помощи колоночной хроматографии на силикагеле, а затем на колонке, заполненной фазой D-ODS-5, YMC, с получением 316 мг желаемого соединения в виде белых кристаллов, что соответствует выходу 52,8%.
Т.пл.: 71,5 - 72,0oC
1H ЯМР (CDCl3) δ млн-1: 7,45 (1H, м), 7,35 (1H, м), 7,25 (1H, ушир.), 7,22 (1H, т, J=8 Гц), 6,95 (1H, д, J=8 Гц), 6,1 (1H, с), 2,65 - 2,5 (2H, м), 2,55 (3H, с), 2,25 (3H, с), 1,7 - 1,5 (2H, м), 1,4 - 1,2 (6H, м), 0,85 (3H, т, J=7 Гц).
ИК (KBr) см-1: 3310, 1643, 1077, 788.
Элементный анализ (%): Вычислено для C19H25NO2: C, 76,22; H, 8,42; N, 4,68. Найдено: C, 76,15; H, 8,54; N, 4,55.
Следуя методике, подобной описанной выше, но используя подходящий реактив Гриньяра вместо гексилмагнийбромида, получали следующие соединения.
Пример 24
3'-Бутил-2,5-диметилфуран-3-карбокси(анилид)
Выход: 36,4%
Т.пл.: 77,0 - 80,0oC
1H ЯМР (CDCL3) δ млн-1: 7,45 (1H, м), 7,35 (1H, м), 7,25 (1H, ушир.), 7,22 (1H, т, J=8 Гц), 6,95 (1H, д, J=8 Гц), 6,1 (1H, с), 2,65 - 2,55 (2H, м), 2,55 (3H, с), 2,25 (3H, с), 1,6 (2H, м), 1,35 (2H, м), 0,92 (1H, т, J=7 Гц).
ИК (KBr) см-1: 3285, 1646, 1075, 702.
Элементный анализ (%): Вычислено для C17H21NO2: C, 75,25; H, 7,80; N, 5,16. Найдено: C, 75,13; H, 7,87; N, 5,13.
Пример 25
3'-Втор-бутил-2,5-диметилфуран-3-карбоксианилид
Выход: 38,1%.
Т. пл.: 80,0 - 81,0oC
1H ЯМР (CDCl3) δ млн-1: 7,4 (1H, м), 7,38 (1H, м), 7,25( 1H, ушир.), 7,22 (1H, т, J=8 Гц), 6,95 (1H, д, J=8 Гц), 6,1 (1H, с), 2,65-2,5 (1H, м), 2,55 (3H, с), 2,25 (3H, с), 1,68-1,5 (1H, м), 1,25 (3H, д, J=7 Гц), 0,85 (3H, т, J=7 Гц).
ИК (KBr) см-1: 3255, 1647, 1078, 791.
Элементный анализ (%): Вычислено для C17H21NO2: C, 75,25; H, 7,80; N, 5,16. Найдено: C, 75,19; H, 7,68; N, 5,14.
Пример 26
3'-Пентил-2,5-диметилфуран-3-карбоксианилид
Выход: 18,3%
Т. пл.: 97,0 - 97,5oC
1H ЯМР (CDCl3 + DMCO) δ млн-1: 7,45 (1H, м), 7,35 (1H, м), 7,28 (1H, ушир. ), 7,25 (1H, т, J=8 Гц), 6,95 (1H, д, J=8 Гц), 6,1 (1H, с), 2,65-2,5 (2H, м), 2,55 (3H, с), 2,25 (3H, с), 1,7-1,5 (2H, м), 1,4-1,2 (4H, м), 0,88 (3H, т, J=7 Гц).
ИК (KBr) см-1: 3304, 1644, 1077, 710.
Элементный анализ (%): Вычислено для C18H23NO2: C, 75,76; H, 8,12; N, 4,91. Найдено: C, 75,77; H, 8,18; N, 5,06.
Пример 27
3'-Циклогексил-2,5-диметилфуран-3-карбоксианилид
Выход: 52,7%.
Т. пл.: 113,0 - 114,5oC
1H ЯМР (CDCl3) δ млн-1: 7,48 (1H, м), 7,35 (1H, м), 7,28 (1H, ушир.), 7,25 (1H, т, J= 8 Гц), 6,98 (1H, д, J=8 Гц), 6,1 (1H, с), 2,55 (3H, с), 2,55-2,45 (1H, м), 2,25 (3H, с), 1,95-1,68 (5H, м), 1,55-1,15 (5H, м).
ИК (KBr) см-1: 3324, 1646, 1230, 1074, 791.
Элементный анализ (%): Вычислено для C19H23NO2: C, 76,74; H, 7,80; N, 4,71. Найдено: C, 76,62; H, 7,78; N, 4,67.
Пример 28
3'-Циклопентил-2,5-диметилфуран-3-карбоксианилид
Выход: 35,9%.
Т. пл.: 92,0 - 93,0oC
1H ЯМР (CDCl3) δ млн-1: 7,45 (1H, м), 7,35 (1H, м), 7,25 (1H, ушир.), 7,22 (1H, т, J=8 Гц), 7,00 (1H, д, J=8 (Гц), 6,1 (1H, с), 3,08-2,9 (1H, м), 2,55 (3H, с), 2,25 (3H, с), 2,15-1,95 (2H, м), 1,9-1,5 (6H, м).
ИК (KBr) см-1: 3322, 1647, 1232, 1076, 700.
Элементный анализ (%): Вычислено для C18H21NO2: C, 76,30; H, 7,47; N, 4,94. Найдено: C, 76,21; H, 7,56; N, 4,93.
Пример 29
3'-Бензил-2,5-диметилфуран-3-карбоксианилид
Выход: 59,8%.
Т. пл.: 123,0 - 125,0oC
1H ЯМР (CDCl3 δ млн-1: 7,45 (1H, м), 7,38 (1H, м), 7,35-7,15 (7H, м), 6,95 (1H, д, J=8 Гц), 3,98 (2H, с), 2,55 (3H, с), 2,25 (3H, с).
ИК (KBr) см-1: 3314, 1640, 1078, 777, 701.
Элементный анализ (%): Вычислено для C21H19NO2: C, 78,66; H, 6,27; N 4,59. Найдено: C, 77,76; H, 6,28; N, 4,55.
Ссылочный пример 1
Этил(2,5-диметилфуран-3-карбоксилат)
К суспензии 2,4 г гидрида натрия (60% дисперсия в минеральном масле) в 10 мл N,N-диметилформамида (ниже сокращенно обозначаемом как ДМФА) по каплям добавляли раствор 6,5 мл этилацетоацетата в 5 мл ДМФА при перемешивании и при охлаждении льдом, и к этой смеси по каплям добавляли 5,7 мл хлорацетона при перемешивании и при охлаждении льдом. После перемешивания при комнатной температуре в течение 3 часов реакционную смесь выливали в воду и проводили экстракцию из водной смеси этилацетатом. Экстракт промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. После отгонки растворителя под пониженным давлением остаток перегоняли в вакууме с получением 8,01 г этил ( α- ацетонитрилацетата), имеющего Т. пл. 105oC/266,6 Па, что соответствует выходу 86%.
К раствору полученного таким образом сложного эфира в 20 мл этанола добавляли 2 г п-толуолсульфоновой кислоты, и получившуюся смесь нагревали с обратным холодильником в течение 2 часов. Реакционной смеси давали охладиться до комнатной температуры и отгоняли растворитель при пониженном давлении. Остаток растворяли в этилацетате и раствор промывали насыщенным водным раствором хлорида натрия, после чего сушили над безводным сульфатом магния. После отгонки растворителя при пониженном давлении остаток очищали при помощи колоночной хроматографии на силикагеле с использованием в качестве элюента смеси н-гексана и этилацетата в соотношении 10:1, с получением 5,14 г этил(2,5-диметилфуран-3-карбоксилата), что соответствует выходу 71%.
Ссылочный пример 2
2,5-Диметилфуран-3-карбоновая кислота
Смесь 3,2 г этил(2,5-диметилфуран-3-карбоксилата), 35 мл этанола и 20 мл 2 н. гидроксида натрия перемешивали при комнатной температуре в течение 1,5 часов, после чего нагревали с обратным холодильником в течение часа. После того, как реакционной смеси давали охладиться до комнатной температуры, ее упаривали под пониженным давлением. Остаток растворяли в воде и подкисляли разбавленной серной кислотой. Выпавшие в осадок кристаллы собирали путем фильтрования, промывали водой и сушили с получением 2,27 г 2,5-диметилфуран-3-карбоновой кислоты, что соответствует выходу 85%.
Соединение, имеющее общую формулу I, упомянутую выше, и состав, содержащий соединение I в качестве активного компонента, которых касается настоящее изобретение, могут применяться путем смешивания с носителями или, если необходимо, с другими добавками, с последующим приготовлением обычно используемых композиций, таких как масляный раствор, эмульсифицируемый концентрат, солюбилизатор, паста, смачиваемый порошок, текучая композиция, сухая текучая композиция, аэрозоль и краска, а затем композиция может использоваться согласно известным способам обработки древесины антисептиками. В качестве добавок, которые подходящим образом используются для того, чтобы улучшить свойства композиции и усилить предохраняющее воздействие на древесину, могут быть упомянуты катионогенные, анионогенные и неионогенные поверхностно-активные вещества, различные высокомолекулярные полимеры, как например метилцеллюлоза и винилацетатный полимер, и гидрофобизирующие добавки, такие как силиконовое масло и парафин. Нет необходимости говорить, что возможно комбинированное использование с другими антисептиками для древесины, фунгицидами и бактерицидами, включая органические соединения йода, такие как Sanplas, IF-1000 и Troysan, азольные соединения, такие как Propiconazole и Tebuconazole, Thiabendazole, Dichlofluanid (дихлорфлуанид), и соединения, представляющие собой четвертичные соли аммония; с инсектицидами, включая пиретроиды, такие как Permethrin (перметрин), Etofenprox, Cypermethrin (циперметрин), Silaneophen, Tralomethrin, фосфорорганические соединения, такие как Chloropyrifos, Phoxin и Propetamphos, и Imidacroprid; и с усиливающими действие средствами, такими как бис-(2,3,3,3-тетрахлорпропиловый)-эфир. При комбинированном использовании таким способом может ожидаться улучшенный эффект. Практически при применении, хотя содержание соединения по настоящему изобретению может изменяться в широких пределах в зависимости от композиции или от объекта, обычно оно может быть пригодным для использования в диапазоне от 0,1 до 95 процентов по весу, предпочтительно от 0,2 до 60 процентов по весу. Эти композиции применимы в обычных способах обработки древесины: например, нанесение покрытия, распыление, обработка погружением, смешивание, пропитка, или обработка смешиванием одновременно с клеем.
Некоторые примеры композиций с соединениями по настоящему изобретению будут показаны ниже, в отношении которых нет необходимости говорить, что соотношение, в котором комбинируются компоненты, и вид добавок могут изменяться в широких пределах (в данных ниже описаниях "часть" во всех случаях значит "часть по весу").
Примеры композиций с антисептиками для древесины
Пример композиции 1 Эмульсифицируемый концентрат
Двадцать частей соединения 1 растворяли в 70 частях ксилола, и затем добавляли 10 частей полиоксиэтиленнонилфенилового эфира и смешивали в достаточной степени, получая эмульсифицируемый концентрат.
Полученный таким образом эмульсифицируемый концентрат разбавляется подходящим количеством воды непосредственно перед использованием и может быть применен для древесных материалов, которые необходимо обработать нанесением покрытия, погружением или обрызгиванием, и, в дополнение, может применяться путем смешивания с клеями, которые используются для фанеры, древесностружечных плит и твердых древесноволокнистых плит.
Пример композиции 2. Масляный раствор
Две части соединения 2 добавляли к 98 частям керосина, получая масляный раствор.
Полученный таким образом масляный раствор может применяться для древесных материалов, которые необходимо обработать обрызгиванием, нанесением покрытия, погружением или пропиткой.
Пример композици 3. Композиция для нанесения покрытия
Десять частей соединения 1, 20 частей баритовой пыли, 10 частей винилового полимера, 25 частей сосновой смолы и 35 частей ксилола смешивали до однородного состояния, получая состав для нанесения покрытия.
Пример композиции 4. Смачиваемый порошок
Двенадцать частей соединения 3, 56 частей глины, 3 части сульфоната натрия - лаурилового спирта и 1 часть поливинилового спирта смешивали до однородного состояния в миксере, а затем измельчали путем использования молотковой мельницы, получая смачиваемый порошок.
Примеры испытаний по защите древесины
Эффективность антисептиков для древесины по настоящему изобретению будет конкретно разъяснена при помощи следующих примеров.
(1) Согласно способу испытания по защите древесины, описанному в Промышленных стандартах Японии [Japan Industrial, Standarts JIS A-9201 (1991)], каждое из испытуемых соединений растворяли до определенной концентрации в метаноле. Раствор вводили при пониженном давлении в заболонь Sugi (японского кедра) (2 х 2 х 1) см, а затем сушили на воздухе. Испытание на устойчивость к атмосферному воздействию, в котором один цикл обработки состоял в перемешивании в воде в течение 8 часов, а затем нагревании в течение 16 часов при 60oC, повторяли 10 раз. Испытуемый материал помещали на флору Serpula lacrymans, которая была предварительно выращена на среде из кварцевого песка (экстракт солода 2%, глюкоза 1%, пептон 0,3% и дрожжи 0,2%), и подвергали форсированному разложению при 20oC в течение 12 недель. Из разности между сухим весом испытуемого продукта перед испытанием и его сухим весом после испытания получали степень снижения веса. Результаты показаны в табл. 2. Тест проводили путем использования 9 образцов для каждого варианта условий испытания, и значения, показанные в табл. 2, являются средними значениями, рассчитанными из данных для 9 образцов.
Контрольное соединение 1: 4-хлорфенил-3-иодпропаргилформаль
Продукт фирмы Nagase Co., Ltd.: IF-1000
Согласно представленным данным, соединения, имеющие общую формулу (I), в заметной степени предотвращали гниение образцов древесины, вызванное древоразлагающими грибками.
(2) Каждый из растворов соединения по настоящему изобретению в метаноле с концентрацией 0,1% в отношении веса к объему и контрольный препарат вводили в тестовый материал [заболонь Sugi (японского кедра), 2 х 2 х 0,5 см] при пониженном давлении, а затем сушили на воздухе. Испытание на устойчивость к атмосферному воздействию, в котором один цикл обработки состоял в промывании (расход около 2 литров в минуту) водой в течение 5 часов, а затем нагревании в течение 19 часов при 60oC, повторяли дважды. После стерилизации сухим воздухом получали испытуемые образцы.
Испытуемый материал помещали на флору Coriolus Versicolor, которая представляет собой разлагающий лигнин грибок, и Tyromyces palustris, которая представляет собой разлагающий целлюлозу грибок, и которые обе являются установленными видами грибков для проб на предохраняющее воздействие антисептиков для древесины. Оба грибка были предварительно выращены на среде из агара (экстракт солода 2%, глюкоза 1% и пептон 0,5%). После того, как образцы древесины подвергались форсированному разрушению при 26oC в течение 3 недель, определяли эффективность по степени роста гиф на испытуемом материале и наличию или отсутствию сниженной максимальной прочности на раздавливание. Результаты показаны в табл. 3.
Эффективность защиты древесины оценивали по следующим критериям.
+ : На испытуемом материале не наблюдалось роста гиф, и не было найдено различий с неповрежденными образцами древесины по максимальной прочности на раздавливание.
+ : На испытуемом материале наблюдался небольшой рост гиф или было обнаружено небольшое снижение максимальной прочности на раздавливание.
- : На испытуемом материале наблюдался рост гиф или было обнаружено явное снижение максимальной прочности на раздавливание.
- : На испытуемом материале наблюдался рост гиф или было обнаружено явное снижение максимальной прочности на раздавливание.
Контрольное соединение 2: 3-Бром-2,3-дииод-2-пропенилэтилкарбонат
Продукт фирмы Sankyo Co., LTD.: Sanplas
Когда нужно применить состав по настоящему изобретению, соотношение, в котором производится комбинация, может быть подходящим образом выбрано в зависимости от вида древесины и вида древесного материала, который необходимо обработать антисептиком для древесины, или способа обработки (например, нанесение покрытия, погружение, распыление, пропитка, смешивание или смешивание совместно с клеем). Обычно соотношение, в котором производится комбинация диметилфуранкарбоксианилида и любого другого антисептика для древесины, может составлять от 240:1 до 1:35, предпочтительно от 30:1 до 1:10, и более предпочтительно от 5:1 до 1:5.
Содержание состава по настоящему изобретению может изменяться в широком диапазоне в зависимости от композиции. В целом, содержание в композиции может составлять от 0,1 до 95%, предпочтительно от 0,2 до 60%.
Некоторые примеры композиций, включающих соединения по настоящему изобретению, будут показаны ниже, в отношении которых нет необходимости говорить, что соотношение, в котором комбинируются компоненты, и вид добавок могут изменяться в широких пределах.
Примеры композиций с защитными составами для древесины
Пример композиции 1 Эмульсифицируемый концентрат
Десять частей соединения 1 растворяли в 30 частях препарата Sanplas и 50 частях ксилола, затем добавляли 10 частей полиоксиэтиленнонилфенилового эфира и смешивали в достаточной степени, получая эмульсифицируемый концентрат.
Полученный таким образом эмульсифицируемый концентрат разбавлялся подходящим количеством воды непосредственно перед использованием и может быть применен для древесных материалов, которые необходимо обработать нанесением покрытия, погружением или обрызгиванием, и, в дополнение, может применяться путем смешивания с клеями, которые используются для фанеры, древесностружечных плит и твердых древесноволокнистых плит.
Пример композиции 2 Масляный раствор
Две части соединения 2 и 1 часть препарата troysan растворяли в 96 частях керосина, получая масляный раствор.
Пример композиции 3 Смачиваемый порошок
Пятнадцать частей соединения 3, 25 частей препарата IF-1000, 56 частей глины, 3 части сульфоната натрия - лаурилового спирта и 1 часть поливинилового спирта смешивали до однородного состояния в миксере, а затем измельчали путем использования молотковой мельницы, получая смачиваемый порошок.
Действие защитных составов для пропитки древесины по настоящему изобретению будет конкретно разъяснено при помощи следующих примеров.
Примеры испытаний защитных составов для древесины
Проба на минимальную тормозящую концентрацию при помощи метода разбавления агара.
В соответствии с методом разбавления агара, на стерилизованную среду (агаровая среда на основе картофельной декстрозы; порошок картофельного экстракта 0,4%, глюкоза 2%, агар 1,5%), приготовленную с содержанием определенных концентраций испытуемых образцов, инокулировали флору (около 4 мм в диаметре) древоразрушающих грибов, Coriolus Versicolor и Tyromyces palustris, которая была предварительно культивирована на том же типе среды. После культивирования при 25oC в течение 5 дней наблюдали за ростом гиф, чтобы определить минимальную тормозящую концентрацию.
Определение того, имеется ли какое-либо усиление действия или нет, описано в работе C. Kull et al., Applied Microbiology 9, 538 - 541 (1961). Испытания проводили согласно обычно используемому методу.
В табл. 4 - 6 и на рисунках 1 (a) - (e) показаны результаты, полученные при сочетании соединения 1 с каждым из препаратов Sanplas, Troysan и IF-1000.
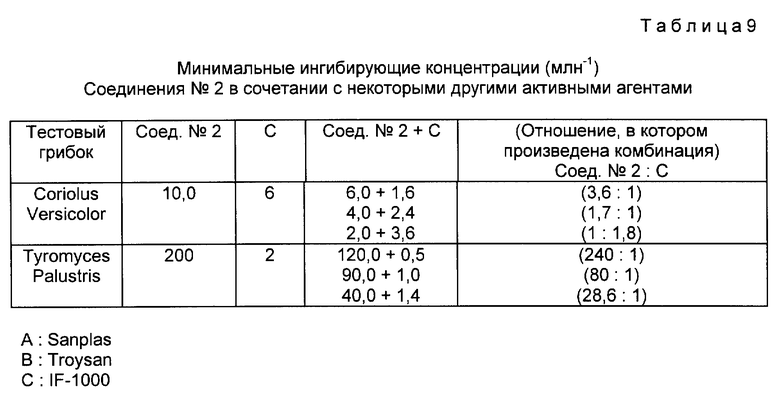
Затем такое же испытание, как описано, было проведено для соединения 2. Результаты показаны в табл. 7 - 9 и на рисунках 2 (a) - (e).
Каждая из кривых минимальной ингибирующей концентрации, показанных на рисунках 1 и 2, лежит ниже диагональной линии, показанной пунктиром.
Эти данные показывают, что производное диметилфуранкарбоксианилида усиливает действие каждого из препаратов Sanplas, Troysan и IF-1000 при комбинации с ними.
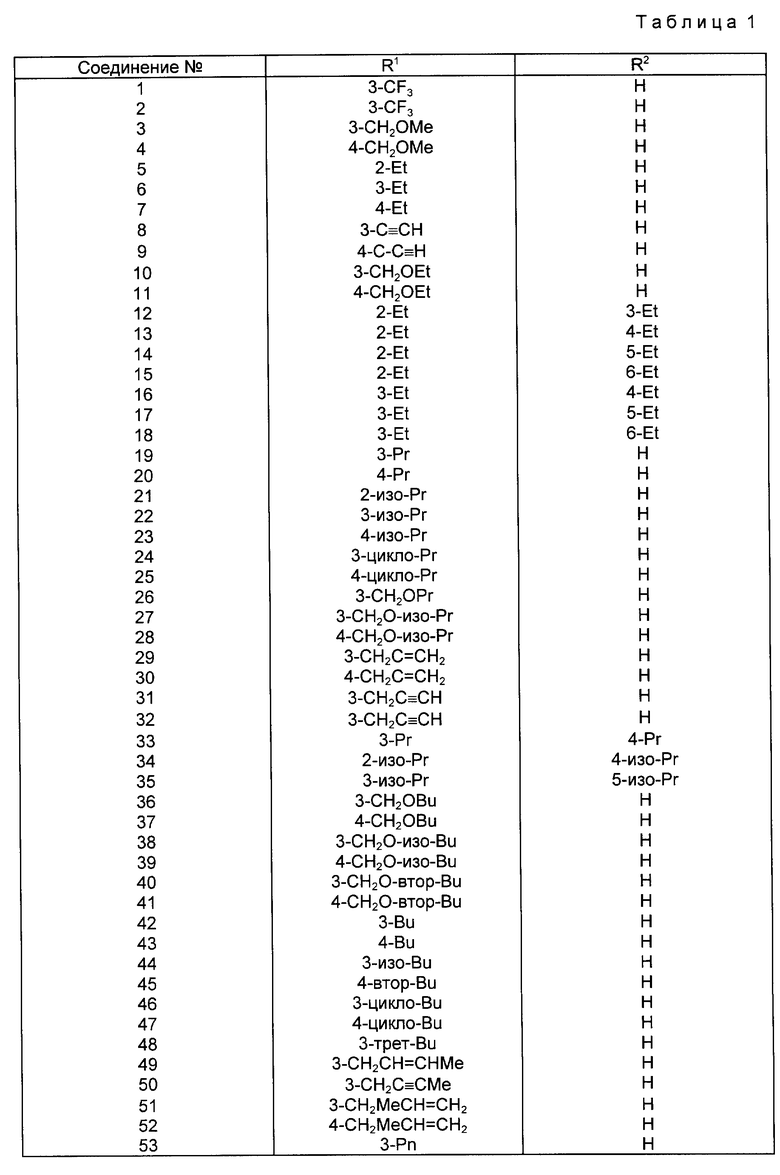
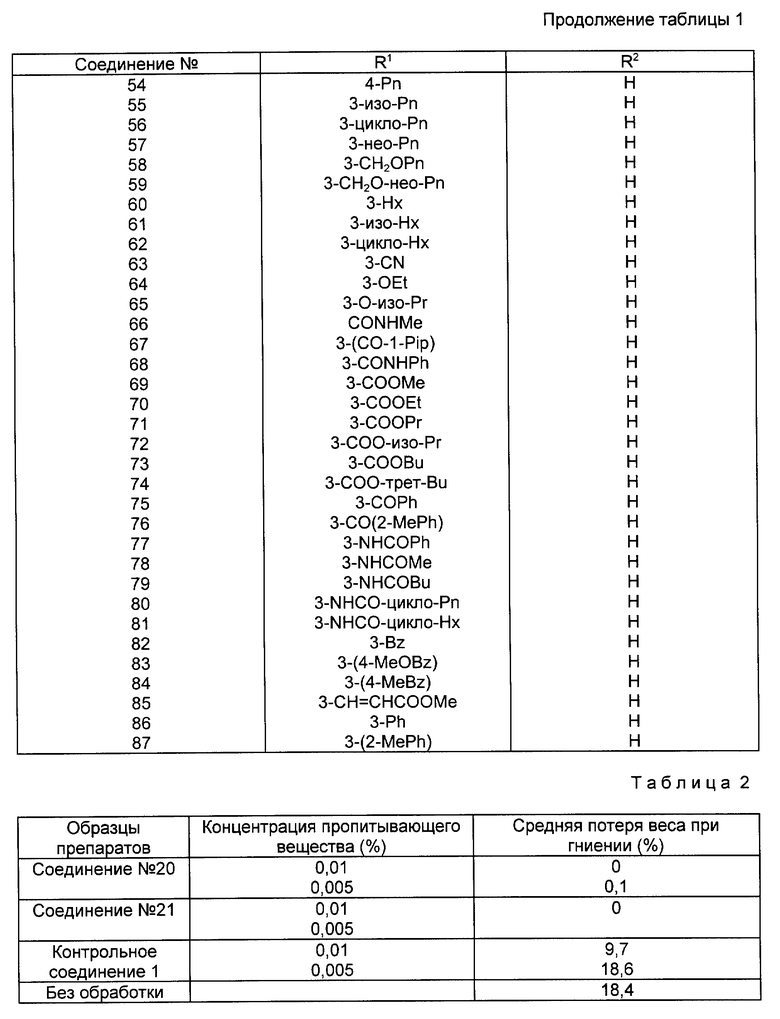



Изобретение относится к диметилфуранкарбоксианилиду общей формулы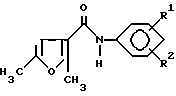
в которой радикалы R1 и R2 могут быть одинаковые или различные, представляющие собой водород, C2-C6- алкил, C3-C6-циклоалкил, C3-C6-алкенил,
C2-C6-алкинил, C1-C3-галогеналкил, бензоильную группу, содержащую заместители, бензоиламиногруппу, которая также может содержать один или два заместителя, C2-C6-алканоиламиногруппу, C3-C6-циклоалкилкарбониламиногруппу, бензильную группу, которая может содержать заместители, фенильную группу с возможными заместителями, а также другие заместители при условии, что одновременно R1 и R2 не являются атомами водорода, вторым условием является то, что один из R1 и R2 не является незамещенной фенильной группой, когда другой из них представляет атом водорода, и третье условие - один из R1 и R2 в ортоположении не представляет собой анилиновое кольцо, C2-C6-алкил, C3-C6-циклоалкил или C2-C6-алкоксигруппу, когда другой из них представляет атом водорода. Изобретение относится также к защитной композиции для древесины, содержащей в качестве активного начала эффективное количество указанного соединения, к способу защиты древесины, заключающемуся в нанесении на нее композиции, содержащей эффективное количество соединения указанной формулы. Изобретение также относится к защитной композиции для древесины, содержащей смесь не менее одного производного соединения указанной формулы, а также не менее одного соединения, выбранного из 3-бром-2,3-дийод-2-пропенилэтилкарбамата, 3-йод-2-пропинилбутилкабамата и 4-хлорфенил-3-йодпропаргилформаля. Изобретение позволяет создать новый антисептик для древесины. Его применение более безопасно, и, кроме того, он может быть использован эффективно в более низких концентрациях. Стоимость антисептика невысока. Усиление действия заключается также в возможном комбинировании с другими компонентами, пригодными в качестве антисептиков. 4 с.з. п. ф-лы, 9 табл., 2 ил.
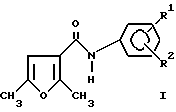
где R1 и R2 - одинаковые или различные, каждый представляет собой атом водорода, C2-C6-алкил, C3-C6-циклоалкил, C3-C6-алкенил, C2-C6-алкинил, C1-C3-галогеналкил, C2-C6-алкоксигруппу, C1-C6-алкокси-C1-C6-алкил, замещенную амидную группу, C1-C6-алкоксикарбонил, бензоильную группу, которая может содержать один или два заместителя, бензоиламиногруппу, которая может содержать один или два заместителя, C2-C6-алканоиламиногруппу, C3-C6- циклоалкилкарбониламиногруппу, бензильную группу, которая может содержать один или два заместителя, фенильную группу, которая может содержать один или два заместителя, или C1-C6-алкоксикарбонил-C2-C5алкениленовую группу, при условии, что (1) R1 и R2 одновременно не являются атомами водорода, (2) один из R1 и R2 не является незамещенной фенильной группой, когда другой из них представляет атом водорода, (3) один из R1 и R2 в ортоположении не представляет собой анилиновое кольцо, C2-C6-алкил, C3-C6-циклоалкил или C2-C6-алкоксигруппу, когда другой из них представляет атом водорода.
где R1 и R2 - одинаковые или различные, каждый представляет собой атом водорода, C2-C6-алкил, C3-C6-циклоалкил, C3-C6-алкенил, C2-C6-алкинил, C1-C3-галогеналкил, C2-C6-алкоксигруппу, C1-C6-алкокси-C1-C6-алкил, замещенную амидную группу, C1-C6-алкоксикарбонил, бензоильную группу, которая может содержать один или два заместителя, бензоил-аминогруппу, которая может содержать один или два заместителя, C2-C6-алканоиламиногруппу, C3-C6-циклоалкилкарбониламиногруппу, бензильную группу, которая может содержать один или два заместителя, фенильную группу, которая может содержать один или два заместителя, или C1-C6-алкоксикарбонил-C2-C6-алкениленовую группу, при условии, что R1 и R2 одновременно не представляют атомы водорода.
| Способ получения производных 2,4-диметил-3-карбоксианилидфурана или их солей | 1974 |
|
SU591145A3 |
| УСТРОЙСТВО для ПРИГОТОВЛЕНИЯ ВОДО-ВОЗДУШНОЙСМЕСИ | 0 |
|
SU332216A1 |
| EP 0532285 A1, 09.09.92 | |||
| Способ футеровки металлических труб термопластичными материалами | 1960 |
|
SU139522A1 |
| Устройство задержки телевизионного сигнала | 1972 |
|
SU545099A1 |
| Устройство для защиты рудничного электровоза постоянного тока | 1976 |
|
SU577145A1 |
Авторы
Даты
1998-10-20—Публикация
1994-04-15—Подача