Изобретение относится к области химической технологии неорганических материалов. Алкоголяты алюминия находят широкое применение в качестве катализаторов различных процессов органической химии, в том числе алкилирования ароматических углеводородов, конденсации и полимеризации, диспропорционирования альдегидов (реакция Тищенко) и ряда других. Они также могут использоваться для селективного восстановления группы C=O в синтезах Меервейна-Понндорфа-Верлея и Опенауэра.
Алкоголяты алюминия находят широкое применение в качестве гидрофобизаторов, сшивающих агентов для эпоксидных и полиэфирных смол, кремнийорганических полимеров, а также добавок к красителям. Продукты их частичного гидролиза и пиролиза - полиорганометаллоксаны - используются как компоненты термостойких покрытий.
В последние десятилетия наблюдается повышенный интерес к алкоголятам алюминия, связанный с использованием продуктов их гидролиза для получения чистого (по химическому и фазовому составу) оксида алюминия и сложных оксидных систем на основе Al2O3. Полученная по алкоксотехнологии окись алюминия отличается по структурным и текстурным характеристикам от традиционной. Варьированием условий гидролиза можно влиять на основные характеристики продукта, в том числе на фазовый состав. Кроме того, температуры фазовых переходов этого продукта обычно имеют более высокие значения. Эти и ряд других соображений обусловили применение продуктов гидролиза алкоголятов алюминия в качестве катализаторов, носителей, пористых мембран, высокотемпературных керамик и т.д.
Известны различные способы получения алкоголятов алюминия, в большинстве своем основанные на реакции металлического алюминия со спиртами. Многие из них требуют внесения в зону реакции катализаторов, содержащих ртуть [Руководство по неорганическому синтезу, т.3, М., Мир, 1985, с. 910-911; А. с. СССР N 240695, кл. C 07 C 31/32, опубл. 01.04.69], хлор [А.с. СССР N 273814, кл. C 07 C 31/32, опубл. 05.02.76], натрий [А.с. СССР N 1065399, кл. C 07 C 31/32, опубл. 07.01.84] и другие добавки [Патент РФ N 2021248, кл. C 07 C 31/32, опубл. 15.10.94], что отражается на химической чистоте продукта. Другие методы требуют особого аппаратурного оформления или особых условий проведения процесса [А.с. СССР N 136372, кл. C 07 C 31/32, опубл. 30.01.61; А.с. СССР N 1065399, кл. C 07 C 31/32, опубл. 07.01.84; Патент РФ N 2005711, кл. C 07 C 31/32, опубл. 15.01.94].
Наиболее близким является способ [А.с. СССР N 742422, кл. C 07 C 31/32, опубл. 25.06.80] , где при получении C3-C4-алкоголятов алюминия в качестве активатора алюминия предлагается использовать металлический галлий. Смесь стружек галлия и алюминия приводится в контакт со спиртом, затем проводят синтез и выделяют продукт.
Основными недостатками метода являются следующие. Во-первых, необходимость введения металлов в виде стружки. Как известно из практики, стадия измельчения весьма трудоемка и сопровождается неизбежной потерей металлов. Кроме того, авторы не предусматривают возможности регенерации галлия для его повторного использования. Наконец, заявлено получение лишь C2-C4-алкоголятов, тогда как для каталитических целей желательно использовать алкоксиды высших спиртов [Родионов Ю.М., Слюсаренко Е.М., Лунин В.В. Перспективы применения алкоксотехнологии в гетерогенном катализе. Успехи химии, 1996, т. 65, вып. 9, с.865-880], так как в этом случае образующиеся оксиды обладают наиболее развитой пористой структурой.
Настоящее изобретение решает задачу получения широкого спектра алкоголятов по упрощенной технологии. При этом повышаются выход и качество целевых продуктов и повышается экологическая безопасность производства.
В настоящем изобретении в качестве активатора алюминия предлагаются галламы некоторых металлов. Под термином "галлама" принято понимать раствор металла в галлии, по своему составу соответствующий эвтектике данной системы и находящийся в жидком состоянии при комнатной температуре [Федоров П.И., Мохосоев М. В. , Алексеев Ф.П. Химия галлия, индия и таллия. Новосибирск, Наука, 1977. с. 224].
В качестве нетоксичных и наиболее доступных для практического использования можно предложить, например, эвтектические системы Ga-In (25±0,2 мас. % In) и Ga-In-Sn (25±0,2 мас.% In; 13±0,2 мас.% Sn). Использование жидких при комнатной температуре систем (галлам) значительно упрощает обеспечение контакта алюминия с активатором по сравнению со способом, предлагаемым в прототипе. При погружении алюминия в галламу в интервале температур плавления галламы и алюминия наступает активация образца. Активированный таким образом алюминий при погружении в спирт проявляет высокую природную химическую активность при комнатной температуре. Допускается использование алюминия в любом виде (гранулы, отрезки проволоки, массивные куски и т.д.). В зависимости от объема и вида исходного алюминия время активирования колеблется от 1 минуты до 100 часов. В случае, когда алюминий активируют погружением последнего в галламу с перемешиванием, после активации алюминий выдерживают при комнатной температуре не менее 1 часа. В случае, когда активируют гранулы, отрезки проволоки, массивные куски и т.д., взаимодействие исходного алюминия проводят при контакте его весовой части с не менее 0,5 весовой части алюминия, предварительно активированного галламами, как указано выше.
Для синтеза используют алифатические C2-C8-спирты (н- и изостроения), а также бензиловый спирт. Для увеличения скорости синтеза температуру процесса рекомендуется поддерживать на 5-10oС ниже точки кипения используемого спирта.
Полученные по этой методике растворы являются очень концентрированными. Например, метод атомно-абсорбционной спектроскопии (ААС) показал в растворе бутилата алюминия в бутаноле концентрацию 4,9 мас.% Al, что соответствует 44,6%-ному раствору алкоголята.
Селективное получение алкоголятов алюминия подтверждено методом ИК-спектроскопии.
Анализ проводился на ИК-спектрометре марки Specord M-80.
Подготовка образца для исследования производилась следующим образом. Насыщенный раствор изобутилата алюминия в изобутаноле был охлажден до 0oC, в результате чего алкоголят частично выделился из раствора. Отфильтрованный на вакуум-фильтре изобутилат был спрессован в таблетку с KBr (около 7 мг алкоголята на 400 мг наполнителя). Регистрация спектров проводилась в области 400-4000 см-1.
В качестве стандарта был взят 60%-ный раствор изобутилата алюминия в изобутиловом спирте (ТУ 6-09-13-513-76). Подготовка образца сравнения и регистрация спектров были идентичны.
На чертеже приведены спектры синтезированного образца (внизу) и стандартного.
Как видно, основные характеристические частоты в спектрах исследуемого образца и образца сравнения совпадают. Наличие полос 1040, 995, 935 см-1 четко идентифицирует изобутилат алюминия.
Спиртовой раствор после фильтрации готов к дальнейшему использованию в зависимости от цели. В частности, его можно непосредственно применять в качестве катализатора органических синтезов, гидролизовать водой или растворами солей и т.д. В случае необходимости использования чистого алкоголята его выделяют известными способами.
Пример по прототипу.
1,26 г стружки алюминия и 0,26 г стружки металлического галлия смешивают в фарфоровой чашке, смесь загружают в круглодонную колбу и приливают 200 г изопропилового спирта. Содержимое колбы нагревают до начала реакции, которое заметно по выделению водорода, после чего нагревание прекращают. Реакция проходит без вскипания и заканчивается через 2 ч. По окончании реакции целевой продукт (изопропилат алюминия) растворяют в толуоле, отфильтровывают от шлама и отгоняют толуол. Выход целевого продукта 184 г (94%). Содержание основного вещества 99,4%.
В приведенном примере по прототипу массовое соотношение алюминия и галлия составляет около 5. При этом весь галлий вводится в реакционную среду и после реакции, вероятно, переходит в шлам. В примере выделение и регенерация галлия не предусмотрены. То есть на 5 частей используемого алюминия приходится 1 массовая часть галлия (20%), редкого, достаточно дорогого металла, который попадает в отходы.
Кроме того, как видно из примера, процесс получения алкоголята - многостадийный. Он включает в себя кроме основной стадии взаимодействия дополнительные стадии отделения продукта от шлама путем растворения продукта в толуоле с последующей перегонкой. Все это неизбежно сопровождается потерями реагентов и негативно отражается на экологическом аспекте.
Предлагаемый нами метод получения алкоголята предполагает активацию алюминия в отдельной емкости. В зону реакции активаторы попадают с алюминием в количестве не более 1% от массы алюминия. После реакции капля активатора легко отделяется от жидких реагентов, поскольку его плотность составляет около 6 г/см3, и регенерируется. При этом потери дорогих металлов сводятся к минимуму.
Сущность предлагаемого изобретения иллюстрируется следующими примерами.
Пример 1. Образец алюминия массой 2,89 г подвергают контакту с галламой индия (25±0,2 мас.% In, остальное галлий) в течение 5 минут при 50oC. После проведенной таким образом активации алюминий отделяют от галламы и выдерживают в течение 1 часа при комнатной температуре. Затем переносят в реактор, в качестве которого можно использовать плоскодонную колбу. В колбу добавляют 50 мл н-бутанола и постепенно повышают температуру реакционной среды. При 80oC скорость процесса высока, и время реакции до полного превращения алюминия составляет 1,5 часа. На дне реактора остается небольшое количество внесенного вместе с алюминием активатора. Он концентрируется в виде одной капли на дне реактора, легко отделяется от спиртового раствора алкоголята, регенерируется и возвращается на активацию.
Для подсчета выхода продукта н-бутилат алюминия гидролизуют избытком воды при нагревании. Образовавшийся гидроксид алюминия отфильтровывают и прокаливают в течение 4 часов при 800oC. Масса оксида после прокаливания 5,38 г, что соответствует выходу алкоголята 98,5%.
Примеры 2-7 проводят аналогично примеру 1.
Пример 8. Образец алюминия массой 5,32 г подвергают контакту с галламой индия (25±0,2 мас.% ln, остальное галлий) в течение 5 минут при 18oC. После проведенной таким образом активации алюминий отделяют от галламы и выдерживают в течение 24 часов при комнатной температуре. Затем переносят в плоскодонную колбу. В колбу добавляют 80 мл н-бутанола и постепенно повышают температуру реакционной среды. При 80oC время реакции до полного превращения алюминия составляет 1 час. На дне реактора остается небольшое количество внесенного вместе с алюминием активатора. Он концентрируется в виде одной капли на дне реактора, легко отделяется от спиртового раствора алкоголята, регенерируется и возвращается на активацию. Выход н-бутилата 96,6%.
Пример 9. Образец алюминия массой 2,14 г подвергают контакту с галламой индия (25±0,2 мас.% In, остальное галлий) в течение 10 минут при 80oC. После этого алюминий отделяют от галламы и выдерживают в течение 4 часов при комнатной температуре. Этот металл приводят в контакт со вторым образцом алюминия массой 3,67 г и выдерживают 3 часа при температуре 80oC. Затем весь металл загружают в плоскодонную колбу, добавляют 90 мл н-гексанола и постепенно повышают температуру реакционной среды. При 155oC время реакции до полного превращения алюминия составляет 2 часа. На дне реактора остается небольшое количество внесенного вместе с алюминием активатора. Он концентрируется в виде одной капли на дне реактора, легко отделяется от спиртового раствора алкоголята, регенерируется и возвращается на активацию. Выход бутилата - 94,7%.
Пример 10. Массивный образец алюминия массой 6 кг подвергают контакту с галламой индия-олова (25±0,2 мас.% In; 13±0,2 мас.% Sn; остальное галлий) следующим образом. В образце высверливаются 4 отверстия диаметром 7,2 мм, глубиной 30 мм на равных расстояниях. В каждое отверстие заливается по 7,5 г галламы. Общее количество активатора составляет 0,5% от массы взятого алюминия. Алюминий выдерживают при температуре 70oC в течение 96 часов. После этого алюминий проявляет природную активность в реакции со спиртами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ АКТИВИРОВАНИЯ АЛЮМИНИЯ И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2009 |
|
RU2414424C2 |
| МЕТАЛЛУГЛЕРОДНЫЙ КАТАЛИЗАТОР | 1994 |
|
RU2096083C1 |
| СПОСОБ АКТИВАЦИИ АЛЮМИНИЯ ДЛЯ ПОЛУЧЕНИЯ ВОДОРОДА | 2014 |
|
RU2606449C2 |
| КАТАЛИЗАТОР СИНТЕЗА β - ПИКОЛИНА КОНДЕНСАЦИЕЙ АКРОЛЕИНА С АММИАКОМ И СПОСОБЫ ЕГО ПРИГОТОВЛЕНИЯ | 1994 |
|
RU2079360C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКИХ МОТОРНЫХ ТОПЛИВ | 1993 |
|
RU2082748C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-1,4-НАФТОХИНОНА | 1997 |
|
RU2142935C1 |
| СПОСОБ ЖИДКОФАЗНОГО ДЕХЛОРИРОВАНИЯ ХЛОРАРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 1996 |
|
RU2100338C1 |
| КАТАЛИЗАТОР СИНТЕЗА МЕТИЛМЕРКАПТАНА | 1997 |
|
RU2120822C1 |
| СПОСОБ ПЕРЕРАБОТКИ МЕТАНА (ВАРИАНТЫ) | 1997 |
|
RU2135441C1 |
| КАТАЛИЗАТОР (ЕГО ВАРИАНТЫ) И ПРОЦЕСС ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 1997 |
|
RU2144844C1 |
Изобретение относится к технологии неорганических материалов. Алкоголяты алюминия применяются как катализаторы в органической химии, гидрофобизаторы и т.д. Интерес к алкоголятам алюминия связан с использованием продуктов их гидролиза для получения чистого оксида алюминия и сложных систем на его основе. Продукты гидролиза алкоголятов алюминия используются как катализаторы, носители, пористые мембраны и т.д. Решаемая изобретением задача заключается в реализации природной активности металлического алюминия в реакции со спиртами. Это позволяет получать целевые продукты высокого качества при соблюдении экологических требований, упрощении технологии и снижении материальных и энергетических затрат. Основным признаком изобретения является активация алюминия галламами индия или индия-олова при контакте поверхности алюминия с галламой и путем диффузии компонентов галламы в объем алюминия. Предложенные способы активации позволяют реализовать реакцию алюминия с алифатическими и ароматическими C2-C8-спиртами с получением высоких выходов целевого продукта. Выход целевых продуктов составляет до 98,5%. 5 з.п. ф-лы, 1 табл., 1 ил.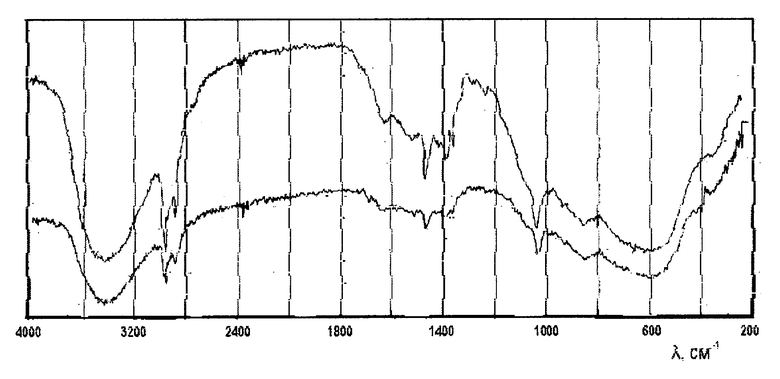
| RU, 2021248, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| RU, 2005711, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| RU, 742422, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Успехи химии, 1996, т | |||
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| Распределительный механизм для четырехтактных двигателей внутреннего горения | 1923 |
|
SU865A1 |
| Федоров П.И | |||
| и др | |||
| Химия галлия, индия и таллия | |||
| - Новосибирск: Наука, 1977, с | |||
| Фотореле для аппарата, служащего для передачи на расстояние изображений | 1920 |
|
SU224A1 |
Авторы
Даты
1999-01-10—Публикация
1997-05-22—Подача