Изобретение относится к области биотехнологии, а именно к технологии получения человеческого эритропоэтина методами генной инженерии.
Эритропоэтин является фактором роста и терминальной дифференцировки предшественников эритроцитов в костном мозге.
Синтез эритропоэтина в организме животных и человека осуществляется в основном в почках и печени и уровень его секреции в норме не превышает нескольких десятков миллиединиц. При ряде патологий, особенно при заболеваниях почек, синтез эндогенного эритропоэтина существенно снижается, что приводит к развитию тяжелых анемических состояний. Введение экзогенного эритропоэтина позволяет эффективно восстанавливать процесс образования эритроцитов, нормализуя тем самым состояние пациентов. В связи с практической невозможностью получения эритропоэтина в достаточных для терапевтического применения количествах из природных источников, широкое распространение получили технологии его изготовления основанные на использовании рекомбинантных клеточных линий животных, способных секретировать человеческий эритропоэтин (рЭПО) при культивировани их на синтетических питательных средах in vitro (акц. заявка РСТ NN 85-03079, кл. C 07 H 7/10, 1985; Евр.пат NN 0205564, кл. C 12 P 21/00, 1990; 0209539, кл. C 07 K 7/10, 1992; 0255231, кл. C 12 P 21/02, 1995).
В качестве продуцентов рЭПО, в основном, используют штаммы клеток млекопитающих, наиболее часто - штаммы культивируемых клеток китайского хомячка В частности, известны такие штаммы-продуценты, как ВСКК(П)-162Д, ВСКК(П)-626Д, (Пат. РФ NN 1555359, кл. C 12 N 5/00, 1990, 2070931, кл. C 12 N 5/10, 1996). Уровень продукции, достигаемый при их культивировании и в стационарных условиях на синтетических питательных средах составляет около 4 мг/л рекомбинантного эритропоэтина.
Недостатками известных методов являются относительно невысокий выход целевого продукта и сложная технология культивирования, а также необходимость периодической амплификации гена эритропоэтина для сохранения достигнутого уровня продукции посредством селекции на питательной среде, содержащей гипоксантин, аминоптерин и тимидин (ГАТ), что удорожает себестоимость производства эритропоэтина.
Прототипом заявляемой группы изобретений являются штамм клеток ВСКК(П)-637Д, полученных посредством трансформации исходной линии клеток плазмидой pSv-dEp-l-Mo несущей полноразмерный ген человеческого эритропоэтина. (Пат. РФ N 2089611, кл. C 12 N 5/16, 1995). Штамм поддерживают на среде Игла с 10% сывороткой крупного рогатого скота (КРС) и в промышленных масштабах культивируют на микроносителях с очисткой конечного продукта хроматографическими методами.
При использовании данного решения уровень синтеза эритропоэтина достигал более высоких значений и составлял 1500-1800 Е на мл.
Основным недостатком данного штамма и способа его применения являются то, что достигаемый в этом случае уровень биосинтеза эритропоэтина все еще остается недостаточным для создания экономически эффективного производства.
Задачей, стоявшей перед авторами являлось получение высокопродуктивного штамма животных клеток, конституитивно продуцирующего рЭПО человека без дополнительной периодической селекции.
Поставленная задача достигается в результате разработки технологии, включающей в себя новый штамм культивируемых клеток яичника китайского хомяка, получившего при регистрации ВСКК (П)-651Д и технологию культивирования этого и ему подобных штаммов.
Штамм был получен по технологии, включавшей в себя трансформацию линии клеток яичника китайского хомяка CHO К1 DHFR-(Urlaub, et аl., 1980, PNAS. USA. , 77, 4461) плазмидой pBD (Glanville, Durham & Palmiter, 1981, Nature, 292, 267-269), несущей MT-I промотор, маркер DHFR+ и полноразмерный ген человеческого эритропоэтина с последующей одношаговой селекции целевых трансфектантов на питательной среде, содержащей 1 мМ метатрексата и последующего клонирования продуцентов методом лимитирующих разбавлений с контролем продуктивности колоний методом твердофазного иммуноферментного анализа.
Полученный штамм клеток (CНО-ЭПО/SPM был депонирован в Российской коллекции клеточных культур под номером ВСКК( П)-651Д
Штамм характеризуется следующими признаками:
1. Морфологические признаки.
Культура клеток представлена на начальном этапе культивирования фибробластоподобными элементами с крупными овальными ядрами, содержащими несколько ядрышек. По мере уплотнения монослоя клетки приобретают округлую, эпителиоподобную форму, при дальнейшем росте культуры наблюдается формирование многослойной клеточной структуры.
2. Культуральные признаки.
Штамм СНО-ЭПО/SPM поддерживается на смеси (50%/50%) питательных сред RPM11640 и DMEM с добавлением 5% сывороточного заменителя FETACLONEll (HighClone, USA) и 40 мкг/мл гентамицина.
Клетки субстратзависимы, при культивировании в богатых питательных средах (при высоком до 10% содержании фетальной сыворотки) склонны к частичному откреплению от субстрата и росту в суспензии посредством образования многоклеточных кластеров. Репассирование клеток осуществляют с помощью 0,25% раствора трипсина, 0,02% раствора версена или их смесью 50%/50%. Кратность рассева 1/3 - 1/5, посевная доза составляет 2-3•104 клеток, на 4 кв. см поверхности культурального флакона. Формирование клеточного монослоя завершается через 2-3 дня после пересева.
3. Устойчивость к селективным факторам.
Штамм проявляет устойчивость к метатрексату в дозе до 1 мМ
4. Криоконсервация.
Криоконсервацию культуры проводят в среде RPMI1640 с добавлением 50% эмбриональной сыворотки и 7% диметилсульфоксида в качестве криопротектора при концентрации клеток 1,5 -2,0 млн. клеток/мл.
Криокультуру хранят в парах жидкого азота или погружением в жидкий азот. Оттаивание культуры проводят посредством быстрого переноса ампулы с культурой на водяную баню при 37oC с последующем центрифугированием и ресуспендированием клеток в свежей ростовой питательной среде. Жизнеспособность культуры после размораживания составляет 85-95%.
5. Контроль видовой идентичности.
Соответствие виду подтверждается чувствительностью к пролину
6. Контаминации.
При контроле клеток штамма на наличие бактериальных, грибных и вирусных контаминаций на пассажах 10 и 40 не обнаружено бактерий, микоплазм, грибов и вирусов.
Основными отличиями нового штамма являлось возможность продуцирования рЭПО в отсутствии селективного давления. Штамм сохранял способность конституитивно продуцировать рЭПО на протяжении более 40 пассажей без снижения уровня продукции и дополнительной селекции.
Особенностью заявляемого способа культивирования является то, что клетки культивируют в роллерных флаконах на питательной среде, содержащей в 1 л следующие ингредиенты:
Fetaclone II - 80- 20 мл
глутамина - 200 мг,
HEPES - 3,57 г,
смесь равных долей сред RPMI 1640 и DMEM - до 1л.
При этом лучшие результаты достигаются при следующих параметрах культивирования: скорость вращения роллерных флаконов -1,5- 2,0 об/мин, а общая продолжительность культивирования составляет не менее 14 суток при длительности каждого накопительного цикла 2 суток.
Как правило, штаммы перед культивированием подращивают в течении не менее 2 суток в роллерных флаконах при скорости вращения 1.5-2.0 об в мин на питательной среде содержащей в 1 л:
эмбриональной сыворотки телят - FCS - 80-120 мл,
глутамина - 200 мг,
гентамицина - 0,04 мг
смесь равных долей сред RPMI 1640 и DMEM - до 1 л.
Лучшие результаты достигаются при использовании для культивирования штамма клеточных культур ВСКК(П)-651Д, однако возможно применение данного способа и для других известных штаммов.
Полезность и применимость полученного штамма клеток и нового способа получения рЭПО для промышленного использования иллюстрируется следующими примерами.
Пример 1. Для оценки продуктивности клеток штамма СНО-ЭПО/SPM предварительно накопленную суспензию клеток высеивали в концентрации 3-10 кл/мл в объеме 100 мл питательной среды ростового состава (50%/50% смесь сред RPMI 1640 и DMEM, содержащей 10 мл эмбриональной сыворотки телят -FCS, 20 мг глутамина и 0.004 мг гентамицина) в каждый из 10 культуральных флаконов Т175 с ростовой поверхностью 175 см2 и объемом 650 мл. Флаконы инкубировали при 37oC в течение 3 суток в стационарных условиях. По окончании инкубации ростовую питательную среду во флаконах заменяли на эквивалентный объем накопительной среды, содержащей в 1 л:
Fetaclone II - 10 мл
глутамина - 200 мг,
HEPES - 3.57 г,
смесь равных долей сред RPMI 1640 и DMEM - до 1 л,
и инкубацию флаконов при 37oC продолжали еще 2 суток. По окончании инкубации накопительную среду из флаконов собирали в сборную емкость и помещали после добавления фенилметилсульфонилфторида (PMSF) для хранения в холодильник при +4oC. В культуральные флаконы с клеточной культурой вносили свежую порцию накопительной среды и весь цикл накопления эритропоэтина повторяли. Собранную накопительную среду сохраняли так же как и на предыдущем цикле. В общей сложности было проведено 7 циклов накопления эритропоэтина и было собрано 6,8 л культуральной жидкости, содержащей эритропоэтин. По окончании накопительного периода клетки из каждого флакона были собраны после обработки клеточного монослоя смесью трипсин/версен (50%/50%) посредством ресуспендирования в 500 мл накопительной среды и их концентрация была определена с помощью гемоцитометра.
Общее количество клеток, собранное с 10 флаконов составило 22,75•107 клеток. Учитывая, что общая ростовая поверхность для 10 флаконов Т175 составляет 1750 см2, средняя плотность культуры на 1 см2 составила (1,3±0,1)• 105 клеток. В собранной накопительной среде определили содержание эритропоэтина с помощью твердофазного иммуноферментного анализа посредством набора реагентов Clinigen фирмы Amgen. Содержание эритропоэтина в собранной накопительной среде составило 1160±120 Е/мл. Таким образом, удельная продуктивность полученного клеточного штамма СНО-ЭПО/SPM составила 5098±527 Е/106 кл/48 ч, что в несколько раз выше, чем достигнуто в прототипе.
Пример 2. Получение рЭПО и его идентификация.
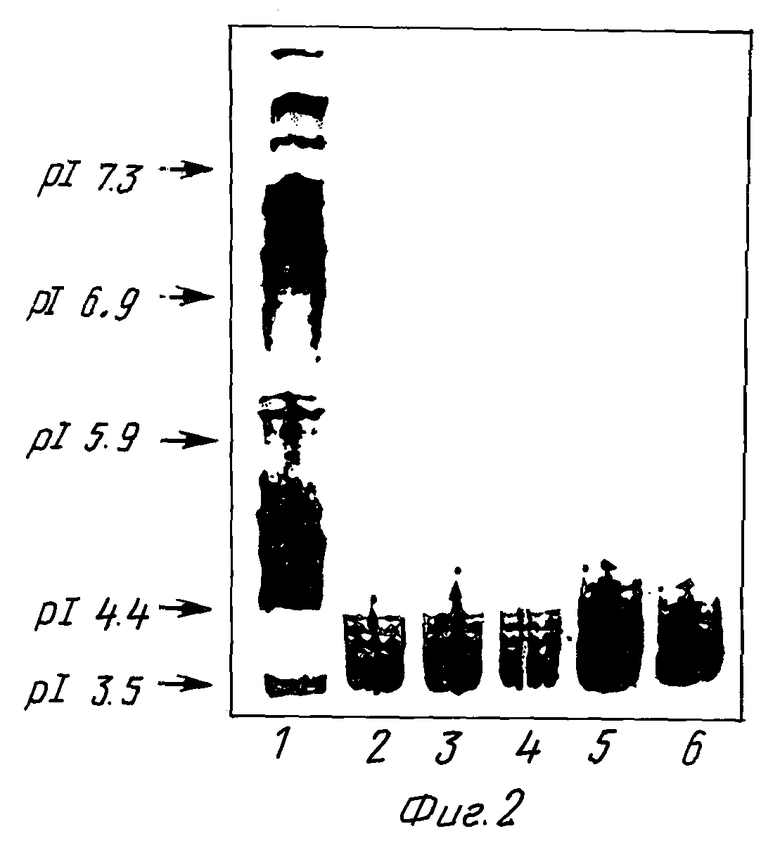
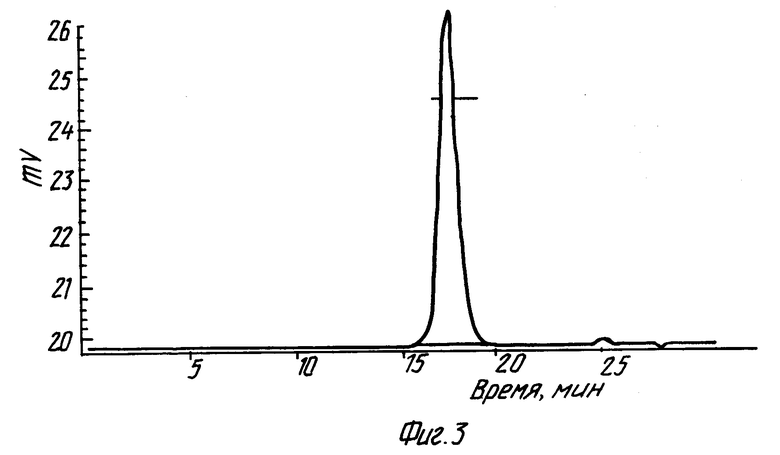
Собранную накопительную среду подвергли очистке с целью выделения и характеристики синтезированного эритропоэтина и доказательства его идентичности природному аналогу. Для этого культуральную жидкость осветляли микрофильтрацией через мембранные фильтры с размером пор 0,8 мкм (Millipore) и очищали посредством иммуноаффинной и ионнообменной хроматографии до гомогенного состояния. Полученный препарат оценивался по следующим критериям: чистота, изоформный состав, идентичность N-концевой цепи, удельная биологическая активность in vivo, иммунологическая идентичность и наличие олигомеров. Полученный препарат эритропоэтина по данным электрофореза в ПААГе и HPLC являлся практически гомогенным и не содержал примесей олигомерных форм эритропоэтина (фиг. 1a, b и 2). Его молекулярная масса составила ≈35 kd, что эвивалентно молекулярной массе природного эритропоэтина. Препарат обладал микрогетерогенностью, выявляемой при изоэлектрофокусировании (фиг. 3) и типичной для эритропоэтина вследствии различий в степени и характере гликозилирования. При изоэлектрофокусировании выявляется 4-6 полос в зонах pl 3.5-4.5, что также характерно для эритропоэтина. Идентичность N-концевой последовательности выделенного эритропоэтина ранее описанной структуре была продемонстрирована посредством твердофазной деградации 16 N-концевых остатков по Эдману (фиг. 4), которые оказались идентичны природному гормону. Удельную биологическую активность полученного эритропоэтина контролировали in vivo на мышах с гипербарически индуцированной анемией по включению в ЭПО-стимулируемые эритробласты 59Fe. В качестве стандарта использовали 2-й международный стандарт эритропоэтина. Удельная активность полученного эритропоэтина составила (140±14,5)• 103 МЕ/мг белка, что соответствует активности чистого эритропоэтина. Иммунологическая идентичность полученного эритропоэтина его природному аналогу была продемонстрирована в конкурентном твердофазном иммуноферментном анализе, где в качестве конкуратора использовался природный эритропоэтин, выделенный из мочи полицетемических пациентов. При 10-кратном избытке холодный природный эритропоэтин подавляет почти на 90% связывание биотинилированного рекомбинантного эритропоэтина с иммобилизованными на поверхности ячеек полистирольного микропланшета (High bond. Costar) поликлональными кроличьими антителами к человеческому эритропоэтину. Таким образом, совокупность использованных критериев позволяет с определенностью утверждать, что продуцируемый штаммом клеток СНО- ЭПО/SPM рекомбинантный белок является эритропоэтином, идентичным природному гормону.
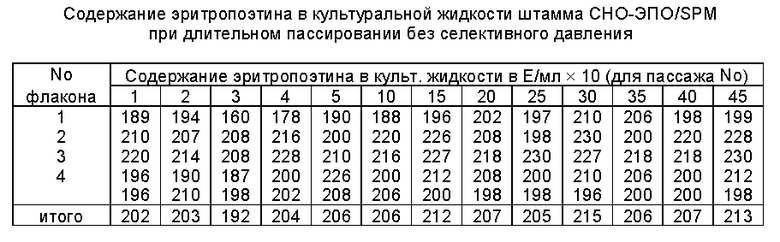
Пример 4. Для того, чтобы продемонстрировать стабильную продуктивность штамма клеток СНО-ЭПО/SPM в отсутствие селективного давления, предварительно подготовленную культуру высеяли в 5 культуральных флаконов Т50 в 10 мл питательной среды ростового состава (см. пример 1) в концентрации 3•104 кл/мл. Флаконы инкубировали при 37oC в стационарных условиях. Каждые 3 дня из каждого флакона отбирали пробы культуральной жидкости для определения содержания в них эритропоэтина, оставшуюся среду удаляли и клеточный монослой трипсинизировали как указано в примере 1. 20% полученной клеточной суспензии высеивали в 10 мл ростовой питательной среды в новый флакон Т50, а остальные клетки помещали в среду для криоконсервации и замораживали для длительного хранения в жидком азоте. Репассирование культур и определение содержания эритропоэтина в культуральной жидкости на каждом пассаже проводили на протяжении 4,5 месяцев (45 пассажей) Полученные результаты представлены в таблице.
Как следует из данных, представленных в таблице, уровень продукции эритропоэтина при пассировании штамма клеток СНО-ЭПО/SPM в отсутствие селективного давления оставался постоянным на протяжении не менее 45 пассажей
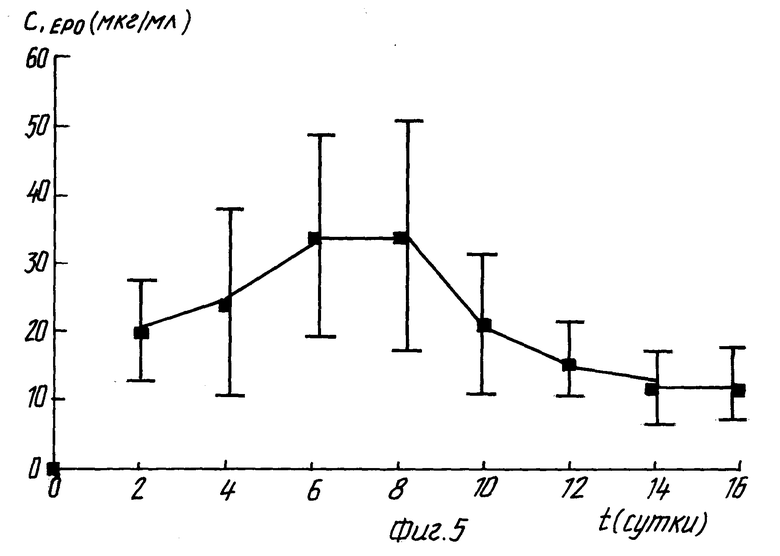
Пример 6. Вариант способа получения рЭПО клеточного штамма СНО-ЭПО/SPM. Предварительно подготовленную суспензию клеток штамма высеяли в роллерные флаконы (V= 2,6 л; S=850 см2) в среде ростового состава (см. пример 1), за исключением того, что вместо эмбриональной сыворотки FCS использовали значительно более дешевую реконструированную сыворотку Fetaclone 11 (HighClone, USA) в конечной пропорции 1: 10 v/v В каждый роллерный флакон высеяли по ≈8•106 клеток в объеме 200 мл. Флаконы установили в роллерный культиватор и инкубировали при +37 С при скорости вращения 0,8 об/мин в течение 3 дней. По истечении этого времени ростовую среду в роллерных флаконах заменили на среду накопительного состава, состоящую из смеси питательных сред RPMI1640 и DMEM - 50%/50%, содержащей 200 мг глутамина, 3.57 r HEPES (pH 7,4) и 10 мл Fetaclone II. В каждый флакон вносили по 400 мл накопительной среды. Инкубацию культур в роллерном культиваторе продолжали еще 48 ч при скорости вращения 1,5-2,0 об/мин. По окончании накопительного времени, культуральную среду из роллерных флаконов собрали в накопительную емкость, а в роллерные флаконы внесли свежую порцию накопительной среды в количестве 400 мл и процедуру накопления полностью повторили, собрав по окончании накопительного времени в накопительную емкость новую порцию культуральной жидкости. Описанную процедуру накопления культуральной жидкости с эритропоэтином повторили 7 раз, остановив ее по причине появления признаков нарушения целостности клеточного монослоя из-за его переуплотнения. В каждой порции собранной культуральной жидкости контролировали содержание эритропоэтина с помощью твердофазного иммуноферментного анализа посредством набора фирмы Amgen. Полученные результаты представлены графически на фиг.5. В данном примере исследование промышленного потенциала было проведено на 30 роллерных флаконах с ростовой поверхностью 850 см2 каждый при объеме накопительной среды 400 мл и времени накопления 48 ч при общем количестве циклов накопления, равном 7. В общей сложности было собрано 84 л культуральной жидкости при содержании эритропоэтина 2611±346 Е/мл или около 1,5 г эритропоэтина. Полученный результат, таким образом, демонстрирует высокий промышленный потенциал предлагаемого штамма клеток.
Пример 7. Вариант способа получения рЭПО. клеточного штамма СНО-ЭПО-1. Предварительно подготовленную суспензию клеток штамма высеяли в 5 роллерных флаконов( V = 2,6; S = 850 кв.см) и далее культивировали в соответствии с условиями примера 6. В результате проведенных экспериментов было собрано 14 л накопительной питательной среды, содержавшей рЭПО 360+80 Е/мл. В стандартных условиях (Авт. св. СССР N 155359, кл. C 12 N 500, 1988) уровень продукции рЭПО для данного штамма составлял 12-15 Е/мл.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ КЛЕТОК ЯИЧНИКОВ КИТАЙСКОГО ХОМЯЧКА СНО-ЕРО 4А9 - ПРОДУЦЕНТ ВЫСОКОСИАЛИРОВАННОГО ЭРИТРОПОЭТИНА | 2016 |
|
RU2652884C1 |
| Штамм линии клеток яичника китайского хомячка | 2023 |
|
RU2805879C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБСТАНЦИИ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА И НАНОКАПСУЛИРОВАННАЯ ФОРМА РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА С ИСПОЛЬЗОВАНИЕМ СУБСТАНЦИИ, ПОЛУЧЕННОЙ УКАЗАННЫМ СПОСОБОМ | 2012 |
|
RU2518329C1 |
| СИНТЕТИЧЕСКАЯ ДНК, КОДИРУЮЩАЯ ЭРИТРОПОЭТИН ЧЕЛОВЕКА, СОДЕРЖАЩИЙ ЕЁ ВЕКТОР, СПОСОБ ПОЛУЧЕНИЯ ШТАММА-ПРОДУЦЕНТА ЭРИТРОПОЭТИНА, ШТАММ-ПРОДУЦЕНТ ЭРИТРОПОЭТИНА | 2014 |
|
RU2548806C1 |
| СПОСОБ ОЧИСТКИ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА | 1998 |
|
RU2145610C1 |
| ШТАММЫ КУЛЬТИВИРУЕМЫХ ГИБРИДОМ МЫШЕЙ - ПРОДУЦЕНТЫ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ЧЕЛОВЕЧЕСКОМУ ЭРИТРОПОЭТИНУ И АНТИТЕЛА, ИМИ ПРОДУЦИРУЕМЫЕ | 1998 |
|
RU2151184C1 |
| ВЕКТОР ЭКСПРЕССИИ, ЭУКАРИОТИЧЕСКИЙ ШТАММ ПРОДУЦЕНТ И СПОСОБ ПОЛУЧЕНИЯ ДАРБЭПОЭТИНА АЛЬФА | 2022 |
|
RU2819866C2 |
| ИММУНОМОДУЛИРУЮЩИЙ ПРЕПАРАТ "БЕТАЛЕЙКИН" | 1998 |
|
RU2128706C1 |
| ГИБРИДНЫЙ БЕЛОК НА ОСНОВЕ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ), И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2515914C1 |
| ШТАММ СНО КУЛЬТИВИРУЕМЫХ КЛЕТОК КИТАЙСКОГО ХОМЯЧКА - ПРОДУЦЕНТ ЭРИТРОПОЭТИНА ЧЕЛОВЕКА | 1995 |
|
RU2089611C1 |

Изобретение относится к биотехнологии и предназначено для получения человеческого эритропоэтина. Способ осуществляют путем культивирования штамма клеток яичника китайского хомячка, трансформированного плазмидой, содержащей ген человеческого эритропоэтина, в ростовой и накопительной питательных средах. Накопительная среда содержит в 1 л Tetaclone 11 (10 мл), глутамин 200 мг, HEDES 3,57 г, смесь равных долей сред RPMI 1640 и DMEM. Штамм получен путем трансформации клеток яичника китайского хомяка СНО К1 DHFR плазмидой рВД, несущей полноразмерный ген человеческого эритропоэтина, с последующей селекцией на среде, содержащей 1 мМ метатрексата, и депонирован под номером ВСКК (П) - 651 Д. Изобретение позволяет получать эритропоэтин в промышленных условиях с высоким выходом. 2 с. и 3 з.п., ф-лы, 5 ил. , 1 табл.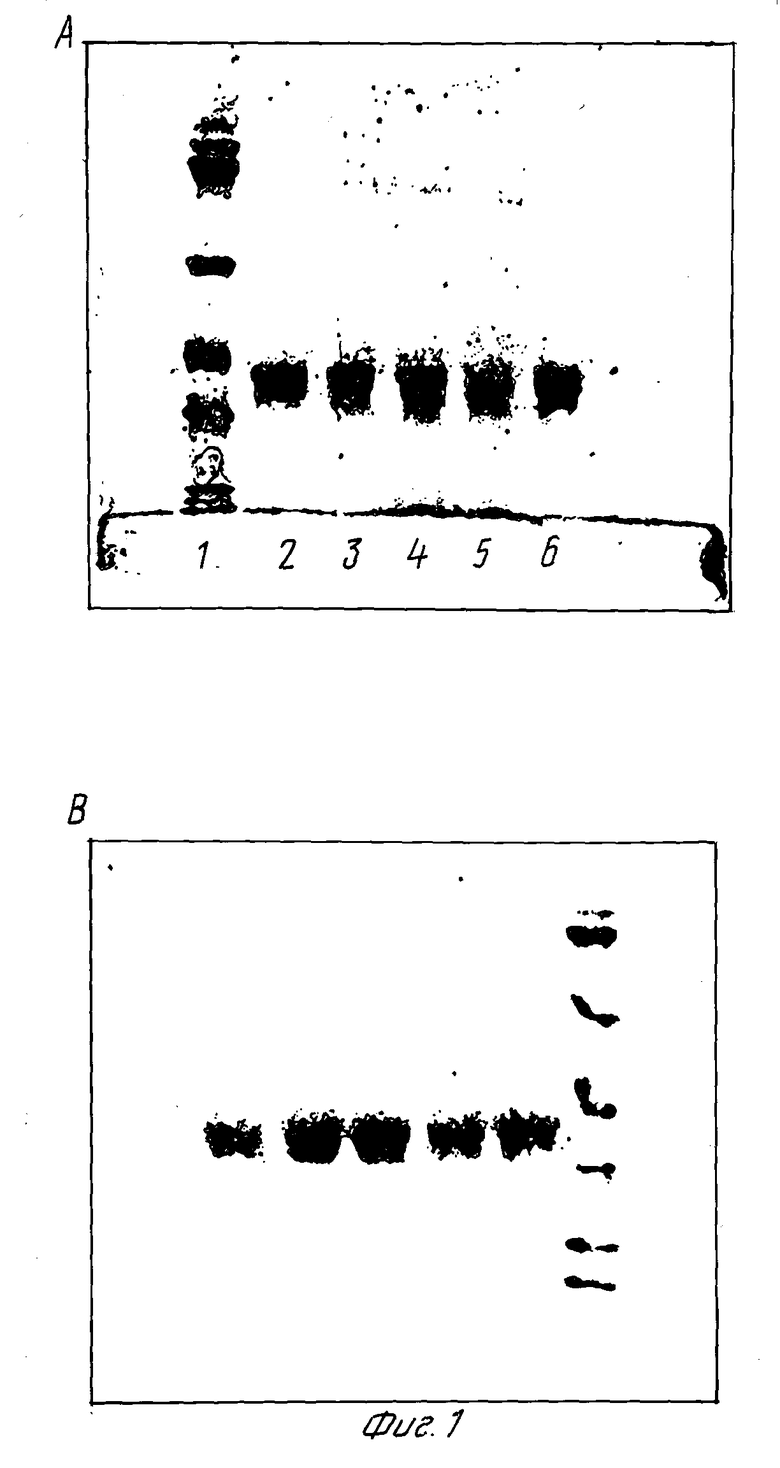
Fetaclone 11, мл - 10
Глутамин, мг - 200
HEPES, г - 3,57
Смесь равных долей сред RPMI 1640 и DMEM, л - До 1
а общая продолжительность культивирования в ростовой среде составляет не менее 2 суток, а в накопительной среде составляет не менее 14 суток при длительности каждого накопительного цикла 2 суток.
Эмбриональная сыворотка телят - FCS, мл - 80 - 120
Глутамин, мг - 200
Гентамицина, мг - 0,04
Смесь равных долей сред RPMI 1640 и DMEM, л - До 1
4. Способ по п.1 или 3, отличающийся тем, что скорость вращения роллерных флаконов на стадии ростового культивирования составляет 1,5 - 2 об/мин.
| ШТАММ СНО КУЛЬТИВИРУЕМЫХ КЛЕТОК КИТАЙСКОГО ХОМЯЧКА - ПРОДУЦЕНТ ЭРИТРОПОЭТИНА ЧЕЛОВЕКА | 1995 |
|
RU2089611C1 |
| Штамм культивируемых клеток китайского хомячка - продуцент эритропоэтина человека | 1988 |
|
SU1555359A1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРЭТИЛА | 0 |
|
SU255231A1 |
| ГЕНЕРАТОР РОЙЕРА | 0 |
|
SU267678A1 |
| US 5441868, 15.08.95. | |||
Даты
1999-01-20—Публикация
1998-02-12—Подача