Изобретение относится, прежде всего, к новым биоактивым продуктам, получаемым из торфа, и к способам получения таких продуктов. Изобретение также относится к фармацевтическим и косметическим композициям, содержащим эти продукты, и к способам получения фармацевтических и/или косметических композиций, содержащих вышеуказанные биоактивные продукты, полученные из торфа.
Известны различные способы экстрагирования торфа с использованием различных экстракционных сред, а также использование таких экстрактов, содержащих полученные из торфа биоактивные ингредиенты, для фармацевтических и косметических целей.
Один из таких известных способов охарактеризован в польском описании изобретения к патенту N 124110 (Chemical Abstract 101(10), 78854e). В соответствии с этим известным способом биоактивные продукты получают из торфа с помощью первичного и вторичного щелочного гидролиза воздушно-сухого неочищенного торфяного материала, затем проводят подкисление полученного таким образом гидролизата и сепарацию нерастворимой твердой части с последующим вторым подщелачиванием, подкислением чистой (прозрачной) жидкой фазы и удалением балластных веществ с помощью спиртовой или эфирной экстракции. В указанном способе водная фаза органической экстракции является жидким биоактивным продуктом, полученным из торфа.
Известный жидкий продукт, который является раствором полученных из торфа активных ингредиентов в сильно концентрированном, почти насыщенном растворе хлорида натрия, полученный в соответствии с вышеуказанной ссылкой на польское описание изобретения к патенту, является нестабильным при хранении в течение длительного времени и, кроме того, содержит - что касается биологической активности композиции - большой избыток неорганических нейтральных веществ. Будучи объемным продуктом, он не удобен в обращении, его трудно хранить и производить.
Главной целью настоящего изобретения является разработка продукта, у которого отсутствуют данные недостатки, т.е. продукта, который является стабильным и может быть легко введен в фармацевтические или ветеринарные продукты, а также в косметические препараты как в твердом виде, так и в виде любого удобного раствора.
В частности, что касается использования полученного из торфа биоактивного продукта для фармацевтических целей, т.е. для получения фармацевтических композиций, то была настоятельная необходимость в разработке твердой формы, которая хорошо подходила был для этих целей. Так как предварительные попытки, связанные с концентрацией известного водного раствора полученных из торфа биоактивных веществ и его обессоливания, не дали положительных результатов в связи с окклюзией активных ингредиентов в кристаллизующуюся твердую фазу, вызывающей уменьшение биологической активности композиции, то было очень трудно найти подходящий способ для превращения жидкой композиции в порошок. Неожиданно было обнаружено, что положительного результата можно достигнуть, если до концентрирования жидкую композицию сначала развести в несколько раз, т. е. разбавить один объем композиции несколькими объемами воды.
Соответственно, настоящее изобретение разрабатывает способ, с помощью которого возможно получение выделенного из торфа биоактивного продукта, отличающегося вышеуказанными преимущественными характеристиками, из высококонцентрированного водного раствора неорганической соли - главным образом хлорида натрия, содержащего полученные из торфа биоактивные ингредиенты с помощью разбавления упомянутого раствора деминерализованной водой, т.е. дистиллированной водой, с последующим обратным осмосом, концентрированием и очисткой. Полученный таким образом раствор может быть легко превращен в стерильный и твердый продукт, подходящий для необходимых целей, посредством стерилизации и распылительной сушки. Разбавление количествами воды предпочтительно осуществляют в несколько раз, предпочтительно от 5 до 8 раз, от количества концентрированного раствора, который необходимо развести.
Данный способ, применяемый для обработки продукта, полученного в соответствии с описанием изобретения к патенту Польши N 124110, заключается в удалении остаточных органических растворителей из постэкстракционной водной фазы, сепарировании нерастворимых частей с помощью фильтрации при пониженном давлении через спекшийся керамический материал, разбавлении растворенного вещества в несколько раз объемом дистиллированной воды и обработке его посредством обессоливания с помощью обратного осмоса для отделения избыточных минеральный солей, в основном хлорида натрия, в виде пермеата. Затем обессоленный раствор концентрируют, очищают с помощью центрифугирования и стерилизуют фильтрацией через мембранный фильтр, например, фильтр "миллипор".
Полученный микробиологический чистый раствор в необязательном порядке может быть подвергнут распылительной сушке. Из стерильного продукта, жидкого или твердого, может быть составлена косметическая, фармацевтическая или ветеринарная композиция. Необязательно, концентрированный и очищенный раствор может быть использован - без стерилизации и распылительной сушки - в любом подходящем разбавлении в качестве компонента во многих косметических композициях.
Предпочтительно, на стадии распылительной сушки температуру на входе устанавливают около 180oC, а температуру на выходе - около 90oC.
В соответствии с патентом Польши N 124110 подкисленный гидролизат, получаемый из торфа, характеризующийся содержанием зольных веществ в количестве 8-30%, степенью распада до 30-70% и значением pH, равным 3,5-7,0, подвергают вторичному гидролизу в водном растворе щелочных веществ при значениях pH от 9,0 до 14,0 и температуры 16-60oC. После отделения осадка фильтрат снова подкисляют до значения pH, равного 3,0-1,0, после чего его концентрируют, нейтрализуют и снова концентрируют досуха. Полученную таким образом сухую массу экстрагируют затем 40-80% водным этанолом при температуре 30-60oC. После отделения от экстракта балластных веществ его концентрируют до получения половинного объема от исходного значения. Остаток экстрагируют этанолом, смешанным с другим органическим растворителем, таким как эфир, хлороформ, бензол, этилацетат, в соотношении от 1:1 до 1:3. Затем водный слой концентрируют до половины от исходного объема, центрифугируют и разделяют на колонках с целлюлозой или биогелем, используя в качестве разделяющей системы воду или 5-10%-ный водный этанол, метанол или ацетон.
Селективное удаление избытка солей или кислот проводят с помощью ионообменной техники.
Полученный в соответствии с указанным патентом продукт содержит, помимо полисахаридов, определенные минеральные соли.
Конечный продукт, полученный таким способом, отличается от соответствующего известного продукта как по химическому составу, так и по более широкому диапазону противораковой активности.
Пример получения продукта по патенту Польши N 124110.
Один килограмм воздушно-сухого торфа измельчают и экстрагируют с применением 8 л 0,1-8,0%-ного водного раствора NaOH в течение 36 часов при комнатной температуре и при постоянном перемешивании. Затем щелочной экстракт центрифугируют для отделения твердых частей, после чего его подкисляют соляной кислотой до значения pH примерно 2 и оставляют на 12 часов. Образующийся при этом осадок отделяют, а прозрачный раствор обрабатывают гидроксидом натрия до достижения значения pH 9, после чего снова фильтруют. Далее фильтрат опять подкисляют соляной кислотой и концентрируют при пониженном давлении до достижения 1/5 от первоначального объема. Концентрированный раствор нейтрализуют гидроксидом натрия и выпаривают досуха. Проводят экстракцию сухой массы водным этанолом. Экстракт отделяют от жирового остатка и неорганических солей. Затем экстракт концентрируют до того момента, когда соли начинают выпадать в осадок. Осадок отделяют, а полученный таким образом фильтрат экстрагируют смесью в пропорции 1:1 этанола и эфира, хлороформа, бензола или этилацетата. Выпавший во второй раз осадок неорганических солей вновь отфильтровывают, а водный фильтрат концентрируют до половинного объема относительно его исходного значения, центрифугируют и фильтруют. Прозрачный фильтрат подвергают хроматографии на колонке с Биогелем Р-2 минус 400 меш (сырой) с использованием в качестве элюента воды или 10% водного этанола, а фракции, обладающие антираковой активностью, собирают.
Полученный препарат представляет собой гигроскопичное, аморфное вещество коричневатого цвета, содержащее примерно 10% воды. Оно водорастворимо и нерастворимо в органических растворителях. После проведения кислотного гидролиза оно дает положительную реакцию при взаимодействии с группой реагентов, применяемых для определения наличия сахаров - глюкозы, галактозы, арабинозы, глюкуроновой кислоты, рамнозы, ксилозы, 6-дезоксиглюкозы и 2-дезоксиглюкозы. ИК-спектр типичен для полисахаридов. После прокаливания при 700oC получают золы, составляющие до 6-10% от исходной массы и содержащие окислы металлов, среди которых найдены такие, как окислы Mo, Cd, Co, N, Mn, Mg, C, V, а также неметаллические окислы, среди которых следует отметить окислы Si и P.
Хотя способ по изобретению описывается в комбинации со способом согласно описанию изобретения к патенту Польши N 124110, его использование не ограничено такой комбинацией, но обычно применимо в контексте способа получения выделенного из торфа биоактивного продукта из высококонцентрированного жидкого раствора неорганических солей, главным образом хлорида натрия, содержащего выделенные из торфа биоактивные ингредиенты.
Полученные из торфа биоактивные продукты, о которых идет речь в данном изобретении, не содержат более 70 вес.%, предпочтительно не более 60 вес.%, неорганических солей, главным образом хлорида натрия. Так как в оптимальном продукте является желательной концентрация хлорида натрия как можно более низкая, главным образом для фармацевтического применения и такого косметического применения, где необходимы более высокие концентрации, т.е. для ухода за лицом, то наиболее предпочтительными являются более низкие концентрации хлорида натрия, такие как 55% и даже ниже, особенно при возможности получения посредством стадий разбавления и обратного осмоса. Если способ ограничивается стадиями концентрирования и очистки, то продукт является концентрированным или сгущенным раствором. "Концентрированный торфяной экстракт", на который ссылаются в этом описании изобретения, является темно-коричневой жидкостью с плотностью 1,02-1,09 г/мл и содержит не менее 5 вес.% сухих твердых веществ. Содержание иона хлорида в сухих твердых веществах, рассчитанное как NaCl, составляет не выше 70%, предпочтительно не выше 60%, и значение pH 1% водного раствора равно 5,0-6,5, обычно 6,0. Отсутствие следующей стадии стерилизации в некоторых случаях не наносит вреда, например, для определенного косметического использования упомянутого концентрированного торфяного экстракта.
С другой стороны, стадия стерилизации может быть обязательной, в частности, если продукт предназначается для приготовления фармацевтических композиций. В этом случае особенно предпочтительной является дополнительная стадия распылительной сушки, если не обязательной. Продукт, полученный после такой стадии распылительной сушки, находится в форме порошка и поэтому особенно годится для приготовления некоторых фармацевтических композиций. Наиболее предпочтительным продуктом такого типа является продукт, выпускаемый под названием "ToLPA®. Torf Preparation" ToLPA® является зарегистрированной торговой маркой Torf Corporation, Mydlana 2, Wroclaw, Poland.
В этом описании к изобретению будет использоваться аббревиатура ТТР для обозначения вышеупомянутого продукта.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим в качестве активного ингредиента полученный из торфа биоактивный продукт, описанный выше, в частности продукт, содержащий не более 70 вес.%, предпочтительно не более 60 вес.%, неорганических солей, главным образом хлорида натрия, по сухим твердым веществам, вместе с фармацевтически приемлемым носителем. Полученный из торфа биоактивный продукт, содержащийся в таких фармацевтических композициях, предпочтительно является ТТР, указанным выше. Фармацевтические препараты содержат полученный из торфа биоактивный продукт и фармацевтически приемлемый носитель, предпочтительно в весовом соотношении от около 1:5 до 1:25, и наиболее предпочтительно между 1:9 и 1: 19.
Кроме того, настоящее изобретение относится к способу приготовления фармацевтической композиции, содержащей полученный из торфа биоактивный продукт в форме геля. Этот способ отличается тем, что стерильный спиртовой травяной экстракт соединяют со стерильным глицерином, стерильным водным - предпочтительно концентрированным - раствором предварительно измельченного в порошок полученного из торфа биоактивного продукта и стерильным ментоловым раствором, и полученную смесь постепенно соединяют с коллоидным кремнеземом для превращения жидкой композиции в форму геля, при этом весовое соотношение жидкой смеси к кремнезему составляет от 90:10 до 94:6. Предпочтительным является использование в качестве порошкообразного или концентрированного полученного из торфа биоактивного продукта ТТР.
Настоящее изобретение также относится к способу приготовления фармацевтической композиции, содержащей полученный из торфа биоактивный продукт, в виде мази. Этот способ отличается тем, что стерильный травяной экстракт постепенно соединяют со стерильным раствором порошкообразного полученного из торфа биоактивного продукта, полученную смесь превращают в гель с помощью добавления коллоидного кремнезема, и полученный таким образом гель растирают в порошок с предварительно стерилизованной смесью жирных компонентов, таких как эуцерин (eucerine) и вазелин, предпочтительно с весовым соотношением жидких компонентов к кремнезему около 30:20 и геля к жирным компонентам от 32:68 до 34:66. Здесь также является предпочтительным использование в качестве порошкообразного или концентрированного полученного из торфа биоактивного продукта ТТР.
Косметические препараты, которые могут включать травяные экстракты, а также другие добавочные и обогащенные компоненты, ароматизирующие компоненты и носители, приемлемые для косметических целей, содержат полученный из торфа биоактивный продукт в соответствии с настоящим изобретением в количестве 0,01-10 вес. %, предпочтительно 0,05-1,00 вес.%, и наиболее предпочтительно 0,05-0,10 вес.%.
Носители могут быть водными растворами спиртов, всеми типами эмульсий, гелями, пенообразующими композициями и жирными носителями. Использование одного определенного носителя, выбранного из группы упомянутых выше веществ, позволяет составлять различные типы косметических препаратов в соответствии с изобретением, таких как тонизирующие средства, кремы, бальзамы, молочко для очищения кожи и т.д. для повседневного ухода за телом, а также шампуни, бальзамы для волос, пеномоющие средства для ванн, все с добавкой полученных из торфа биоактивных продуктов.
Выделенные из торфа биоактивные продукты (сокращенно торфяные экстракты), полученные из исходного неочищенного торфяного материала, такие как (среди других) лечебные грязи, содержат хорошо сбалансированные количества минеральных или органических соединений, таких как минеральные соли следующих элементов: B, Si, Ab, Fe, Mg, Mn, Cu, Si, Ni, Ca, Ag и Na; органические соединения, такие как аминокислоты в свободной форме и в виде солей; полисахариды, частично разложившиеся/реагирующие - в случае гидролиза - до дезоксисахаридов и/или аминосахаридов. Торф, в частности лечебная грязь, известен и изучается как материал биологического растительного и микробиологического происхождения; благодаря содержанию в нем питательных и стимулирующих компонентов он обладает целебным воздействием на организм человека и млекопитающего; следовательно, полученные из торфа биоактивные композиции содержат вышеупомянутые вещества в пропорциях, характерных для живых организмов; это можно рассматривать как объяснение полезного воздействия косметических и фармацевтических препаратов, содержащих полученные из торфа активные продукты и композиции. Особенно хороший эффект при применении новых косметических композиций наблюдают в том случае, когда в композиции также присутствуют травяные экстракты. Выбор подходящего травяного экстракта основан на известном обычном использовании таких экстрактов в косметике с изменением активности препаратов и позволяя тем самым приспособить содержание косметических препаратов к требованиям и нуждам больных.
Настоящее изобретение более подробно характеризуется и объясняется нижеследующими примерами.
Пример 1.
Исходя из 1000 кг воздушно-сухого неочищенного торфяного материала, обработанного затем, например, по технологии согласно польскому патенту N 124110, получают раствор выделенных из торфа биоактивных ингредиентов в насыщенном водном растворе хлорида натрия в количестве около 10 л. Раствор фильтруют через спеченный керамический материал при пониженном давлении для того, чтобы очистить его перед обессоливанием. Полученный таким образом чистый раствор содержит около 95% NaCl сухой массы. Сухая масса составляет около 32 вес.% раствора. Объем чистого раствора равен приблизительно 7 л.
Чистый раствор разбавляют в 5-6 раз дистиллированной водой, и в разведенной форме подвергают обессоливанию, которое проводят, используя метод обратного осмоса и пользуясь прибором DDS. Обессоливание осуществляют в течение 3-4 часов, посредством чего избыток минеральных солей - в основном NaCl - отделяют в виде пермеата. Обессоленная композиция содержит примерно 65-70% хлорида натрия в твердом виде. Полученный таким образом раствор объемом 6-7 л концентрируют в 4-5 раз в роторном испарителе Bucchi до получения концентрированного раствора, содержащего примерно 20% сухих веществ. Полученный в результате концентрированный раствор очищают, используя центрифугу Biotuga-Herabus (сепаратор потоков), и затем стерилизуют фильтрацией через фильтр Millipore®.
Полученный микробиологически чистый раствор высушивают распылительной сушкой в сушилке Anhydro при температуре на выходе 90oC и температуре, устанавливаемой на входе, 180oC. Выход сухого порошка равен примерно 200 г.
Пример 2.
Продукт, полученный в примере 1, используют для приготовления фармацевтических композиций в виде геля и мази, содержащих также травяные экстракты, которые синергетически усиливают эффект лечения некоторых заболеваний. Например, гель и мазь от варикозной язвы ног получают следующим образом: 20 г экстракта каштана конского (hippocastanaceous), 10 г экстракта календулы, 60 г глицерина, 0,1 г ТТР в виде порошка, полученного как описано выше в примере 1, 0,1 г салициловой кислоты, 1,0 г дистиллированной воды и 8,8 г Aerosil® коллоидного кремнезема используют для получения препарата в виде геля.
Жидкие (нелетучие) ингредиенты стерилизуют перед использованием с помощью нагревания с обратным холодильником в течение двух часов. Травяные экстракты соединяют с глицерином и водным раствором ТТР, а также с ментолом, и к полученной смеси постепенно добавляют кремнезем при постоянном перемешивании.
Подобным образом, для получения композиции в форме мази используют следующие ингредиенты: 20 г экстракта каштана конского (hippocastanaceous), 10 г экстракта календулы, 0,1 г салициловой кислоты, 0,1 ТТР в виде порошка, полученного как описано выше в примере 1, и 2,0 г Aerosil® (коллоидного кремнезема).
В качестве жирных компонентов используют смесь следующих веществ: 22 г эуцерина (eucerine) и 45,8 г вазелина. Травяные экстракты стерилизуют при помощи нагревания с обратным холодильником в течение примерно 2 часов. Жидкие ингредиенты осторожно соединяют с кремнеземом для получения геля, который в свою очередь растирают со стерильными жидкими компонентами, охлажденными до комнатной температуры. Получают стабильную мазь, которая не разделяется при хранении.
Гель и мазь, полученные как указано выше, одновременно применяют для лечения варикозной язвы ног. Язвы обрабатывают гелевым препаратом, тогда как непораженную кожу вокруг них обрабатывают мазью. Полагают, что добавка коллоидного кремнезема способствует быстрому подсушиванию, в то время как травяные и выделенные из торфа ингредиенты являются ответственными за лечебный эффект препарата. Жирные компоненты помогают сохранять эластичность корки на ране (струпа) и кожи. Полученные результаты сравнивают с результатами, полученными на контрольной группе пациентов, которых лечат новым методом, выбирали из группы пациентов, страдающих заболеванием в течение многих месяцев (иногда лет) без заметного улучшения. Пациенты, подвергшиеся лечению композициями в соответствии с изобретением, показывают лучшие результаты уже в течение первых нескольких недель по сравнению с контрольной группой пациентов.
Пример 3.
Продукты, полученные в примере 1, используют для приготовления фармацевтических композиций в виде таблеток или гранул, которые помещают в капсулы.
Стерильную полученную из торфа биоактивную композицию в виде порошка соединяют с носителем в весовом соотношении 1:9. В качестве носителя используют MYVATEX® (торговое название продукта фирмы Истмен-Кодак), смесь лактозы и смазывающих веществ в весовом соотношении 44:1. Лактозу с размерами частиц 50 меш и MYVATEX®TL мелко измельчают таким образом, что примерно 70% от их веса проходит через сито 100 меш. Из части полученной смеси активной композиции и носителя образуют таблетки, содержащие 5 мг активных ингредиентов. Общая масса каждой таблетки составляет 50 мг. Другую часть этой смеси активной композиции и носителя гранулируют, используя d.s. этанола (40 об. %). Гранулы просеивают сквозь сито и, если это необходимо, размалывают, и затем помещают в капсулы в таком количестве, чтобы каждая капсула содержала 5 мг активных ингредиентов посредством использования ТТР в смеси с носителем в соотношении 1:19.
Таблетки, полученные как указано выше, испытывают с целью измерения времени их дезинтеграции в искусственном желудочном соке при температуре 37oC±2oC, используя оборудование ErweKa. Искусственный желудочный сок готовят следующим образом: 2,0 г хлорида натрия, 3,2 г пепсина растворяют в 7 мл соляной кислоты и доводят дистиллированной водой до общего объема 1000 мл. Значение pH полученного раствора составляет примерно 1,2. Время дезинтеграции таблетки, имеющей диаметр 5,1 мм и общую массу 0,0498 г, составляет 6 минут.
Следующие примеры относятся к многочисленным косметическим препаратам согласно настоящему изобретению, имеющим различные композиционные формы и созданным для различного применения, содержащим целебные добавки биоактивных ингредиентов, полученных из торфа. Среди других описаны такие препараты, как тонизирующие средства, бальзамы, кремы, молочко, шампуни, пеномоющие средства для ванн и др.
Пример 4.
В реакционный сосуд, оборудованный мешалкой, помещают 150 г экстракта ромашки, полученного экстракцией соцветия ромашки раствором этанол:вода 1:1, а также 1 г ТТР, как описано выше. К полученной смеси добавляют 50 г глицерина. Три вещества перемешивают для получения однородной смеси. Затем в этот же сосуд вливают вторую предварительно приготовленную смесь. Она включает 340 г раствора этанол:вода 95:5, 1 г салициловой кислоты и 0,5 г ментола. Две смеси перемешивают для образования однородного раствора. После этого добавляют 3 г ароматизирующей композиции TILIANA H4308. TILIANA H 4308 является продуктом Fabryka Syntetykow Zapachowych Pollena-Aroma (фабрика синтетических ароматизирующих веществ Pollena-Arema, Варшава, Польша). Раствор затем доводят до общего объема 1000 мл, добавляя 454,5 г дистиллированной воды, перемешивание продолжают до тех пор, пока не образуется гомогенная смесь. В вышеуказанной методике используют 86%-ный глицерин, ментол и воду в соответствии с требованиями польской Pharmacopea FPIV и этанол в концентрации 95% в соответствии с польскими промышленными стандартами BN-75/6193-01.
Использованный концентрированный торфяной экстракт является темно-коричневой жидкостью с плотностью 1,020-1,090 г/мл, и содержание сухих твердых веществ составляет не менее 5%, значение pH 1%-ного водного раствора равно 5,0-6,5. Экстракт ромашки является красно-коричневой жидкостью с плотностью 0,9160-0,9503 г/мл и содержанием этанола 52-56 об.%.
Тонизирующие препараты, полученные как описано выше, являются пригодными для всех типов кожи. Они представляют собой чистые (прозрачные) жидкости без каких-либо твердых веществ. Они имеют желтый цвет. Значение pH равно 4,28, и содержание этанола - 45,92 об.%. Общая кислотность, которую считают по содержанию салициловой кислоты, составляет не менее 0,1 вес.%, а именно 0,23 вес. % При хранении в течение 12 месяцев препарат не изменил ни одной из своих вышеуказанных характеристик.
Пример 5.
Повторяют процедуру, описанную выше в примере 4, с тем только отличием, что вместо экстракта ромашки и ароматизирующей композиции TILIANA H4308 используют экстракт цветков ноготков и композицию FINUS H4625 (также продукт Fabryka Syntetykow Zapachowych Pollena-Aroma) таким же образом и в таких же молярных и объемных соотношениях. Полученный тонизирующий препарат подходит для сухой и нежной кожи. Он также является чистой жидкостью без каких-либо твердых частиц. Значение pH составляет 4,30, общее содержание этанола 45,82 об. % и общая кислотность 0,27 об.%. При хранении в течение 12 месяцев препарат не изменяет своих свойств, так же как препарат, полученный согласно примеру 4.
Пример 6.
Повторяют процедуру из примера 4, за исключением того, что вместо экстракта ромашки выбирают экстракт листьев шалфея, а вместо TILIANA H4308 выбирают ароматизирующую композицию LELIA 90368 (Pollena-Aroma, Warsaw). Экстракт листьев шалфея получают экстракцией сухих листьев шалфея этанолом при 50oC, и он имеет коричневый цвет, характерный запах шалфея и плотность 0,9160-0,9503, он содержит 52-56% этанола. Полученный агент для ухода за кожей особенно подходит для жирной кожи. Он является чистой и гомогенной жидкостью, имеющей темно-желтый цвет; значение pH, содержание этанола и кислотность являются аналогичными значениям агента для ухода за кожей согласно примеру 4.
Пример 7.
Следующая композиция является особенно эффективным гелем для предотвращения или лечения пародонтоза, г:
Экстракт ромашки - 34,0
Экстракт листьев шалфея - 3,0
Салициловая кислота - 0,3
Ментол - 0,2
ТТР - 0,1
Общая масса промышленного геля в качестве основы - 100,0
Пример 8.
В реакционный сосуд объемом 2000 мл, оснащенный механической мешалкой, вносят тщательно взвешенные компоненты:
270 г экстракта ромашки, полученного экстракцией цветков ромашки 50%-ным этанолом; экстракт является красно-коричневой жидкостью, имеющей плотность 0,9160-0,9503 г/мл, и содержание этанола составляет примерно 55 об.%;
50 г глицерина, 86%, согласно требованиям Polish Pharmacopea FPIV;
30 г экстракта мыльнянки лекарственной, полученного экстракцией корней мыльнянки лекарственной 70%-ным этанолом, экстракт является красно-коричневой жидкостью, плотность составляет 0,9630-0,9810 г/мл, а содержание этанола - примерно 75 об.%;
1,0 г изобретенного концентрированного торфяного экстракта, который является темно-коричневой жидкостью с плотностью 1,02-1,09 г/мл, содержит не более 2% ионов хлорида, которые рассчитывают по хлориду натрия, содержание сухих твердых веществ составляет не менее 5%, значение pH 1%-ного водного раствора экстракта равно 6,0.
Названные выше ингредиенты тщательно смешивают. Туда же добавляют предварительно приготовленный раствор 1 г салициловой кислоты в 260 г 95%-ного этанола. К смешанному раствору добавляют 383 г дистиллированной воды и 5 г ароматизирующей композиции TILIANA H4308 и перемешивают до получения однородного раствора. Препарат подвергают анализу и хранят в бутылках для розничной торговли объемом 200 мл. Полученный препарат является пригодным для ухода за волосами. Он является прозрачной, слегка опалесцирующей жидкостью, содержащей примерно 45 об.% этанола; значение pH равно 4,5; общая кислотность, которую рассчитывают по салициловой кислоте, составляет не менее 0,1 вес.%. Препарат пригоден для светлых волос. Качество препарата на протяжении 12 месяцев хранения остается неизменным.
Пример 9.
Повторяют процедуру, описанную в примере 8, за исключением того, что вместо экстракта ромашки и композиции TILIANA H4308 используют в такой же последовательности и соотношении: травяной экстракт хвоща и ароматизирующую композицию PINUS Н4625. Травяной экстракт хвоща является зелено-коричневой жидкостью с плотностью 0,9160-0,9503 г/мл и содержанием этанола 55 об.%.
Полученный препарат пригоден для всех типов волос. Он является чистой и прозрачной жидкостью без каких-либо твердых частей желто-коричневого цвета, значение pH, содержание этанола, общая кислотность, а также стабильность после хранения в течение 12 месяцев остаются неизменными и имеют такие же величины, как у препарата, описанного в примере 6.
Пример 10.
Процедуру, описанную в примере 8, повторяют с аналогичными результатами. Единственным отличием является то, что вместо экстракта ромашки и композиции TILIANA H4308 используют экстракт листьев жгучей крапивы и ароматизирующую композицию LELTA 90368 (продукт этой же Fabryka Syntetykow Zapachowych Pollena-Aroma) в такой же последовательности и в том же соотношении. Используемый травяной экстракт имеет оливково-зеленый цвет, плотность 0,9160-0,9503 г/мл и содержание этанола примерно 55 об.%. Препарат подходит для всех типов волос.
Пример 11.
Обычно косметическое молочко является дисперсией жирных веществ, воздействующих как химически, так и механически на кожу. Фактически, благодаря удобному способу применения и лучшему взаимодействию жидкости и кожи целесообразно использовать жидкость, в частности эмульсионные кремы. Они легко проникают в глубокие слои кожи и таким образом предотвращают изменения кожи в связи с возрастом. Косметическое молочко в основном используют для очищения сухой и нежной кожи. Соответственно, оно не должно содержать агрессивных летучих масел, и в то же время оно часто содержит подходящие травяные экстракты, такие как экстракт ромашки или экстракт зародышей пшеницы. Добавление полученных из торфа биоактивных продуктов в такое косметическое молочко еще более усиливают его положительный эффект. В частности, состав нового средства является следующим, г:
ТТР - 0,05
Экстракт алоэ - 20,00
Глицерин - 3,00
Эуцерин - 2,00
Белое парафиновое масло - 1,00
Триэтиламин - 1,00
Aerosil(R)(коллоидный кремнезем) - 4,00
Пример 12.
Улучшенные результаты по восстановлению наблюдают при использовании ТТР и тщательно отобранных жирных носителей в составе классических питательных и восстанавливающих кремов. ТТР используют в количестве 0,01-1,00 вес.% в комбинации с травяным экстрактом (выбор зависит от типа кожи, для которой предназначается крем) в количестве по крайней мере 0,05-1,00 вес.%, антибактериальным препаратом в количестве 0,05-1,00 вес.%, синтетической ароматизирующей композицией в количестве 0,01-0,05 вес.% и жирным носителем в виде водной эмульсии, составляющей 97,00-99,50 вес.% всей композиции. Необходимо, чтобы жирная композиция была хорошим носителем для активных ингредиентов и чтобы она являлась приемлемой для кожи. Предпочтительно, она является эмульсией (все количества даны в вес.%) 35-45 эуцерина, 8-14 вазелина, 2,5-4 оливкового масла, 6-10 глицерина и 35-40 воды. Предпочтительными травяными экстрактами являются экстракт цветков ноготков, экстракт ромашки, экстракт тимьяна и т.п.
Предпочтительными рецептами являются следующие, вес.ч.:
1 рецепт
Эуцерин - 39,00
Вазелин - 11,50
Оливковое масло - 3,13
Глицерин - 7,80
Вода - 38,00
NIPAGINA (антибактериальный препарат) - 0,40
ТТР - 0,05
Экстракт ноготков - 0,10
Синтетическое ароматизирующее вещество - 0,02
Всего - 100,00
2 рецепт
Эуцерин - 42,00
Вазелин - 8,50
Оливковое масло - 3,08
Глицерин - 7,90
Вода - 38,00
NIPAGINA (антибактериальный препарат) - 0,40
ТТР - 0,05
Экстракт ромашки - 0,02
Синтетическое ароматизирующее вещество - 0,05
Всего - 100,00
Пример 13.
Препарат для применения после бритья содержит ТТР в качестве торфяного экстракта в количестве 0,01-1 вес.%, травяные экстракты в количестве 1-30 вес.%, глицерин в количестве 1-8 вес.%, салициловую кислоту и ментол в водно-спиртовом растворе. Предпочтительными травяными экстрактами являются: экстракты ромашки, ноготков, тимьяна, алоэ и аналогичные экстракты лекарственных растений. Добавка глицерина также является полезной в связи с его воздействием на эластичность кожи. Он ускоряет нанесение препарата на лицо, а также его проникновение в более глубокие слои кожи, усиливая таким образом целебный эффект активных торфяной композиции и травяных экстрактов. Предпочтительным рецептом является следующий, вес.ч.:
ТТР - 0,10
Экстракт ромашки - 15,00
Глицерин - 5,00
Ментол - 0,10
Салициловая кислота - 0,10
Этанол (конц. 95%) - 10,00
Ароматизирующая композиция - 0,30
Дистиллированная вода добавление до - 100,00
Пример 14.
Композицию шампуня готовят в соответствии со следующим рецептом, г (вес. %):
Травяной экстракт Фуллера - 15,0 (7,5)
Экстракт листьев жгучей крапивы - 20,0 (10,0)
GAMAL SBS-11 (детергент) - 30,0 (15,0)
GAMAL NO-3 (детергент) - 20,0 (10,0)
Aseptina (асептина) - 0,4 (0,2)
Этанол - 1,6 (0,8)
BRONOPOL (консервант) - 0,04 (0,02)
Хлорид натрия - 6,0 (3,0)
Вода - 106,96 (53,48)
Всего: - 200,0 (100,0)
К 92 весовым частям вышеуказанной композиции шампуня добавляют 8 весовых частей ТТР для получения 100 весовых частей шампуня согласно изобретению. Вместо экстракта листьев жгучей крапивы могут быть использованы другие травяные экстракты.
Пример 15.
Готовят следующую композицию шампуня, г:
Экстракт конского каштана - 13,00
Экстракт ноготков - 22,00
GAMAL SBS-11 - 30,00
GAMAL NO-3 - 20,00
Aseptina (асептина) - 0,40
Этанол - 1,60
BPONOPOL - 0,04
Хлорид натрия - 6,00
Вода - 106,96
Всего: - 200,00
Пример 16.
Зубная паста содержит ТТР в качестве концентрированного торфяного экстракта в количестве 0,01-0,10 вес. %, эфирные масла или их композиции или другие фруктовые эссенции в количестве 1-10 вес.%, глицерин в количестве 5-10 вес. %, травяные экстракты в количестве 0,10-10 вес.% и чистящие вещества в количестве 20-35 вес.%, красители и отбеливающие вещества в количестве 1-2 вес.%.
Двуокись титана может быть использована в качестве отбеливающего компонента; ТТР сам по себе может служить антибактериальной добавкой; экстракты листьев шалфея, ромашки или цветков ноготков используют в качестве полезных предпочтительных травяных экстрактов.
Предпочтительным рецептом является следующий, г:
Осажденный карбонат кальция - 150,00
Карбонат магния - 60,00
Глицерин - 70,00
Травяной экстракт - 5,00
ТТР - 0,50
Двуокись титана - 10,00
Эфирные масла (или мятная, лимонная и т.п. эссенция) - 5,00
Вода - 400,00
Краситель - Следовые количества
Пример 17.
Приготовление соли для ванн. В способе получения выделенного из торфа биоактивного продукта согласно настоящему изобретению, в частности при превращении жидкой формы в порошок, присутствует стадия обессоливания, на которой хлорид натрия отделяют как побочный продукт. В вышеупомянутом побочном продукте 95% составляет хлорид натрия; другими минеральными солями, которые отделяют, являются соли кальция, соли магния, в основном хлориды и сульфаты; эти солевые продукты также содержат некоторые органические полученные из торфа низкомолекулярные соединения, откклюдированные внутри кристаллической структуры этих неорганических солей. Эти органические соединения являются компонентами ТТР и являются - среди других - полисахаридами, аминокислотами, фульвокислотами (fulvic acids) и т.п. Наличие этих компонентов в солевых побочных продуктах является полезным при использовании соли в качестве соли для ванн, так как они могут давать дополнительный полезный эффект к стандартной активности соли для ванн. Этот побочный продукт тестируют соответствующим образом по его химическим и физическим свойствам в Бальнеологическом Институте в Познани, в Польше, для выяснения возможности использования его в косметических ваннах. Так как этими исследованиями не было обнаружено никаких нежелательных свойств этого продукта, то было разрешено использовать его для косметических целей.
Предпочтительным является следующий рецепт, г:
Соль (NaCl), содержащая окклюдированный ТТР - 97,00
Хвойное эфирное масло или композиция эфирных масел - 3,00
Пример 18.
Новый бальзам для волос содержит ТТР в количестве 0,01-1 вес.%, травяной экстракт в количестве 0,01-10 вес.%, антиэлектростатические компоненты в количестве 3-4 вес.%, компоненты, предотвращающие чрезмерное высушивание волос и кожи в количестве до 2 вес.%, глицерин в количестве 1-5 вес.%, консервант и стибилизаторы в количестве 0,05-0,50 вес.% и воду - до общих 100 вес.%.
В качестве антиэлектростатического компонента данный бальзам содержит спиртовой раствор триметиламина и соль хлорид аммония, полученную из жирных аминов животного происхождения; в качестве загустителя, играющего роль также и стабилизирующего агента, - косметический спирт; в качестве агента, предотвращающего чрезмерное высушивание волос и кожи - растительные масла, которые одновременно являются коэмульгирующим агентом; и глицерин - для облегчения нанесения и впитывания бальзама, особенно его активных ингредиентов, т.е. ТТР и травяных экстрактов. Так как кислая среда препятствует размножению бактерий, то бальзам в соответствии с изобретением содержит лимонную или фумаровую кислоту в количестве 0,1%, а также консервант, известный под названием BRONOPOL и ароматизирующую композицию.
Предпочтительным является следующий рецепт, вес.%:
Спиртовой раствор триметиламина и солей хлорида аммония - 3-4
Косметические спирты - 3-4
ТТР - 0,01-10
Сгущенные травяные экстракты - 0,01-10
Глицерин - 1,5
Растительные масла - До 2
Лимонная или фумаровая кислота - 0,1
BRONOPOL - 0,1
Ароматизирующая композиция - 0,3
Дистиллированная вода - До 100
Пример 19.
Косметические маски являются известными косметическими препаратами, служащими для многих целей. В связи с тем, что лечебные грязи оказывают благотворное воздействие на кожу и тело, то также возможно и применение оставшегося после экстракции торфа, который получают с помощью способа сепарирования биоактивных выделенных из торфа композиций, для косметических целей. Оставшийся после экстракции торф содержит раствор активных тел, которые высвобождаются в процессе щелочного гидролиза, благодаря необычайно высокой сорбционной способности торфа после нейтрализации. Поэтому его можно использовать в качестве полезного компонента косметических масок. С целью обогащения оставшегося после экстракции торфа большим количеством ценных компонентов добавляют природные лечебные грязи и фракции гумминовой кислоты, которые присутствуют в природном торфе, и их отделяют в процессе получения выделенных из торфа биоактивных композиций из щелочного гидролизата. Эта композиции проверяют в вышеуказанном Бальнеологическом Институте и находят ее пригодной для косметического использования.
Предпочтительным является следующий состав, г:
Полученный после экстракции торф - 100,00
Природная лечебная грязь или торф - 20,00
Фракция гуминовой кислоты - 10,00
Карбонат магния - 10,00
Окись цинка - 5,00
Лимонная кислота или подобная ей - 0,1
Травяной экстракт или растительный материал в виде порошка - 5,0
Дистиллированная вода -
Следующие положения и объяснения относятся к биологическому аспекту продуктов настоящего изобретения, т. е. к их биоактивным характеристикам и к совместимости этих продуктов, в частности, с точки зрения их использования в качестве фармацевтических препаратов. Далее будут использоваться следующие сокращения:
TTp ToLPA® - торфяной препарат (торговая марка Торф Корпорейшн, Вроцлав, улица Mydlana 2, Польша).
IFN - интерферон, существует в виде повсеместного цитокина (гормон ткани). Гены IFN присутствуют во всех клетках. IFN в основном индуцируется протеинами или гликопротеинами. Вещества, стимулирующие гены IFN к продуцированию IFN, называются индукторами. Процесс индуцирования IFN является регулируемым с высокой точностью сложным биохимическим процессом; обнаружены негативные и позитивные регуляторные гены, контролирующие продукцию IFN. Небольшие количества IFN могут продуцироваться спонтанно, без какого-либо обнаруживаемого индуктора. Такие IFN иногда называют "физиологическими IFN".
IFN существует в природе в трех молекулярных формах:
IFN-α (или лейкоцитный),
IFN-β (фибропластовый) и
IFN-γ (иммунный).
IFN-α и IFN-β относятся к типу I-IFN, а IFN-α - к типу II-IFN. Основными биологическими действиями IFN являются антивирусная, антипролиферационная (противораковая) и иммуномодулирующая активность. В продаже имеются различные формы IFN в виде естественных и рекомбинатных препаратов, и их используют в качестве лекарства для лечения опухолевых, вирусных и некоторых других заболеваний.
CTL = цитолитический Т-лимфоцит.
NK-клетки = естественные клетки-киллеры.
IL-1, IL-2 - хорошо известные интерлейкины, стимулирующие пролиферацию Т-клеток и других лимфоидных клеток, включая В-клетки.
RPMI 1640 - культура ткани (среда) для выращивания лейкоцитов человека и др. (аббревиатура Roswell Park Memorial Institute, Buffalo).
PCS = фетальная телячья сыворотка (для анализа с лейкоцитами ее необходимо предварительно проверить, так как она может содержать митогенные вещества, имитирующие действие интерлейкинов).
EMCY = вирус энцефаломиокардита, вирус мыши (Mouse picorna virus), непатогенный для человека, его часто используют в качестве вируса при контрольном заражении в биологических анализах.
А-549 = клеточная линия аденокарциномы человека - используют в биологических анализах IFN из-за ее высокой чувствительности к IFN α β и γ. Линия рекомендуется для такого использования экспертами WHO (Всемирная организация здравоохранения, Женева), по IFN-стандартизации.
MTT = бромид 3-[4,5-диметилтиазол-2-ил]-2,5-дифенил-тетразолия. Реагент используют для измерения лизиса клеток или роста клеток в некоторых биологических анализах, при помощи сканирующего устройства ELISA (Hansen и др., Immunol, Meth, 1980, 119, 203-210).
L 929 = клеточная линия мыши, используемая обычно для анализа мышиного IFN и TNF человека или мыши.
TNF = фактор некроза опухолей, цитокин (относительно небольшой белок, очень чувствительный к протеолитическим ферментам), продуцируемый моноцитами и макрофагами (TNF-α также известен как фактор некроза опухолей кахектин, вызывающий кахексию (истощение) у людей и животных), продуцируется после стимуляции LPS (липополисахаридами) вирусами, бактериями и многими другими агентами, очень токсичен для многих зараженных вирусами клеток и клеток новообразований; также может играть роль фактора роста для фибропластов. Связан с воспалительными реакциями. Родственная форма TNF-β (лимфотоксин) продуцируется Т-клетками и некоторыми другими клетками.
PBL = лейкоциты периферической крови, выделенной из светлого слоя кровяного сгустка (мед. - лейкоцитарная пленка) (промежуточная фаза между красными (кровяными) клетками и плазмой). Реактивность PBL отдельных доноров на различные цитокиновые индукторы производит впечатление зависимой от генетической системы доноров. Были идентифицированы высокоотвечающие респондеры и низкоотвечающие респондеры. Это также относится к чувствительности PBL на TTP.
Вариации отдельных ответов на индукторы IFN или TNF являются более очевидными при использовании слабых индукторов, а не очень сильных индукторов, таких как вирусы. Это происходит благодаря тому, что реакции на слабые индукторы является типом "все или ничего", тогда как вирусы почти всегда индуцируют определяемые количества цитокинов.
Толерантность к индуктору - называется также гипореактивным состоянием. Происходит после введения одной дозы индуктора, например, после 20 часов воздействия PBL на индуктор (например, вирус); клетки прекращают дальнейшее продуцирование IFN. Гипореактивное состояние длится обычно около 7 дней. Оно может быть полное или частичное. Такая реактивность затрудняет терапевтическое применение сильных индукторов и/или делает его неэффективным. Слабые IFN-индукторы либо не индуцируют гипореактивное состояние, либо толерантность является незначительной.
Некоторые натуральные лекарства, выделенные из лекарственных растений, обладают иммуномодулирующими свойствами. ТТР производит впечатление одного из них. ТТР изменяет многие различные иммунные функции in vitro и in vivo. Он инициирует сбалансированную иммуностимуляцию посредством способности неспецифической активации всех эффекторных путей (CD4-хелпера, слабо CD8-супрессора, CTL, NK-клетки и активированного макрофага) без цитотоксичности для нормальных тканей.
ТТР оказывает тонизирующее воздействие на заживление обычных ран. Низкие дозы ТТР слабо стимулируют продуцирование IL-1 и IL-2. Высокие дозы могут ингибировать синтез цитокина.
С ТТР проводят соответствующие опыты посредством следующих методов:
PBL из крови здоровых доноров очищают с помощью обработки хлоридом аммония. Культуральной средой является RPMI 1640 плюс 10% FCS. Культивируют примерно 8•106 клеток/мл в течение 20 часов при 37oC, 5% CO2. Антивирусную активность интерферона анализируют по цитопатическому эффекту ингибирования EMCY в клетках A549 человека. Также используют метод МТТ для измерения лизиса клеток.
Активность TNF измеряют в клетках L 929. Для определения типа IFN отдельные образцы IFN обрабатывают различными сыворотками анти-IFN в течение 1 часа. Их антивирусную активность сравнивают с необработанными препаратами.
Опыты показывают, что ТТР стимулирует продуцирование эндогенных интерферонов (IFN) и фактор некроза опухолей (TNF). Ответ является соответствующим дозе.
Семь исследуемых производственных упаковок (партий) ТТР имеют сопоставимую биологическую активность как иммуностимулирующие и цитокиновые индукторы. Наблюдают значительные отклонения в ответе на ТТР лейкоцитов каждого донора крови. нескольких доноров оказалось иммунологически толерантными. Это может являться отражением генетического фона.
Используют сильнодействующие поликлональные антисыворотки, такие как анти-IFN-α (Cantell), анти-IFN-α Ly (Hamaiwa) от K. Fantes и анти-IFN-γ (Cantell) для нейтрализации антивирусной активности в супернатантах PBL, обработанных в течение 20 часов ТТР.
Результаты анализов нейтрализации оказываются сходными с отпечатками пальцев каждого отдельного донора крови. Другими словами, пропорции типов IFN, индуцируемых каждым индивидуумом, значительно отличаются. Разделение PBL на вязкие (adherent) и невязкие (non-adherent) фракции может усилить индуцированный цитокиновый синтез.
Гипореактивность (толерантность) к индуцированию IFN посредством NDY, наблюдается в течение 20 часов после начального стимулирования PBL с помощью ТТР, является либо минимальной, либо отсутствует.
Все семь упаковок партий ТТР, испытываемой в PBL человека в качестве IFN и TNF индукторов, оказались активными в отношении индукции IFN и/или TNF. Оптимальной концентрацией ТТР для индукции IFN является 30-100 μг/мл и для индукции TNF - 100-200 μг/мл. Доза 200 μг/мл может быть субтоксической для pBL, однако синтез TNF происходит гораздо быстрее, чем синтез IFN, и быстрее, чем рост небольшой цитотоксичности.
Из вышеизложенного можно сделать вывод о том, что активным началом фармацевтических препаратов на основе ТТР является иммуноактивная фракция экстракта торфа, содержащая органику главным образом связанные сахара, аминокислоты, уроновые кислоты, вещества гуминовой кислоты, и минеральные соли, включая микроэлементы. ЛД50 для животных составляет > 2400 мг/кг per OS.
Не было обнаружено ни мутагенной, ни генотоксической, ни эмбриотоксической, ни тератогенной или канцерогенной активности ТТР. ТТР не показывает никаких аллергенных свойств, а также не имеет никаких вызывающих местное раздражение свойств.
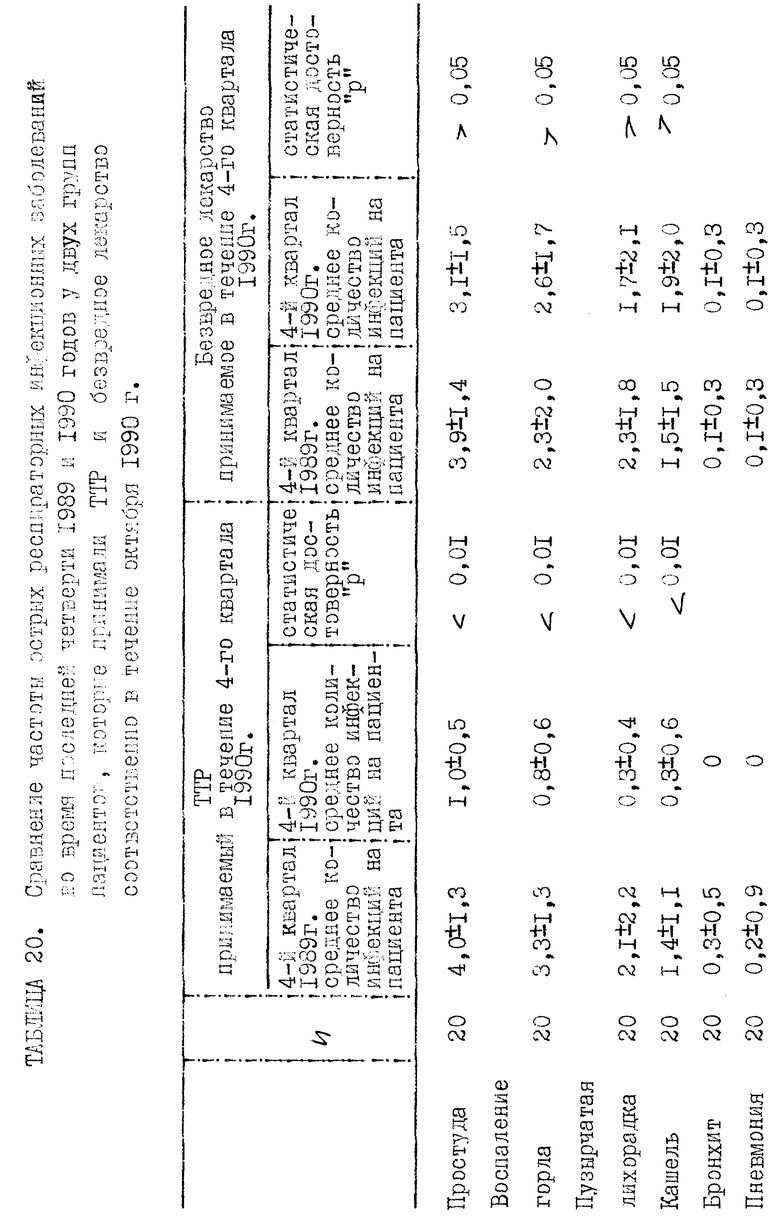
Терапевтические показания включают хронические и рецидивные воспаления респираторного тракта и варикозные язвы нижней части ног, добавочное лечение влагалищных эрозий и пародонтозные заболевания.
Из клинических наблюдений следует, что ТТР может быть использован в качестве иммуномодулятора в поддерживающей терапии некоторых опухолевых заболеваний. ТТР принимают внутрь (таблетки 5 мг) или локально.
Особенно уместным и важным является тот факт, что PBL, обработанный ТТР в течение 20 часов при 37oC, не дает гипореактивного состояния, так как они сохраняют способность продуцировать IFN после индукции посредством NDV (Newcastle Desease Virus - Ньюкаслский болезнетворный вирус), очень сильного индуктора IFN.
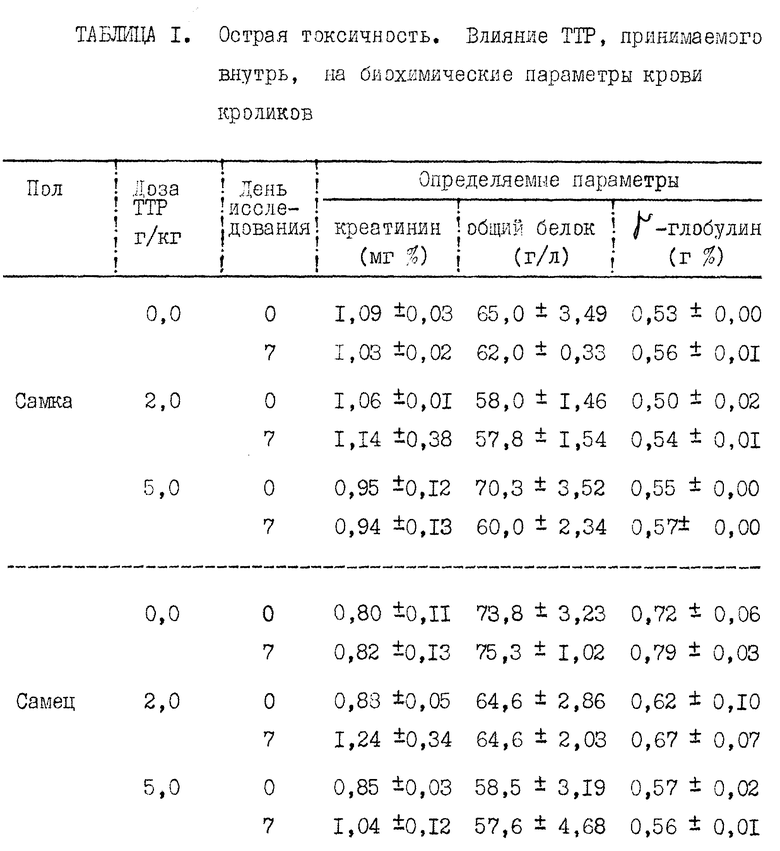
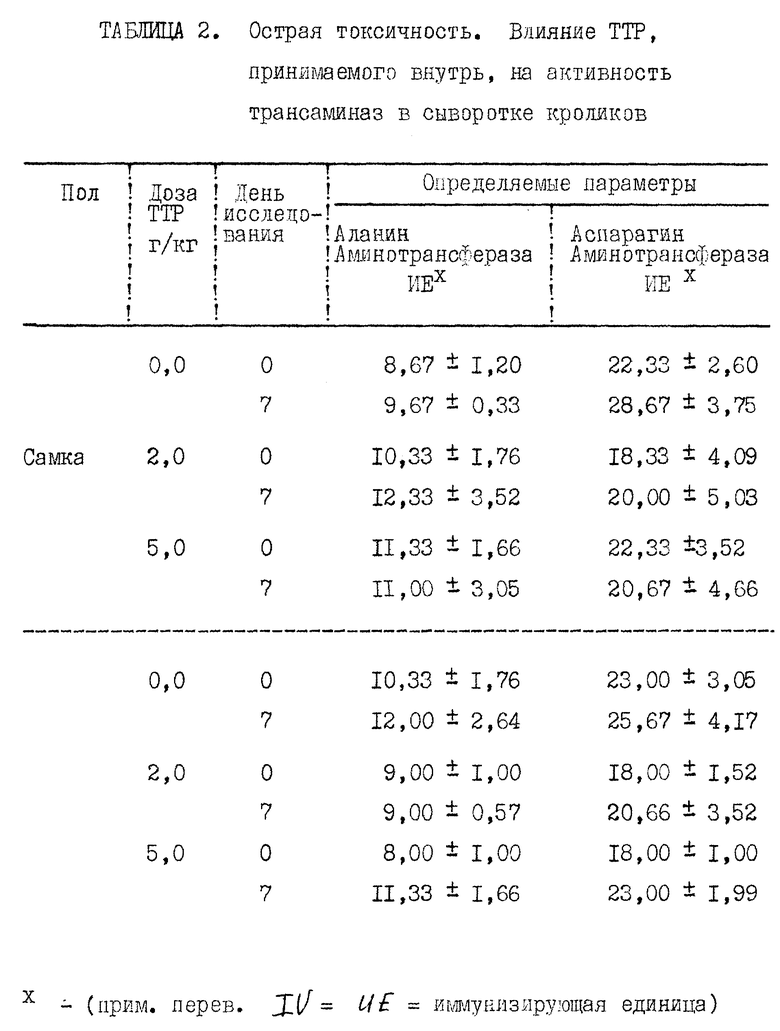
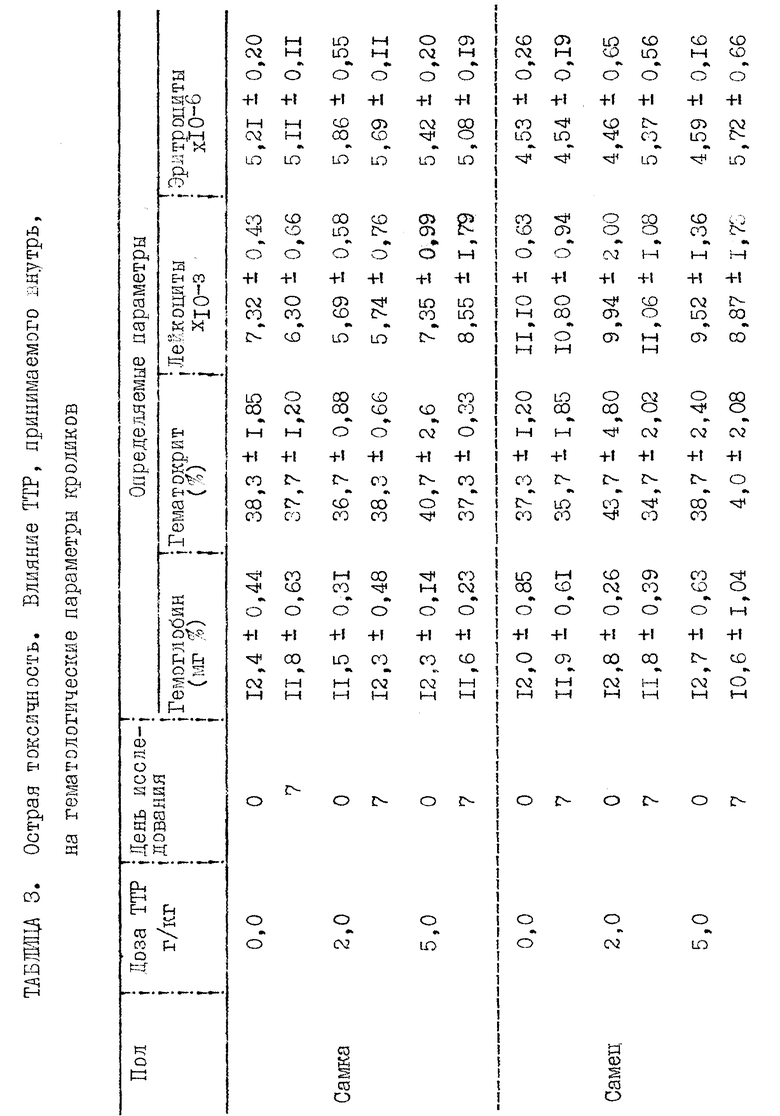
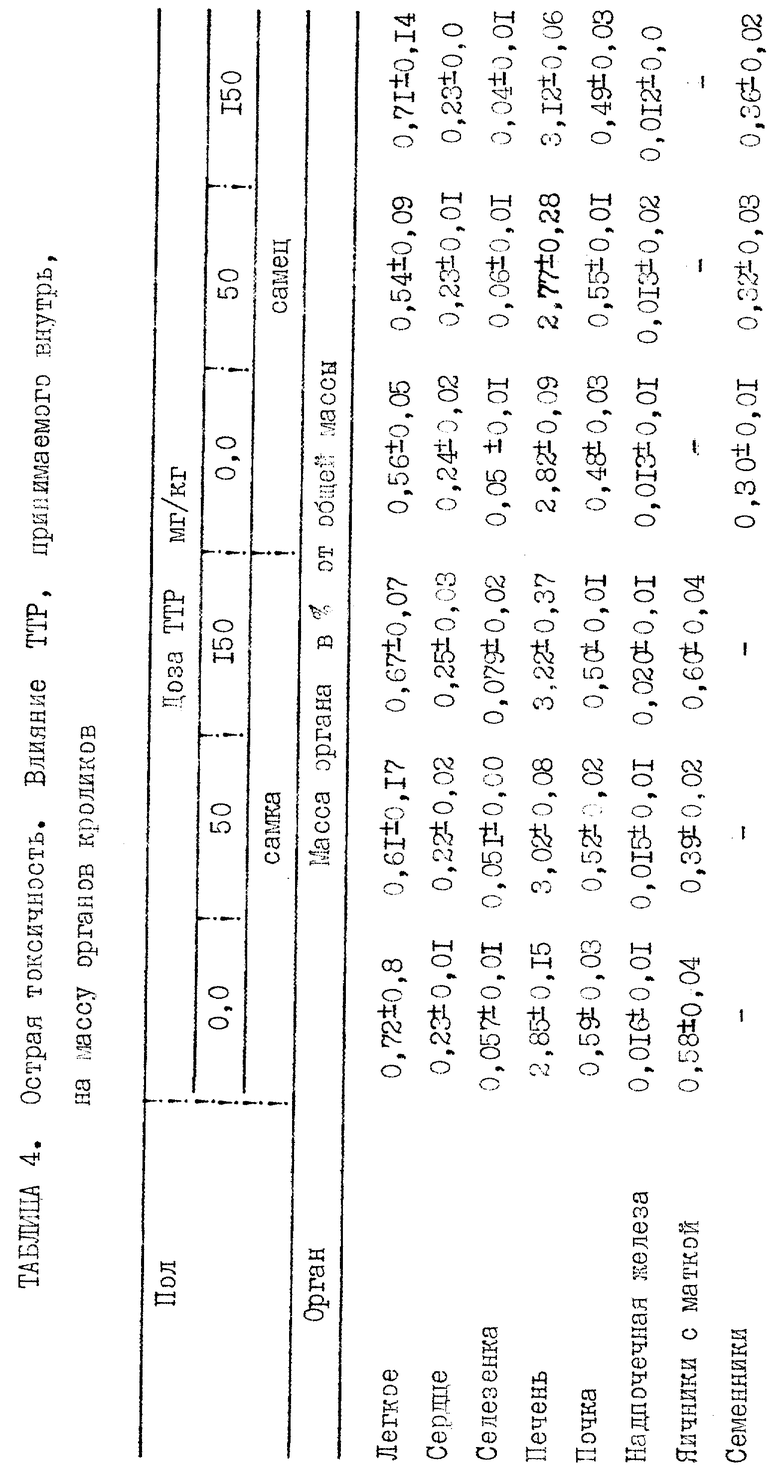
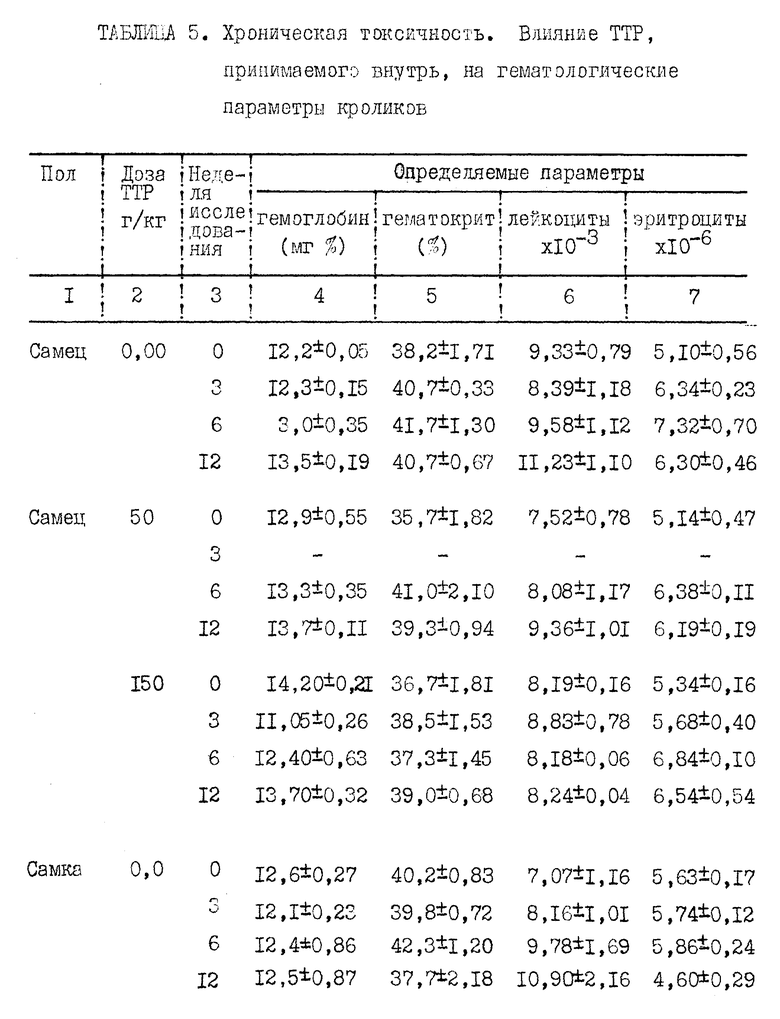
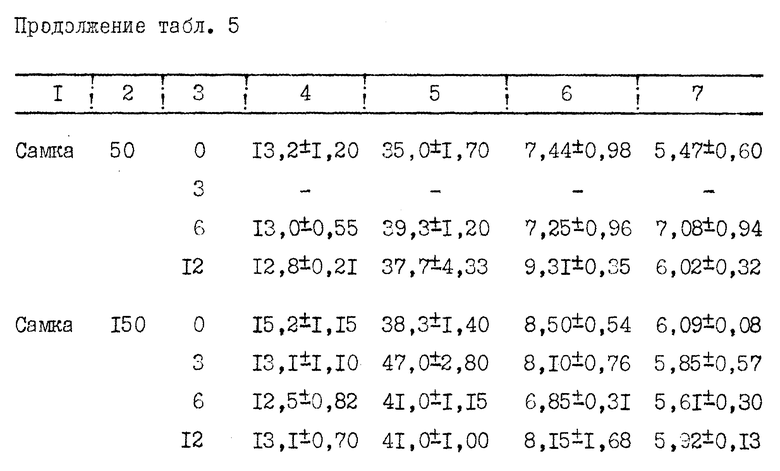
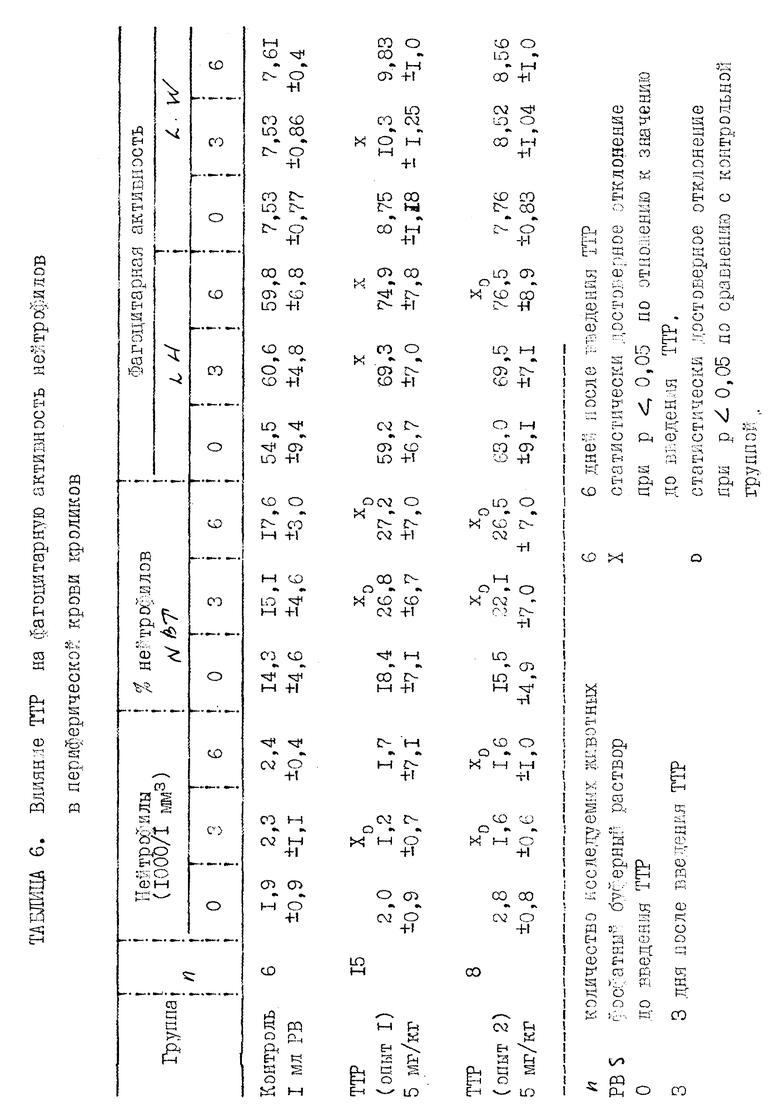
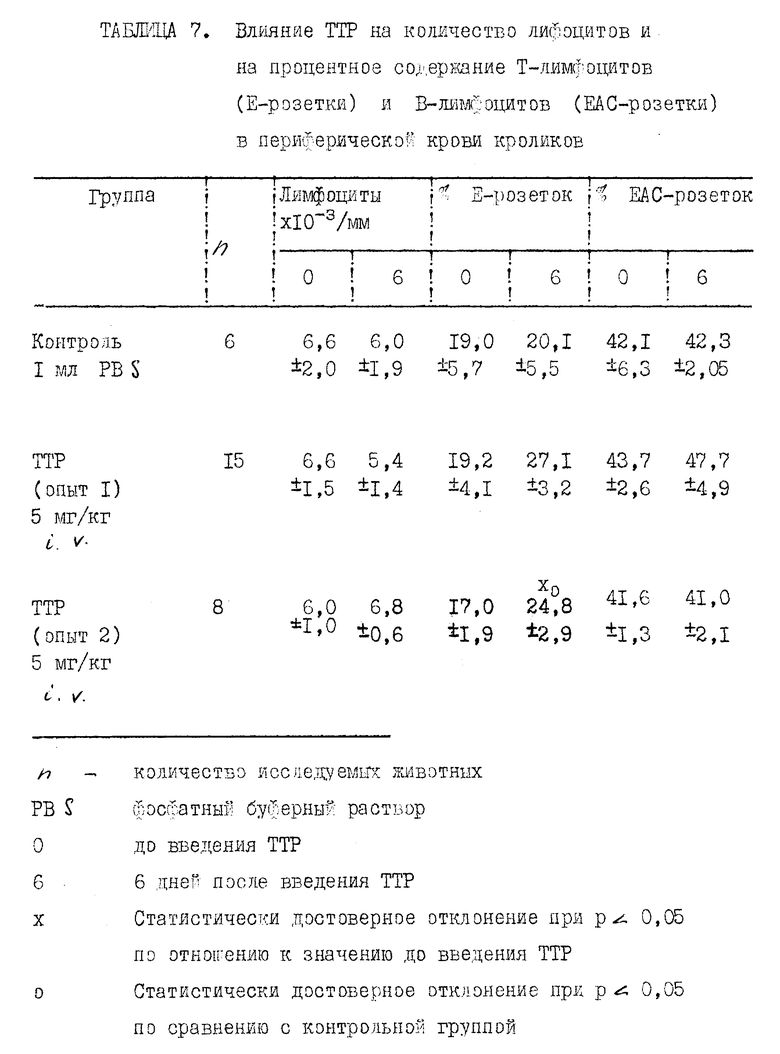
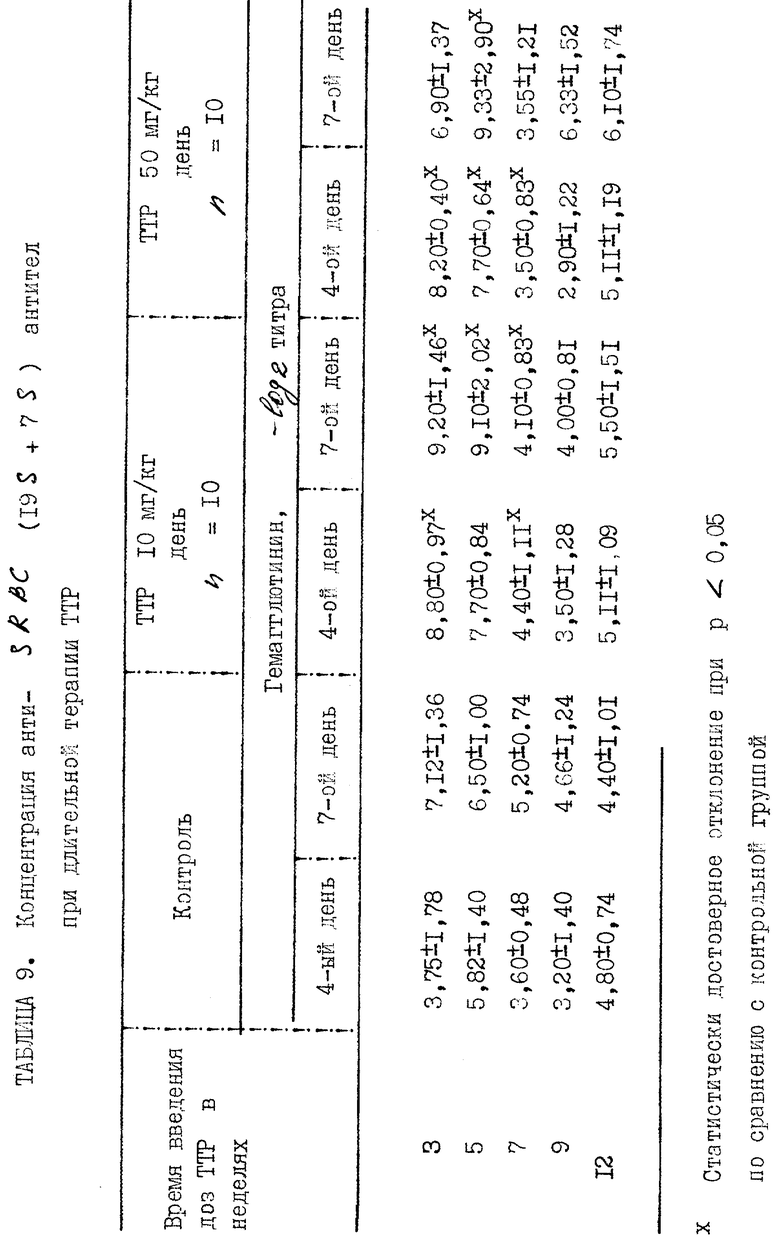
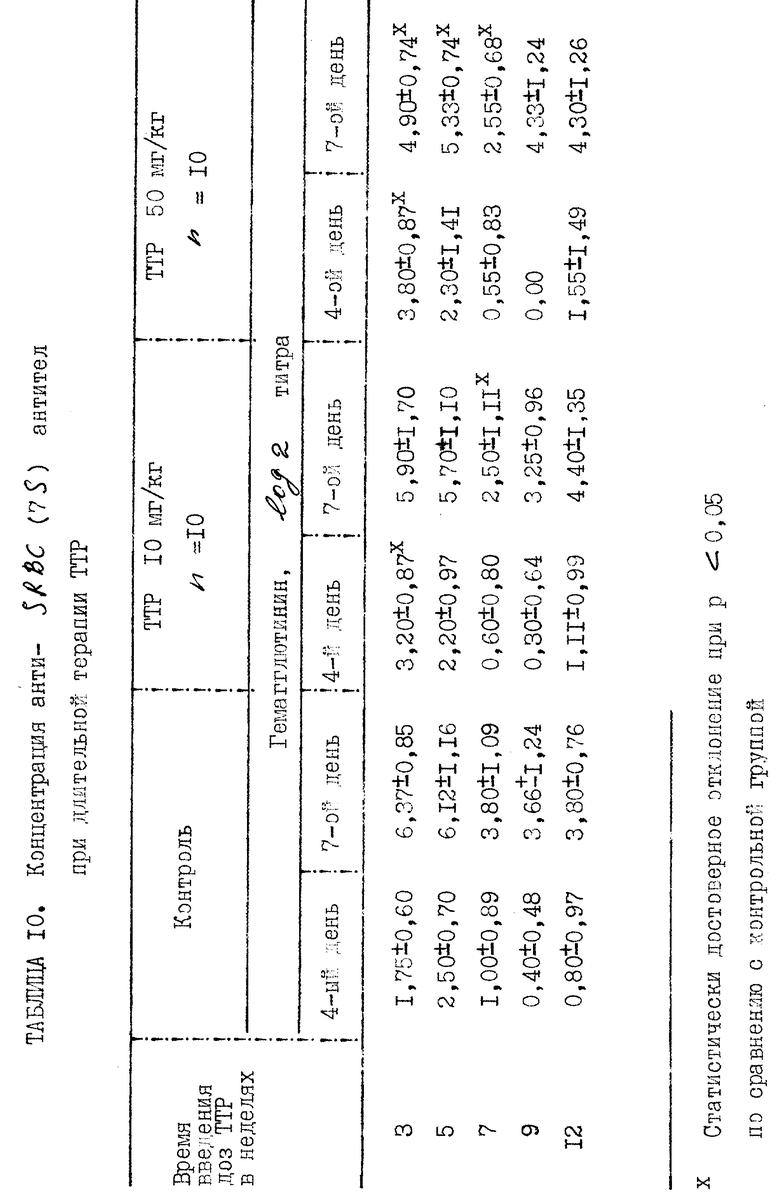
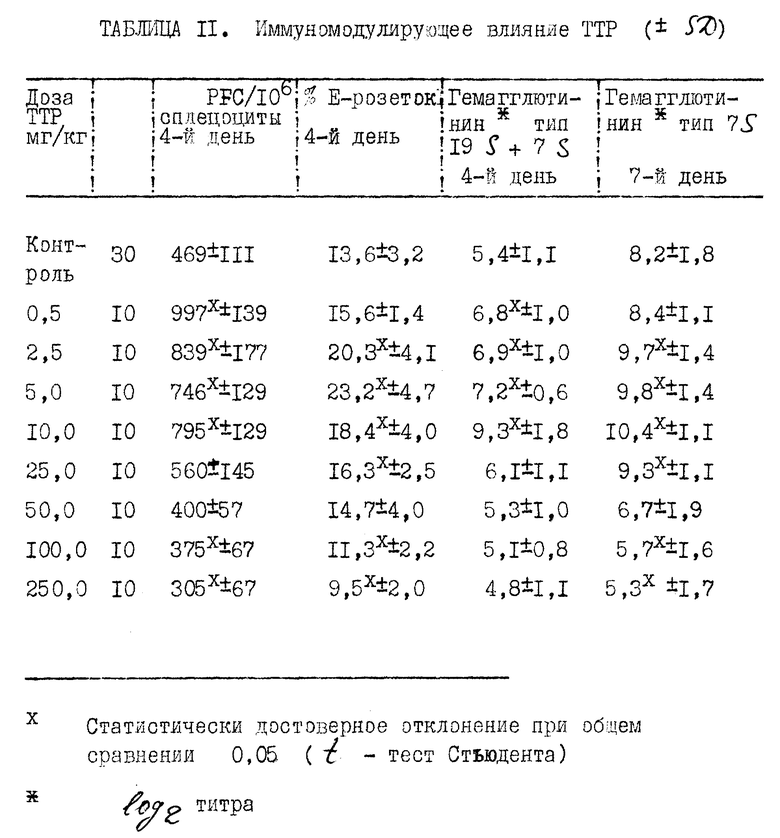
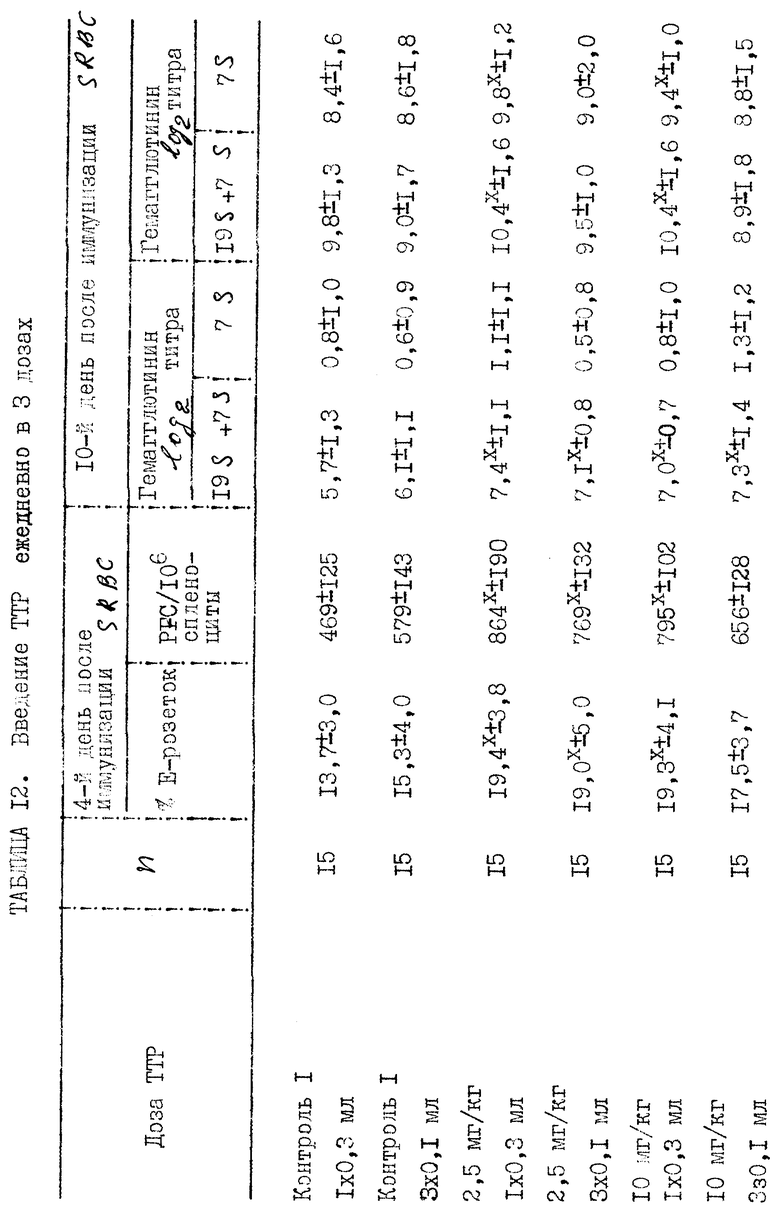
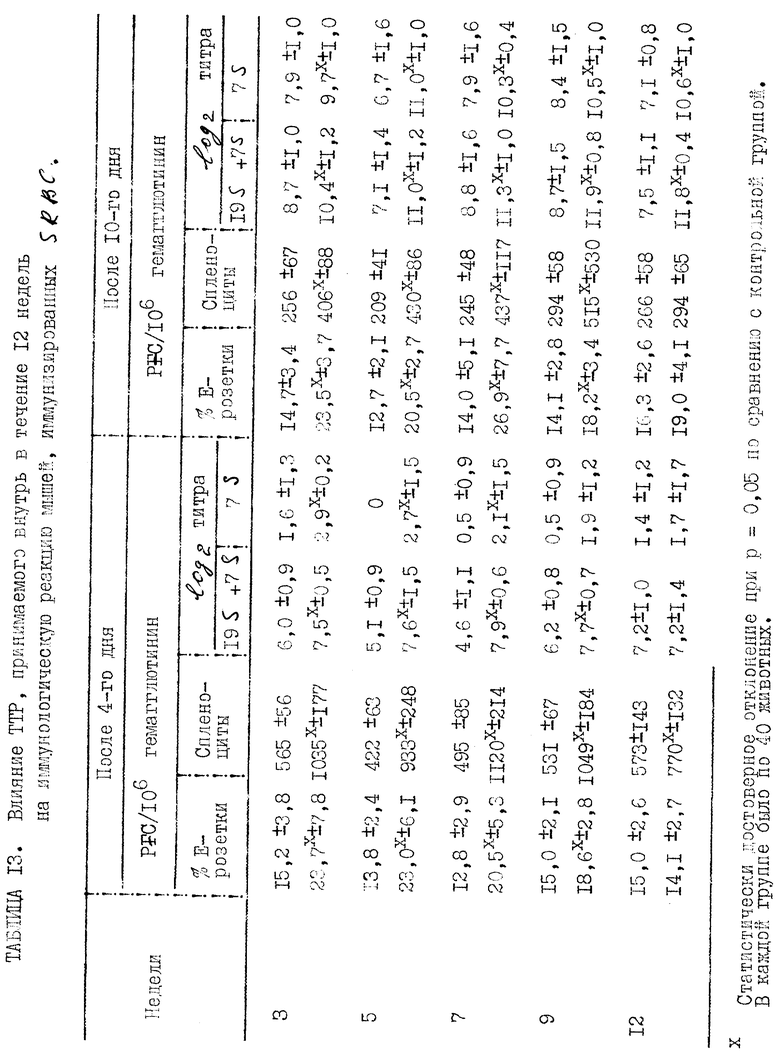
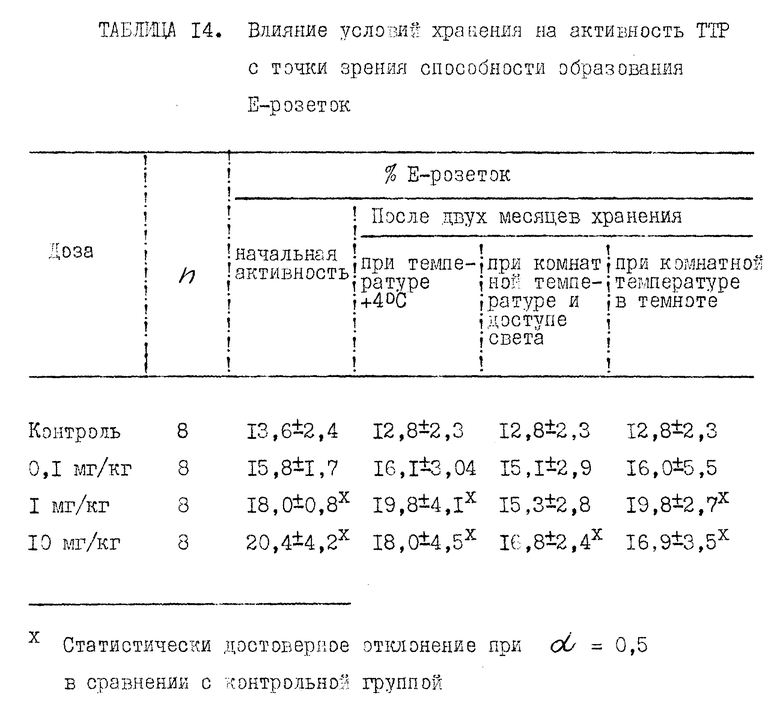
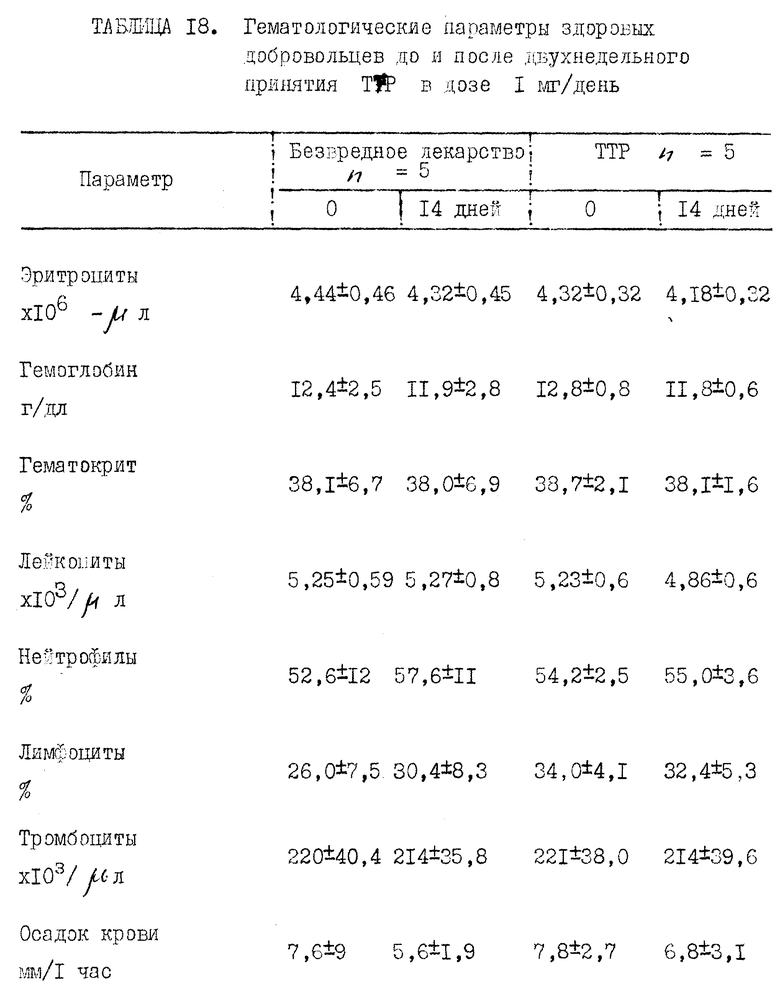
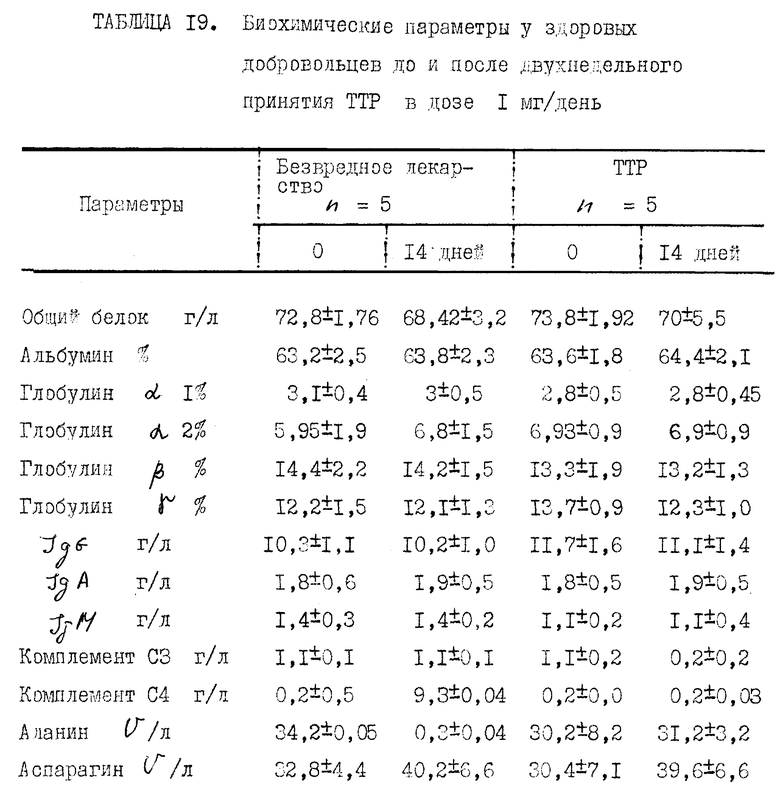
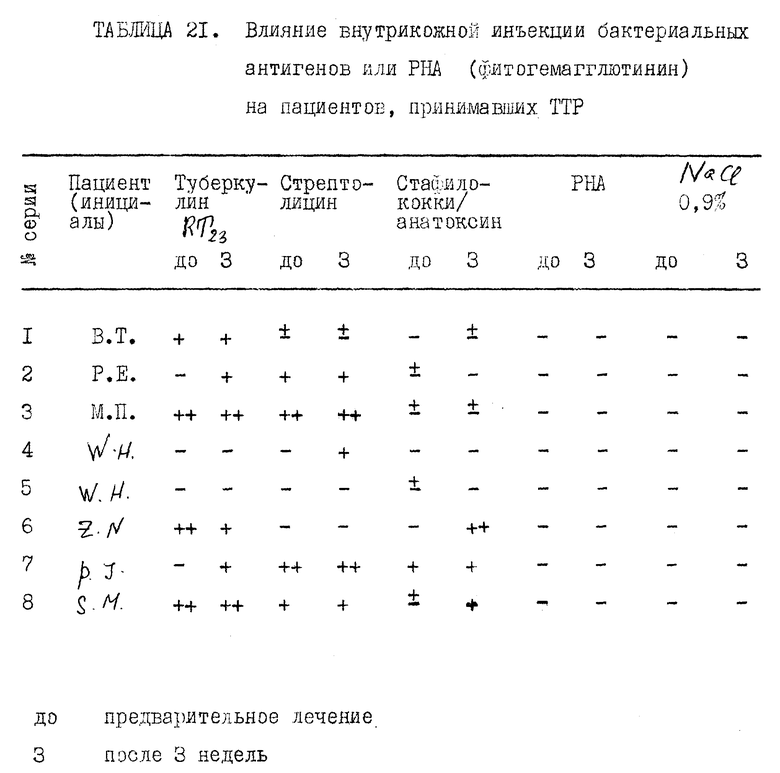
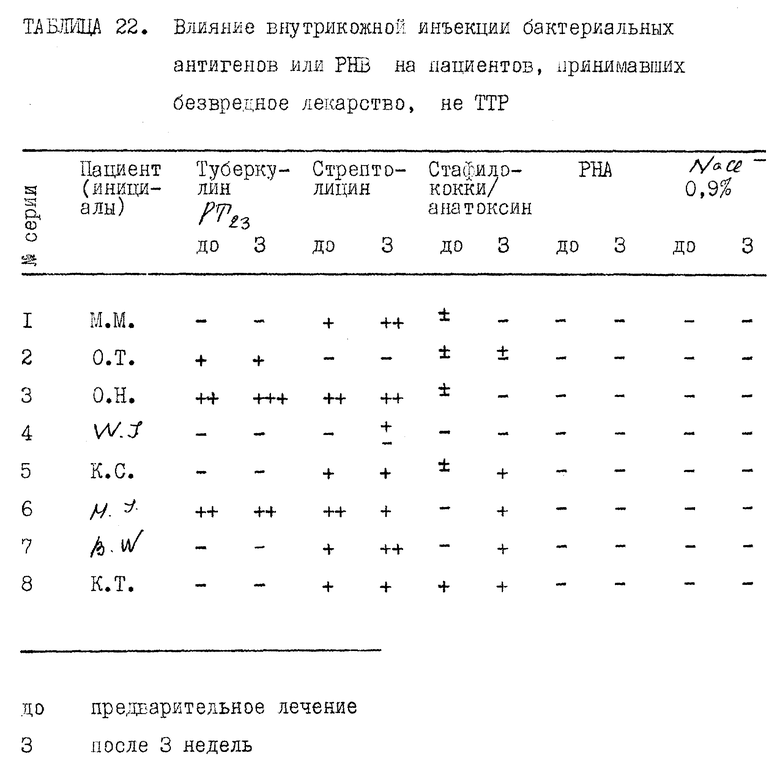
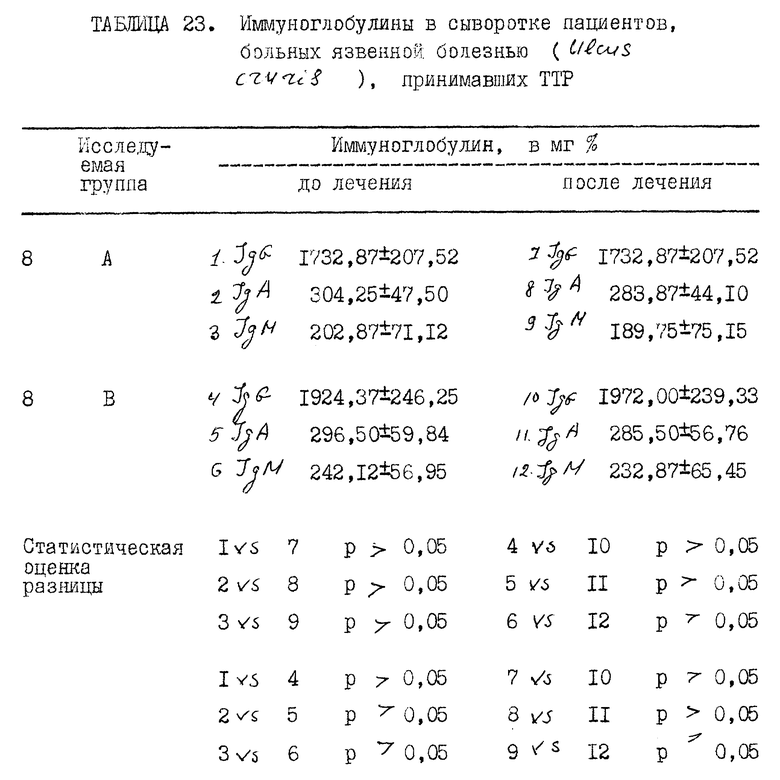
Прилагаемые таблицы 1-23 относятся к различным биологическим, например токсикологическим, гематологическим и иммунологическим опытам. Эти таблицы являются вполне ясными и могут служить для биолога источником информации, относящейся к совместимости и биологической активности ТТР.
Необходимо отметить, что концентрация активных ингредиентов в фармацевтических препаратах, как указано в пункте 13 формулы изобретения, может быть выше, чем в косметических композициях (как указано в пункте 14) в связи со следующими причинами.
Фармацевтические препараты готовят в единичных дозировках, где содержание активных ингредиентов находится под строгим контролем, например, в таблетках, где концентрацию подбирают соответственно размеру таблетки, содержащей эффективную дневную дозу (или ее часть) активного ингредиента.
Концентрация активного ингредиента, например, ТТР, в гранулах, которыми заполнены капсулы, предпочтительно составляет только 5 вес.% для того, чтобы получить достаточный размер таблетки и для удобства соответствующих операций на аппарате, который делает капсулы.
Другой причиной является то, что большинство фармацевтических препаратов принимают вовнутрь, и активный ингредиент распространяется по всему телу. Хотя он достигает клеток кожи в очень низких концентрациях, терапевтический эффект является значительным.
Кроме того, косметические композиции - в противоположность фармацевтическим препаратам - используют в неконтролируемых концентрациях, применяют локально, с различной степенью проникновения к различным клеткам.
Некоторые композиции, такие как шампунь, которые почти немедленно смывают, находятся в контакте с телом или волосами в течение короткого периода времени и могут содержать соответственно больше целебного компонента; другие применяют несколько раз в день и поэтому должны иметь более низкое содержание активного ингредиента.
Наконец, как в случае с зубной пастой, которая находится в контакте со слизистой оболочкой рта, где проникновение активных ингредиентов значительно облегчается, чем при контакте с кожей, концентрация активных ингредиентов может быть ниже.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ НА ОСНОВЕ РЕАКЦИИ АМАДОРИ, ИХ ПРИМЕНЕНИЕ, СПОСОБ ПОЛУЧЕНИЯ И СОСТАВЫ НА ИХ ОСНОВЕ | 1993 |
|
RU2141337C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИММУНОГЕННОЙ АКТИВНОСТИ БИОАКТИВНЫХ СОЕДИНЕНИЙ И СОСТАВ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2125727C1 |
| УСТРОЙСТВО ДЛЯ ЭКСТРАГИРОВАНИЯ ТОРФА | 1994 |
|
RU2123025C1 |
| СПОСОБ ЭКСТРАГИРОВАНИЯ ТОРФА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2085572C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ КОМПОЗИЦИЯ ФИТАОН-2,2 И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2106874C1 |
| КОМПОЗИЦИИ | 2015 |
|
RU2707282C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО, КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭТО СРЕДСТВО, СПОСОБ ЛЕЧЕНИЯ КОЖНЫХ И СИСТЕМНЫХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 1997 |
|
RU2151589C1 |
| КОМПОЗИЦИИ ДЛЯ КОСМЕТИЧЕСКИХ ПРЕПАРАТОВ, СРЕДСТВ ЛИЧНОЙ ГИГИЕНЫ, КОМПОНЕНТОВ ОЧИЩАЮЩЕГО ДЕЙСТВИЯ, ПИЩЕВЫХ ДОБАВОК, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2001 |
|
RU2251405C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ АТОПИЧЕСКОГО ДЕРМАТИТА, СОДЕРЖАЩАЯ МОНОАЦЕТИЛДИАЦИЛГЛИЦЕРИНОВОЕ СОЕДИНЕНИЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2014 |
|
RU2640503C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЛУКОВЫЙ ЭКСТРАКТ И ЛИПОСОМЫ | 2012 |
|
RU2665946C2 |




Изобретение касается биоактивных продуктов из торфа, содержащих не более 70 вес.%, предпочтительно не более 60 вес.% неорганических солей, особенно хлорида натрия, от веса сухого вещества. Эти продукты получают способом, по которому высококонцентрированный водный раствор неорганических солей, особенно хлорида натрия, содержащий биоактивные ингредиенты торфа, разбавляют деминерализованной водой и подвергают обратному осмосу для обессоливания раствора, при этом неорганические соли удаляются, а полученный раствор концентрируют и осветляют, и, возможно, по меньшей мере на одной дальнейшей стадии раствор стерилизуют и/или сушат распылением. Фармацевтический состав, содержащий биоактивный продукт из торфа в виде геля, приготавливают посредством объединения стерильного спиртового растительного экстракта со стерильным глицерином, стерильным водным раствором предварительно порошкового биоактивного продукта из торфа и стерильного ментолового раствора. Полученную смесь постепенно соединяют с коллоидным кремниевым ангидридом для превращения жидкой композиции в гель, при этом весовое соотношение жидкой смеси к кремниевому ангидриду предпочтительно составляет от 90:10 до 94:6. Косметический препарат, такой как гель, мазь, бальзам, шампунь, солевой состав для ванн и т.д., содержит активный ингредиент в виде растворимого биоактивного торфяного продукта в количестве 0,01 - 10 вес.%, предпочтительно 0,05 - 1 вес.%, еще более предпочтительно 0,05-0,10 вес.%. Технический результат предложения заключается в разработке продукта, который является стабильным и может быть легко введен в фармацевтические и ветеринарные препараты. 5 с. и 18 з.п.ф-лы, 23 табл.
Приоритет по пунктам:
15.07.91 по пп.1 - 23;
16.03.91 по пп.11, 14 и 20 - 22;
17.05.91 по пп.11, 14 и 20 - 22;
03.06.91 по пп.11, 14 и 20 - 22;
10.06.91 по пп.20 - 22;
17.06.91 по пп.20 - 22.
| Способ полимеризации альфа-олефинов | 1959 |
|
SU124110A3 |
| Способ извлечения эстрогенов | 1991 |
|
SU1826908A3 |
| Труды института курортологии.-М., 1962, с.53-55 | |||
| Муравьев И.А | |||
| Технология лекарств.-М.: Медицина, 1971, с.275 | |||
| Машковский М.Д., Лекарственные средства.-М.: Медицина, 1989, ч.II, с.33, 76. | |||
Авторы
Даты
1999-02-27—Публикация
1992-03-04—Подача