Настоящее изобретение касается новых алкильных производных тразодона, обладающих фармакологической активностью, фармацевтических составов, содержащих их, способа их получения и промежуточных соединений, пригодных для их получения.
Тразодон формулы (T) является препаратом, известным около двадцати лет и широко использующимся в качестве антидепрессанта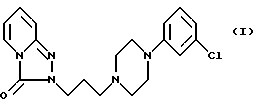
С другой стороны некоторые авторы также сообщают о некоторых диазепин- подобных клинических действиях данного препарата (Burger's Medicinal Chemistry, 4th ed. (1981)).
Хотя необходимо еще полностью понять механизм его действия почти определенно он связан с вмешательством тразадона в систему аминергической передачи центральной нервной системы.
Изучение химического связывания показывает, что тразодон проявляет определенную степень вмешательства со следующими рецепторами (см. табл.1).
Действие на адренергические рецепторы (альфа 1 и альфа 2), по-видимому, обуславливает некоторые спорадические побочные эффекты тразодона, такие как гипотония и приапизм, насколько нам известно, оно не относится к психофармакологической активности.
В настоящее время неожиданно найдено, что соединения формулы (I)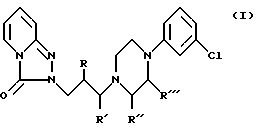
где только один из R, R', R'' и R''' является алкилом и другие - H, и их соли с физиологически приемлемыми органическими или неорганическими кислотами, имеют пониженное сродство с адренергическими рецепторами (см. табл. 2).
Кроме того, соединения формулы (I) превосходят тразодон, когда речь идет о ЛД50 (см. табл.3).
Поэтому первой целью настоящего изобретения является предоставление соединений формулы (I), где только один из R, R', R'' и R''' является алкилом, а другие - H и их солей с физиологически приемлемыми органическими или неорганическими солями.
Примерами подходящих физиологических приемлемых неорганических и органических кислот являются соляная, бромистоводородная, фосфорная, серная, молочная, янтарная, винная, уксусная, лимонная, бензойная, нафталин-2-сульфоновая, адипиновая и пимелиновая кислоты.
Предпочтительно, соединения формулы (I) получают согласно следующей схеме реакций
Схема реакции 1.
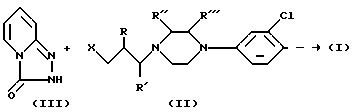
где R, R', R'' и R''' имеют значения, описанные выше и
X - обычная уходящая группа, выбранная из класса, включающего хлор, бром, -O-SO2AlK, -O-SO2Ar.
Стадия, показанная на реакционной схеме 1, по существу включает алкилирование алифатической вторичной аминогруппы и может выполняться согласно обычной методике (J. March, Advanced Organic Chemistry, 3rd Ed., J. Wiley & Sons, N. V., стр. 364-365).
Соединение формулы (III) вводится в реакцию в форме соли с щелочным металлом, такой как, например, соль натрия, описанная в патенте США 3381009.
В уходящих группах -O-SO2AlK и -O-SOAr, Alk и Ar означают алкил и арил (J. March, Advanced Organic Chemistry, 3rd Ed., J. Wiley & Sons, N. V., page 312). Предпочтительно, Alk - метил и Аr - фенил, толил и п-бромфенил.
Реакция предпочтительно выполняется взаимодействием натриевой соли соединения формулы (III) с соединением формулы (II) с присутствием подходящих органических растворителей или смеси органических растворителей при температуре от 40oC и температуре кипения реакционной смеси. Примерами подходящих органических растворителей являются ароматические углеводороды, алифатические спирты и их смеси.
Примерами предпочтительных ароматических углеводородов являются: бензол, толуол и ксилол. Примерами предпочтительных алифатических спиртов являются бутиловый, трет-бутиловый, втор-бутиловый, изобутиловый, пентиловый и трет-пентиловый спирт. Примером предпочтительного амида является диметилформамид.
Промежуточное соединение формулы (II) - новое.
Поэтому дополнительной целью этого изобретения является получение соединения формулы (II), где R, R', R'', R''' и X имеют значения, приведенные выше.
Промежуточные соединения формулы (II) могут быть получены по следующей схеме реакции
Схема реакции 2.
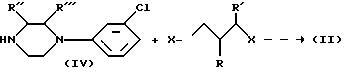
где X, R, R', R'' и R''' имеют значения, указанные выше.
Стадия, приведенная на реакционной схеме 2, выполняется предпочтительно при добавлении пиперазинового соединения формулы (IV) к водной смеси бифункционального алкилирующего агента формулы X-CH2-CHR-CHR'-X с подходящим производным щелочного металла.
Пиперазиновое соединение формулы (IV) предпочтительно растворяют в подходящем органическом растворителе, таком как, например, ароматический углеводород или кетон. Примерами подходящих ароматических растворителей являются бензол, толуол и ксилол. Примерами подходящих кетонов - ацетон и метилизобутилкетон.
Примерами подходящих производных щелочного металла являются карбонат натрия и калия или гидроокись натрия и калия.
Пиперазиновое соединение формулы (IV), где R'' = R''' = H является известным соединением (G.B. Pollard et al., J.O.C. 24, 764 (1959)), в то время как соединения формулы (IV), где R''' - H и R'' - C1-C3-алкил - новые и могут быть получены по следующей схеме реакции.
Схема реакции 3.
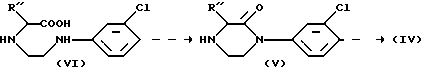
Замыкание кольца в 2-R''-(3-хлорфенил)-3,6-диазагексановой кислоте формулы (VI), приводящее к образованию соответствующего пиперазинона формулы (V), предпочтительно выполняется обработкой низшего эфира гексановой кислоты формулы (VI) соответствующим конденсирующим агентом в присутствии разбавителя.
Примером подходящего конденсирующего агента является гидрид натрия, тионилхлорид и хлористый водород.
Растворитель выбирают в зависимости от конденсирующего агента согласно критериям, хорошо известным по предшествующим работам. Например, если конденсирующий агент - NaH, то подходящими растворителями являются ароматические углеводороды, такие как бензол, толуол и ксилол, в то время как низшие галоидированные углеводороды, такие как хлороформ и хлористый метилен предпочтительны при использовании тионилхлорида в качестве конденсирующего агента.
Последующее восстановление пиперазиновых соединений формулы (V) приводит к соответствующим пиперазиновым соединениям формулы (IV), восстановление выполняется с помощью обычного восстановителя, такого как алюмогидрид лития.
Оба пиперазиновых соединения формулы (V) и 2-замещенные (3-хлорфенил)-3,6-диазагексановые кислоты формулы (VI), где R'' - C1-C3-алкил, являются также новыми соединениями.
Они поэтому также являются целью настоящего изобретения.
Соединения формулы (I) могут иметь асимметрический атом углерода. Поэтому следующей целью настоящего изобретения является получение как отдельных оптических активных изомеров формулы (I), так и их смесей.
Соединения формулы (I) данного изобретения будут применимы во всех тех терапевтических областях, где является эффективным тразодон, например, при депрессии, однако без проявления нежелательного побочного действия тразодона, такого как гипотония и приапизм. В частности соединения формулы (I) изобретения являются многообещающими при лечении состояния страха.
При практическом применении в терапии соединения формулы (I) и их физиологически приемлемые соли с кислотами могут вводиться и как сами по себе, но более предпочтительно введение их в форме фармацевтических составов.
Вышеназванные составы являются другой целью настоящего изобретения и содержат терапевтически эффективное количество одного или более соединений формулы (I) или их солей с физиологически приемлемыми кислотами вместе с жидкими или твердыми фармацевтическими эксципиентами для системного или местного применения.
Фармацевтические составы настоящего изобретения могут быть твердыми, например таблетки, покрытые сахаром, пластинки, капсулы, порошки и медленно высвобождающиеся формы, или полутвердыми, например, суппозитории, крема и мази, или жидкими, такими как растворы, суспензии и эмульсии.
Кроме обычных эксципиентов составы могут содержать приемлемые фармацевтические добавки, такие как предохраняющие вещества, стабилизаторы, эмульгаторы, соли для регулирования осмотического давления, буферы, отдушки и красители.
Когда требуется особая терапия, составы этого изобретения могут включать другие совместимые активные ингредиенты, которые при сопутствующем введении дают полезный терапевтический эффект.
При практическом использовании в терапии эффективное количество соединения формулы (I), требуемое для введения, изменяется в широких пределах в зависимости от таких факторов, как специфические терапевтические требования, фармацевтический состав, путь введения, вес тела и эффективность конкретного соединения изобретения Однако оптимальное значение эффективного количества может быть легко определено с помощью обычных методик.
В основном суточная доза соединений формулы (I) предпочтительно варьируют от 10 до 600 мг; однако в отсутствие побочного эффекта может быт увеличена до 1200 мг.
Фармацевтические составы изобретения могут быть получены с помощью обычных методик фармацевтической химии, включая смешение, гранулирование, прессование, в случае необходимости или разнообразное сочетание смешения и растворения ингредиентов, когда это уместно для получения требуемого продукта.
Для лучшего иллюстрирования изобретения ниже приводятся следующие примеры.
Пример 1.
1-(3-Хлорфенил)-3-метил-пиперазин-2-он
(формула (V), R'' = CH3)
Раствор 76 г N-(3-хлорфенил)-этилдиамина (J. Med. Chem.9, hh. 858-60 (1966)), 60 мл этилового эфира 2-бромпропионовой кислоты и 63 мл триэтиламина в 400 мл толуола кипятят 15 часов, охлаждают, промывают водой, сушат азеотропной перегонкой и добавляют постепенно 9 г гидрида натрия (суспензия в масле, 60%).При добавлении гидрида натрия наблюдают самопроизвольное нагревание смеси. Реакционную смесь перемешивают в течение 1,5 часов при 60oC (экстремальное нагревание), охлаждают, вносят воду. Органический слой отделяют, сушат и упаривают в вакууме. Остаток (48 г) перегоняют и получают 35 г 1-(3-Хлорфенил)-3 метил-пиперазин-2-она (температура кипения 160oC при 0,5 мм Hq. Гидрохлорид соединения имеет т.пл. 170,5-171oC.
Пример 2.
1-(3-Хлорфенил)-3-метил-пиперазин-2-он
(формула (V), R'' = CH2H5)
Раствор 102 г N-(3-хлорфенил)-этилдиамина, 117 г элитового спирта 2-броммасляной кислоты и 84 мл триэтиламина в 500 мл толуола кипятят 6 часов, охлаждают, промывают водой, растворитель упаривают в вакууме. Маслообразный остаток (175 г) суспендируют в 650 мл раствора 2 M NaOH, смесь нагревают при энергичном перемешивании при 70oC до полного растворения масла (приблизительно 2 часа). Результирующий раствор подкисляют и твердый осадок отфильтровывают и получают (3- хлорфенил-2-этил-3,6-диазагексановую кислоту (формула VI), R'' = этил), т.пл. 207-208oC. Элементный анализ находился в соответствии с формулой C12H17ClN2O2.
К раствору полученной выше кислоты в 1,8 хлороформа прибавляют по каплям тионилхлорид, кипятят 3 часа, растворитель упаривают и остаток суспендируют в растворе 70 мл триэтиламина в 1.8 г толуола, нагревают при перемешивании 2 часа при 70oC, охлаждают, фильтруют для удаления гидрохлорида триэтиламина и упаривают в вакууме. Остаток перегоняют и собирают фракцию между 195 и 200oC при 0.3 мм Hq. Гидрохлорид названного соединения имеет т.пл. 149-152oC.
Пример 3.
1-(3-Хлорфенил)-3-этил-пиперазин
(формула (IV), R'' = CH2H5)
К суспензии 31.5 г алюмогидрида лития в 650 мл этилового эфира прибавляют при энергичном перемешивании по каплям, так чтобы растворитель кипел мягко, раствор 66 г пиперазинонового соединения из примера 2 в 350 мл этилового эфира. После добавления результирующую смесь кипятят 2 часа, затем избыток гидрида разлагают водой и органическое основание выделяют по обычной методик. Гидрохлорид названного соединения, перекристализованный из изопропилового спирта, имеет т.пл. 179-181oC
Пример 4.
1-(3-Хлорфенил)-3-метил-пиперазин
(формула (IV), R'' = CH3)
1-(3-Хлорфенил)-3-метил-пиперазин получают по той же методике, которая приведена в примере 3, но из пиперазинового соединения из примера 1.
Гидрохлорид названного соединения имеет т.пл.178-178.5oC (из этилацетата).
Пример 5.
1-(3-Хлорфенил)-4-(3-хлор-2-метилпропил)-пиперазин
(формула (II), R = CH3, R' = R'' = R''' = H).
К смеси 150 мл 1-бром-3-хлор-2-метилпропана, 55 г карбоната калия и 4 мл воды при 60oC при энергичной перемешивании прибавляют по каплям раствор 40 г 3-хлорфенил-пиперазина в 50 мл толуола. После окончания добавления смесь перемешивают 48 часов, отфильтровывают твердый осадок, фильтрат упаривают, остаток хроматографируют на колонке с силикагелем при элюировании смесью гексан-этилацетат= 1-1. Получают 25 г продукта и используют для следующей стадии. Гидрохлорид названного соединения имеет т.пл.178-179oC (из изопропилового спирта).
Пример 6.
После методик, таких как описано в примере 3, пригодные соединения формулы (IV) реагируют с пригодными дигалогеналканами с образованием соответствующих соединений формулы (II):
-1-(3-хлорфенил)-4-(3-хлор-1-метилпропил)пиперазин
(R' = CH3, R = R'' = R''' = H)
Дигидрохлорид соединения имеет т.пл. 160-162oC (разлож.);
-1-(3-хлорфенил)-4-(3-хлорпропил)-3-метил-пиперазин
(R'' = CH3, R = R' = R''' = H)
Дигидрохлорид соединения имеет т.пл. 174-176oC (разлож.).
Пример 7.
2-[3-[4-(3-хлорфенил)-1-пиперазин] -2-метилпропил]-1,2,4-триазол[4,3- а] пиридин-3-(2H)-он
(формула (I), R = CH3, R' = R'' = R''' = H).
Смесь 43 г продукта из примера 5, 23,6 г натриевой соли 1,2,4- триазол[4,3-а]-пиридин-3-(2H)-она (Итальянская патентная заявка N 27806/65), 300 мл ксилола и 30 мл изобутилового спирта нагревают и кипятят 8 часов, разбавляют равным объемом воды.
Остаток, полученный после удаления растворителя из органической фазы, превращают в соответствующий гидрохлорид с раствором 2M соляной кислоты. После перекристаллизации из воды получают 35 г продукта с т.пл. 196- 198oC.
Элементный анализ и данные спектрометрического анализа соответствуют структуре названного соединения.
Пример 8.
По методикам, аналогичным описанным в примере 7, получают следующие соединения формулы (I):
-2-[3-[4-(3-хлорфенил)-1-пиперазинил] -3-метилпропил]-1,2,4-триазол[4,3- а] -пиридин-3-(2H)-он (R' = CH3, R = R'' = R''' = H) (из 1,2,4- триазол[4,3-а] -пиридин-3-(2H)-она и соединения формулы (II), где R = R'' = R''' = H, R' = CH3)
Дигидрохлорид гидрат, т.пл.184-194oC;
-2-[3-[4-(3-хлорфенил)-1-(2-этил)-пиперазинил] -пропил] -1,2,4- триазол[4,3-а] -пиридин-3(2H)-он (R'' = этил, R = R' = R''' = H) (из 1,2,4-триазол[4,3-а] -пиридин-3-(2H)-она и соединения формулы (II), где R'' = этил, R = R' = R''' = H)
Гидрохлорид, т.пл. 180-182oC;
-2-[3-[4-(3-хлорфенил)-1-(2-метил)-пиперазинил] -пропил] -1,2,4- триазол[4,3-а]-пиридин-3-(2H)-он (R'' = CH3), R = R' = R''' = H) (из 1,2, 4-триазол[4,3-а]-пиридин-3-(2H)-она и соединения формулы (II), где R'' = CH3, R = R' = R''' = H,) X = Cl
Гидрохлорид, т.пл. 189-190oC;
-2-[3-[4-(3-хлорфенил)-1-(3-метил)-пиперазинил] -пропил] -1,2,4- триазол[4,3-а] -пиридин-3-(2H)-он (R'' = CH3, R = R' = R'' = H) (из 1,2,4-триазол[4,3-а] -пиридин-3-(2H)-она и соединения формулы (II), где R''' = CH3), R = R' = R'' = H) X = Cl
Гидрохлорид, т.пл. 178-180oC;
| название | год | авторы | номер документа |
|---|---|---|---|
| (S)- ИЛИ (R)-ЭНАНТИОМЕРЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ | 1994 |
|
RU2128180C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ АЗОЛОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2128659C1 |
| ПРОИЗВОДНЫЕ ПИРИДИНОНА И ПИРИДАЗИНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ПОЛИ(ADP-РИБОЗА) ПОЛИМЕРАЗЫ (PARP) | 2007 |
|
RU2472782C2 |
| ПРОИЗВОДНЫЕ МОЧЕВИНЫ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ, СРЕДИ ПРОЧЕГО, ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНОГО ПУТИ | 2011 |
|
RU2586223C2 |
| ТРИЦИКЛИЧЕСКИЕ 5,6-ДИГИДРО-9H-ПИРАЗОЛО[3,4-С]-1,2,4-ТРИАЗОЛО [4,3-А] ПИРИДИНЫ, СПОСОБ ИНГИБИРОВАНИЯ ФОСФОДИЭСТЕРАЗЫ ТИПА IУ И СПОСОБ ИНГИБИРОВАНИЯ ПРОДУЦИРОВАНИЯ ФАКТОРА ОПУХОЛЕСПЕЦИФИЧЕСКОГО НЕКРОЗА | 1996 |
|
RU2161158C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ КОЛИТА | 2010 |
|
RU2518416C2 |
| ТРИАЗОЛОПИРИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2561104C2 |
| ИНГИБИТОРЫ КИНАЗЫ | 2012 |
|
RU2623734C9 |
| ИНГИБИРОВАНИЕ ФЕРМЕНТОВ | 2013 |
|
RU2638537C2 |
| ТРИАЗОЛПИРИДИНОВЫЕ СОЕДИНЕНИЯ, ИНГИБИРУЮЩИЕ JAK, И СПОСОБЫ | 2009 |
|
RU2560153C2 |


Алкильные производные тразодона общей формулы I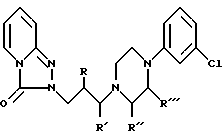
в которой только один из R, R', R" и R"' представляет С1-C3-алкил, а другие являются водородом, и их соли с физиологически приемлемыми неорганическими или неорганическими кислотами получают взаимодействием соединения формулы III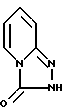
или его соли со щелочным металлом с пиперазиновым соединением формулы II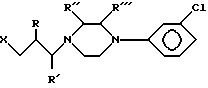
где R, R', R", R"' принимают значения, указанные для формулы I, а Х - хлор или бром при температуре кипения реакционной смеси. Соединения формулы I по сравнению с тразодоном имеют пониженное сродство с адренергическими рецепторами и превосходят тразодон, когда речи идет о ЛД50. 7 с. и 3 з.п. ф-лы.
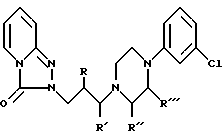
в которой только один из R, R', R'' и R''' представляет C1-C3 алкил, а другие являются водородом, и их соли с физиологически приемлемыми органическими или неорганическими кислотами.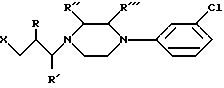
в которой только один из R, R', R'' и R''' представляет C1-C3 алкил, а другие являются водородом, и
Х представляет уходящую группу, выбранную из группы, включающей хлор, бром.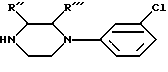
в которой R''' представляет водород, а R'' представляет C1-C3 алкил.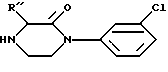
в которой R'' представляет C1-C3 алкил.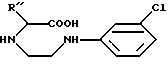
в которой R'' представляет C1-C3 алкил.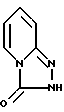
или его соль со щелочным металлом подвергают взаимодейстию с пиперазиновым соединением формулы II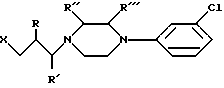
в которой R, R', R'', R''' и Х имеют значения, определенные в п.2, в присутствии органического разбавителя при температуре кипения реакционной смеси.
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU102A1 |
| US 4308207, 1981 | |||
| GB 1592329, 1981 | |||
| Ребристый каток | 1922 |
|
SU121A1 |
| US 4390695, 1983 | |||
| GB 1554275, 1979 | |||
| Устройство для перемножения двух величин | 1952 |
|
SU100505A2 |
| J.Med | |||
| Chem., v 34, p | |||
| Устройство для радиопередачи | 1925 |
|
SU2633A1 |
| Adv | |||
| Heterocyclic | |||
| Chem., 1972, 14, 99. | |||
Авторы
Даты
1999-02-27—Публикация
1993-01-14—Подача