Настоящее изобретение относится к производным пиридинона и пиридазинона, которые являются ингибиторами фермента поли(ADP-рибоза)полимеразы (PARP), ранее известной как поли(ADP-рибоза)синтаза и поли(ADP-рибозил)трансфераза. Соединения по настоящему изобретению могут быть применены для монотерапии опухолей со специфическими нарушениями в путях восстановления ДНК и как усиливающие агенты для определенных повреждающих ДНК агентов, таких как противораковые средства и радиотерапия. Далее соединения по настоящему изобретению могут быть применены для лечения клеточного некроза (при ударе и инфаркте миокарда), уменьшения воспаления и тканевого повреждения, лечения ретровирусных инфекций и защиты от токсичности химиотерапии.
Поли(ADP-рибоза)полимераза (PARP) образована надсемейством восемнадцати белков, содержащих каталитические домены PARP (Bioassays (2004) 26:1148). Эти белки включают PARP-1, PARP-2, PARP-3, танкиразу-1, танкиразу-2, vaultPARP и TiPARP. PARP-1, основной представитель надсемейства, состоит из трех доменов: амино (N)-концевого ДНК-связывающего домена (DBD), содержащего два цинк-содержащих фрагмента, автомодифицирующего домена и карбокси-(C)-концевого каталитического домена.
PARP представляют собой ядерные и цитоплазматические ферменты, которые расщепляют NAD+ до никотинамида и ADP-рибозы для получения длинных и разветвленных полимеров ADP-рибозы на целевых белках, включая топоизомеразы, гистоны и конкретно PARP (Biochem. Biophys. Res. Commun. (1998) 245:1-10).
Поли-ADP-рибозилирование участвует в нескольких биологических процессах, включая восстановление ДНК, генной транскрипции, прохождении клеточного цикла, гибели клеток, хроматиновых функциях и стабильности генома.
Каталитическая активность PARP-1 и PARP-2, как было показано, прямо активируется разрывами нити ДНК (см. Pharmacological Research (2005) 52:25-33). В ответ на повреждение ДНК PARP-1 связывается с однонитевым и двунитевым разрывами ДНК. В нормальных физиологических условиях активность PARP минимальна, однако при повреждении ДНК имеет место немедленная активация активности PARP, возрастающей до 500 раз. Как PARP-1, так и PARP-2 обнаруживают обрывы нити ДНК, действуя в качестве определителей разрыва ДНК, обеспечивая быстрые сигналы остановки транскрипции и притока ферментов, требующихся для восстановления ДНК в точке повреждения. Поскольку радиотерапии и многие химиотерапевтические способы терапии рака действуют под влиянием индуцирующего повреждения ДНК, ингибиторы PARP могут быть применены как химио- и радиосенсибилизаторы при лечении рака. Ингибиторы PARP, как сообщалось, являются эффективными в радиосенсибилизации гипоксических опухолевых клеток (патенты US 5032617, 5215738 и 5041653).
Большинство биологических эффектов PARP относятся к этому процессу поли-ADP-рибозилирования, который влияет на свойства и функции целевых белков; к PAR-олигомерам, которые, когда отщепляются от поли-ADP-рибозилированных белков, создают различные клеточные эффекты; физической ассоциации PARP с ядерными белками с образованием функциональных комплексов и снижению клеточного уровня их субстрата, NAD+ (Nature Review (2005) 4:421-440).
Кроме участия в восстановлении ДНК, PARP также может действовать как медиатор гибели клеток. Его избыточная активация при патологических состояниях, таких как ишемия и реперфузионное повреждение, может приводить к значительному уменьшению уровня межклеточного NAD+, что может вести к ослаблению нескольких NAD+ зависимых метаболических путей и приводить к гибели клеток (см. Pharmacological Research (2005) 52:44-59). В результате активации PARP уровни NAD+ значительно падают. Экстенсивная активация PARP ведет к значительному уменьшению уровней NAD+ в клетках, страдающих от крупного повреждения ДНК. Короткий период полураспада поли(ADP-рибозы) приводит к большой скорости круговорота, если один раз поли(ADP-рибоза) образуется, она быстро разлагается всегда активной поли(ADP-рибоза) гликогидролазой (PARG). PARP и PARG образуют цикл, который конвертирует большое количество NAD+ в ADP-рибозу, вызывая падение NAD+ и ATP до уровня менее чем 20% от нормального уровня. Такой сценарий является особенно пагубным при ишемии, когда потеря кислорода уже значительно подрывает выход клеточной энергии. Последующее продуцирование свободных радикалов в течение реперфузии, как предполагается, является основной причиной повреждения ткани. Часть падения уровня ATP, которое является типичным для многих органов при ишемии и реперфузии, может быть связана со снижением уровня NAD+ благодаря кругообороту поли(ADP-рибозы). Таким образом, ингибирование PARP, как ожидается, сберегает уровень клеточной энергии, таким образом потенцируя выживание ишемических тканей после удара. Соединения, которые являются ингибиторами PARP, следовательно, могут быть применены для лечения состояний, которые возникают из опосредованной PARP гибели клеток, включая неврологические состояния, такие как удар, травма и болезнь Паркинсона.
Ингибиторы PARP, как было показано, могут быть применены для специфического уничтожения BRCA-1 и BRCA-2 дефицитных опухолей (Nature (2005) 434:913-916 и 917-921; и Cancer Biology & Therapy (2005) 4:934-936).
Ингибиторы PARP, как было показано, являются селективными для уничтожения клеток с дефектами в ATM, ДНК_PK или KU80 (Nucleic Acid Research (2006) 34: 1685-1691).
Ингибиторы PARP, как было показано, усиливают эффективность противораковых лекарственных средств (Pharmacological Research (2005) 52:25-33), включая соединения платины, такие как цисплатин и карбоплатин (Cancer Chemother. Pharmacol. (1993) 33:157-162 и Mol. Cancer Ther. (2003) 2:371-382). Ингибиторы PARP, как было показано, увеличивают антиопухолевую активность ингибиторов топоизомеразы I, таких как иринотекан и топотекан (Mol. Cancer Ther. (2003) 2:371-382; и Clin. Cancer Res. (2000) 6:2860-2867), и это было продемонстрировано на моделях in vivo (J. Natl. Cancer Inst. (2004) 96:56-67).
Ингибиторы PARP, как было показано, возвращают чувствительность к цитотоксическим и антипролиферативным эффектам темозоломида (TMZ) (см. Curr. Med. Chem. (2002) 9:1285-1301 и Med. Chem. Rev. Online (2004) 1: 144-150). Это было продемонстрировано на ряде моделей in vitro (Br. J. Cancer (1995) 72:849-856; Br J. Cancer (1996) 74:1030-1036; Mol Pharmacol (1997) 52:249-258; Leukemia (1999) 13:901-909; Glia (2002) 40:44-54; и Clin. Cancer Res. (2000) 6:2860-2867 и (2004) 10:881-889) и моделях in vivo (Blood (2002) 99:2241-2244; Clin. Cancer Res. (2003) 9:5370-5379 и J. Natl. Cancer Inst. (2004) 96:56-67). Как было показано, ингибиторы PARP также предотвращают появление некроза, индуцируемого селективными N3-аденинметилирующими агентами, такими как MeOSO2(CH2)-лекситропсин (Me-Lex) (Pharmacological Research (2005) 52:25-33).
Ингибиторы PARP, как было показано, действуют как радиационные сенсибилизаторы. Ингибиторы PARP, как сообщалось, являются эффективными в отношении радиосенсибилизированных (гипоксических) опухолевых клеток и эффективны при предотвращении восстановления опухолевых клеток после потенциально летального (Br. J. Cancer (1984) 49 (Suppl. VI):34-42; и Int. J. Radiat Bioi. (1999) 75:91-100) и близкого к летальному (Clin. Oncol. (2004) 16(l):29-39) повреждения ДНК после радиационной терапии, предположительно посредством их способности предотвращать соединения разрывов нити ДНК и путем сильного влияния на несколько сигнальных путей при повреждении ДНК.
Ингибиторы PARP, как было показано, могут быть применены для лечения острых и хронических миокардиальных заболеваний (см. Pharmacological Research (2005) 52:34-43). Например, было продемонстрировано, что одиночные инъекции ингибиторов PARP уменьшают размер инфаркта, вызываемого ишемией и реперфузией сердца или скелетной мышцы на кроликах. В этих исследованиях одиночная инъекция 3-аминобензамида (10 мг/кг), за одну минуту до окклюзии или за одну минуту до реперфузии, вызывает аналогичные уменьшения размера инфаркта в сердце (32-42%), в то время как 1,5-дигидроксиизохинолин (1 мг/кг), другой ингибитор PARP, уменьшает размер инфаркта в сопоставимой степени (38-48%). Эти результаты делают корректным предположение, что ингибиторы PARP могут восстанавливать поврежденное ранее ишемией сердце или реперфузионное повреждение скелетной мышечной ткани (PNAS (1997) 94:679-683). Подобные результаты также были установлены на свиньях (Eur. J. Pharmacol. (1998) 359:143-150 и Ann. Thorac. Surg. (2002) 73:575-581) и на собаках (Shock. (2004) 21:426-32).
Ингибиторы PARP, как было показано, могут быть применены для лечения определенных сосудистых заболеваний, септического шока, ишемического повреждения и нейротоксичности (Biochim. Biophys. Acta (1989) 1014:1-7; J. Clin. Invest. (1997) 100: 723-735). Повреждение ДНК радикалами кислорода, которое ведет к разрывам нити в ДНК, которое затем идентифицируется PARP, является основным фактором, вносящим вклад в такие болезненные состояния, как показано исследованиями ингибитора PARP (J. Neurosci. Res. (1994) 39:38-46 и PNAS (1996) 93:4688-4692). Также, как было продемонстрировано, PARP играет роль в патогенезе геморрагического шока (PNAS (2000) 97:10203-10208).
Ингибиторы PARP, как было показано, могут быть применены для лечения воспалительных заболеваний (см. Pharmacological Research (2005) 52:72-82 и 83-92).
Также было продемонстрировано, что эффективная ретровирусная инфекция клеток млекопитающих блокируется ингибированием активности PARP. Такое ингибирование рекомбинантных ретровирусных векторных инфекций, как было показано, имеет место в различных типах клеток (J. Virology, (1996) 70(6):3992-4000). Таким образом, ингибиторы PARP исследуются для применения в качестве антивирусных терапий и для лечения рака (WO 91/18591).
Эксперименты in vitro и in vivo продемонстрировали, что ингибиторы PARP могут быть применены для лечения или предупреждения аутоиммунных заболеваний, таких как диабет I типа и осложнения при диабете (Pharmacological Research (2005) 52:60-71).
Ингибирование PARP было предположено в качестве причины отсрочки характеристик старения в человеческих фибробластах (Biochem. Biophys. Res. Comm. (1994) 201(2):665-672 и Pharmacological Research (2005) 52:93-99). Это может быть связано с ролью, которую PARP играет в контролировании теломерной функции (Nature Gen., (1999) 23(l):76-80).
Огромное большинство ингибиторов PARP, опубликованных к настоящему времени, взаимодействует с никотинамид-связывающим доменом фермента и ведет себя как конкурентные ингибиторы в отношении NAD+ (Expert Opin. Ther. Patents (2004) 14:1531-1551). Структурные аналоги никотинамида, такие как бензамид и производные, были среди первых соединений, исследованных в качестве ингибиторов PARP. Однако эти молекулы имеют слабую подавляющую активность и обладают другими эффектами, не связанными с ингибированием PARP. Таким образом, существует необходимость в нахождении мощных ингибиторов фермента PARP.
US 2005/0234236 описывает способ для синтеза пиридазинонов, WO 2004/085406 описывает бензилпиридазиноны в качестве ингибиторов обратной транскриптазы и EP 0810218 описывает бензилпиридазиноны в качестве ингибиторов COX I и COX II.
Теперь неожиданно впервые найдено, что производные пиридинона и пиридазинона по настоящему изобретению проявляют высокую степень ингибирования активности PARP.
Соединения по настоящему изобретению могут быть применены для ингибирования поли(ADP-рибоза)полимеразы (PARP). В частности, они могут быть применены в качестве ингибиторов PARP-1 и/или PARP-2. Настоящее изобретение предоставляет применение соединения формулы I:
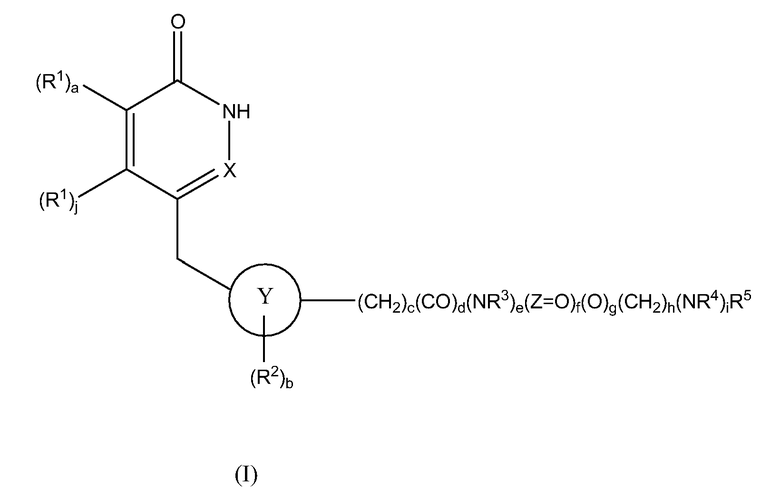 ,
,
где
a равно 0 или 1;
b равно 0, 1, 2 или 3;
c равно 0, 1, 2, 3, 4, 5 или 6;
d равно 0 или 1;
e равно 0 или 1;
f равно 0 или 1;
g равно 0 или 1;
h равно 0, 1, 2, 3, 4, 5 или 6;
i равно 0 или 1;
j равно 0 или 1;
X представляет собой N или CH;
Y представляет собой C6-10-арил, 5-членный ненасыщенный гетероцикл, содержащий 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N и S, но не более чем один из которых представляет собой O или S, или 6-членный ненасыщенный гетероцикл, содержащий 1, 2, 3 или 4 атома азота;
Z представляет собой C или SO;
R1, каждый независимо, представляет собой C1-6-алкил, галоген-C1-6-алкил, галоген или циано;
R2, каждый независимо, представляет собой гидрокси, галоген, циано, нитро, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси или NRaRb;
R3 представляет собой водород или C1-6-алкил;
R4 представляет собой водород или C1-6-алкил;
R5 представляет собой водород, гидрокси, циано, оксо, галоген, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкилкарбонил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой C6-10-арил; C6-10-арилкарбонил; C3-10-циклоалкил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-15-членное ненасыщенное, частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6;
A, каждый независимо, представляет собой простую связь, O, C=O, (C=O)NR7, NR7(C=O), (C=O)O, O(C=O), (C=S)NR7, NR7 или S(O)r;
q, каждый независимо, равен 0, 1, 2, 3 или 4;
r равно 0, 1 или 2;
R6, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, NRaRb или цикл, который представляет собой: C3-10-циклоалкил; C6-10-арил; C6-10-арилокси; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома, независимо выбранных из N, О и S; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8;
R7 представляет собой водород или R6;
R8, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C1-6-алкокси, C2-10-алкенил, галоген-C1-6-алкил, галоген-C1-6-алкокси, -O(C=O)C1-6-алкил, -(C=O)OC1-6-алкил, NRaRb или цикл, который представляет собой C3-10-циклоалкил, C6-10-арил, C6-10-арил-C1-6-алкил, C6-10-арилкарбонил, C6-10-арилоксикарбонил, C6-10-арил-C1-6-алкоксикарбонил, 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; или 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из галогена, C1-6-алкила или галоген-C1-6-алкила;
каждый из R9 и R10 независимо представляет собой водород, галоген, С1-6-алкил или галоген-C1-6-алкил;
каждый из Ra и Rb независимо представляет собой водород, C1-6-алкил, C3-10-циклоалкил, C3-10-циклоалкил-C1-6-алкил, C6-10-арил или C6-10-арил-C1-6-алкил;
или его фармацевтически приемлемой соли или таутомера для приготовления лекарственного средства для лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP).
Настоящее изобретение также предоставляет способ лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP), где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
В варианте осуществления состояния, которые могут быть излечены путем ингибирования поли(ADP-рибоза)полимеразы (PARP), включают воспалительные заболевания; реперфузионные травмы; ишемические состояния; удар; хроническую и острую почечную недостаточность; сосудистые заболевания, отличные от кардиососудистых заболеваний; кардиососудистые заболевания; сахарный диабет; рак, особенно рак, который является дефицитным в отношении зависимой от гомологичной рекомбинации (HR) репаразной активности в отношении двухнитевого разрыва ДНК, например BRCA-1 или BRCA-2 дефицитных опухолях; нейродегенеративные заболевания; ретровирусные инфекции; повреждение сетчатки; старение кожи; индуцированное УФ-светом повреждение кожи и преждевременное старение.
В варианте осуществления состояния, при которых могут быть достигнуты улучшения путем ингибирования поли(ADP-рибоза)полимеразы (PARP), являются выбранными из реперфузионных травм; ишемических состояний; удара; хронической и острой почечной недостаточности; сосудистых заболеваний, отличных от кардиососудистых заболеваний; кардиососудистых заболеваний; сахарного диабета; рака, особенно рака, который является дефицитным в отношении зависимой от гомологичной рекомбинации (HR) репаразной активности в отношении двухнитевого разрыва ДНК, например BRCA-1 или BRCA-2 дефицитных опухолях; нейродегенеративных заболеваний; ретровирусных инфекций; повреждения сетчатки; старения кожи; индуцированного УФ-светом повреждения кожи и преждевременного старения.
В варианте осуществления для каждого из указанных выше вариантов осуществления
R2, каждый независимо, представляет собой гидрокси, галоген, циано, нитро, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси или галоген-C1-6-алкокси;
R5 представляет собой водород, гидрокси, циано, оксо, галоген, C1-6-алкил, C2-10-алкенил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкилкарбонил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой C6-10-арил; C6-10-арилкарбонил; C3-10-циклоалкил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6;
R6, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6алкил, C2-10-алкенил, галоген-С1-6-алкил или цикл, который представляет собой C6-10-арил; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота; или 7-10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8;
R8, каждый независимо, представляет собой гидрокси, оксо, циано, галоген, нитро, C1-6-алкил, C1-6-алкокси, C2-10-алкенил, галоген-C1-6-алкил, галоген-C1-6-алкокси, -O(C=O)C1-6-алкил, -(C=O)OC1-6-алкил, амино, C1-6-алкиламино, ди(C1-6-алкил)амино, C6-10-арил, 5-членное гетероароматическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S, не более чем один гетероатом из которых представляет собой O или S; или 6-членное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота.
Настоящее изобретение также предоставляет новые соединения формулы I:
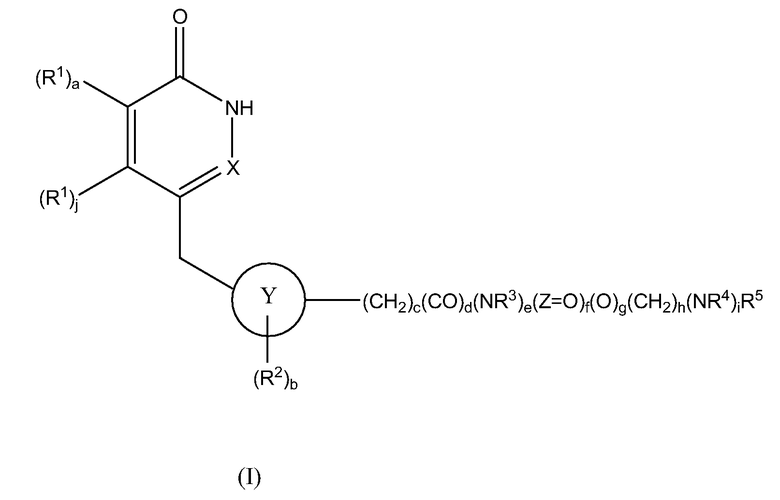 ,
,
в которой
a, b, c, d, e, f, g, h, i, j, X, Y, Z, R1, R2, R3, R4 и R5 определены выше; при условии что:
(a) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой O-мостик, R2 представляет собой фтор, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным циклом, выбранным из C6-10-арила, 5-членного гетероароматического кольца, 6-членного гетероароматического кольца или 7-15-членного ненасыщенного или частично насыщенного гетероциклического кольца;
(b) если X представляет собой N и Y представляет собой фенил, нафтил или 9- или 10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1 или 2 гетероатома, выбранных из N, O и S, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкилкарбонил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(c) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой CO-мостик, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным фенилом, пиридинилом, тиенилом или фурилом;
или их фармацевтически приемлемые соли или таутомеры.
В варианте осуществления:
(a) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой O-мостик, R2 представляет собой фтор, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным циклом, выбранным из C6-10-арила, 5-членного гетероароматического кольца, 6-членного гетероароматического кольца или 7-10-членного ненасыщенного или частично насыщенного гетероциклического кольца;
(b) если X представляет собой N и Y представляет собой фенил, нафтил или 9- или 10-членное ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 1 или 2 гетероатома, выбранные из N, O и S, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(c) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой CO-мостик, X представляет собой N и Y представляет собой фенил, то R5 не является необязательно замещенным фенилом, пиридинилом, тиенилом или фурилом.
В варианте осуществления сумма a и j равна 1 или 2.
В варианте осуществления b равно 0 или 1. В другом варианте осуществления b равно 1.
В варианте осуществления c равно 0.
В варианте осуществления d равно 1.
В варианте осуществления e равно 0.
В варианте осуществления f равно 0.
В варианте осуществления g равно 0.
В варианте осуществления h равно 0.
В варианте осуществления i равно 0.
В варианте осуществления j равно 0. В другом варианте осуществления j равно 1.
В варианте осуществления X представляет собой N. В другом варианте осуществления X представляет собой CH.
В варианте осуществления Y представляет собой фенил, пиридинил, пиримидинил, фурил или тиенил.
В другом варианте осуществления Y представляет собой C6-10-арил.
В частности, группа Y представляет собой фенил.
В варианте осуществления R1 представляет собой фтор-C1-3-алкил, галоген или C1-6-алкил. В другом варианте осуществления R1 представляет собой C1-6-алкил.
Предпочтительная R1 группа представляет собой этил. Более предпочтительные R1 группы представляют собой метил и изопропил.
В варианте осуществления R2 представляет собой галоген, C1-6-алкокси, амино, C1-6-алкиламино или ди(C1-6-алкил)амино.
В другом варианте осуществления R2 представляет собой фтор-C1-3-алкил или галоген.
В другом варианте осуществления R2 представляет собой галоген, например фтор или хлор.
Предпочтительно, R2 группа представляет собой фтор. Более предпочтительные R2 группы представляют собой диметиламино, изопропокси и метокси.
В варианте осуществления R5 представляет собой водород, гидрокси, циано, галоген, C2-10-алкенил, С1-6-алкилкарбонил, C1-6-алкокси, C1-6-алкоксикарбонил, карбокси, нитро или цикл, который представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; или 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное ненасыщенное, частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В другом варианте осуществления R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N или 5-, 6- или 7-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CH2)qR6.
В варианте осуществления R5 представляет собой диазепанил, пиперидинил, пиперазинил, пирролидинил, спиробензофуранпиперидинил, тетрагидроимидазопиразинил, тетрагидротриазолопиразинил, диазаспиродеканил, тетрагидропиразолопиридинил, диазаспирононанил, имидазолидинил, азетидинил или тетрагидротриазолопиридинил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6.
В варианте осуществления, когда R5 представляет собой цикл, цикл является необязательно замещенным одной, двумя или тремя независимо выбранными A-(CR9R10)qR6 группами. В варианте осуществления, когда R5 представляет собой цикл, цикл является незамещенным или монозамещенным.
В варианте осуществления, когда R6 представляет собой цикл, он является необязательно замещенным одной, двумя или тремя группами, независимо выбранными из R8. В другом варианте осуществления, когда R6 представляет собой цикл, он является незамещенным, монозамещенным или дизамещенным.
В варианте осуществления, когда R8 представляет собой цикл, он является необязательно замещенным одной, двумя или тремя группами из независимо выбранных групп. В другом варианте осуществления, когда R8 представляет собой цикл, он является незамещенным, монозамещенным или дизамещенным.
В варианте осуществления R7 представляет собой водород.
В варианте осуществления A представляет собой прямую связь, O, CO или NH.
В другом варианте осуществления A представляет собой прямую связь, CO или NH. В другом варианте осуществления A представляет собой прямую связь или карбонил. Предпочтительная A группа представляет собой CO.
В варианте осуществления q равно 0, 1 или 2. В другом варианте осуществления q равно 0.
В варианте осуществления R6 представляет собой оксо, C1-6-алкил, галоген-C1-6-алкил, амино, C1-6-алкиламино, (диC1-6-алкил)амино или цикл, который представляет собой пиримидинил, пиридинил, пиразолил, фенил, пиразинил, тетрагидроизохинолинил, циклопентил, тетрагидрофуранил, пирролидинил, пиперидинил, хиназолинил, фенокси, фурил, бензодиоксолил, тиенил, циклопропил или азетидинил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из R8.
В другом варианте осуществления R6 представляет собой C1-6-алкил.
В варианте осуществления R8 представляет собой циано, галоген, C1-6-алкил, галоген-C1-6-алкил, C1-6-алкокси, амино, C1-6-алкиламино, ди(C1-6-алкил)амино, (C3-10-циклоалкил-C1-6-алкил)амино, C6-10-ариламино, (C6-10-арил-C1-6-алкил)амино или цикл, который представляет собой C6-10-арил, C6-10-арил-C1-6-алкил, C6-10-арилкарбонил, C6-10-арилоксикарбонил или C6-10-арил-C1-6-алкоксикарбонил; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из галогена и C1-6-алкила.
Предпочтительные R8 группы включают метокси, хлор, метил, трифторметил, фтор, циано, метиламино, пропил, диметиламино, бензил, бензоксикарбонил, фениламино, амино, бензиламино, (циклопропилметил)амино, изобутиламино, фторбензил, метилбензил, нафтилметил и этил.
В варианте осуществления каждый из R9 и R10 независимо представляет собой водород, метил, фтор или трифторметил.
В другом варианте осуществления каждый из R9 и R10 представляет собой атом водорода.
Предпочтительная R6 группа представляет собой метил. Более предпочтительные R6 группы включают пиримидинил, пиридинил, метоксипиридинил, диметиламино, пиразолил, хлорпиридинил, фенил, диметилпиразинил, метоксифенил, тетрагидроизохинолинил, циклопентил, трифторметил, метиламино, дифторметил, изопропил, тетрагидрофуранил, пирролидинил, пиперидинил, хиназолинил, метилфенил, (трифторметил)фенил, фторфенокси, цианопиридинил, дифторфенил, фурил, метилпирролидинил, бензодиоксолил, тиенил, циклопропил, оксо, дифторазетидинил, (метиламино)циклопентил, пропилпирролидинил, метилпиперидинил, (диметиламино)циклопропил, бензилпирролидинил, (метиламино)циклопропил, метилазетидинил, (бензоксикарбонил)метилпиперидинил, (фениламино)циклопентил, аминоциклопентил, (бензиламино)циклопентил, [(циклопропилметил)амино]циклопентил, (изобутиламино)циклопентил, (фторбензил)пирролидинил, (метилбензил)пирролидинил, (нафтилметил)пирролидинил и этилпирролидинил.
Таким образом, предпочтительные R5 группы представляют собой диазепанил и ацетилдиазепанил. Более предпочтительные R5 группы представляют собой пиримидинилдиазепанил, пиридинилпиперидинил, [(пиридинилметил)окси]пиперидинил, (метоксипиридинил)пиперазинил, пиридинилпирролидинил, [(диметиламино)метил]пиперидинил, спиробензофуранпиперидинил, (пиразолилэтил)пиперидинил, (хлорпиридинил)пиперазинил, бензилтетрагидроимидазопиразинил, (диметилпиразинил)пиперазинил, фенилтетрагидроимидазопиразинил, (метоксибензил)пиперазинил, тетрагидроизохинолинилпиперидинил, пиперазинил, фенилпиперазинил, бензилпиперазинил, (пиридинилметил)пиперазинил, (циклопентилкарбонил)диазепанил, (трифторметил)тетрагидротриазолопиразинил, пропионилпиперазинил, [(метил)(метиламино)пропаноил]пиперазинил, (дифторацетил)пиперазинил, (трифторпропаноил)пиперазинил, изобутирилпиперазинил, (пиридинилкарбонил)пиперазинил, (тетрагидрофурилкарбонил)пиперазинил, [(метил)(диметиламино)пропаноил]пиперазинил, (пентафторпропаноил)пиперазинил, (пирролидинилкарбонил)пиперазинил, (трифторацетил)пиперазинил, пиперидинилпиперидинил, пирролидинилпиперидинил, хиназолинилпиперазинил, пиримидинилпиперазинил, диазаспиродеканил, (метилфенил)тетрагидротриазолопиразинил, [(трифторметил)фенил]тетрагидротриазолопиразинил, [(фторфенокси)метил]тетрагидротриазолопиразинил, (цианопиридинил)пиперазинил, (метил)диазаспиродеканил, (дифторфенил)тетрагидротриазолопиразинил, [(диметиламино)метил]тетрагидротриазолопиразинил, фурилтетрагидротриазолопиразинил, (пентафторэтил)тетрагидротриазолопиразинил, {[(трифторметил)фенил]амино}тетрагидротриазолопиразинил, (метилпролил)пиперазинил, фенилтетрагидротриазолопиразинил, бензодиоксолилтетрагидротриазолопиразинил, тиенилтетрагидротриазолопиразинил, циклопропилтетрагидропиразолопиридинил, (трифторметил)тетрагидропиразолопиридинил, пиридинилтетрагидротриазолопиразинил, диазаспирононанил, метилдиоксиимидазолидинил, (пирролидинилметил)азетидинил, (дифторазетидинил)пиперидинил, (трифторэтил)тетрагидротриазолопиридинил, {[(метиламино)циклопентил]карбонил}пиперазинил, метилдиазаспирононанил, [(пропилпирролидинил)карбонил]пиперазинил, (пиперидинилкарбонил)пиперазинил, [(метилпиперидинил)карбонил]пиперазинил, {[(диметиламино)циклопропил]карбонил}пиперидинил, [(диметиламино)пропаноил]пиперидинил, [(бензилпирролидинил)карбонил]пиперазинил, (пирролидинилкарбонил)пиперазинил, {[(метиламино)циклопропил]карбонил}пиперазинил, [(метилазетидинил)карбонил]пиперазинил, [(метилпирролидинил)карбонил]пиперидинил, [(диметиламино)трифторпропанонил]пиперазинил, [(метилпиперидинил)карбонил]пиперидинил, {[(бензоксикарбонил)метилпиперидинил]карбонил}пиперидинил, [(диметиламино)метилэтил]тетрагидротриазолопиразинил, (трифторэтил)тетрагидротриазолопиридинил, [(пирролидинил)ацетил]пиперидинил, этилдиазаспиродеканил, (циклопропилметил)диазаспиродеканил, [(анилиноциклопентил)карбонил]пиперазинил, [(аминоциклопентил)карбонил]пиперазинил, {[(бензиламино)циклопентил]карбонил}пиперазинил, ({[(циклопропилметил)амино]циклопентил}карбонил)пиперазинил, {[(изобутиламино)циклопентил]карбонил}пиперазинил, [(фторбензил)пролил]пиперазинил, [(метилбензил)пролил]пиперазинил, [(нафтилметил)пролил]пиперазинил и (этилпролил)пиперазинил.
Предпочтительные R5 группы представляют собой 1,4-диазепан-1-ил и 4-ацетил-1,4-диазепан-1-ил. Более предпочтительные R5 группы представляют собой 4-(пиримидин-2-ил)-1,4-диазепан-1-ил, 4-(пиридин-4-ил)пиперидин-1-ил, 4-[(пиридин-2-илметил)окси]пиперидин-1-ил, 3-[(пиридин-2-илметил)окси]пиперидин-1-ил, 4-(5-метоксипиридин-2-ил)пиперазин-1-ил, 4-(4-метоксипиридин-2-ил)пиперазин-1-ил, 3-пиридин-4-илпирролидин-1-ил, 3-[(диметиламино)метил]пиперидин-1-ил, 1'H-спиро[1-бензофуран-3,4'-пиперидин]-1'-ил, 4-(1H-пиразол-1-илэтил)пиперидин-1-ил, 4-(5-хлорпиридин-2-ил)пиперазин-1-ил, 4-(6-метоксипиридин-2-ил)пиперазин-1-ил, 3-бензил-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-7-ил, 4-(3,6-диметилпиразин-2-ил)пиперазин-1-ил, 3-фенил-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-7-ил, 4-(3-метоксибензил)пиперазин-1-ил, 4-(1,2,3,4-тетрагидроизохинолин-2-ил)пиперидин-1-ил, пиперазин-1-ил, 2-фенилпиперазин-1-ил, 2-бензилпиперазин-1-ил, 3-(пиридин-3-илметил)пиперазин-1-ил, 4-(циклопентилкарбонил)-1,4-диазепан-1-ил, 3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил, 4-пропионилпиперазин-1-ил, 4-[2-метил-2-(метиламино)пропаноил]пиперазин-1-ил, 4-(дифторацетил)пиперазин-1-ил, 4-(3,3,3-трифторпропаноил)пиперазин-1-ил, 4-изобутирилпиперазин-1-ил, 4-(пиридин-2-илкарбонил)пиперазин-1-ил, 4-(тетрагидрофуран-2-илкарбонил)пиперазин-1-ил, 4-[2-метил-2-(диметиламино)пропаноил]пиперазин-1-ил, 4-(2,2,3,3,3-пентафторпропаноил)пиперазин-1-ил, 4-(пирролидин-1-илкарбонил)пиперазин-1-ил, 4-(трифторацетил)пиперазин-1-ил, 4-(пиперидин-1-ил)пиперидин-1-ил, 4-(пирролидин-1-ил)пиперидин-1-ил, 4-(хиназолин-4-ил)пиперазин-1-ил, 4-(пиримидин-2-ил)пиперазин-1-ил, 8-аза-1-азониаспиро[4,5]декан-8-ил, 3-(3-метилфенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-[4-(трифторметил)фенил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-[(4-фторфенокси)метил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 4-(3-цианопиридин-2-ил)пиперазин-1-ил, 1-метил-8-аза-1-азониаспиро[4,5]декан-8-ил, 3-(3,5-дифторфенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-[(диметиламино)метил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-(2-фурил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-(пентафторэтил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-{[4-(трифторметил)фенил]амино}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 4-(2-метилпролил)пиперазин-1-ил, 3-фенил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-(1,3-бензодиоксол-5-ил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3,-a]пиразин-7-ил, 3-(2-тиенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 3-циклопропил-4,5,6,7-тетрагидро-1H-пиразоло[3,4-c]пиридин-6-ил, 3-(трифторметил)-4,5,6,7-тетрагидро-1H-пиразоло[3,4-c]пиридин-6-ил, 3-(трифторметил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин-5-ил, 3-пиридин-3-ил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ил, 7-аза-1-азониаспиро[3,5]нонан-7-ил, 4-метил-2,5-диоксоимидазолидин-1-ил, 3-(пирролидин-1-илметил)азетидин-1-ил, 4-(3,3-дифторазетидин-1-ил)пиперидин-1-ил, 1-(2,2,2-трифторэтил)-4,5,6,7-тетрагидро-1H-[1,2,3]триазоло[4,5-c]пиридин-5-ил, 4-{[1-(метиламино)циклопентил]карбонил}пиперазин-1-ил, 1-метил-7-аза-1-азониаспиро[3,5]нонан-7-ил, 8-аза-2-азониаспиро[4,5]декан-8-ил, 4-[(2-пропилпирролидин-2-ил)карбонил]пиперазин-1-ил, 2-метил-8-аза-2-азониаспиро[4,5]декан-8-ил, 4-(пиперидин-3-илкарбонил)пиперазин-1-ил, 4-[(1-метилпиперидин-3-ил)карбонил]пиперазин-1-ил, 4-{[1-(диметиламино)циклопропил]карбонил}пиперидин-1-ил, 4-[3-(диметиламино)пропаноил]пиперидин-1-ил, 4-[(2-бензилпирролидин-2-ил)карбонил]пиперазин-1-ил, 4-(пирролидин-3-илкарбонил)пиперазин-1-ил, 4-{[1-(метиламино)циклопропил]карбонил}пиперазин-1-ил, 4-[(2-метилазетидин-2-ил)карбонил]пиперазин-1-ил, 4-[(1-метилпирролидин-3-ил)карбонил]пиперидин-1-ил, 4-[2-(диметиламино)-3,3,3-трифторпропаноил]пиперазин-1-ил, 4-[(2-метилпиперидин-2-ил)карбонил]пиперидин-1-ил, 4-{[1-(бензоксикарбонил)-2-метилпиперидин-2-ил]карбонил}пиперидин-1-ил, 3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил, 1-(2,2,2-трифторэтил)-1,4,6,7-тетрагидро-5H-[1,2,3]триазоло[4,5-c]пиридин-5-ил, 4-[(2S)-пирролидин-2-илацетил]пиперидин-1-ил, 1-этил-8-аза-1-азониаспиро[4,5]декан-8-ил, 1-(циклопропилметил)-8-аза-1-азониаспиро[4,5]декан-8-ил, 4-[(1-анилино циклопентил)карбонил]пиперазин-1-ил, 4-[(1-аминоциклопентил]карбонил}пиперазин-1-ил, 4-{[1-(бензиламино)циклопентил]карбонил}пиперазин-1-ил, 4-({1-[(циклопропилметил)амино]циклопентил}карбонил)пиперазин-1-ил, 4-{[1-(изобутиламино)циклопентил]карбонил}пиперазин-1-ил, 4-[2-(4-фторбензил)пролил]пиперазин-1-ил, 4-[2-(4-метилбензил)пролил]пиперазин-1-ил, 4-[2-(нафтилметил)пролил]пиперазин-1-ил и 4-(2-этилпролил)пиперазин-1-ил.
В варианте осуществления каждый из Ra и Rb независимо представляет собой водород, метил, фенил, бензил или циклопропилметил.
В другом варианте осуществления каждый из Ra и Rb независимо представляет собой водород или C1-6-алкил, например метил.
Настоящее изобретение также предоставляет соединения формулы II:
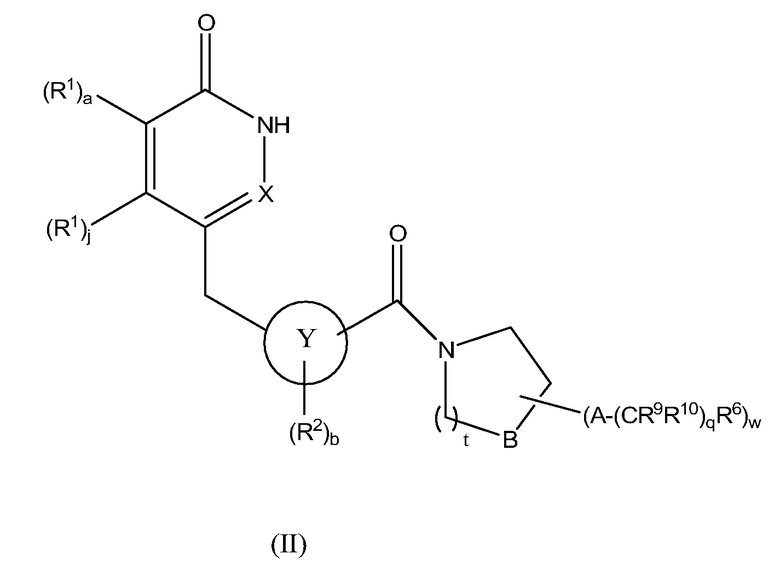 ,
,
где
a, b, j, q, A, X, Y, R1, R2, R6, R9 и R10 определены выше;
t равно 0, 1, 2 или 3;
если t равно 0, то B представляет собой CH2;
если t равно 1, 2 или 3, то B представляет собой CH2, NH или O;
w равно 0, 1, 2 или 3;
или их фармацевтически приемлемые соли или таутомеры.
С целью исключить двусмысленное толкование A-(CR9R10)qR6 может быть присоединен к циклу, содержащему B, в любом замещаемом положении.
Предпочтительные варианты осуществления со ссылкой на формулу II определены ранее для формулы I с необходимыми поправками.
В варианте осуществления каждый из R9 и R10 представляет собой водород.
В варианте осуществления t равно 3.
В варианте осуществления B представляет собой NH.
В варианте осуществления w равно 0.
Настоящее изобретение также предоставляет соединения формулы III:
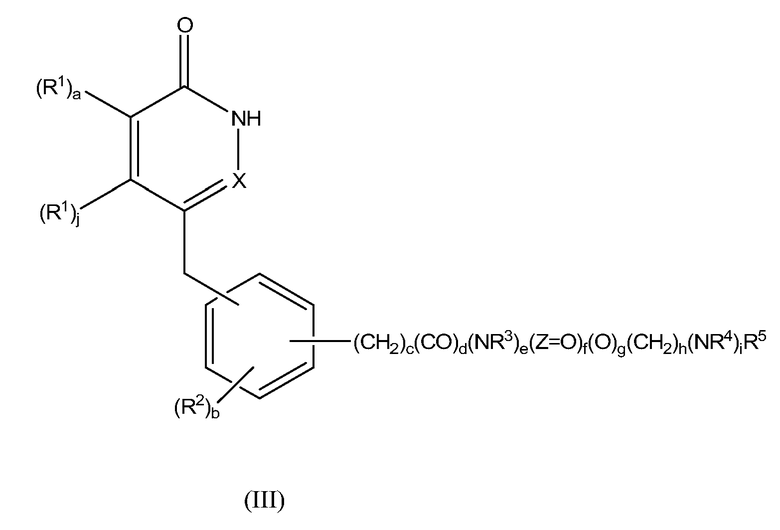 ,
,
где
a, b, c, d, e, f, g, h, i, j, X, Y, Z, R1, R2, R3, R4 и R5 определены выше;
при условии что
(a) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой O-мостик, R2 представляет собой фтор и X представляет собой N, то R5 не является необязательно замещенным циклом, выбранным из C6-10-арила, 5-членного гетероароматического кольца, 6-членного гетероароматического кольца или 7-15-членного ненасыщенного или частично насыщенного гетероциклического кольца;
(b) если X представляет собой N, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкилкарбонил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(c) если (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)i представляет собой CO-мостик и X представляет собой N, то R5 не представляет собой необязательно замещенный фенил, пиридинил, тиенил или фурил; или их фармацевтически приемлемые соли или таутомеры.
Настоящее изобретение также предоставляет соединения формулы IV:
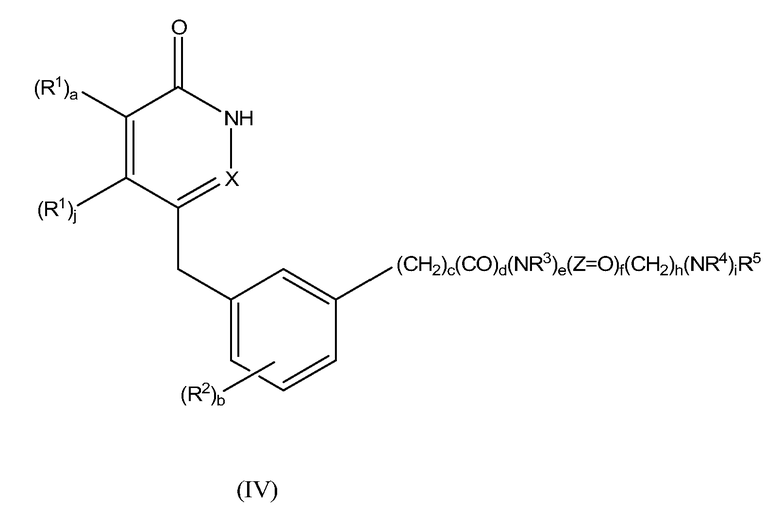 ,
,
где
a, b, c, d, e, f, h, i, j, X, Y, Z, R1, R2, R3 и R4 определены выше;
R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6;
или их фармацевтически приемлемые соли или таутомеры.
Настоящее изобретение также предоставляет соединения формулы V:
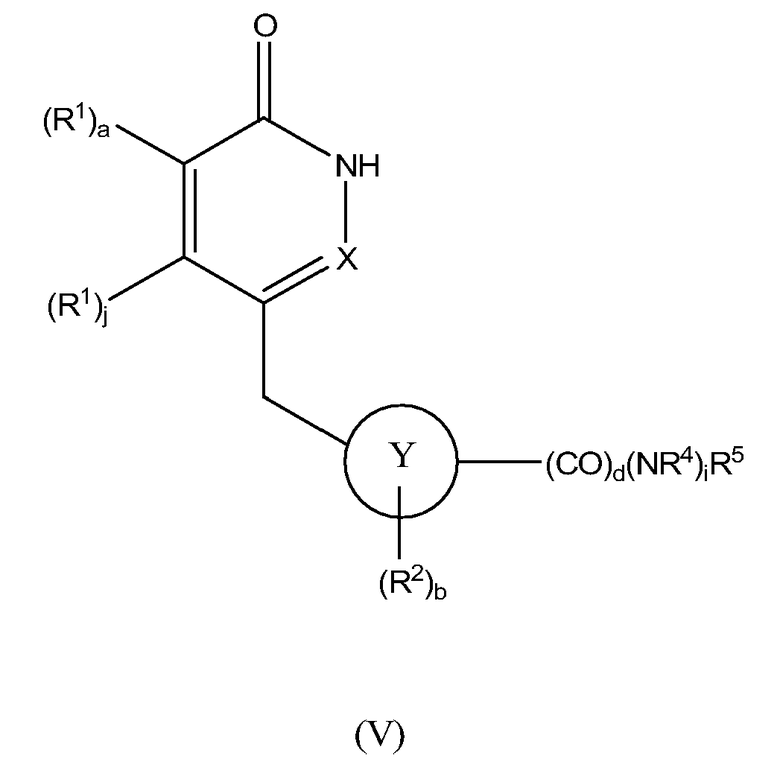 ,
,
где
a, b, d, i, j, X, Y, R1, R2, R4 и R5 определены выше; при условии что
(a) если X представляет собой N, то R5 не представляет собой C1-6-алкил, галоген-C1-6-алкил, гидрокси-C1-6-алкил, C1-6-алкокси, галоген-C1-6-алкокси, C1-6-алкилкарбонил или необязательно замещенный C3-10-циклоалкил, фенил, нафтил, пиридинил, пиридин-N-оксид, индол, индол-N-оксид, хинолин, хинолин-N-оксид, пиримидинил, пиразинил или пирролил; и
(b) если d равно 1, i равно 0 и X представляет собой N, то R5 не представляет собой необязательно замещенный фенил, пиридинил, тиенил или фурил;
или его фармацевтически приемлемую соль или таутомер.
Настоящее изобретение также предоставляет новые соединения формулы VI:
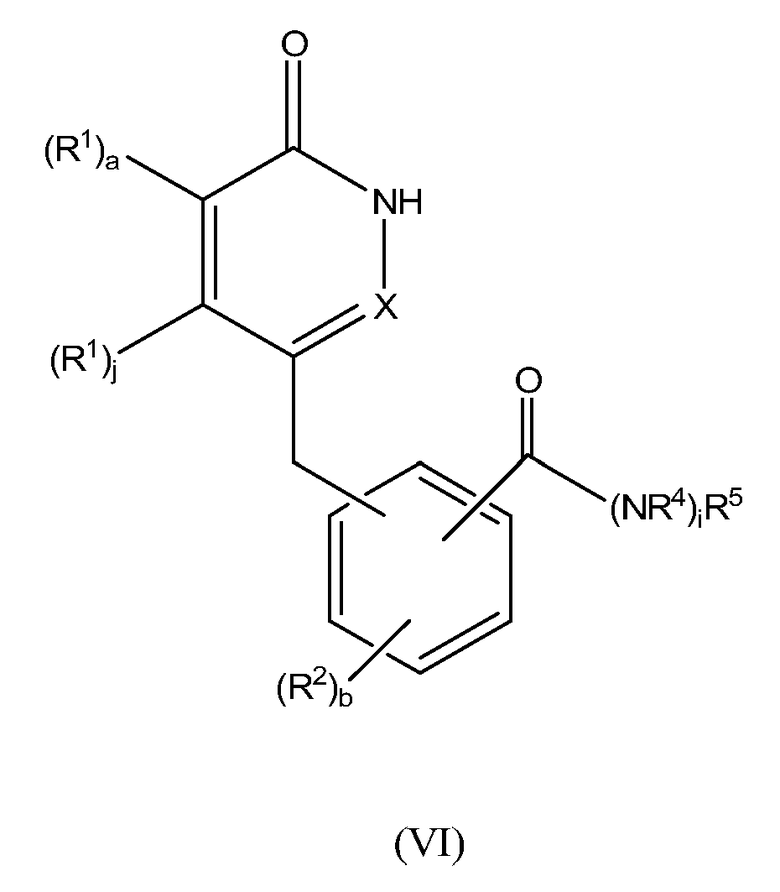 ,
,
где
a, b, c, d, e, f, h, i, j, X, Y, Z, R1, R2, R3 и R4 определены выше;
R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6;
или его фармацевтически приемлемую соль или таутомер.
Настоящее изобретение также предоставляет соединения формулы VII:
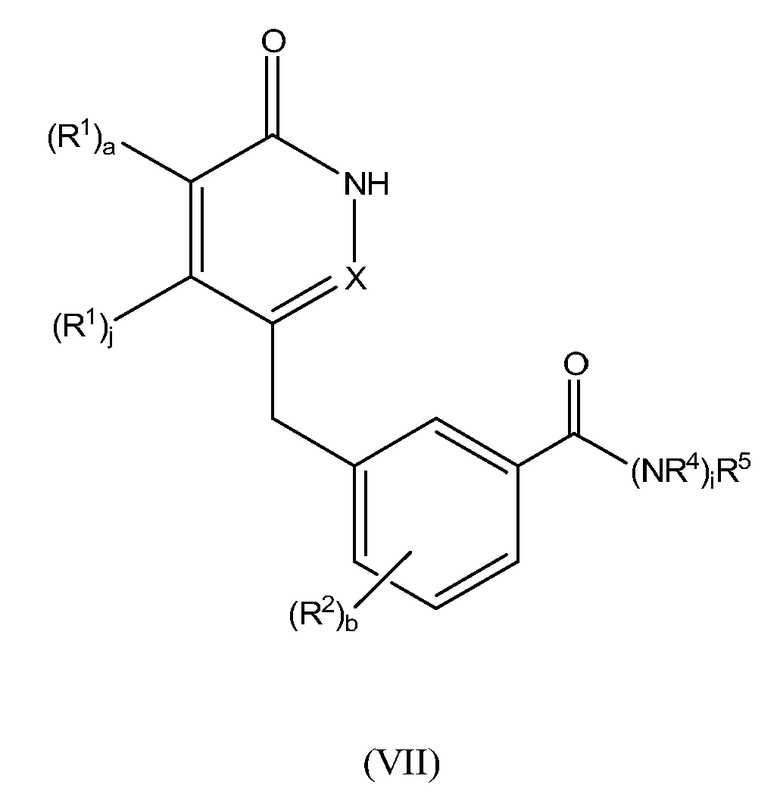 ,
,
где
a, b, j, i, X, R1, R2 и R4 определены выше;
R5 представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S; любое из указанных колец необязательно замещено одной или несколькими группами, независимо выбранными из A-(CR9R10)qR6; или его фармацевтически приемлемую соль или таутомер.
Настоящее изобретение также предоставляет соединения формулы VIII:
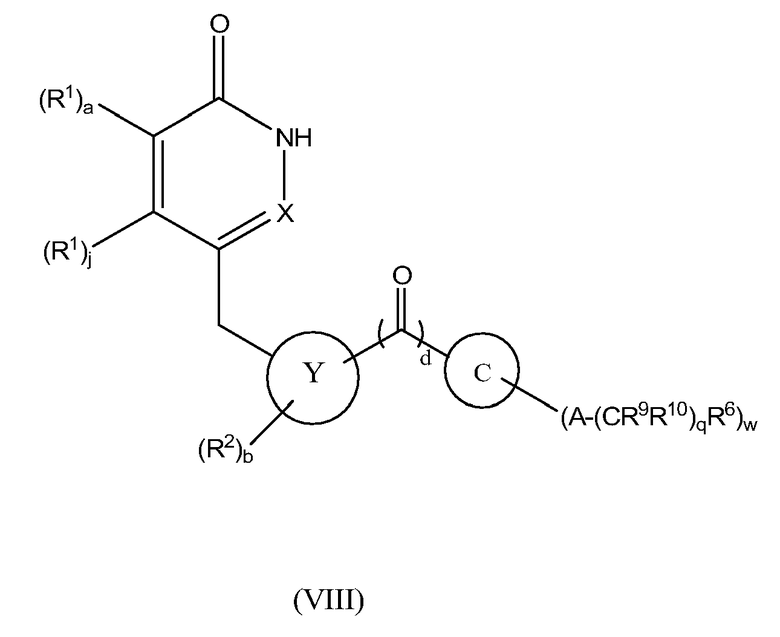 ,
,
где
a, b, d, Y, R1 и R2 определены выше;
C представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S;
или их фармацевтически приемлемые соли или таутомеры.
Настоящее изобретение также предоставляет соединения формулы IX:
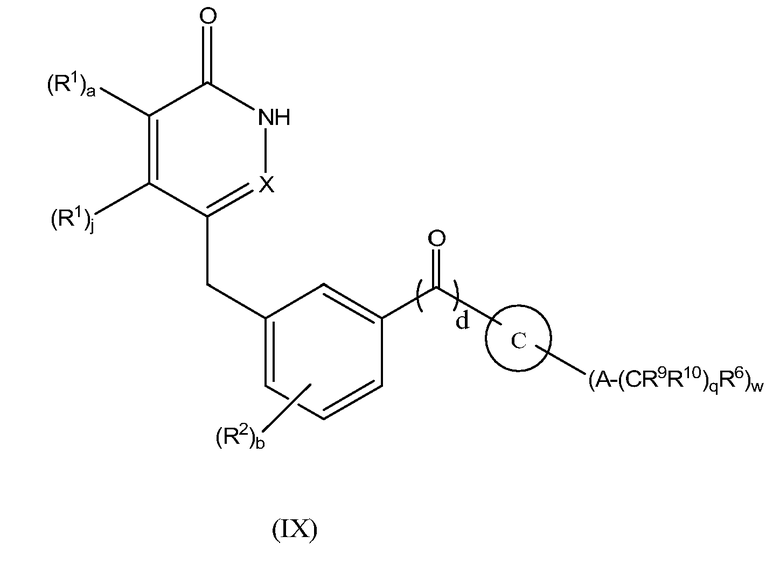 ,
,
где
a, b, d, q, j, A, R1, R2, R6, R9, R10 определены выше;
C представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, 5- или 6-членное насыщенное или частично насыщенное гетероциклическое кольцо, содержащее один, два или три атома N и ноль или один атом O, или 7-15-членное частично насыщенное или насыщенное гетероциклическое кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из N, O и S;
или их фармацевтически приемлемые соли или таутомеры.
Предпочтительные C группы представляют собой диазепанил, пиперидинил, пиперазинил, пирролидинил, спиробензофуранпиперидинил, тетрагидроимидазопиразинил, тетрагидротриазолопиразинил, диазаспиродеканил, тетрагидропиразолопиридинил, диазаспирононанил, имидазолидинил, азетидинил или тетрагидротриазолопиридинил.
В варианте осуществления предоставлены соединения по любой из формул II-XI, в которых X представляет собой N.
В варианте осуществления предоставлены соединения по любой из формул II-XI, в которых b равно 0 или 1 и R представляет собой фтор.
В варианте осуществления предоставлены соединения формул II, X и XI, w равно 0 или 1.
Предпочтительные варианты осуществления со ссылкой на формулы III, IV, V, VI, VII и VIII определены ранее для формул I и II с необходимыми поправками.
Настоящее изобретение также включает, в пределах его объема, N-оксиды соединений формулы I выше. В общем, такие N-оксиды могут быть получены из любого доступного атома азота. N-оксиды могут быть получены традиционными методами, такими как взаимодействие соединения формулы I с оксоном в присутствии влажного оксида алюминия.
Настоящее изобретение включает, в пределах его объема, пролекарства соединений формулы I выше. В общем, такие пролекарства будут являться функциональными производными соединений формулы I, которые легко конвертируемы in vivo в требующееся соединение формулы I. Традиционные методики для выбора и получения пригодных пролекарств описаны, например, в "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985.
Пролекарство может являться фармакологически неактивным производным биологически активного вещества ("исходное лекарственное средство" или "исходная молекула"), которые требуют превращения внутри организма для того, чтобы высвободить активное лекарственное средство, и которые имеют улучшенные свойства доставки по сравнению с исходной молекулой лекарственного средства. Превращение in vivo может иметь место, например, в результате некоторого метаболического процесса, такого как химический или энзиматический гидролиз карбонового, фосфорного или сульфатного сложного эфира, или при восстановлении или окислении чувствительной функциональной группы.
Настоящее изобретение включает, в пределах его объема, сольваты соединений формулы I и их солей, например гидраты.
Соединения по настоящему изобретению могут иметь асимметричные центры, хиральные оси и хиральные плоскости (как описано в E.L. Eliel and S.H. Wilen, Stereochemistry of Carbon Compounds, John Wiley & Sons, New York, 1994, pages 1119-1190) и присутствовать в виде рацематов, рацемических смесей и как индивидуальные диастереомеры, со всеми возможными изомерами и их смесями, включая оптические изомеры, все такие стереоизомеры включаются в настоящее изобретение.
Соединения, впервые описанные здесь, могут существовать как таутомеры, и обе таутомерные формы предназначены для включения в объем изобретения, даже если только изображена одна таутомерная структура. Например, соединения формулы I могут превращаться в таутомеры соединений со следующий структурой:
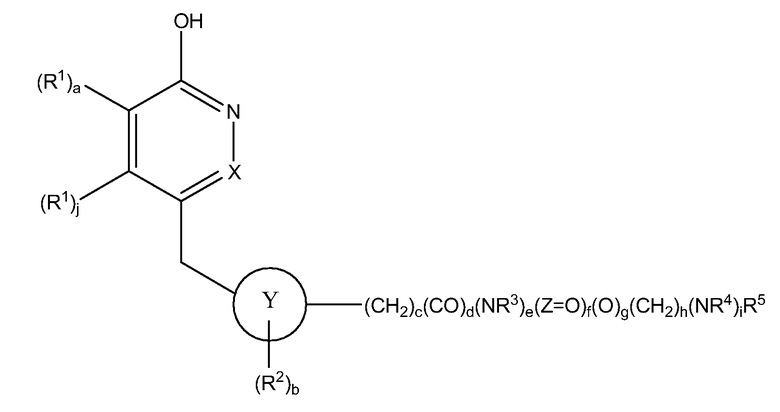
Соединения могут существовать в различных изомерных формах, все из которых включаются в объем настоящего изобретения.
Соединения могут существовать в виде ряда различных полиморфных форм.
Когда любая переменная (например, R1 и R2 и т.д.) встречается более чем один раз в любой компоненте, ее определение в каждом случае является независимым от каждого другого случая. Также сочетания заместителей и переменных являются допустимыми, только если такие сочетания приводят к стабильным соединениям. Линии, проведенные к циклическими системам от заместителей, показывают, что указанная связь может быть присоединена к любому из кольцевых атомов, допустимому для размещения заместителей.
Понятно, что заместители и тип замещения в соединениях по настоящему изобретению могут быть выбраны специалистом в области техники для получения соединений, которые являются химически стабильными и которые могут быть легко синтезировали посредством методик, известных в технике, так же как теми способами, которые указаны ниже, из легко доступных исходных веществ. Если заместитель сам по себе является замещенным более чем одной группой, понятно, что эти множественные группы могут находиться на том же атоме углерода или на различных атомах углерода, если в результате достигается стабильная структура. Фраза "необязательно замещенный" должна считаться эквивалентной фразе "незамещенный или замещенный одним или несколькими заместителями", и в таких случаях предпочтительный вариант осуществления будет иметь от нуля до трех заместителей. Более предпочтительно, имеется от нуля до двух заместителей. Заместитель в насыщенном, частично насыщенном или ненасыщенном гетероцикле может быть присоединен при любом замещаемом положении.
Применяемый здесь термин "алкил" предназначен включать как разветвленные, линейнозвенные, так и циклические насыщенные алифатические углеводородные группы, имеющие определенное число атомов углерода. Например, "C1-6-алкил" определяется как включающий группы, имеющие 1, 2, 3, 4, 5 или 6 атомов углерода линейного, разветвленного или циклического строения. Например, "C1-6-алкил" специально включает метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, изобутил, пентил, гексил, циклопропил, циклобутил, циклопентил и циклогексил и так далее. Предпочтительные алкильные группы представляют собой метил и этил. Термин "циклоалкил" обозначает моноциклическую, бициклическую или полициклическую насыщенную алифатическую углеводородную группу, имеющую определенное число атомов углерода. Например, "C3-7-циклоалкил" включает циклопропил, метилциклопропил, 2,2-диметилциклобутил, 2-этилциклопентил, циклогексил и так далее. В варианте осуществления изобретения термин "циклоалкил" включает группы, описанные непосредственно выше, и дополнительно включает моноциклические ненасыщенные алифатические углеводородные группы. Например, "циклоалкил", как определяется в этом варианте осуществления, включает циклопропил, метилциклопропил, 2,2-диметилциклобутил, 2-этилциклопентил, циклогексил, циклопентенил, циклобутенил, 7,7-диметилбицикло[2,2,1]гептил и так далее. Предпочтительные циклоалкильные группы представляют собой циклопропил, циклобутил, циклопентил и циклогексил.
Применяемый здесь термин "C2-6-алкенил" относится к неароматическому углеводородному радикалу, линейному или разветвленному, содержащему от 2 до 6 атомов углерода и по меньшей мере одну углерод-углеродную двойную связь. Предпочтительно, присутствует одна углерод-углеродная двойная связь, и могут присутствовать до четырех неароматических углерод-углеродных двойных связей. Алкенильные группы включают этенил, пропенил, бутенил и 2-метилбутенил. Предпочтительные алкенильные группы включают этенил и пропенил.
Применяемый здесь термин "C2-6-алкинил" относится к углеводородному радикалу, линейному или разветвленному, содержащему от 2 до 6 атомов углерода и по меньшей мере одну углерод-углеродную тройную связь. Могут присутствовать до трех углерод-углеродных тройных связей. Алкинильные группы включают этинил, пропинил, бутинил, 3-метилбутинил и так далее. Предпочтительные алкинильные группы включают этинил и пропинил.
"Алкокси" представляет собой алкильную группу указанного числа атомов углерода, присоединенную через кислородный мостик. "Алкокси", таким образом, включает определение алкила, приведенное выше. Примеры приемлемых алкоксигрупп включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси, трет-бутокси, циклопропилокси, циклобутилокси и циклопентилокси. Предпочтительные алкоксигруппы представляют собой метокси и этокси. Термин "C6-10-арилокси" может рассматриваться аналогичным образом. Предпочтительной из таких групп является фенокси.
Термины "галоген-C1-6-алкил" и "галоген-C1-6-алкокси" обозначают C1-6-алкил или C1-6-алкоксигруппу, в который один или несколько (в частности, 1-3) атомов водорода замещены на атомы галогена, особенно атомы фтора или хлора. Предпочтительными являются фтор-C1-6-алкил и фтор-C1-6-алкоксигруппы, в частности фтор-C1-3-алкил и фтор-C1-3-алкоксигруппы, например CF3, CHF2, CH2F, CH2CH2F, CH2CHF2, CH2CF3, OCF3, OCHF2, OCH2F, OCH2CH2F, OCH2CHF2 или OCH2CF3, и наиболее предпочтительно CF3, OCF3 и OCHF2.
Применяемый здесь термин "гидрокси-C1-6-алкил" обозначает группу, в которой один или несколько (в частности, 1-3) атомов водорода замещены на гидроксигруппы. Предпочтительными являются CH2OH, CH2CHOH и CHOHCH3.
Применяемый здесь термин "C1-6-алкилкарбонил" или "C1-6-алкоксикарбонил" обозначает C1-6-алкильный или C1-6-алкоксильный радикал соответственно, присоединенный через карбонильный (C=O) радикал. Приемлемые примеры С1-6-алкилкарбонильных групп включают метилкарбонил, этилкарбонил, пропилкарбонил, изопропилкарбонил и трет-бутилкарбонил. Примеры C1-6-алкоксикарбонила включают метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил и трет-бутоксикарбонил. Термин "C6-10-арилкарбонил" может быть истолкован аналогичным образом.
Циклы, присутствующие в соединениях по настоящему изобретению, могут являться моноциклическими или полициклическими, особенно бициклическими. Полициклические кольца могут являться конденсированными, мостиковыми или спиросочлененными.
Применяемый здесь термин "C6-10-арил" предназначен обозначать любой стабильный моноциклический или бициклический углеродный цикл, имеющий от 6 до 10 атомов, где по меньшей мере один цикл является ароматическим. Примеры таких арильных фрагментов включают фенил, нафтил, тетрагидронафтил, инданил и тетрагидробензо[7]аннулен. Предпочтительная арильная группа представляет собой фенил или нафтил, особенно фенил.
7-15-членные гетероциклы включают 7-, 8-, 9-, 10-, 11-, 12-, 13-, 14- и 15-членные гетероциклы.
Примерами предпочтительных гетероциклов по настоящему изобретению являются бензимидазолил, бензофурандионил, бензофуранил, бензофуразанил, бензопиразолил, бензотриазолил, бензотиенил, бензоксазолил, бензоксазолонил, бензотиазолил, бензотиадиазолил, бензодиоксолил, бензоксадиазолил, бензоизоксазолил, бензоизотиазолил, хроменил, хроманил, изохроманил, карбазолил, карболинил, циннолинил, эпоксидил, фурил, фуразанил, имидазолил, индолинил, индолил, индолизинил, индолинил, изоиндолинил, индазолил, изобензофуранил, изоиндолил, изохинолил, изотиазолил, изоксазолил, нафтпиридинил, оксадиазолил, оксазолил, оксазолинил, изоксазолинил, оксетанил, пуринил, пиранил, пиразинил, пиразолил, пиридазинил, пиридопиридинил, пиридазинил, пиридинил, пиримидинил, триазинил, тетразинил, пирролил, хиназолинил, хинолинил, хиноксалинил, хинолизинил, тетрагидропиранил, тетрагидротиопиранил, тетрагидроизохинолинил, тетразолил, тетразолопиридил, тиадиазолил, тиазолил, тиенил, триазолил, азетидинил, 1,4-диоксанил, гексагидроазепинил, пиперазинил, пиперидил, пиридин-2-онил, пирролидинил, имидазолинил, имидазолидинил, пиразолинил, пирролинил, морфолинил, тиоморфолинил, дигидробензоимидазолил, дигидробензофуранил, дигидробензотиофенил, дигидробензоксазолил, дигидрофуранил, дигидроимидазолил, дигидроиндолил, дигидроизооксазолил, дигидроизотиазолил, дигидрооксадиазолил, дигидрооксазолил, дигидропиразинил, дигидропиразолил, дигидропиридинил, дигидропиримидинил, дигидропирролил, дигидрохинолинил, дигидроизохинолинил, дигидротетразолил, дигидротиадиазолил, дигидротиазолил, дигидротиенил, дигидротриазолил, дигидроазетидинил, дигидроизохроменил, дигидрохроменил, дигидроимидазолонил, дигидротриазолонил, дигидробензодиоксиинил, дигидротиазолопиримидинил, дигидроимидазопиразинил, метилендиоксибензоил, тетрагидрофуранил, тетрагидротиенил, тетрагидрохинолинил, тиазолидинонил, имидазолонил, изоиндолинонил, октагидрохинолизинил, октагидроизоиндолил, имидазопиридинил, азабициклогептанил, хроменонил, триазолопиримидинил, дигидробензоксазинил, тиазолотриазолил, азониабициклогептанил, азониабициклооктанил, фталазинил, нафтиридинил, хиназолинил, птеридинил, дигидрохиназолинил, дигидрофталазинил, бензизоксазолил, тетрагидронафтиридинил, дибензо[b,d]фуранил, дигидробензотиазолил, имидазотиазолил, тетрагидроиндазолил, тетрагидробензотиенил, гексагидронафтиридинил, тетрагидроимидазопиридинил, тетрагидроимидазопиразинил, пирролопиридинил, диазепанил и их N-оксиды. Дополнительные примеры включают спиробензофуранпиперидинил, тетрагидротриазолопиразинил, диазаспиродеканил, тетрагидропиразолопиридинил, диазаспирононанил и тетрагидротриазолопиридинил.
Предпочтительный 4-членный насыщенный гетероцикл представляет собой азетидинил. Присоединение гетероциклического заместителя может иметь место через атом углерода или через гетероатом.
Предпочтительными 5-, 6- или 7-членными насыщенными или частично насыщенными гетероциклами являются пирролидинил, пиперидинил, пиперазинил, морфолинил, тетрагидрофуран, тиоморфолинил и диазепанил. Более предпочтительным циклом является имидазолидинил.
Предпочтительными 5-членными гетероароматическими кольцами являются тиенил, тиазолил, пиразолил, изоксазолил, изотиазолил, имидазолил, тиадиазолил, оксазолил, оксадиазолил, триазолил, тетразолил, фурил и пирролил.
Предпочтительными 6-членными гетероароматическми циклами являются пиридинил, пиримидинил, пиридазинил и пиразинил.
Предпочтительными 7-10-членными частично насыщенными или ненасыщенными гетероциклическими кольцами являются тетрагидрохинолинил, хинолинил, индолил, имидазопиридинил, бензотиазолил, хиноксалинил, бензотиадиазолил, бензоксазолил, дигидробензодиоксинил, бензотриазолил, бензодиоксолил, дигидроизоиндолил, дигидроиндолил, тетрагидроизохинолинил, изохинолинил, бензоизотиазолил, дигидроимидазопиразинил, бензотиенил, бензоксадиазолил, тиазолотриазолил, дигидротиазолопиримидинил, дигидробензоксазинил, дигидробензофуранил, бензимидазолил, бензофуранил, дигидробензоксазолил, дигидрохиназолинил, дигидрофталазинил, индазолил, бензизоксазолил, тетрагидронафтиридинил, триазолопиримидинил, дибензо[b,d]фуранил, нафтиридинил, дигидрохинолинил, дигидроизохроменил, дигидрохроменил, дигидробензотиазолил, имидазотиазолил, тетрагидроиндазолил, тетрагидробензотиенил, гексагидронафтиридинил, тетрагидроимидазопиридинил, тетрагидроимидазопиразинил, пирролопиридинил, хиназолинил и индолизинил. Дополнительные 7-15-членные ненасыщенные, частично насыщенные или насыщенные гетероциклические кольца включают спиробензофуранпиперидинил, тетрагидротриазолопиразинил, диазаспиродеканил, тетрагидропиразолопиридинил, диазаспирононанил и тетрагидротриазолопиридинил.
Применяемый здесь термин "галоген" относится к фтору, хлору, брому и йоду, из которых фтор и хлор являются предпочтительными.
Предпочтительные соединения в пределах объема настоящего изобретения представляют собой
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
6-{3-[(4-ацетил-1,4-диазепан-1-ил)карбонил]-4-фторбензил}-4-этилпиридазин-3(2H)-он;
1-ацетил-4-{5-[(6-хлор-4-этилпиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан;
и их фармацевтически приемлемые соли, свободные основания и таутомеры.
Особенно предпочтительные соединения в пределах объема настоящего изобретения представляют собой
4-этил-6-(4-фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)пиридазин-3(2H)-он;
трифторацетат 4-{5-[(5-этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{2-фтор-5-[(5-изопропил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 1-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,2-диметил-1-оксопропан-2-аммония;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-1-азониаспиро[4,5]декан;
бис(трифторацетат) 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-2-ий-3-ил)метил]-2-фторбензоил}-1-метил-8-аза-1-азониаспиро[4,5]декана;
трифторацетат 4-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-N,N-диметил-2-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензоламмония;
трифторацетат 6-(4-изопропокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
6-(4-фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он;
6-(4-фтор-3-{[4-(2-метилпролил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-[4-фтор-3-(4-метил-2,5-диоксоимидазолидин-1-ил)бензил]-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(3-{[3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}-4-фторбензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат (2R)-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилазетидиния;
трифторацетат 6-{4-фтор-3-[(4-{[1-(изобутиламино)циклопентил] карбонил}пиперазин-1-ил)карбонил]бензил}-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ил)пиримидин-1-ия;
трифторацетат 4-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пиридиния;
трифторацетат 2-{[(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)окси]метил}пиридиния;
трифторацетат 2-{[(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-3-ил)окси]метил}пиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-5-метоксипиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-4-метоксипиридиния;
трифторацетат 4-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пирролидин-3-ил)пиридиния;
трифторацетат 1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-3-ил)-N,N-диметилметанаммония;
4-этил-6-[4-фтор-3-(1'Η-спиро[1-бензофуран-3,4'-пиперидин]-1'-илкарбонил)бензил]пиридазин-3(2H)-он;
трифторацетат 1-[2-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)этил]-1H-пиразол-2-ия;
трифторацетат 5-хлор-2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-6-метоксипиридиния;
трифторацетат 3-бензил-7-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидроимидазо[1,2-a]пиразин-1-ия;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-3,6-диметилпиразин-1-ия;
трифторацетат 4-этил-6-{4-фтор-3-[(3-фенил-5,6-дигидроимидазо[1,2-a]пиразин-7(8H)-ил)карбонил]бензил}-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-(3-метоксибензил)пиперазин-1-ия;
трифторацетат 2-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)-1,2,3,4-тетрагидроизохинолиния;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-фенилпиперазин-1-ия;
трифторацетат 3-бензил-4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
бис(трифторацетат) 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-2-(пиридиний-3-илметил)пиперазин-1-ия;
6-(3-{[4-(циклопентилкарбонил)-1,4-диазепан-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2H)-он;
6-(3-{[4-(циклопентилкарбонил)-1,4-диазепан-1-ил]карбонил}-4-фторбензил)-4-этилпиридазин-3(2H)-он;
трифторацетат 4-{5-[(4,5-диэтил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{2-фтор-5-[(5-изопропил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
6-{4-фтор-3-[(4-пропионилпиперазин-1-ил)карбонил]бензил}-4,5-диметилпиридазин-3(2H)-он;
6-(3-{[4-(дифторацетил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2H)-он;
6-(4-фтор-3-{[4-(3,3,3-трифторпропаноил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-{4-фтор-3-[(4-изобутирилпиперазин-1-ил)карбонил]бензил}-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пиридиния;
6-(4-фтор-3-{[4-(тетрагидрофуран-2-илкарбонил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 1-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,N,2-триметил-1-оксопропан-2-аммония;
трифторацетат 6-(4-фтор-3-{[4-(2,2,3,3,3-пентафторпропаноил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(4-фтор-3-{[4-(пирролидин-1-илкарбонил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(4-фтор-3-{[4-(трифторацетил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 1-(1-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пиперидиния;
трифторацетат 1-(1-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пирролидиния;
трифторацетат 4-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)хиназолин-1-ия;
трифторацетат 2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиримидин-1-ия;
бис(трифторацетат) 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(3-метилфенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1,4-диия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-[4-(трифторметил)фенил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-[(4-фторфенокси)метил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-2-ия;
трифторацетат 3-циано-2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиридиния;
трифторацетат 3-(3,5-дифторфенил)-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
бис(трифторацетат) 3-[(диметиламмонио)метил]-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-2-ия;
трифторацетат (7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-3-ил)-N,N-диметилметанаммония;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(2-фурил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(пентафторэтил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-{[4-(трифторметил)фенил]амино}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
хлорид 2-[(4-{2-фтор-5-[(6-гидрокси-4,5-диметилпиридазин-3-ил)метил]бензоил}пиперазин-1-ил)карбонил]-2-метилпирролидиния;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-фенил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 3-(1,3-бензодиоксол-5-ил)-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(2-тиенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия;
трифторацетат 3-циклопропил-6-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-4,5,6,7-тетрагидро-1H-пиразоло[3,4-c]пиридин-2-ия;
трифторацетат 6-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(трифторметил)-4,5,6,7-тетрагидро-1H-пиразоло[3,4-c]пиридин-2-ия;
трифторацетат 5-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(трифторметил)-4,5,6,7-тетрагидро-1H-пиразоло[4,3-c]пиридин-2-ия;
бис(трифторацетат) 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-пиридиний-3-ил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-2-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-7-аза-1-азониаспиро[3,5]нонана;
трифторацетат 1-[(1-{3-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}азетидин-3-ил)метил]пирролидиния;
трифторацетат 1-(1-{3-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)-3,3-дифторазетидиния;
трифторацетат 5-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-(2,2,2-трифторэтил)-4,5,6,7-тетрагидро-1H-[1,2,3]триазоло[4,5-c]пиридин-3-ия;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N-метилциклопентанаммония;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-метил-7-аза-1-азониаспиро[3,5]нонана;
трифторацетат 6-(4-метокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-2-азониаспиро[4,5]декана;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-пропилпирролидиния;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-2-метил-8-аза-2-азониаспиро[4,5]декана;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пиперидиния;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-1-метилпиперидиния;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N,N-диметилциклопропанаммония;
трифторацетат 3-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,N-диметил-3-оксопропан-1-аммония;
трифторацетат 2-бензил-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пирролидиния;
трифторацетат 4,5-диметил-6-(3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)пиридазин-3(2H)-он;
трифторацетат 6-[3-(1,8-диазаспиро[4,5]дец-8-илкарбонил)-4-фторбензил]-4-этил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пирролидиния;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N-метилциклопропанаммония;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-1-метилпирролидиния;
трифторацетат 3-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-1,1,1-трифтор-N,N-диметил-3-оксопропан-2-амминия;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилпиперидиния;
бензил 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилпиперидин-1-карбоксилат;
4-этил-6-(4-фтор-3-{[1-(2,2,2-трифторэтил)-1,4,6,7-тетрагидро-5h-[1,2,3]триазоло[4,5-c]пиридин-5-ил]карбонил}бензил)пиридазин-3(2H)-он;
трифторацетат 4-этил-6-{4-фтор-3-[(1-метил-1,8-диазаспиро[4,5]дец-8-ил)карбонил]бензил}-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат (2S)-2-[2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-2-оксоэтил]пирролидиния;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-этил-8-аза-1-азониаспиро[4,5]декана;
трифторацетат 1-(циклопропилметил)-8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-1-азониаспиро[4,5]декана;
6-[3-({4-[(1-анилиноциклопентил)карбонил]пиперазин-1-ил}карбонил)-4-фторбензил]-4,5-диметилпиридазин-3(2H)-он;
6-[3-({4-[(1-аминоциклопентил)карбонил]пиперазин-1-ил}карбонил)-4-фторбензил]-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-{3-[(4-{[1-(бензиламино)циклопентил]карбонил}пиперазин-1-ил)карбонил]-4-фторбензил}-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-(3-{[4-({1-[(циклопропилметил)амино]циклопентил}карбонил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(4-фторбензил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(4-метилбензил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(1-нафтилметил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2H)-он;
трифторацетат 6-(3-{[4-(2-этилпролил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2H)-он;
и их фармацевтически приемлемые соли, свободные основания и таутомеры.
В настоящее изобретение включены соединения формулы I в виде свободных оснований, а также их фармацевтически приемлемые соли и стереоизомеры. Соединения по настоящему изобретению могут быть протонированы по атому(ам) азота амина и/или содержащему атом азота гетероциклическому фрагменту с образованием соли. Термин "свободное основание" относится к аминным соединениям в несолевой форме. Включенные фармацевтически приемлемые соли не только включают соли, представленные примерами описанных здесь специфических соединений, но также все типичные фармацевтически приемлемые соли свободных форм соединений формулы I. Свободная форма специфической соли описанных соединений может быть выделена с применением методик, известных в технике. Например, свободная форма может быть регенерирована путем обработки соли с пригодным разбавленным водным раствором основания, таким как разбавленный водный NaOH, карбонат калия, аммиак и бикарбонат натрия. Свободные формы могут до некоторой степени отличаться от их соответствующих солевых форм по определенным физическим свойствам, таким как растворимость в полярных растворителях, но соли присоединения кислоты и основания являются фармацевтически эквивалентными их соответствующим свободным формам для целей изобретения.
Фармацевтически приемлемые соли соединений по настоящему изобретению могут быть синтезированы из соединений по настоящему изобретению, которые содержат основный или кислотный фрагмент, традиционными химическими способами. В целом, соли основных соединений приготавливаются или путем ионообменной хроматографии или путем реакции свободного основания со стехиометрическими количествами или с избытком желаемой солеобразующей неорганической или органической кислоты в пригодном растворителе или различных сочетаний растворителей. Аналогичным образом, соли кислотных соединений приготавливаются реакциями с соответствующим неорганическим или органическим основанием.
Таким образом, фармацевтически приемлемые соли соединений по настоящему изобретению включают традиционные нетоксичные соли соединений по настоящему изобретению, как образуемых путем реакции основного соединения по настоящему изобретению с неорганической, органической или полимерной кислотой. Например, традиционные нетоксичные соли включают те, что произведены от неорганических кислот, таких как соляная, бромистоводородная, йодистоводородная, серная, сернистая, сульфаминовая, фосфорная, фосфористая, азотная и подобные, а также соли, полученные из органических кислот, таких как уксусная, пропионовая, янтарная, гликолевая, стеариновая, молочная, яблочная, винная, лимонная, аскорбиновая, памовая, малеиновая, гидроксималеиновая, фенилуксусная, глутаминовая, бензойная, салициловая, сульфаниловая, 2-ацетоксибензойная, фумаровая, толуолсульфоновая, метансульфоновая, этандисульфоновая, щавелевая, изотионовая, пальмитиновая, глюконовая, аскорбиновая, фенилуксусная, аспаргиновая, коричная, пировиноградная, этансульфоновая, этандисульфоновая, валериановая, трифторуксусная и подобные. Примеры пригодных полимерных солей включают те, что произведены от полимерных кислот, таких как дубильная кислота, карбоксиметилцеллюлоза. Предпочтительно, фармацевтически приемлемая соль по настоящему изобретению содержит 1 эквивалент соединения формулы (I) и 1, 2 или 3 эквивалента неорганической или органической кислоты. Более предпочтительно, фармацевтически приемлемые соли по настоящему изобретению представляют собой трифторацетатные или хлоридные соли, особенно трифторацетатные соли.
Когда соединение по настоящему изобретению является кислотным, термин пригодные "фармацевтически приемлемые соли" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований, включая неорганические основания и органические основания. Соли, полученные из неорганических оснований, включают алюминиевые, аммониевые, кальциевые, медные, трехвалентного железа, двухвалентного железа, литиевые, магниевые, соли трехвалентного марганца, двухвалентного марганца, калиевые, натриевые, цинковые и подобные. Особенно предпочтительными являются аммониевые, кальциевые, магниевые, калиевые и натриевые соли. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклические амины и анионные ионообменные смолы, такие как аргининовые, лизиновые, с бетаином кофеина, холиновые, N,N1-дибензилэтилендиаминовые, этиламиновые, диэтиламиновые, 2-диэтиламиноэтаноловые, 2-диметиламиноэтаноловые, этаноламиновые, диэтаноламиновые, этилендиаминовые, N-этилморфолиновые, N-этилпиперидиновые, глюкаминовые, глюкозаминовые, гистидиновые, гидрабаминовые, изопропиламиновые, лизиновые, метилглюкаминовые, морфолиновые, пиперазиновые, пиперидиновые, полиаминовые смолы, прокаиновые, пуриновые, теоброминовые, триэтиламиновые, триметиламиновые, трипропиламиновые, трометаминовые, дициклогексиламиновые, бутиламиновые, бензиламиновые, фенилбензиламиновые, трометаминовые и подобные.
Получение фармацевтически приемлемых солей описано выше, и другие типичные фармацевтически приемлемые соли более полно описаны в Berg et al. (1977) J. Pharm. Sci., "Pharmaceutical Salts", 66:1-19.
Можно также отметить, что соединения по настоящему изобретению потенциально являются внутренними солями или цвиттерионами, так как в физиологических условиях депротонированный кислотный фрагмент в соединении, такой как карбоксильная группа, может являться анионным, и этот электрический заряд может затем внутри молекулы уравновешивать катионный заряд протонированного или алкилированного основного фрагмента, такого как четвертичный атом азота.
Соединения по изобретению могут быть применены в способе лечения человека или животного с помощью лекарственной терапии.
Изобретение предоставляет соединения для применения для лечения и предупреждения состояний, которые могут быть улучшены путем ингибирования поли(ADP-рибоза)полимеразы (PARP) (см., например, Nature Review Drug Discovery (2005) 4:421-440).
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP).
Настоящее изобретение также предоставляет способ лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования поли(ADP-рибоза)полимеразы (PARP), где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Ингибиторы PARP по настоящему изобретению могут быть применены для лечения болезней, определенных в WO 2005/082368.
Соединения по изобретению могут быть применены для лечения воспалительных заболеваний, включая состояния, полученные в результате отторжения трансплантации органа, таких как хронические воспалительные заболевания суставов, включая артрит, ревматоидный артрит, остеоартрит и заболевания костей, связанные с увеличенной резорбцией кости; воспалительные заболевания кишечника, такие как илеиты, язвенный колит, синдром Баррета и болезнь Крона; воспалительные легочные заболевания, такие как астма, синдром респираторного дистресса у взрослых и хронический обструктивный легочный синдром; воспалительные заболевания глаз, включая дистрофию роговицы, трахому, онхоцеркоз, увеит, симпатическое воспаление глаза и эндофтальмит; хронические воспалительные заболевания десен, включая гингивиты и периодонтиты; туберкулез; проказу; воспалительные заболевания почек, включая осложнения на почках, гломерулонефрит и нефроз; воспалительные заболевания кожи, включая склеродерматит, псориаз и экзему; воспалительные заболевания центральной нервной системы, включая хронические демиелинизирующие заболевания нервной системы, рассеянный склероз, обусловленную СПИД дегенерацию нервной ткани и болезнь Альцгеймера, инфекционный менингит, энцефаломиелит, болезнь Паркинсона, болезнь Гентингтона, боковой амиотрофический склероз и вирусный или аутоиммунный энцефалит; осложнения при диабете, включая, без ограничения, иммунокомплексный васкулит, системную красную волчанку (SLE); воспалительные заболевания сердца, такие как кардиомиопатия, ишемическая болезнь сердца, гиперхолестеринемия и атеросклероз; а также другие различные заболевания, которые могут иметь значительные компоненты воспаления, включая преклампсию, хроническую недостаточность печени, травму мозга и спинного мозга и синдром множественной дисфункции органов (MODS) (множественная недостаточность органов (MOF)). Воспалительная болезнь также может представлять собой системное воспаление организма, представленное примерами грам-положительного или грам-отрицательного шока, геморрагического или анафилактического шока или шока, вызываемого противораковой химиотерапией, как ответ на провоспалительные цитокины, например шока, ассоциированного с провоспалительными цитокинами. Такой шок может быть вызван, например, химиотерапевтическим препаратом, который вводится с целью лечения рака.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения воспалительных заболеваний.
Настоящее изобретение также предоставляет способ лечения или предупреждения воспалительных заболеваний, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения реперфузионных травм, полученных от естественным образом происходящих эпизодов и в течение хирургических вмешательств, таких как кишечное реперфузионное повреждение; миокардиальное реперфузионное повреждение; реперфузионное повреждение, полученное при операции на сердце в условиях искусственного кровообращения, хирургическая операция по поводу аневризмы аорты, хирургическая эндартерэктомия на сонной артерии или геморрагический шок; и повреждение при восстановлении насыщения кислородом, полученное при трансплантации органов, таких как сердце, легкое, печень, почка, поджелудочная железа, кишка и роговица.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения реперфузионных травм.
Настоящее изобретение также предоставляет способ лечения или предупреждения реперфузионных травм, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены при лечении и предотвращении ишемических состояний, включая те, что получены при трансплантации органа, таких как стабильная стенокардия, нестабильная стенокардия, ишемия миокарда, печеночная ишемия, мезентериальная ишемия артерии, кишечная ишемия, кризисная ишемия конечности, хроническая кризисная ишемия конечности, церебральная ишемия, острая сердечная ишемия, ишемическая болезнь почки, ишемическая болезнь печени, ишемическое расстройство сетчатки, септический шок и ишемическая болезнь центральной нервной системы, такая как удар или церебральная ишемия.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения ишемических состояний.
Настоящее изобретение также предоставляет способ лечения или предупреждения ишемических состояний, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения удара.
Настоящее изобретение также предоставляет способ лечения или предупреждения удара, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения хронической или острой почечной недостаточности.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения почечной недостаточности.
Настоящее изобретение также предоставляет способ лечения или предупреждения почечной недостаточности, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения сосудистых заболеваний, отличных от кардиососудистых заболеваний, таких как периферическое окклюзивное поражение артерии, облитерирующий тромбоваскулит, болезнь и синдром Рейнауда, акроцианоз, эритромелалгия, тромбоз вен, варикоз вен, артериовенозная фистула, лимфедема и липедема.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения сосудистых заболеваний, отличных от кардиососудистых заболеваний.
Настоящее изобретение также предоставляет способ лечения или предупреждения сосудистых заболеваний, отличных от кардиососудистых заболеваний, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения кардиососудистых заболеваний, таких как хроническая сердечная недостаточность, атеросклероз, застойная сердечная недостаточность, шок кровообращения, кардиомиопатия, пересадка сердца, инфаркт миокарда и аритмия сердца, такая как фибрилляция предсердий, суправентрикулярная тахикардия, трепетание предсердий и пароксизмальная суправентрикулярная тахикардия.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения кардиососудистых заболеваний.
Настоящее изобретение также предоставляет способ лечения или предупреждения кардиососудистых заболеваний, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения и предупреждения сахарного диабета, включая диабет I типа (инсулинзависимый сахарный диабет), диабет II типа (независимый от инсулина сахарный диабет), диабет при беременности, аутоиммунный диабет, инсулинопатии, диабет, обусловленный заболеванием поджелудочной железы, диабет, ассоциированный с другими эндокринными болезнями (такими, как синдром Кушинга, акромегалия, хромаффиноцитома, глюкагонома, первичный альдостеронизм или соматостатинома), синдром устойчивости к инсулину типа A, синдром устойчивости к инсулину типа B, липатрофический диабет и диабет, вызываемый 3-клеточными токсинами. Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения осложнений при диабете, таких как диабетическая катаракта, глаукома, ретинопатия, нефропатия (такая, как микроалюминурия и прогрессирующая диабетическая нефропатия), полиневропатия, гангрена ноги, атеросклероз коронарной артерии, болезнь периферических артерий, некетонная гипергликемическая-гиперосмотическая кома, мононевропатия, вегетативная невропатия, язвы на ногах, заболевания суставов и осложнения на коже или слизистых (такие, как инфекция, пятна на голени, кандидозная инфекция или местный липоидный некроз при диабетическом ожирении), гиперлипидемия, гипертензия, синдром устойчивости к инсулину, болезнь коронарной артерии, ретинопатия, диабетическая невропатия, полиневропатия, мононевропатии, вегетативная невропатия, язва ног, заболевание сустава, грибковая инфекция, бактериальная инфекция и кардиомиопатия.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения диабета.
Настоящее изобретение также предоставляет способ лечения или предупреждения диабета, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения рака, включая солидные опухоли, такие как фибросаркома, миксосаркома, липосаркома, хондросаркома, остеогенная саркома, хордома, ангиопластическая саркома, эндотелиосаркома, лимфангиосаркома, лимфангиоэндотелиосаркома, синовиома, мезотелиома, опухоль Юинга, леймиосаркома, рабдомиосаркома, рак ободочной кишки, колоректальный рак, рак почки, рак поджелудочной железы, рак кости, рак груди, рак яичников, рак простаты, рак пищевода, рак желудка, рак ротовой полости, рак носовой полости, рак гортани, сквамозно-клеточная карцинома, базальноклеточная карцинома, аденокарцинома, карцинома потовых желез, карцинома сальных желез, сосочковая карцинома, папиллярные аденокарциномы, цистаденокарцинома, карцинома мозга, бронхогенная карцинома, почечноклеточная карцинома, гепатома, карцинома желчных протоков, хориокарцинома, сперматоцитома, эмбриональная карцинома, опухоль Вильмса, рак шейки матки, рак матки, рак яичка, мелкоклеточная карцинома легкого, карцинома мочевого пузыря, рак легкого, эпителиальная карцинома, рак кожи, меланома, нейробластома и ретинобластома; раки крови, такие как острая лимфобластная лейкемия ("ALL"), острая лимфобластная B-клеточная лейкемия, острая лимфобластная T-клеточная лейкемия, острая миелобластная лейкемия ("AML"), острая промиелоцитарная лейкемия ("APL"), острая монобластная лейкемия, острая эритролейкозная лейкемия, острая мегакариобластная лейкемия, острая миеломоноцитная лейкемия, острая нелимфоцитная лейкемия, острая недифференцированная лейкемия, хроническая миелоцитарная лейкемия ("CML"), хроническая лимфоцитарная лейкемия ("CLL"), волосковоклетчатая лейкемия и множественная миелома; острая и хроническая лейкемии, такие как лимфобластная, миелогенная, лимфоцитарная, миелоцитарная лейкемии; лимфомы, такие как лимфогранулематоз, не-ходжкинская лимфома, множественная миелома, макроглобулинемия Вальденсброма, болезнь тяжелых цепей и полицитемия Вакеза-Ослера; рак ЦНС и рак мозга, такие как глиома, пилоидная астроцитома, астроцитома, анапластическая астроцитома, множественная глиобластома, медулобластома, краниофарингиома, эпендимальная глиома, аденома шишковидного тела, гемангиобластома, слуховая неврома, олигодендроглиома, менингиома, вестибулярная шваннома, аденома, метастатическая опухоль мозга, менингиома, спинальньная опухоль и медуллобластома.
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения рака.
Настоящее изобретение также предоставляет способ лечения или предупреждения рака, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут применяться для лечения рака, который является дефицитным в отношении зависимой от гомологичной рекомбинации (HR) репаразной активности в отношении двухнитевого разрыва ДНК (см. WO 2006/021801).
Зависимая от HR репаразная функция в отношении двухнитевого разрыва ДНК восстанавливает разрывы двойной нити (DSB) в ДНК через гомологичные механизмы для восстановления непрерывной спирали ДНК (Nat. Genet. (2001) 27(3):247-254). Компоненты зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК включают, без ограничения, ATM (NM-000051), RAD51 (NM-002875), RAD51 L1 (NM-002877), RAD51C (NM-002876), RAD51L3 (NM-002878), DMCl (NM-007068), XRCC2 (NM7005431), XRCC3 (NM-005432), RAD52 (NM-002879), RAD54L (NM-003579), RAD54B (NM-012415), BRCA-1 (NM-007295), BRCA-2 (NM-000059), RAD50 (NM-005732), MREI 1A (NM-005590), NBSI (NM-002485), ADPRT (PARP-1), ADPRTL2 (PARP-2), CTPS, RPA, RPA1, RPA2, RPA3, XPD, ERCC1, XPF, MMS19, RAD51p, RAD51D, DMC1, XRCCR, RAD50, MRE11, NB51, WRN, BLMKU70, RU80, ATRCHKl, CHK2, FANCA, FANCB, FANCC, FANCD1, FANCD2, FANCE, FANCF, FANCG, RAD1 и RAD9. Другие белки, участвующие в зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК, включают регуляторные факторы, такие как EMSY (Cell (2003) 115:523-535).
Рак, который является дефицитным в отношении зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК, может включать или состоять из одной или нескольких раковых клеток, которые имеют уменьшенную или отключенную по сравнению с нормальными клетками способность восстанавливать двухнитевые разрывы ДНК по этому пути, то есть активность зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК может быть уменьшена или отключена в одной или нескольких раковых клетках.
Активность одного или нескольких компонентов зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК может быть отключена в одной или нескольких раковых клетках индивидуума, имеющего рак, который является дефицитным в отношении зависимой от HR способности восстанавливать двухнитевые разрывы ДНК. Компоненты зависимой от HR репаразной системы для двухнитевого разрыва ДНК хорошо охарактеризованы в уровне техники (см., например, Science (2001) 291:1284-1289) и включают компоненты, перечисленные выше.
Настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения рака, который является дефицитным в отношении зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК.
Настоящее изобретение также предоставляет способ лечения или предупреждения рака, который является дефицитным в отношении зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
В варианте осуществления раковые клетки являются дефицитными в зависимой от HR репаразной активности в отношении двухнитевого разрыва ДНК для одного или нескольких фенотипов, выбранных из ATM (NM-000051), RAD51 (NM-002875), RAD51 L1 (NM-002877), RAD51C (NM-002876), RAD51L3 (NM-002878), DMCl (NM-007068), XRCC2 (NM7005431), XRCC3 (NM-005432), RAD52 (NM-002879), RAD54L (NM-003579), RAD54B (NM-012415), BRCA-1 (NM-007295), BRCA-2 (NM-000059), RAD50 (NM-005732), MREI 1A (NM-005590), NBSl (NM-002485), ADPRT (PARP-1), ADPRTL2 (PARP-2), CTPS, RPA, RPA1, RPA2, RPA3, XPD, ERCC1, XPF, MMS19, RAD51p, RAD51D, DMC1, XRCCR, RAD50, MRE11, NB51, WRN, BLMKU70, RU80, ATRCHK1, CHK2, FANCA, FANCB, FANCC, FANCD1, FANCD2, FANCE, FANCF, FANCG, RAD1 и RAD9.
В другом варианте осуществления раковые клетки имеют BRCAl и/или BRCA2 дефицитный фенотип. Раковые клетки с этим фенотипом могут являться дефицитными в отношении BRCA1 и/или BRCA2, то есть экспрессия и/или активность BRCA1 и/или BRCA2 может быть уменьшена или отключена в раковых клетках, например, путем мутации или полиморфизма в кодировании нуклеиновой кислоты или посредством амплификации, мутации или полиморфизма в генном кодировании регуляторного фактора, например гена EMSY, который кодирует регуляторный фактор BRCA2 (Cell (2003) 115:523-535).
BRCA-1 и BRCA-2 представляют собой известные опухолевые супрессоры, чьи аллели немутантного типа часто теряются в опухолях гетерозиготных носителей (Oncogene, (2002) 21(58):8981-93; Trends Mol Med., (2002) 8(12):571-6). Взаимосвязь BRCA-1 и/или BRCA-2 мутаций с раком груди была хороша охарактеризована (Exp. Clin. Cancer Res., (2002) 21 (S Suppl):9-12). Амплификация гена EMSY, который кодирует BRCA-2-связывающий фактор, также, как известно, ассоциирована с раком груди и яичников. Носители мутаций в BRCA-1 и/или BRCA-2 также находятся при повышенном риске рака яичника, простаты и поджелудочной железы. Определение вариаций в BRCA-1 и BRCA-2 является хорошо известным в области техники и описано, например, в EP 699754, EP 705903, Genet. Test (1992) 1:75-83; Cancer Treat Res (2002) 107:29-59; Neoplasm (2003) 50(4):246-50; Ceska Gynekol (2003) 68(1): 11-16). Определение амплификации BRCA-2-связывающего фактора EMSY описано в Cell 115:523-535. Ингибиторы PARP, как было показано, могут быть применены для специфического умерщвления BRCA-1 и BRCA-2 дефицитных опухолей (Nature (2005) 434:913-916 и 917-920).
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения BRCA-1 или BRCA-2 дефицитных опухолей.
Настоящее изобретение также предоставляет способ лечения или предупреждения BRCA-1 или BRCA-2 дефицитных опухолей, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
В варианте осуществления ингибиторы PARP по настоящему изобретению могут быть применены в профилактической терапии для удаления BRCA2-дефицитных клеток (см. Cancer Res. (2005) 65: 10145).
Соединения по настоящему изобретению могут быть применены для лечения или предупреждения нейродегенеративных заболеваний, включая опосредованную полиглутаминовым ростом дегенерацию нервной ткани, хорею Гентингтона, болезнь Кеннеди, спиноцеребральную атаксию, дентаторубральную и паллидолюисовую атрофию (DRPLA), опосредованную агрегацией белка дегенерацию нервной ткани, болезнь Мачадо-Джозефа, болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз, губкообразную энцефалопатию, прионовую болезнь и рассеянный склероз (MS).
Таким образом, настоящее изобретение предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для лечения или предупреждения нейродегенеративных заболеваний.
Настоящее изобретение также предоставляет способ для лечения или предупреждения нейродегенеративных заболеваний, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения формулы I или композиции, включающей соединение формулы I.
Соединения по настоящему изобретению также могут быть применены для лечения или предупреждения ретровирусной инфекции (патент США 5652260), повреждения сетчатки (Curr. Eye Res. (2004), 29:403), старения кожи и индуцированного УФ-светом повреждения кожи (патент США 5589483 и Biochem. Pharmacol (2002) 63:921).
Соединения по изобретению могут быть применены для лечения или предупреждения преждевременного старения и отсрочки начала связанной с возрастом клеточной дисфункции (Pharmacological Research (2005) 52:93-99).
Согласно стандартной фармацевтической практике соединения по настоящему изобретению могут быть введены млекопитающим, предпочтительно человеку, или отдельно или в сочетании с фармацевтически приемлемыми носителями, эксципиентами, разбавителями, адъювантами, наполнителями, буферами, стабилизаторами, консервантами, смазками, в фармацевтической композиции.
Соединения по настоящему изобретению могут быть введены индивидууму любым удобным способом введения, или системно/периферически, или в месте желаемого действия, включая, без ограничения, оральный (например, путем глотания); местный (включая, например, чрескожный, интраназальный, в глаз, защечный и подъязычно); легочный (например, путем ингаляционной или инсуффляционной терапии с применением, например, аэрозоля, например, через рот или нос); ректальный; вагинальный; парентеральный (например, путем инъекции, включая подкожную, внутрикожную, внутримышечную, внутривенную, внутриартериальную, внутрисердечную, интратекальную, внутриспинальньную, интракапсулярную, субкапсулярную, внутриглазную, внутрибрюшинную, внутритрахейную, подкутикулярную, внутрисуставную, субарахноидальную и интрастернальную); и путем имплантации депо (например, подкожно или внутримышечно).
Индивидуум может представлять собой эукариота, животное, позвоночное животное, млекопитающее, грызуна (например, морская свинка, хомяк, крыса, мышь), относящегося к семейству мышиных (например, мышь), относящегося к семейству псовых (например, собака), относящегося к семейству кошачьих (например, кошка), относящегося к семейству лошадиных (например, лошадь), относящегося к семейству приматов, относящегося к семейству обезьян (например, обезьяна или человекообразная обезьяна), обезьяну (например, мартышка, павиан), человекообразную обезьяну (например, горилла, шимпанзе, орангутанг, гиббон) или человека.
Изобретение также предоставляет фармацевтические композиции, включающие один или несколько соединений по настоящему изобретению и фармацевтически приемлемый носитель. Фармацевтические композиции, содержащие активный компонент, могут быть в форме, пригодной для орального применения, например в форме таблеток, пастилок, лепешек, водных или масляных суспензий, дисперсных порошков или гранул, эмульсий, жестких или мягких капсул, сиропов или эликсиров. Композиции, предназначенные для орального применения, могут быть получены по любому способу, известному в области техники для производства фармацевтических композиций, и такие композиции могут содержать один или несколько агентов, выбранных из группы, состоящей из подсластителей, ароматизирующих веществ, окрашивающих агентов и консервирующих агентов для того, чтобы обеспечить фармацевтически элегантный и приемлемый по органолептическим свойствам препарат. Таблетки содержат активный компонент в смеси с нетоксичными фармацевтически приемлемыми наполнителями, которые являются пригодными для производства таблеток. Эти наполнители могут представлять собой, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактозу, фосфат кальция или фосфат натрия; гранулирующие и дезинтегрирующие агенты, например микрокристаллическую целлюлозу, натрий-кросскармелозу, кукурузный крахмал или альгиновую кислоту; связывающие агенты, например крахмал, желатин, поливинилпирролидон или аравийскую камедь, и смазывающие агенты, например стеарат магния, стеариновую кислоту или тальк. Таблетки могут являться непокрытыми, или они могут быть покрыты известными методиками для маскирования неприятного вкуса лекарственного средства или отсроченной дезинтеграции и абсорбции в желудочно-кишечном тракте и, таким образом, обеспечения длительного действия в течение более продолжительного периода. Например, могут применяться водорастворимое маскирующее вкус вещество, такое как гидроксипропилметилцеллюлоза или гидроксипропилцеллюлоза, или вещество, задерживающее момент начала действия, такое как этилцеллюлоза, ацетатбутират целлюлозы.
Композиции для орального применения также могут быть представлены в виде жестких желатиновых капсул, где активный компонент смешивается с инертным твердым разбавителем, например карбонатом кальция, фосфатом кальция или белой глиной, или в виде мягких желатиновых капсул, где активный компонент смешивается с водорастворимым носителем, таким как полиэтиленгликоль, или масляной средой, например арахисовым маслом, жидким парафином или оливковым маслом.
Водные суспензии содержат активное вещество в смеси с наполнителями, пригодными для производства водных суспензий. Такие наполнители представляют собой суспендирующие агенты, например натрий-карбоксиметилцеллюлозу, метилцеллюлозу, гидроксипропилметилцеллюлозу, альгинат натрия, поливинилпирролидон, трагакантовую камедь и гуммиарабик; диспергирующие или смачивающие агенты могут представлять собой фосфолипиды природного происхождения, например лецитин, или продукты конденсации алкиленоксида с жирными кислотами, например полиоксиэтиленстеаратом, или продукты конденсации этиленоксида с длинноцепочечными алифатическими спиртами, например гептадекаэтиленоксиэтанолом, или продукты конденсации этиленоксида с частичными сложными эфирами, производными от жирных кислот и гексита, такого как моноолеат полиоксиэтиленсорбита, или продукты конденсации этиленоксида с частичными сложными эфирами, производными от жирных кислот и ангидридов гексита, например моноолеата полиэтиленсорбитана. Водные суспензии могут также содержать один или несколько консервантов, например этил или н-пропил пара-гидроксибензоат, один или несколько окрашивающих агентов, одно или несколько ароматизирующих веществ и один или несколько подсластитетелей, таких как сахароза, сахарин или аспартам.
Масляные суспензии могут быть составлены путем суспендирования активного компонента в растительном масле, например арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, например пчелиный воск, твердый парафин или цетиловый спирт. Подсластитетели, такие как те, что указаны выше, и ароматизирующие вещества могут быть добавлены для обеспечения приемлемого по органолептическим свойствам орального препарата. Эти композиции могут консервироваться путем добавления антиоксиданта, такого как бутилированный гидроксианизол или альфа-токоферол.
Диспергируемые порошки и гранулы, пригодные для получения водной суспензии путем добавления воды, предоставляют активный компонент в смеси с диспергирующим или смачивающим агентом, суспендирующим агентом и одним или несколькими консервантами. Пригодные диспергирующие или смачивающие агенты и суспендирующие агенты представлены примерами, как те, что уже упомянуты выше. Дополнительные наполнители, например подслащивающие, придающие вкус и окрашивающие агенты, также могут присутствовать. Эти композиции могут консервироваться путем добавления антиоксиданта, такого как аскорбиновая кислота.
Фармацевтические композиции по изобретению также могут присутствовать в форме эмульсий масло-в-воде. Масляная фаза может представлять собой растительное масло, например оливковое масло или арахисовое масло, или минеральное масло, например жидкий парафин или их смеси. Пригодные эмульсифицирующие агенты могут представлять собой фосфолипиды природного происхождения, например соевый лецитин, и эфиры или частичные сложные эфиры, полученные из жирных кислот и ангидридов гексита, например моноолеата сорбита, и продукты конденсации упомянутых частичных сложных эфиров с этиленоксидом, например моноолеатом полиоксиэтиленсорбита. Эмульсии могут также содержать подсластители, ароматизирующие вещества, консерванты и антиоксиданты.
Сиропы и эликсиры могут быть рецептурированы с подсластителями, например глицерином, пропиленгликолем, сорбитом или сахарозой. Такие композиции могут также содержать успокоительное средство, консервант, агенты для придания вкуса, окрашивающие агенты и антиоксиданты.
Фармацевтические композиции могут находиться в форме стерильных инъецируемых водных растворов. Приемлемые носители и растворители, которые могут быть применены, представляют собой воду, раствор Рингера и изотонический раствор хлорида натрия.
Стерильные инъецируемые препараты также могут представлять собой стерильную инъецируемую микроэмульсию масло-в-воде, где активный компонент растворен в масляной фазе. Например, активный компонент может быть сначала растворен в смеси соевого масла и лецитина. Масляный раствор затем вводится в воду и глицериновую смесь и обрабатывается до образования микроэмульсии.
Инъецируемые растворы или микроэмульсии могут быть введены в поток крови пациента локальной болюсной инъекцией. Альтернативно, может быть благоприятно вводить раствор или микроэмульсию таким способом, чтобы поддерживать постоянной концентрацию циркулирующего соединения по настоящему изобретению. Для того чтобы поддерживать такую концентрацию постоянной, может быть применено устройство постоянной внутривенной доставки. Примером такого устройства является модель внутривенного насоса Deltec CADD-PLUS™ 5400.
Фармацевтические композиции могут находиться в форме стерильной инъецируемой водной или масляной суспензии для внутримышечного и подкожного введения. Эта суспензия может рецептурироваться способами, известными в технике, с применением тех пригодных диспергирующих или смачивающих агентов и суспендирующих агентов, которые упоминались выше. Стерильный инъецируемый препарат также может представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например в виде раствора в 1,3-бутандиоле. В добавление, стерильные, нелетучие масла обычно применяются в качестве растворителя или суспендирующей среды. Для этой цели может применяться любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. В добавление, жирные кислоты, такие как олеиновая кислота, находят применение при приготовлении инъецируемых растворов.
Соединения формулы I также могут вводиться в форме суппозиториев для ректального введения лекарственного средства. Эти композиции могут быть получены путем смешивания лекарственного средства с пригодным нераздражающим наполнителем, который является твердым при обычных температурах, но жидкостью при ректальной температуре и будет, следовательно, расплавляться в прямой кишке для высвобождения лекарственного средства. Такие вещества включают масло кокоса, обработанный глицерином желатин, гидрированные растительные масла, смеси полиэтиленгликолей различных молекулярных масс и сложные эфиры жирных кислот с полиэтиленгликолем.
Для местного нанесения применяются кремы, мази, желе, растворы или суспензии и т.д., содержащие соединение формулы I. (Для целей этого изобретения местное нанесение будет включать лосьоны для рта и жидкости для полоскания.)
Соединения по настоящему изобретению могут быть введены в интраназальной форме путем местного применения пригодных интраназальных носителей и устройств доставки или чрескожными путями, с применением форм чрескожных поверхностных пластырей, хорошо известных для специалистов в данной области техники. При введении в форме чрескожной системы доставки введение лекарственной дозы будет, конечно, скорее непрерывным, чем с интервалами во время режима дозирования. Соединения по настоящему изобретению также могут применяться в виде суппозиториев, используя основу, такую как масло кокоса, и обработанный глицерином желатин, гидрированные растительные масла, смеси полиэтиленгликолей различных молекулярных масс и сложные эфиры жирных кислот с полиэтиленгликолем.
Когда соединение по этому изобретению вводится индивидууму, выбранный уровнь дозировки будет зависеть от разнообразных факторов, включая, без ограничения, активность конкретного соединения, тяжесть индивидуальныых симптомов, путь введения, время введения, скорость выделения соединения, продолжительность лечения, другие лекарственные средства, соединения и/или вещества, применяемые в сочетании, и возраст, пол, массу, состояние, общий уровень здоровья и предшествующую историю болезни пациента. Количество соединения и путь введения будут в конечном счете находиться на усмотрении лечащего врача, хотя в целом дозировка будет достигать локальных концентраций в точке действия, которая достигает желаемого эффекта, не вызывая значительных вредных или опасных побочных эффектов.
Введение in vivo может быть осуществлено в виде одной дозы, постоянно или прерывисто (например, в разделенных дозах через соответствующие интервалы времени) в течение лечения. Способы определения наиболее эффективных методов и дозировки введения хорошо известны специалистам в данной области и будут варьировать в зависимости от композиции, применяемой для терапии, целей терапии, целевой клетки, подвергающейся лечению, и индивидуума, подвергающегося лечению. Могут быть проведены одиночные или множественные введения с уровнем дозы и режимом, выбранным лечащим врачом.
В общем, пригодная доза активного соединения находится в диапазоне от около 100 мкг до приблизительно 250 мг на килограмм массы тела индивидуума в день. Если активное соединение представляет собой соль, сложный эфир, пролекарство или подобное, введенное количество вычисляется на основании исходного соединения, и, таким образом, используемая фактическая масса соответственно увеличивается.
Соединения по настоящему изобретению также могут быть применены в сочетании с противораковыми средствами или химиотерапевтическими препаратами.
Соединения по настоящему изобретению могут быть применены в качестве химио- и радиосенсибилизаторов для лечения рака. Они могут быть применены для лечения млекопитающих, которые ранее проходили или в текущее время проходят лечение по поводу рака. Такие предшествующие лечения включают предшествующую химиотерапию, радиационную терапию, хирургическое вмешательство или иммунотерапию, такую как противораковые вакцины.
Таким образом, настоящее изобретение предоставляет сочетание соединения формулы I и противоракового средства для одновременного, раздельного или последовательного введения.
Настоящее изобретение также предоставляет соединение формулы I, предназначенное для приготовления лекарственного средства для применения в качестве дополнения при терапии рака или для усиления действия на опухолевые клетки ионизирующего облучения или химиотерапевтических препаратов.
Настоящее изобретение также предоставляет способ химиотерапии или радиотерапии, где способ включает введение пациенту, нуждающемуся в этом, эффективного количества соединения формулы I или композиции, включающей соединение формулы I в сочетании с ионизирующим облучением или химиотерапевтическими препаратами.
В комбинированной терапии соединение по настоящему изобретению может быть введено перед (например, за 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель), одновременно с или после (например, через 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель) введения другого противоракового средства индивидууму, нуждающегося в таком лечении. В различных вариантах осуществления соединения по настоящему изобретению и другие противораковые средства вводятся с интервалом в 1 минуту, с интервалом 10 минут, с интервалом 30 минут, с интервалом менее чем 1 час, с интервалом от 1 часа до 2 часов, с интервалом от 2 часов до 3 часов, с интервалом от 3 часов до 4 часов, с интервалом от 4 часов до 5 часов, с интервалом от 5 часов до 6 часов, с интервалом от 6 часов до 7 часов, с интервалом от 7 часов до 8 часов, с интервалом от 8 часов до 9 часов, с интервалом от 9 часов до 10 часов, с интервалом от 10 часов до 11 часов, с интервалом от 11 часов до 12 часов, с интервалом не более чем 24 часа или с интервалом не более чем 48 часов.
Соединения по настоящему изобретению и другое противораковое средство могут действовать аддитивно или синергически. Синергическое сочетание настоящих соединений и других противораковых средств может допускать применение меньших дозировок одного или обоих из этих средств, и/или менее частое дозирование одного или обоих соединений по настоящему изобретению и других противораковых средств, и/или при менее частом введении средств может уменьшиться любая токсичность, ассоциированная с введением агентов индивидууму, без уменьшения эффективности средств в эффективности лечения рака. В добавление, синергический эффект может приводить к улучшенной эффективности этих средств при лечении рака и/или уменьшению любых неблагоприятных или нежелательных побочных эффектов, ассоциированных с применением любого из средств в отдельности.
Примеры противораковых средств или химиотерапевтических препаратов для применения в сочетании с соединениями по настоящему изобретению могут быть найдены в Cancer Principles and Practice of Oncology by V.T. Devita and S. Hellman (editors), 6 th edition (February 15, 2001), Lippincott Williams & Wilkins Publishers. Специалист в данной области техники должен быть способен распознавать, какие сочетания средств могли бы быть применены, основываясь на конкретных характеристиках лекарственных средств и присутствующего рака. Такие противораковые средства включают, без ограничения, следующие: ингибиторы HDAC, модуляторы эстрогенового рецептора, модуляторы рецептора андрогена, модуляторы ретиноидных рецепторов, цитотоксичные/цитостатические агенты, антипролиферативные агенты, ингибиторы пренил-протеинтрансферазы, ингибиторы HMG-CoA-редуктазы, ингибиторы протеазы ВИЧ, ингибиторы обратной транскриптазы и другие ингибиторы ангиогенеза, ингибиторы клеточной пролиферации и активации систем жизнеобеспечения, индуцирующих апоптоз агентов и агентов, которые влияют на контрольные точки клеточного цикла. Соединения по настоящему изобретению являются особенно применимыми, когда применяются совместно с радиационной терапией.
Примеры "ингибиторов HDAC" включают субероиланилидгидроксамовую кислоту (SAHA), LAQ824, LBH589, PXD101, MS275, FK228, валпроевую кислоту, масляную кислоту и CI-994.
Термин "модуляторы эстрогенового рецептора" относится к соединениям, которые взаимодействуют с или ингибируют связывание эстрогена с рецептором, безотносительно к механизму. Примеры модуляторов эстрогенового рецептора включают, без ограничения, тамоксифен, ралоксифен, идоксифен, LY353381, LY1 17081, торемифен, фулвестрант, 4-[7-(2,2-диметил-1-оксопропокси-4-метил-2-[4-[2-(1-пиперидинил)этокси]фенил]-2H-1-бензопиран-3-ил]фенил-2,2-диметилпропаноат, 4,4'-дигидроксибензофенон-2,4-динитрофенилгидразон и SH646.
Термин "модуляторы рецептора андрогена" относится к соединениям, которые взаимодействуют или ингибируют связывание андрогенов с рецептором, безотносительно к механизму. Примеры модуляторов рецептора андрогена включают финастерид и другие ингибиторы 5α-редуктазы, нилутамид, флутамид, бикалутамид, лиарозол и ацетат абиратерона.
Термин "модуляторы ретиноидного рецептора" относится к соединениям, которые взаимодействуют или ингибируют связывание ретиноидов с рецептором, безотносительно к механизму. Примеры таких модуляторов ретиноидного рецептора включают бексаротен, третиноин, 13-цис-ретиновую кислоту, 9-цис-ретиновую кислоту, α-дифторметилорнитин, ILX23-7553, транс-N-(4'-гидроксифенил)ретинамид, и N-4-карбоксифенилретинамид.
Термин "цитотоксичные/цитостатические средства" относится к соединениям, которые вызывают гибель клетки или ингибируют клеточную пролиферацию в основном путем прямого взаимодействия с функционированием клетки или ингибируют или влияют на митоз клетки, включая алкилирующие агенты, факторы некроза опухоли, интеркаляторы, активирующие гипоксию соединения, ингибиторы микротрубочек/стабилизирующие микротрубочки агенты, ингибиторы митотических кинезинов, ингибиторы киназ, участвующих в развитии митоза, антиметаболиты, модификаторы биологического ответа; гормональные/противогормональные терапевтические препараты, гематопоэтические факторы роста, терапевтические средства направленного действия на основе моноклональных антител, ингибиторы топоизомеразы, ингибиторы протеасом и ингибиторы убихитин-лигазы.
Примеры цитотоксичных средств включают, без ограничения, циклофосфамид, хлорамбуцил-кармустин (BCNU), ломустин (CCNU), бусулфан, треосулфан, сертенеф, качектин, ифосфамид, тазонермин, лонидамин, карбоплатин, алтретамин, преднимустин, дибромдулцитол, ранимустин, фотемустин, недаплатин, ароплатин, оксалиплатин, темозоломид, метил метансульфонат, прокарбазин, дакарбазин, гептаплатин, эстрамустин, тозилат импросулфана, трофосфамид, нимустин, хлорид диброспидия, пумитепа, лобаплатин, сатраплатин, профиромицин, цисплатин, ирофулвен, дексифосфамид, цис-аминдихлор(2-метилпиридин)платина, бензилгуанин, глуфосфамид, GPX100, (транс, транс, транс)-бис-µ-(гексан-1,6-диамин)-µ-[диаминплатина(II)]бис[диамин(хлор)платина(II)]тетрахлорид, диаризидинилспермин, триоксид мышьяка, 1-(11-додециламино-10-гидроксиундецил)-3,7-диметилксантин, зорубицин, идарубицин, даунорубицин, бисантрен, митоксантрон, пирарубицин, пинафид, валрубицин, амрубицин, доксорубицин, эпирубицин, пирарубицин, антинеопластон, 3'-деамино-3'-морфолино-13-дезоксо-10-гидроксикарминомицин, аннамицин, галарубицин, элинафид, MEN 10755 и 4-деметокси-3-деамино-3-азиридинил-4-метилсульфонилдаунорубицин (см. WO 00/50032).
В варианте осуществления соединения по настоящему изобретению могут быть применены в сочетании с алкилирующими средствами.
Примеры алкилирующих средств включают, без ограничения, азотные горчичные масла: циклофосфамид, ифосфамид, трофосфамид и хлорамбуцил; нитрозомочевины: кармустин (BCNU) и ломустин (CCNU); алкилсульфонаты: бусулфан и треосулфан; триазины: дакарбазин, прокарбазин и темозоломид; содержащие платину комплексы: цисплатин, карбоплатин, ароплатин и оксалиплатин.
В варианте осуществления алкилирующее средство представляет собой дакарбазин. Дакарбазин может быть введен индивидууму при дозировках, находящихся в диапазоне от около 150 мг/м2 (площади поверхности тела индивидуума) до приблизительно 250 мг/м2. В другом варианте осуществления дакарбазин вводится внутривенно индивидууму один раз в день последовательно в течение пяти дней с дозой, находящейся в диапазоне от около 150 мг/м2 до около 250 мг/м2.
В варианте осуществления алкилирующее средство представляет собой прокарбазин. Прокарбазин может быть введен индивидууму при дозировках, находящихся в диапазоне от около 50 мг/м2 (площади поверхности тела индивидуума) до приблизительно 100 мг/м2. В другом варианте осуществления прокарбазин вводится внутривенно индивидууму один раз в день последовательно в течение пяти дней с дозой, находящейся в диапазоне от около 50 мг/м2 до около 100 мг/м2.
В варианте осуществления алкилирующее средство представляет собой темозоломид. Темозоломид может быть введен индивидууму при дозировках, находящихся в диапазоне от около 150 мг/м2 (площади поверхности тела индивидуума) до приблизительно 200 мг/м2. В другом варианте осуществления темозоломид вводится орально животному один раз в день последовательно в течение пяти дней с дозой, находящейся в диапазоне от около 150 мг/м2 до около 200 мг/м2.
Примеры антимитотических агентов включают аллоколхицин, галихондрин B, колхицин, производное колхицина, долстатин 10, маитанзин, ризоксин, тиоколхицин и тритил-цистеин.
Примером активирующего гипоксию соединения является тирапазамин.
Примеры ингибиторов протеасом включают, без ограничения, лактацистин, бортезомиб, эпоксомицин и пептидные альдегиды, такие как MG 132, MG 115 и PSI.
Примеры ингибиторов микротрубочек/стабилизирующих микротрубочки агентов включают паклитаксель, сульфат виндезина, винкристин, винбластин, винорелбин, 3',4'-дидегидро-4'-дезокси-8'-норвинкалейкобластин, доцетаксол, ризоксин, доластатин, исетионат мивобулина, ауристатин, цемадотин, RPR1 09881, BMS184476, винфлунин, криптофицин, 2,3,4,5,6-пентафтор-N-(3-фтор-4-метоксифенил)бензолсульфонамид, ангидровинбластин, N,N-диметил-L-валил-L-валил-N-метил-L-валил-L-пролил-L-пролин-трет-бутиламид, TDX258, эпотилоны (см., например, патенты США № 6284781 и 6288237) и BMS 188797.
Некоторые примеры ингибиторов топоизомеразы представляют собой топотекан, гикаптамин, иринотекан, рубитекан, эксатекан, гиметекан, дифломотекан, силил-камптотецины, 9-аминокамптотецин, камптотецин, криснатол, митомицин C, 6-этоксипропионил-3',4'-O-экзобензилиден-чартреусин, 9-метокси-N,N-диметил-5-нитропиразоло[3,4,5-kl]акридин-2-(6H)пропанамин, 1-амино-9-этил-5-фтор-2,3-дигидро-9-гидрокси-4-метил-1H,12H-бензо[de]пирано[3',4':b,7]-индолизино[1,2-b]хинолин-10,13(9H,15H)дион, луртотекан, 7-[2-(N-изопропиламино)этил]-(20S)-камптотецин, BNP1350, BNPI1100, BN80915, BN80942, фосфат этопозида, тенипозид, зобузоксан, 2'-диметиламино-2'-дезоксиэтопозид, GL331, N-[2-(диметиламино)этил]-9-гидрокси-5,6-диметил-6H-пиридо[4,3-b]карбазол-1-карбоксамид, асулакрин, (5a,5aB,8aa,9b)-9-[2-[N-[2-(диметиламино)этил]-N-метиламино]этил]-5-[4-гидрокси-3,5-диметоксифенил]-5,5a,6,8,8a,9-гексогидрофуро(3',4':6,7)нафто(2,3-d)-1,3-диоксол-6-он, 2,3-(метилендиокси)-5-метил-7-гидрокси-8-метоксибензо[c]- фенантридиниум, 6,9-бис[(2-аминоэтил)амино]бензо[g]изохинолин-5,10-дион, 5-(3-аминопропиламино)-7,10-дигидрокси-2-(2-гидроксиэтиламинометил)-6H-пиразоло[4,5,1-de]акридин-6-он, N-[1-[2(диэтиламино)этиламино]-7-метокси-9-оксо-9H-тиоксантен-4-илметил]формамид, N-(2-(диметиламино)этил)акридин-4-карбоксамид, 6-[[2-(диметиламино)этил]амино]-3-гидрокси-7H-индено[2,1-c]хинолин-7-он, димесна; некамптотециновые ингибиторы топоизомеразы-1, такие как индолокарбазолы; и двойные ингибиторы топоизомеразы-1 и II, такие как бензофеназины, XR20 115761MLN 576 и бензопиридоиндолы.
В варианте осуществления ингибитор топоизомеразы представляет собой иринотекан. Иринотекан может быть введен индивидууму при дозировках, находящихся в диапазоне от около 50 мг/м2 (площади поверхности тела индивидуума) до приблизительно 150 мг/м2. В другом варианте осуществления иринотекан вводится внутривенно индивидууму один раз в день последовательно в течение пяти дней с дозой, находящейся в диапазоне от около 50 мг/м2 до около 150 мг/м2 в течение дней 1-5, затем снова внутривенно один раз в день последовательно в течение пяти дней в течение дней 28-32 с дозой, находящейся в диапазоне от около 50 мг/м2 до около 150 мг/м2, затем снова внутривенно один раз в день последовательно в течение пяти дней в течение дней 55-59 с дозой, находящейся в диапазоне от около 50 мг/м2 до около 150 мг/м2.
Примеры ингибиторов митотических кинезинов и, в частности, митотического кинезина человека KSP описаны в публикациях PCT WO 01/30768, WO 01/98278, WO 02/056880, WO 03/050064, WO 03/050122, WO 03/049527, WO 03/049679, WO 03/049678, WO 03/039460, WO 03/079973, WO 03/099211, WO 2004/039774, WO 03/105855, WO 03/106417, WO 2004/087050, WO 2004/058700, WO 2004/058148 и WO 2004/037171 и заявках на патент США 2004/132830 и США 2004/132719. В варианте осуществления ингибиторы митотических кинезинов включают, без ограничения, ингибиторы KSP, ингибиторы MKLP1, ингибиторы CENP-E, ингибиторы MCAK, ингибиторы Kif14, ингибиторы Mphosph1 и ингибиторы Rab6-KIFL.
Определение "ингибиторы киназ, участвующих в прохождении митоза" включает, без ограничения, ингибиторы аврора-киназы, ингибиторы Polo-аналогичных киназ (PLK) (в частности, ингибиторы PLK-I), ингибиторы bub-1 и ингибиторы bub-Rl.
Термин "антипролиферативные агенты" включает антисмысловые РНК и ДНК олигонуклеотиды, такие как G3139, ODN698, RVASKRAS, GEM231, INX3001, и антиметаболиты, такие как эноцитабин, кармофур, тегафур, пентостатин, доксифлуридин, триметрексат, флударабин, капецитабин, галоцитабин, цитарабин оцфосфат, фостеабин гидрат натрия, ралтитрексед, палтитрексид, эмитефур, тиазофурин, децитабин, нолатрексед, пеметрексед, нелзарабин, 2'-дезокси-2'-метилиденцитидин, 2'-фторметилен-2'-дезоксицитидин, N-[5-(2,3-дигидро-бензофурил)сульфонил]-N'-(3,4- дихлорфенил)мочевина, N6-[4-дезокси-4-[N2-[2(E),4(E)-тетрадекадиеноил]глициламино]-L-глицеро-B-L-манногептопиранозил]аденин, аплидин, эцтеинасцидин, троксацитабин, 4-[2-амино-4-оксо-4,6,7,8-тетрагидро-3H-пиримидино[5,4-b][1,4]тиазин-6-ил-(S)-этил]-2,5-тиеноил-L-глутаминовая кислота, аминоптерин, 5-флуроурацил, аланозин, эфир 11-ацетил-8-(карбамоилоксиметил)-4-формил-6-метокси-14-окса-1,11-диазатетрацикло(7.4.1.0.0)-тетрадека-2,4,6-триен-9-ил уксусной кислоты, сваинзонин, лометрексол, дексразоксан, метиониназа, 2'-циано-2'-дезокси-N4-пальмитоил-1-В-D-арабинофуранозилцитозин и тиосемикарбазон 3-аминопиридин-2-карбоксальдегид.
Примеры терапевтических средств направленного действия на основе моноклональных антител включают те терапевтические препараты, которые содержат цитотоксичные агенты или радиоизотопы, присоединенные к моноклональным антителам, специфичным к раковой клетке или специфичным к клетке-мишени. Примеры включают Бексар.
Термин "ингибиторы HMG-CoA-редуктазы" относится к ингибиторам 3-гидрокси-3-метилглутарил-CoA-редуктазы. Примеры ингибиторов HMG-CoA-редуктазы, которые могут быть применены, включают, без ограничения, ловастатин (MEVACOR®; см. патенты США № 4231938, 4294926 и 4319039), симвастатин (ZOCOR®; см. патенты США № 4444784, 4820850 и 4916239), правастатин (PRAVACHOL®; см. патенты США № 4346227, 4537859, 4410629, 5030447 и 5180589), флувастатин (LESCOL®; см. патенты США № 5354772, 4911165, 4929437, 5189164, 5118853, 5290946 и 5356896) и аторвастатин (LIPITOR®; см. патенты США № 5273995, 4681893, 5489691 и 5342952). Структурные формулы этих и дополнительных ингибиторов HMG-CoA-редуктазы, которые могут быть применены в способах по настоящему изобретению, описаны на странице 87 M. Yalpani, "Cholesterol Lowering Drugs", Chemistry & Industry, p. 85-89 (5 февраля 1996 года) и в патентах США № 4782084 и 4885314. Применяемый здесь термин «ингибитор HMG-CoA редуктазы» включает все фармацевтически приемлемые формы лактона и открытой кислоты (то есть если лактонный цикл открывается с образованием свободной кислоты), а также солевые и эфирные формы соединений, которые имеют подавляющую активность в отношении HMG-CoA редуктазы, и, следовательно, применение таких форм солей, сложных эфиров, кислоты с открытой цепью и лактона включены в объем настоящего изобретения.
Термин "ингибитор пренил-протеинтрансферазы" относится к соединению, которое ингибирует или одну, или любую комбинацию ферментов пренил-протеинтрансфераз, включая фарнезил-протеинтрансферазу (FPTase), геранилгеранил-протеинтрансферазу типа I (GGPTase-I) и геранилгеранил-протеинтрансферазу типа II (GGPTase-II, также обозначаемую как Rab GGPTase).
Примеры ингибиторов пренил-протеинтрансфераз могут быть найдены в следующих публикациях и патентах: WO 96/30343, WO 97/18813, WO 97/21701, WO 97/23478, WO 97/38665, WO 98/28980, WO 98/29119, WO 95/32987, патент США № 5420245, патент США № 5523430, патент США № 5532359, патент США № 5510510, патент США № 5589485, патент США № 5602098, публикация европейского патента 0618221, публикация европейского патента 0675112, публикация европейского патента 0604181, публикация европейского патента 0696593, WO 94/19357, WO 95/08542, WO 95/11917, WO 95/12612, WO 95/12572, WO 95/10514, патент США № 5661152, WO 95/10515, WO 95/10516, WO 95/24612, WO 95/34535, WO 95/25086, WO 96/05529, WO 96/06138, WO 96/06193, WO 96/16443, WO 96/21701, WO 96/21456, WO 96/22278, WO 96/24611, WO 96/24612, WO 96/05168, WO 96/05169, WO 96/00736, патент США № 5571792, WO 96/17861, WO 96/33159, WO 96/34850, WO 96/34851, WO 96/30017, WO 96/30018, WO 96/30362, WO 96/30363, WO 96/31111, WO 96/31477, WO 96/31478, WO 96/31501, WO 97/00252, WO 97/03047, WO 97/03050, WO 97/04785, WO 97/02920, WO 97/17070, WO 97/23478, WO 97/26246, WO 97/30053, WO 97/44350, WO 98/02436 и патент США № 5532359. В качестве примера влияния ингибитора пренил-протеинтрансферазы на ангиогенез см. European J. of Cancer (1999), 35(9): 1394-1401.
Термин "ингибиторы ангиогенеза" относится к соединениям, которые ингибируют образование новых кровеносных сосудов, безотносительно к механизму. Примеры ингибиторов ангиогенеза включают, без ограничения, ингибиторы тирозинкиназ, такие как ингибиторы тирозинкиназных рецепторов Flt-1 (VEGFR1) и Flk-1/KDR (VEGFR2), ингибиторы факторов роста эпидермиса, фибробластов или тромбоцитов, ингибиторы MMP (металлопротеаза матрикса), блокаторы интегрина, интерферон-α, интерлейкин-12, полисульфат пентозана, ингибиторы циклооксигеназы, включая нестероидные противовоспалительные средства (NSAID), подобные аспирину и ибупрофену, так же как селективные ингибиторы циклооксигеназы-2, подобные целекоксибу и рофекоксибу (PNAS (1992) 89:7384; JNCI (1982) 69:475; Arch. Opthalmol. (1990) 108:573; Anat. Rec. (1994) 238:68; FEBS Letters (1995) 372:83; Clin. Orthop. (1995) 313:76; J. Mol. Endocrinol. (1996) 16:107; Jpn. J. Pharmacol. (1997) 75:105; Cancer Res. (1997) 57:1625 (1997); Cell (1998) 93:705; Intl. J. Mol. Med. (1998) 2:715; J. Biol. Chem. (1999) 274:9116)), стероидные противовоспалительные средства (такие, как кортикостероиды, минералокортикоиды, дексаметазон, преднизон, преднизолон, метилпред, бетаметазон), карбоксиамидотриазол, комбретастатин A-4, скваламин, 6-O-хлорацетилкарбонил)фумагиллол, талидомид, ангиостатин, тропонин-1, антагонисты ангиотензина II (см. J. Lab. Clin. Med. (1985) 105:141-145), антитела к VEGF (см. Nature Biotechnology (1999) 17:963-968; Kim et al. (1993), Nature 362:841-844; WO 00/44777; и WO 00/61186).
Другие терапевтические препараты, которые модулируют или ингибируют ангиогенез и также могут применяться в сочетании с соединениями по настоящему изобретению, включают агенты, которые модулируют или ингибируют системы свертывания крови и фибринолиза (см. обзор в Clin. Chem. La. Med. (2000) 38:679-692). Примеры таких агентов, которые модулируют или ингибируют пути коагуляции и фибринолиза, включают, без ограничения, гепарин (см. THRomb. Haemost. (1998) 80:10-23), низкомолекулярные гепарины и ингибиторы карбоксипептидазы U (также известные как ингибиторы активного тромбина, ингибитор активируемого фибринолиза [TAFIa]) (см. Thrombosis Res. (2001) 101:329-354). Ингибиторы TAFIa были описаны в публикации PCT WO 03/013526 и патенте США № 60/349925 (опубликован 18 января 2002 года).
Определение "средства, которые взаимодействуют с контрольными точками клеточного цикла" относится к соединениям, которые ингибируют белковые киназы, которые преобразуют сигналы контрольных точек клеточного цикла, таким образом сенсибилизируя раковую клетку к повреждающим ДНК средствам. Такие агенты включают ингибиторы ATR, ATM, Chk1 и Chk2 киназы и ингибиторы cdk- и cdc-киназ и специально представлены примерами 7-гидроксистауроспорин, стауроспорин, флавопиридол, CYC202 (Cyclacel) и BMS-387032.
Определение "ингибиторы клеточной пролиферации и путей активации систем жизнеобеспечения" относится к фармацевтическим агентам, которые ингибируют поверхностные рецепторы клетки и исходящий поток каскадов сигнальной трансдукции этих поверхностных рецепторов. Такие агенты включают ингибиторы EGFR (например, гефитиниб и эрлотиниб), ингибиторы ERB-2 (например, трастузумаб), ингибиторы IGFR (например, те, что впервые описаны в WO 03/059951), ингибиторы цитокиновых рецепторов, ингибиторы MET, ингибиторы PI3K (например, LY294002), серин/треониновых киназ (включая, без ограничения, ингибиторы Akt, такие как описанные в WO 03/086404, WO 03/086403, WO 03/086394, WO 03/086279, WO 02/083675, WO 02/083139, WO 02/083140 и WO 02/083138, ингибиторы Raf-киназы (например, BAY-43-9006), ингибиторы MEK (например, CI-1040 и PD-098059) и ингибиторы mTOR (например, Виет CCI-779 и Ариад AP23573). Такие агенты включают соединения низкомолекулярного ингибитора и антагонисты на основе антител.
Термин "индуцирующие апоптоз средства" включает активаторы членов семейства TNF-рецептора (включая TRAIL-рецепторы).
Изобретение также включает сочетание с NSAID, которые являются селективными ингибиторами COX-2. Для целей этого описания NSAID, которые являются селективными ингибиторами COX-2, определяются как те, что обладают по меньшей мере 100-кратной специфичностью в отношении ингибирования COX-2 по сравнению с COX-1, которая измеряется через отношение IC50 для COX-2 к IC50 для COX-1, определенным через клеточное или микросомальное исследования. Такие соединения включают, без ограничения, те, что впервые описаны в патенте США 5474995, патенте США 5861419, патенте США 6001843, патенте США 6020343, патенте США 5409944, патенте США 5436265, патенте США 5536752, патенте США 5550142, патенте США 5604260, патенте США 5698584, патенте США 5710140, WO 94/15932, патенте США 5344991, патенте США 5134142, патенте США 5380738, патенте США 5393790, патенте США 5466823, патенте США 5633272 и патенте США 5932598, все из которых включены в данное описание в качестве ссылки.
Ингибиторы COX-2, которые являются особенно применимыми для лечения в способе по настоящему изобретению, представляют собой 5-хлор-3-(4-метилсульфонил)фенил-2-(2-метил-5-пиридинил)пиридин или его фармацевтически приемлемую соль.
Соединения, которые были описаны как специфические ингибиторы COX-2 и, следовательно, которые могут быть применены по настоящему изобретению, включают, без ограничения, парекоксиб, CELEBREX® и BEXTRA® или их фармацевтически приемлемую соль.
Другие примеры ингибиторов ангиогенеза включают, без ограничения, эндостатин, украин, ранпирназа, IM862, 5-метокси-4-[2-метил-3-(3-метил-2-бутенил)оксиранил]-1-оксаспиро[2,5]окт-6-ил(хлорацетил)карбамат, ацетилдинаналин, 5-амино-1-[[3,5-дихлор-4-(4-хлорбензоил)фенил]метил]-1H-1,2,3-триазол-4-карбоксамид, CM101, скваламин, комбретастатин, RPI4610, NX31838, фосфат сульфатированной маннопентозы, 7,7-(карбонил-бис[имино-N-метил-4,2-пирролокарбонилимино[N-метил-4,2-пиррол]карбонилимино]-бис-(1,3-нафталиндисульфонат) и 3-[(2,4-диметилпиррол-5-ил)метилен]-2-индолинон (SU5416).
Как описано выше, термин "блокаторы интегрина" относится к соединениям, которые селективно противодействуют, ингибируют или препятствуют связыванию физиологического лиганда с αvβ3-интегрином, к соединениям, которые селективно противодействуют, ингибируют или препятствуют связыванию физиологического лиганда с αvβ5-интегрином, к соединениям, которые противодействуют, ингибируют или препятствуют связыванию физиологического лиганда как с αvβ3-интегрином, так и с αvβ5-интегрином, и к соединениям, которые противодействуют, ингибируют или препятствуют активности конкретного интегрина(ов), экспрессируемого(ых) в эдотелиальных клетках капилляров. Термин также относится к антагонистам αvβ6-, αvβ8-, α1β1-, α2β1-, α5β1-, α6β1- и α6β4-интегринов. Термин также относится к антагонистам любой комбинации из αvβ3-, αvβ5-, αvβ6-, αvβ8-, α1β1-, α2β1-, β5α1-, α6β1- и α6β4-интегринов.
Некоторые специфические примеры тирозинкиназных ингибиторов включают N-(трифторметилфенил)-5-метилизоксазол-4-карбоксамид, 3-[(2,4-диметилпиррол-5-ил)метилиденил)индолин-2-он, 17-(аллиламино)-17-деметоксигелданамицин, 4-(3-хлор-4-фторфениламино)-7-метокси-6-[3-(4-морфолинил)пропокси]хиназолин, N-(3-этинилфенил)-6,7-бис(2-метоксиэтокси)-4-хиназолинамин, BIBX1382, 2,3,9,10,11,12-гексагидро-10-(гидроксиметил)-10-гидрокси-9-метил-9,12-эпокси-1H-дииндоло[1,2,3-fg:3',2',1'-kl]пирроло[3,4-i][1,6]бензодиазоцин-1-он, SH268, генистеин, STI571, CEP2563, сульфонат 4-(3-хлорфениламино)-5,6-диметил-7H-пирроло[2,3-d]пиримидинметан, 4-(3-бром-4-гидроксифенил)амино-6,7-диметоксихиназолин, 4-(4'-гидроксифенил)амино-6,7-диметоксихиназолин, SU6668, STI571A, N-4-хлорфенил-4-(4-пиридилметил)-1-фталазинамин и EMD121974.
В варианте осуществления соединения по настоящему изобретению могут быть применены для лечения или предупреждения внешних признаков некроза, вызываемых селективными N3-аденин метилирующими средствами, такими как MeOSO2(CH2)-лекситропсин (Me-Lex).
Сочетания с соединениями, отличными от противораковых средств, также включают в способы по настоящему изобретению. Например, сочетания заявленных в настоящем изобретении соединений с PPAR-γ (то есть PPAR-гамма) агонистами и PPAR-δ (то есть PPAR-дельта) агонистами могут быть применены при лечении определенных злокачественных опухолей. PPAR-γ и PPAR-δ представляют собой ядерные пероксисомные пролиферативно активированные γ- и δ-рецепторы. Экспрессия PPAR-γ в эндотелиальных клетках и ее участие в ангиогенезе было описано в литературе (см. J. Cardiovasc. Pharmacol. (1998) 31:909-913; J. Biol. Chem. (1999) 274:9116-9121; Invest. Ophthalmol Vis. Sci. (2000) 41:2309-2317). Было показано, что PPAR-γ агонисты ингибируют ангиогенный ответ к VEGF in vitro; как троглитазон, так и малеат розиглитазона ингибируют развитие ретинальной неоваскуляризации у мыши (Arch. Ophthalmol. (2001) 119:709-717). Примеры PPAR-γ агонистов и PPAR-γ/α-агонистов включают, без ограничения, тиазолидиндионы (такие, как DRF2725, CS-011, троглитазон, розиглитазон и пиоглитазон), фенофибрат, гемфиброзил, клофибрат, GW2570, SB219994, AR-H039242, JTT-501, MCC-555, GW2331, GW409544, NN2344, KRP297, NP0110, DRF4158, NN622, GI262570, PNU182716, DRF552926, 2-[(5,7-дипропил-3-трифторметил-1,2-бензизоксазол-6-ил)окси]-2-метилпропионовую кислоту (впервые описанную в USSN 09/782856) и 2(R)-7-(3-(2-хлор-4-(4-фторфенокси)фенокси)пропокси)-2-этилхроман-2-карбоновую кислоту (впервые описана в USSN 60/235708 и 60/244697).
Другой вариант осуществления по настоящему изобретению состоит в применении впервые описанных в настоящем изобретении соединений в сочетании с противовирусными средствами (такими, как аналоги нуклеозидов, включая ганцикловир для лечения рака, см. WO 98/04290).
Другой вариант осуществления настоящего изобретения заключается в применении впервые описанных в настоящем изобретении соединений в сочетании с генной терапией для лечения рака. Для обзора генетических подходов к лечению рака см. Hall et al. (Am. J. Hum. Genet. (1997) 61:785-789) и Kufe et al. (Cancer Medicine, 5th Ed, p.876-889, BC Decker, Hamilton 2000). Генная терапия может быть применена для высвобождения любого подавляющего опухоль гена. Примеры таких генов включают, без ограничения, p53, который может быть высвобожден путем рекомбинантного вирус-опосредованного генного переноса (см., например, патент США № 6069134), uPA/uPAR антагонист (Adenovirus-Mediated Delivery of a uPA/uPAR Antagonist Suppresses Angiogenesis-Dependent Tumor Growth and Dissemination in Mice," Gene Therapy, August (1998) 5(8): 1105-13), гамма-интерферон (J. Immunol. (2000) 164:217-222).
Соединения по настоящему изобретению также могут вводиться в сочетании с ингибитором врожденной мультилекарственной устойчивости (MDR), в частности MDR, ассоциированной с высокими уровнями экспрессии транспортных белков. Такие MDR ингибиторы включают ингибиторы п-гликопротеина (P-gp), такого как LY335979, XR9576, OC144-093, R101922, VX853, верапамил и PSC833 (валсподар).
Соединение по настоящему изобретению может быть применено в сочетании с противорвотными средствами для лечения тошноты или рвоты, включая острую, запаздывающую, латентную и опережающую рвоты, которые могут возникать при применении соединения по настоящему изобретению, отдельно или с радиационной терапией. Для предотвращения или лечения рвоты соединение по настоящему изобретению может быть применено в сочетании с другими противорвотными агентами, особенно антагонистами рецептора нейрокинина-1, антагонистами 5-HT3-рецептора, такими как ондансетрон, гранисетрон, трописетрон и затисетрон, агонистами GABAB-рецептора, таким как баклофен, кортикостероидом, таким как Декадрон (дексаметазон), Кеналог, Аристокорт, Назалид, Преферид, Бенекортен или другими, такими как те, что впервые описаны в патентах США № 2789118, 2990401, 3048581, 3126375, 3929768, 3996359, 3928326 и 3749712, антидопаминэргическими средствами, такими как фенотиазины (например, прохлорперазин, флуфеназин, тиоридазин и мезоридазин), метоклопрамид или дронабинол. В варианте осуществления противорвотный агент, выбранный из антагониста рецептора нейрокинина-1, антагониста 5-HT3-рецептора и кортикостероида, вводится в качестве адъюванта для лечения или предупреждения рвоты, которая может возникать при введении соединений по настоящему изобретению.
Антагонисты рецептора нейрокинина-1 для применения в сочетании с соединениями по настоящему изобретению были полностью описаны, например, в патенте США № 5162339, 5232929, 5242930, 5373003, 5387595, 5459270, 5494926, 5496833, 5637699, 5719147; публикации европейского патента № EP 0360390, 0394989, 0428434, 0429366, 0430771, 0436334, 0443132, 0482539, 0498069, 0499313, 0512901, 0512902, 0514273, 0514274, 0514275, 0514276, 0515681, 0517589, 0520555, 0522808, 0528495, 0532456, 0533280, 0536817, 0545478, 0558156, 0577394, 0585913, 0590152, 0599538, 0610793, 0634402, 0686629, 0693489, 0694535, 0699655, 0699674, 0707006, 0708101, 0709375, 0709376, 0714891, 0723959, 0733632 и 0776893; публикации международного патента PCT № WO 90/05525, 90/05729, 91/09844, 91/18899, 92/01688, 92/06079, 92/12151, 92/15585, 92/17449, 92/20661, 92/20676, 92/21677, 92/22569, 93/00330, 93/00331, 93/01159, 93/01165, 93/01169, 93/01170, 93/06099, 93/09116, 93/10073, 93/14084, 93/14113, 93/18023, 93/19064, 93/21155, 93/21181, 93/23380, 93/24465, 94/00440, 94/01402, 94/02461, 94/02595, 94/03429, 94/03445, 94/04494, 94/04496, 94/05625, 94/07843, 94/08997, 94/10165, 94/10167, 94/10168, 94/10170, 94/11368, 94/13639, 94/13663, 94/14767, 94/15903, 94/19320, 94/19323, 94/20500, 94/26735, 94/26740, 94/29309, 95/02595, 95/04040, 95/04042, 95/06645, 95/07886, 95/07908, 95/08549, 95/11880, 95/14017, 95/15311, 95/16679, 95/17382, 95/18124, 95/18129, 95/19344, 95/20575, 95/21819, 95/22525, 95/23798, 95/26338, 95/28418, 95/30674, 95/30687, 95/33744, 96/05181, 96/05193, 96/05203, 96/06094, 96/07649, 96/10562, 96/16939, 96/18643, 96/20197, 96/21661, 96/29304, 96/29317, 96/29326, 96/29328, 96/31214, 96/32385, 96/37489, 97/01553, 97/01554, 97/03066, 97/08144, 97/14671, 97/17362, 97/18206, 97/19084, 97/19942 и 97/21702; и в публикации патента Великобритании № 2266529, 2268931, 2269170, 2269590, 2271774, 2292144, 2293168, 2293169 и 2302689. Получение таких соединений подробно описано в вышеупомянутых патентах и публикациях, которые включены в данное описание в качестве ссылки.
В варианте осуществления антагонист рецептора нейрокинина-1 для применения в сочетании с соединениями по настоящему изобретению выбран из 2-(R)-(1-(R)-(3,5-бис(трифторметил)фенил)этокси)-3-(S)-(4-фторфенил)-4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)морфолина или его фармацевтически приемлемой соли, которая описана в патенте США № 5719147.
Соединение по настоящему изобретению также может вводиться в сочетании со средством, которое может быть применено для лечения анемии. Такое средство для лечения анемии представляет собой, например, активатор рецептора непрерывного эритропоэза (такой, как эпоэтин альфа).
Соединение по настоящему изобретению также может вводиться в сочетании со средством, которое может быть применено для лечения нейтропении. Таким средством для лечения нейтропении является, например, гемопоэтический фактор роста, который регулирует продукцию и функцию нейтрофилов, таких как колониестимулирующий фактор гранулоцитов человека (G-CSF). Примеры G-CSF включают филграстим.
Соединение по настоящему изобретению также может вводиться с иммуноактиваторами, такими как левамизол, изопринозин и задаксин.
Соединение по настоящему изобретению также может быть применено для лечения или предупреждения рака, включая рак кости, в сочетании с бис-фосфонатами (понятно, включают бис-фосфонаты, дифосфонаты, бис-фосфоновые кислоты и дифосфоновые кислоты). Примеры бис-фосфонатов включают, без ограничения: этидронат (Didronel), памидронат (Aredia), алендронат (Fosamax), риседронат (Actonel), золедронат (Zometa), ибандронат (Boniva), инкадронат или цимадронат, клодронат, EB-1053, минодронат, неридронат, пиридронат и тилудронат, включая любые и все их фармацевтически приемлемые соли, производные, гидраты и смеси.
Таким образом, объем настоящего изобретения включает применение заявленных в настоящем изобретении соединений в сочетании с ионизирующим облучением и/или в сочетании со вторым соединением, выбранным из ингибиторов HDAC, модулятора эстрогенового рецептора, модулятора рецептора андрогена, модулятора ретиноидного рецептора, цитотоксичного/цитостатического агента, антипролиферативного агента, ингибитора пренил-протеинтрансферазы, ингибитора HMG-CoA-редуктазы, ингибитора ангиогенеза, PPAR-γ агониста, PPAR-δ агониста, антивирусного агента, ингибитора врожденной мультилекарственной устойчивости, противорвотного агента, агента, который может быть применен при лечении анемии, агента, который может быть применен при лечении нейтропении, иммуноактиваторного лекарственного средства, ингибитора клеточной пролиферации и активации систем жизнеобеспечения, агента, который влияет на контрольные точки клеточного цикла, вызывающего апоптоз агента и бис-фосфоната.
Термин "введение" и его варианты (например, "назначение" соединения) в ссылке на соединение по изобретению обозначает введение соединения или пролекарства соединения в организм животного, нуждающегося в таком лечении. Когда соединение по изобретению или его пролекарство предоставляется в сочетании с одним или несколькими другими активными агентами (например, цитотоксичным агентом и т.д.), термин "введение" и его варианты, каждый, как понятно, включают одновременное и последовательное введение соединения или его пролекарства и других агентов.
Применяемый здесь термин "композиция" включает продукт, состоящий из определенных компонентов в определенных количествах, так же как любой продукт, который возникает, прямо или непрямо, из сочетания определенных компонентов в определенных количествах.
Применяемый здесь термин "терапевтически эффективное количество" обозначает количество активного соединения или фармацевтического агента, который вызывает в ткани, системе, животном или человеке биологический или медицинский ответ, который является желательным для научного работника, ветеринара, семейного врача или клинициста.
Термин "лечение" относится к лечению млекопитающего, подверженного патологическому состоянию, и относится к эффекту, который улучшает состояние посредством умерщвления раковых клеток, но также к эффекту, который приводит к замедлению прогрессирования состояния и включает уменьшение скорости прогрессирования, удержание скорости прогрессирования, улучшение состояния и излечение. Также включенным является лечение в качестве профилактической меры (то есть профилактика).
Термин "фармацевтически приемлемый", применяемый здесь, относится к соединениям, веществам, композициям и/или дозированным формам, которые, в пределах объема озвученного медицинского диагноза, пригодны для применения в контакте с тканями индивидуума (например, человека) без избыточной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, термин соотносится с приемлемым соотношением преимущество/риск. Каждый носитель, наполнитель и т.д. должен также быть "приемлемым" в смысле совместимости с другими компонентами композиции.
Термин "добавка" относится к применению соединений в сочетании с известными терапевтическими методами. Такие методы включают цитотоксичные режимы введения лекарственных средств и/или ионизирующего облучения, которые применяются при лечении различных типов рака. В частности, активные соединения, известные как потенцирующие действия ряда противораковых химиотерапевтических лечений, которые включают топоизомеразный класс токсинов (например, топотекан, иринотекан, рубитекан), большинство известных алкилирующих агентов (например, DTIC, темозоламид) и основанные на платине лекарственные средства (например, карбоплатин, цисплатин), применяют при лечении рака.
В варианте осуществления ингибитор ангиогенеза, применяемый как второе соединение, является выбранным из ингибитора тирозинкиназ, ингибитора фактора роста эпидермиса, ингибитора фактора роста фибробластов, ингибитора фактора роста тромбоцитов, ингибитора MMP (металлопротеазы матрикса), блокатора интегрина, интерферона-α, интерлейкина-12, полисульфата пентозана, ингибитора циклооксигеназы, карбоксиамидотриазола, комбретастатина A-4, скваламина, 6-О-хлорацетилкарбонил)фумагиллола, талидомида, ангиостатина, тропонина-1 или антител к VEGF. В варианте осуществления модулятор эстрогенового рецептора представляет собой тамоксифен или ралоксифен.
Также включенным в объем формулы изобретения является способ лечения рака, который состоит во введении терапевтически эффективного количества соединения формулы I в сочетании с радиационной терапией и/или в сочетании с соединением, выбранным из ингибиторов HDAC, модулятора эстрогенового рецептора, модулятора рецептора андрогена, модулятора ретиноидного рецептора, цитотоксичного/цитостатического агента, антипролиферативного агента, ингибитора пренил-протеинтрансферазы, ингибитора HMG-CoA-редуктазы, ингибитора ангиогенеза, PPAR-γ-агониста, PPAR-δ-агониста, противовирусного агента, ингибитора врожденной мультилекарственной устойчивости, противорвотного агента, агента, который может быть применен для лечения анемии, агента, который может быть применен для лечения нейтропении, иммуноактиватора, ингибитора клеточной пролиферации и активации систем жизнеобеспечения, агента, который взаимодействует с контрольными точками клеточного цикла, агента, вызывающего апоптоз, и бис-фосфоната.
Следующий вариант осуществления изобретения представляет собой способ лечения рака, который включает введение терапевтически эффективного количества соединения формулы I в сочетании с паклитакселем или трастузумабом.
Далее изобретение включает способ лечения или предупреждения рака, который включает введение терапевтически эффективного количества соединения формулы I в сочетании с ингибитором COX-2.
Настоящее изобретение также включает фармацевтическую композицию, которая может быть применена для лечения или предупреждения рака, которая включает терапевтически эффективное количество соединения формулы I и соединения, выбранного из ингибиторов HDAC, модуляторов эстрогенового рецептора, модулятора рецептора андрогена, модулятора ретиноидного рецептора, цитотоксичного/цитостатического средства, антипролиферативного агента, ингибитора пренил-протеинтрансферазы, ингибитора HMG-CoA-редуктазы, ингибитора протеазы ВИЧ, ингибитора обратной транскриптазы, ингибитора ангиогенеза, агониста PPAR-γ, агониста PPAR-δ, противовирусного агента, ингибитора клеточной пролиферации и активации систем жизнеобеспечения, агента, который взаимодействует с контрольными точками клеточного цикла, вызывающего апоптоз агента и бис-фосфоната.
Эти и другие аспекты изобретения будут очевидны из содержащегося здесь обсуждения.
Аббревиатуры, используемые при описании реакций в приведенных ниже примерах :
AcOH (уксусная кислота); DCM (хлористый метилен); DIPEA (N,N'-диизопропилэтиламин); DMA (N,N-диметилацетамид); DMAP (4-диметиламинопиридин); ДМФА (диметилформамид); ДМСО (диметилсульфоксид); eq. (эквивалент); EtOAc (этилацетат); HBTU (гексафторфосфат O-бензотриазол-N,N,N',N'-тетраметил-урония); NaH (гидрид натрия); ЯМР (ядерный магнитный резонанс); PyBOP (1H-бензотриазол-1-илокситрипирролидинофосфоний); RP-HPLC (обратнофазная жидкостная хроматография высокого разрешения); RT (комнатная температура); sat. aq. (насыщенный водный); TBTU (тетрафторборат O-(1H-бензотриазол-1-ил)-N,N,N',N'-тетраметилурония); TEA (триэтиламин); TFA (трифторуксусная кислота) и THF (тетрагидрофуран).
Соединения формулы I, где c равно 0 и d равно 1, могут быть получены путем конденсации соединения формулы IA со соединением формулы IB:
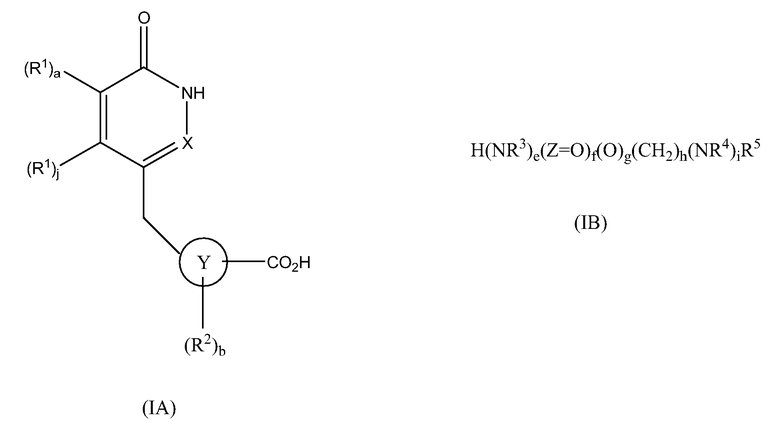 ,
,
где a, b, e, f, g, h, i, j, X, Y, Z, R1, R2, R3, R4 и R5 определены выше. Реакция обычно может быть проведена в присутствии сшивающих агентов, таких как HBTU и DIPEA, в растворителе, таком как DMA, при температуре, близкой к комнатной. Также может применяться сшивающий агент, такой как TBTU, и растворитель, такой как ДМФА. Аналогичные условия сочетания могут быть применены на любой стадии в синтезе соединений формулы I с применением соответствующих комбинаций исходных веществ.
Соединения формулы IA могут быть получены путем одновременного гидролиза и декарбоксилирования соединения формулы IC:
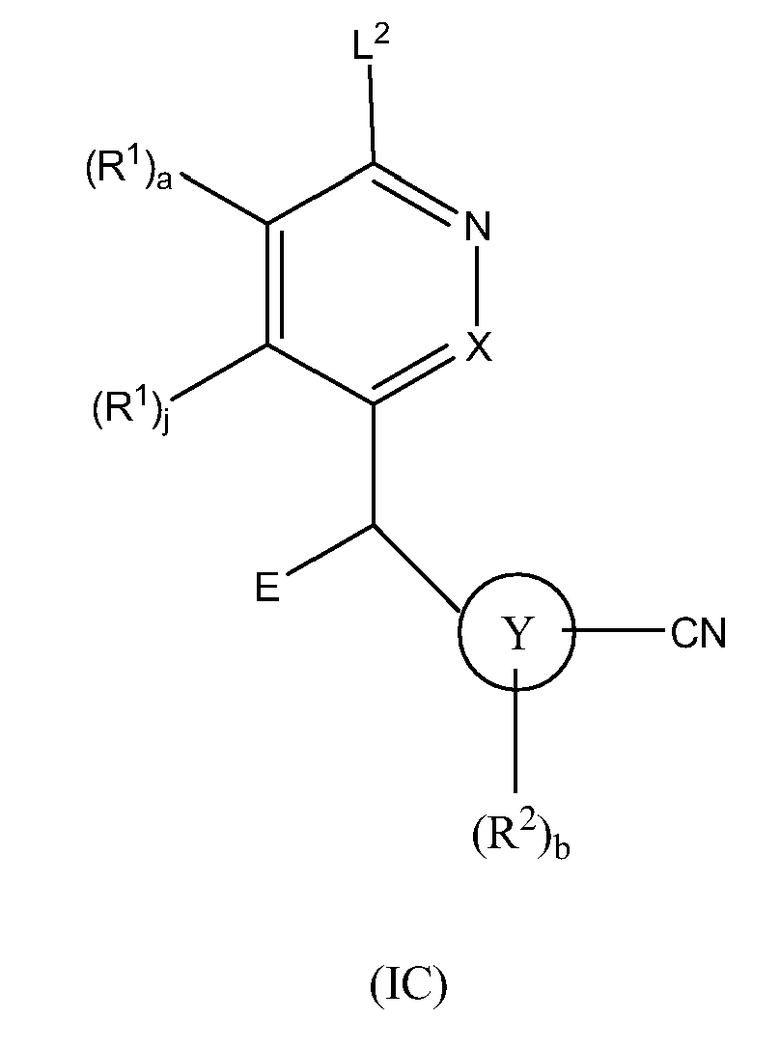 ,
,
где a, b, j, R1, R2, X и Y определены выше, E представляет собой электроноакцепторную группу, такую как циано, и L представляет собой уходящую группу, такую как галоген, например фтор или хлор. Реакция обычно проводится в кислотных или основных условиях. Например, основание, такое как NaOH, может быть использовано при температуре около 90°C. Реакция может быть проведена в растворителях, таких как AcOH и HCl, при кипячении с обратным холодильником.
Соединения формулы IC могут быть получены путем реакции соединения формулы ID со соединением формулы IE:
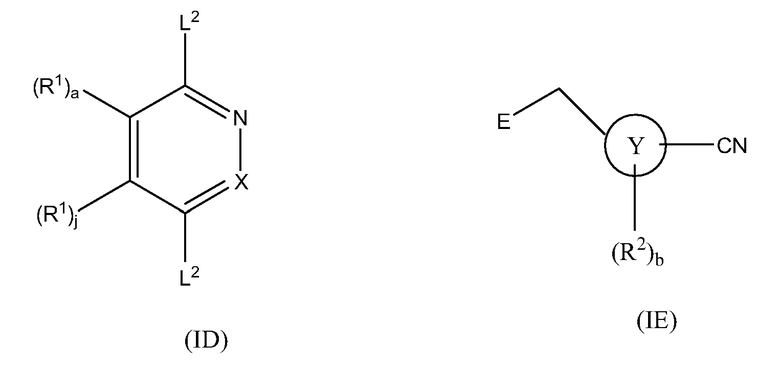 ,
,
где a, b, j, R1, R2, X, Y, E и L2, каждый независимо, определены выше. Реакция обычно проводится в присутствии основания, такого как NaH, в растворителе, таком как ДМФА, при температуре от около 0°C до комнатной температуры.
Альтернативно, соединения формулы I могут быть получены путем одновременного гидролиза и декарбоксилирования соединения формулы IF:
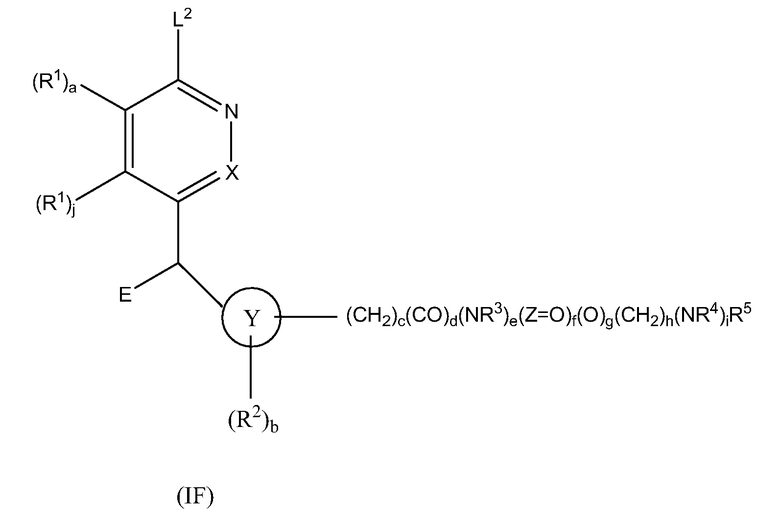 ,
,
где a, b, c, d, e, f, g, h, i, j, X, Y, Z, R1, R2, R3, R4, R5, L2 и E определены выше. Реакция обычно проводится в кислотных или основных условиях.
Соединения формулы IF могут быть получены путем реакции соединения формулы ID с соединением формулы IG:
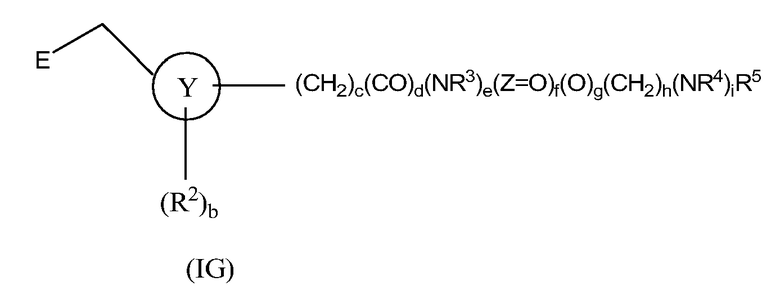 ,
,
где b, c, d, e, f, g, h, i, Y, Z, R2, R3, R4, R5 и E определены выше. Реакция обычно проводится в присутствии основания, такого как NaH, в растворителе, таком как ДМФА, при температуре от около 0°C до комнатной температуры.
Если синтез промежуточных соединений и исходных веществ не описан, эти соединения являются коммерчески доступными или могут быть приготовлены из коммерчески доступных соединений стандартными способами или путем расширения приведенных здесь примеров.
Соединения формулы I могут быть превращены в другие соединения формулы I известными способами или способами, описанными в примерах.
При проведении любой из синтетических последовательностей, описанных здесь, может быть необходимо и/или желательно защищать чувствительные или реакционноспособные группы в любой из участвующих молекул. Это может быть достигнуто посредством традиционных защитных групп, таких как те, что описаны в Protecting Groups in Organic Synthesis, 3rd Edition, Greene, T. W. and Wuts, P. G. M.; Wiley Interscience, 1999 and Kocienski, P. J. Protecting Groups, Thieme, 1994. Защитные группы могут быть удалены на подходящей последующей стадии с применением способов, известных из уровня техники. Например, если присутствует защитная группа Boc, она может быть удалена путем добавления TFA в растворителях, таких как DCM и/или MeCN, при температуре, близкой к комнатной. Альтернативно могут применяться EtOAc в присутствии HCl и 1,4-диоксан при температуре, близкой к комнатной. Бензилкарбонильная защитная группа может быть удалена гидрированием с применением стандартных способов, таких как действие катализатора, такого как Pd/C, в растворителе, таком как метанол, в атмосфере водорода.
Соединения по настоящему изобретению получали согласно следующим схемам. Все переменные находятся в пределах определенных выше формул.
Схема 1
Соединения, описанные в этом изобретении, могут быть получены с применением способов, описанных ниже. Например, 3,6-дихлор-4-алкилпиридазин и 3,6-дихлор-4,5-диалкилпиридазины могут быть получены, как описано ниже, путем радикального присоединения к дихлорпиридазину, соответствующие радикалы генерируются декарбоксилированием соответствующей алкановой кислоты действием аммоний пероксодисульфата в присутствии Ag(I), как описано в Org. Prep. + Proc. Int. 1988, 20, 117. Реакция замещенных производных 3,6-дихлорпиридазина с (гетеро)ароматической группой, несущей активированную метиленовую группу, активированную электроноакцепторной группой, такой как сложный эфир или нитрил, в присутствии основания, допускает замещение хлорных групп, что приводит к смеси двух региоизомерных 3-((гетеро)арилметил)пиридазинов. Гидролиз этой изомерной смеси с одновременным декарбоксилированием и гидролизом иминохлоридной группы приводит к образованию желаемого блока. На этой стадии смесь изомеров может быть разделена (схема 1).
Схема 1
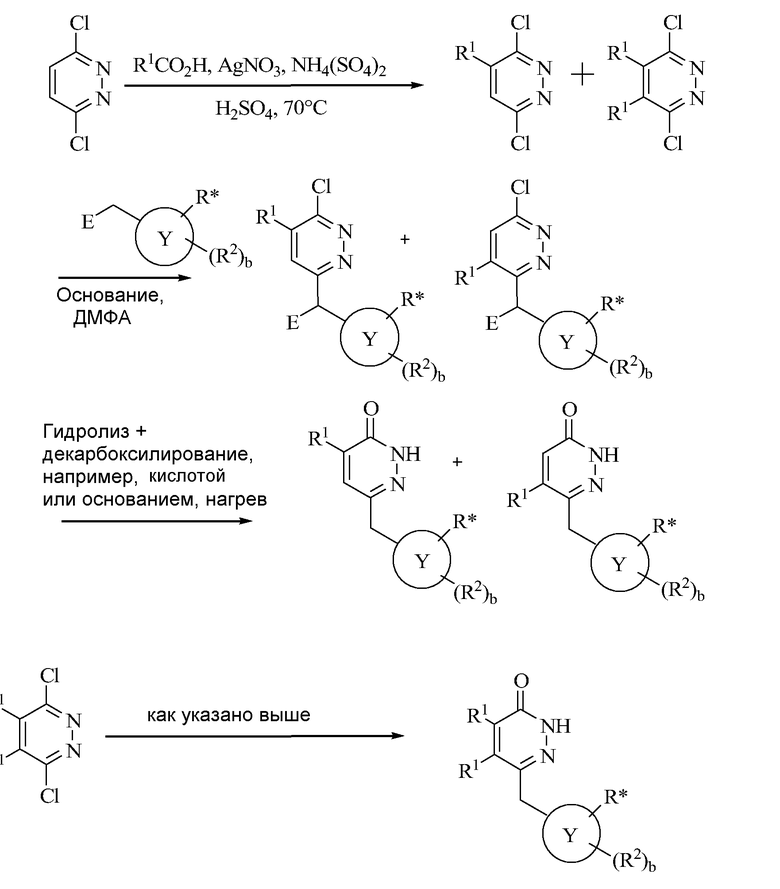
где
E представляет собой электроноакцепторную группу, например -CO2-алкил, -CN;
R* представляет собой (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)iR5;
R1 представляет собой C1-6-алкил; и
все переменные определены выше.
Схема 2
В определенных обстоятельствах (гетеро)ароматическая группа может нести заготовку функциональной группы, которая может далее быть конвертирована с образованием других производных. Например, (гетеро)ароматический нитрил может сохраняться неизменным при прохождении через синтетическую последовательность. Эта функциональная группа может быть гидролизована во время реакции декарбоксилирования для получения соответствующей карбоновой кислоты. В свою очередь, она может быть введена в сочетание с различными аминами для получения желаемых ингибиторов PARP (схема 2).
Схема 2
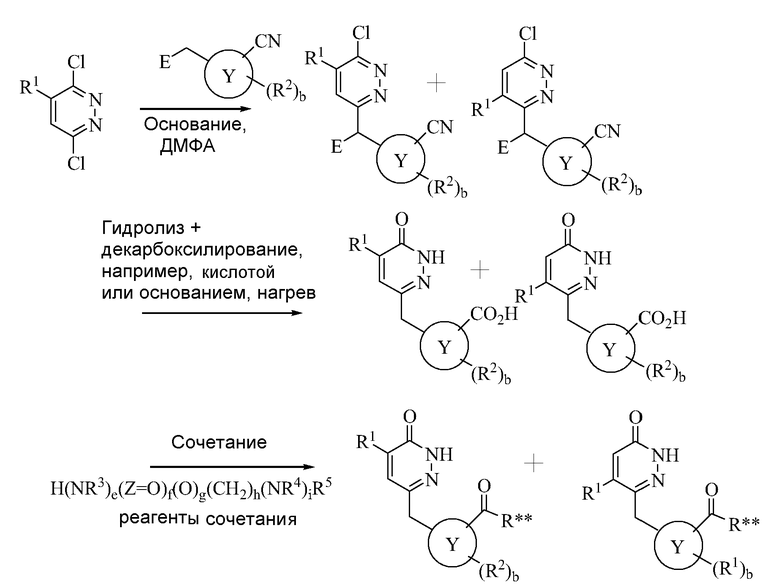
где
E представляет собой электроноакцепторную группу, например -CO2-алкил, -CN;
R** = (NR3)c(Z=O)f(O)g(CH2)h(NR4)iR5; и
все переменные определены выше.
Ингибиторы по настоящему изобретению могут быть трансформированы в другие родственные производные стандартными превращениями, известными для специалистов в данной области, например реакциями сочетания аминогруппы с карбоновыми кислотами с применением реагентов сочетания, аналогичных HBTU, HATU, TBTU и PyBoP, или с активированными ацильными группами; реакциями сульфонилирования с применением сульфонилхлоридов; или реакциями восстановительного аминирования с использованием карбонильного производного и аминогруппы, с использованием восстанавливающего реагента, подобного цианоборгидриду натрия.
Схема 3
3,6-дихлор-4-алкилпиридазин может быть получен путем присоединения алкильного радикала к дихлорпиридазину, как описано ранее. Затем могут быть получены асимметричные 3,6-дихлор-4-алкил-5-алкил*-пиридазины, реакцией со вторым алкильным радикалом путем декарбоксилирования соответствующей алкановой кислоты с пероксодисульфатом аммония в присутствии Ag(I), как описано в Org. Prep. + Proc. Int. 1988, 20, 117. Реакционные последовательности, которые описаны выше, позволяют создавать желаемые ингибиторы PARP (схема 3).
Схема 3
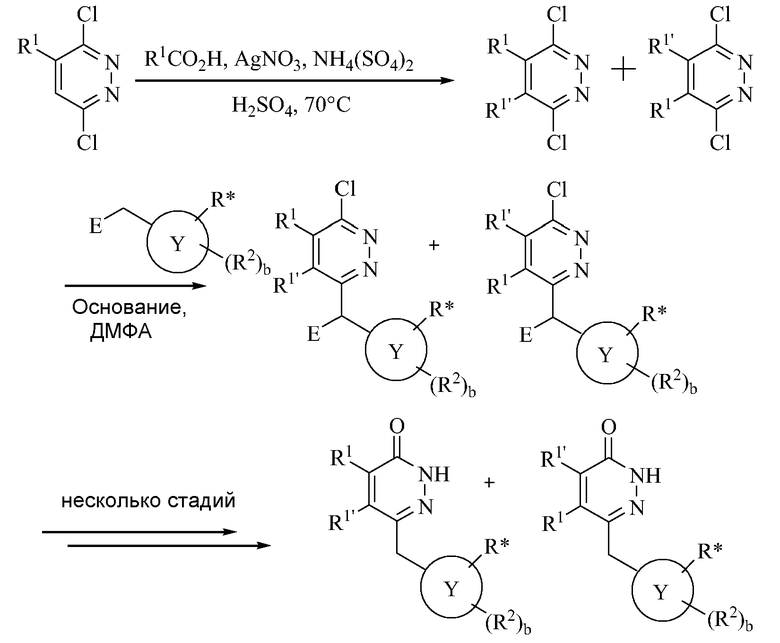
где
E представляет собой электроноакцепторную группу, например -CO2-алкил, -CN;
R* представляет собой (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)iR5;
R1 и R1' представляют собой C1-6-алкил; и
все переменные определены выше.
Схема 4
Альтернативный способ конвертировать эти ингибиторы PARP в родственные соединения состоит в применении реакции Курциуса. Соединение, содержащее группу карбоновой кислоты, может быть обработано дифенилфосфорилазидом в спиртовом растворителе при кипячении с обратным холодильником и может претерпевать перегруппировку Курциуса, приводящую к соответствующему карбамату. Этот карбамат затем может быть гидролизован в кислотных условиях до соответствующего производного (гетеро)анилина, которое затем может быть переработано в желаемые ингибиторы PARP путем реакции сочетания в стандартных условиях (схема 8). Аналогичным образом, производное (гетеро)анилина также может быть введено в сочетание с ацилангидридом и затем далее циклизовано в соответствующий имид путем добавления взаимодействующего реагента, такого как TBTU. Альтернативно, (гетеро)аналид может быть введен во взаимодействие с карбоновой кислотой, содержащей карбаматный фрагмент, затем подвергнут микроволновому облучению в присутствии DMAP, что делает возможной циклизацию до соответствующей циклической мочевины.
Схема 4
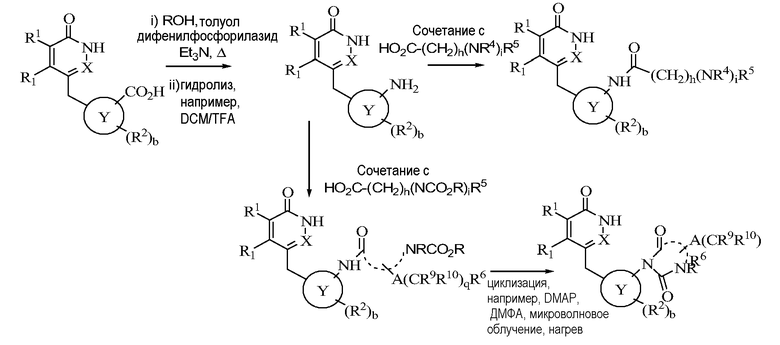
где
R и R1 представляют собой низший алкил и
все переменные определены выше;
Δ нагрев.
Схема 5
Следующий способ конвертировать один тип ингибитора в другой состоит в проведении реакции нуклеофильного ароматического замещения в Y-кольце. Например, группа галогена, например фторид, в (гетеро)ароматическом кольце может быть замещена на ион алкоксида или аминогруппу. Обработка алкоксидом натрия в кипящем с обратным холодильником спиртовом растворителе позволяет вводить алкоксигруппу в Y-кольцо. Альтернативно, энергичное нагревание субстрата в растворе амина в полярном растворителе, подобном ДМФА, в запаянной реакционной емкости позволяет ввести алкиламино- и диалкиламиногруппы в Y-кольцо. Последующие операции с функциональными группами, такие как гидролиз нитрильных групп в сильноосновных средах при кипячении с обратным холодильником и взаимодействие, приводят к желаемым ингибиторам PARP (схема 5).
Схема 5
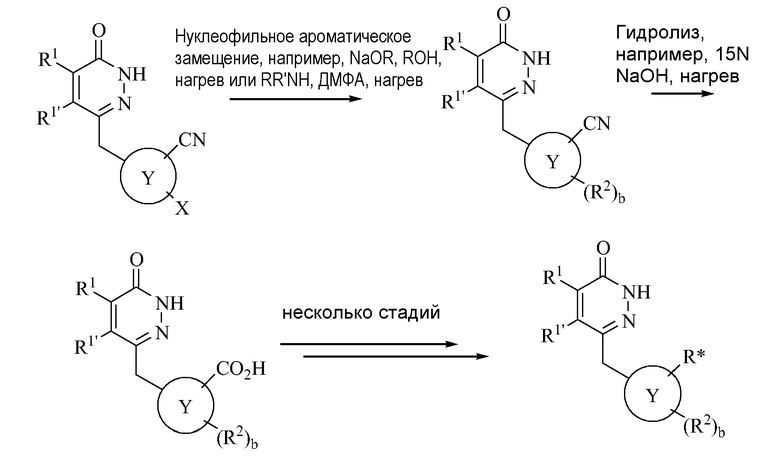
где
X = галоген, например фтор;
R* представляет собой (CH2)c(CO)d(NR3)e(Z=O)f(O)g(CH2)h(NR4)iR5;
R, R', R1 и R1' представляют собой C1-6-алкил;
и все переменные определены выше.
Соединения, описанные представленными здесь примерами, тестировались в описанных ниже исследованиях и, как было найдено, имели IC50-величины менее 5 мкМ.
Исследование PARP-1 с анализом сцинтилляционного приближения (SPA)
Реагенты
Буфер для исследования: 100 мМ Трис, pH 8, 4 мМ MgCl2, 4 мМ спермина, 200 мМ KCl, 0,04% Nonidet P-40.
Ферментная смесь: буфер для исследования (12,5 мкл), 100 мМ DTT (0,5 мкл), PARP-1 (5 нМ, Trevigen 4668-500-01), H2O (до 35 мкл).
Смесь никотинамид - адениновый динуклеотид (NAD)/ДНК: [3H-NAD] (250 мкCi/мл, 0,4 мкл, счетчик Perkin-Elmer NET-443H), NAD (1,5 мМ, 0,05 мкл, от SIGMA N-1511), биотинилированный-NAD (250 мкM, 0,03 мкл, Trevigen 4670-500-01), активированный тимус теленка (1 мг/мл, 0,05 мкл, от Amersham Biosciences 27-4575), H2O (до l0 мкл).
Смесь для проявления: стрептавидиновые SPA-бусы (5 мг/мл от Amersham Biosciences RPNQ 0007), растворенные в 500 мМ растворе ЭДТА.
Проведение эксперимента
Реакцию проводили в 96-луночном микропланшете с конечным объемом 50 мкл/лунка. После добавления 5 мкл 5% раствора соединения в ДМСО добавляли ферментную смесь (35 мкл), реакция начинается при добавлении смеси NAD/ДНК (10 мкл) и инкубировании в течение 2 часов при комнатной температуре. Реакцию останавливали добавлением смеси для проявления (25 мкл) и инкубирования в течение 15 мин при комнатной температуре. Измерение проводили на приборе Packard TOP COUNT.
ПРИМЕР 1
Трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (A4)
Стадия 1: 5-[(6-хлор-5-этилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (A1) и 5-[(6-хлор-4-этилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (A2)
К охлаждаемому льдом раствору 5-(цианометил)-2-фторбензонитрила (1 экв.) и 3,6-дихлор-4-этилпиридазина (1,9 экв.) (Ссылка: Org. Prep. + Proc. Int. 1988, 20, 117 и патент США 4628088, 1986) в ДМФА порциями добавляли NaH (2,1 экв.). Реакционную смесь перемешивали при 0°C в течение 15 мин, затем отогревали до комнатной температуры и перемешивали в течение 2 часов. Реакцию тушили с насыщенным водным NaHCO3 и экстрагировали EtOAc. Объединенные органические фракции промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Смесь изомеров 4- и 5-этилпиридазина разделяли хроматографией на силикагеле, элюировали смесью Гексаны:EtOAc 9:1, что дало сначала 5-замещенный изомер (A1) и затем 4-замещенный изомер (A2).
5-[(6-хлор-5-этилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (A1): 1H-ЯМР (300 МГц, CDCl3) δ: 7,80-7,78 (2H, м), 7,48 (1H, с), 7,31-7,29 (1H, м), 5,63 (1H, с), 2,81 (2H, кв.д, J=7,6 и 3,1 Гц), 1,31 (3H, т, J=7,6 Гц). MS (ES) для C15H10ClFN4 рассчитано: 300/302, найдено: 301/303 (M+H)+.
5-[(6-хлор-4-этилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (A2): 1H-ЯМР (400 МГц, CDCl3) δ: 7,75-7,67 (2H, м), 7,45 (1H, с), 7,30 (1H, т, J=8,6 Гц), 5,74 (1H, с), 2,80-2,70 (1H, м), 2,60-2,50 (1H, м), 1,26 (3H, т, J=7,3 Гц). MS (ES) для C15H10ClFN4 рассчитано: 300/302, найдено: 301/303 (M+H)+.
Стадия 2: 5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензойная кислота (A3)
Смесь A1 (1 экв.) в AcOH, концентрированную HCl и H2O (1:2:1, 0,065 M), нагревали при кипячении с обратным холодильником в течение ночи, затем охлаждали до комнатной температуры и разбавляли H2O и EtOAc, затем отделяли. Водную фазу промывали EtOAc и объединенные экстракты промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Сырой продукт растворяли в AcOH и добавляли NaOAc (2 экв.). Полученный раствор нагревали при кипячении с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали и смесь экстрагировали EtOAc. Органическую фазу промывали дважды насыщенным солевым раствором, высушивали (Na2SO4) и растворитель удаляли под пониженным давлением. Остаток суспендировали в H2O и к полученной суспензии добавляли водный раствор 23 M NaOH (8 экв.) и нагревали до 90°C в течение 30 мин. Реакционный раствор охлаждали, затем подкисляли до pH 4 действием 2 M HCl. Смесь перемешивали в течение 10 мин и фильтровали. Полученное твердое вещество промывали последовательно H2O, гексанами, Et2O, EtOAc и высушивали в высоком вакууме, что дало указанное в заголовке соединение в виде слабо-оранжевого порошка.
1H-ЯМР (300 МГц, ДМСО-d6) δ: 13,30 (0,5H, ушир.с), 12,74 (1H, с), 7,78-7,75 (1H, м), 7,53 (1H, м), 7,31-7,25 (1H, м), 7,72 (1H, с), 3,94 (2H, с), 2,45 (2H, J=7,5 Гц), 1,11 (3H, т, J=7,5 Гц). MS (ES) для C14H13FN2O3 рассчитано: 276, найдено: 277 (M+H)+.
Стадия 3: трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (A4)
К раствору A3 (1 экв.) в DMA добавляли HBTU (2 экв.), трет-бутил 1-гомопиперазинкарбоксилат (1,9 экв.) и DIPEA (3,4 экв.). Смесь перемешивали в течение ночи при комнатной температуре, затем реакционную смесь концентрировали, сырой продукт растворяли в DCM, промывали дважды с H2O, высушивали (Na2SO4) и концентрировали под пониженным давлением. Полученное оранжевое масло растворяли в смеси 6 M HCl/EtOH (2:1) и смесь перемешивали при комнатной температуре в течение 1 часа. Раствор концентрировали, подщелачивали концентрированным водным раствором NH3 до pH 9, затем органические вещества экстрагировали DCM. Объединенные органические фракции промывали H2O насыщенным солевым раствором, высушивали (Na2SO4) и растворитель удаляли под пониженным давлением. Остаток очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов (колонка: Water X-Terra C18), объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение, в виде бесцветного порошка. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,76 (1H, с), 8,79 (2H, ушир.с), 7,45-7,27 (3H, м), 7,19 (1H, с), 3,93 (2H, с), 3,85-3,74 (2H, м), 3,56 (1H, м), 3,39-3,20 (5H, м), 2,45 (2H, J=7,5 Гц), 2,08-1,91 (2H, м), 1,11 (3H, т, J=7,5 Гц). MS (ES) для C19H23FN4O2 рассчитано: 358, найдено: 359 (M+H)+.
ПРИМЕР 2
Трифторацетат 4-{5-[(4-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (B3)
Стадия 1: 5-[(6-хлор-4-этилпиридазин-3-ил)метил]-2-фторбензойная кислота (B1)
Раствор из примера 1, A2 (1 экв.) в AcOH:концентрированный HCl:H2O (1:10:1, 0,065 M) нагревали при кипячении с обратным холодильником в течение ночи. Реакционную смесь затем охлаждали до комнатной температуры и разбавляли водой/EtOAc. Органическую фазу промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. MS (ES) для C14H12ClFN2O2 рассчитано: 294/296, найдено: 295/297 (M+H)+.
Стадия 2: трифторацетат 4-{5-[(6-хлор-4-этилпиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (B2)
К раствору B1 (1 экв.) в DMA добавляли HBTU (2 экв.), трет-бутил 1-гомопиперазинкарбоксилат (2 экв.) и DIPEA (3,1 экв.) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали под пониженным давлением и сырой продукт растворяли в DCM, промывали H2O (2×), высушивали (Na2SO4) и растворитель удаляли под пониженным давлением. Полученный сырой продукт растворяли в растворе 6 M HCl:EtOH (3:1) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционный раствор концентрировали, подщелачивали водным аммиаком до pH 9 и смесь экстрагировали DCM. Объединенные органические фракции промывали водой, насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Остаток очищали методом препаративной RP-HPLC, с применением H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов (колонка: Water X-Terra C18). Объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение, в виде желтого масла. MS (ES) для C19H22ClFN4O рассчитано: 376/378, найдено: 377/379 (M+H)+.
Стадия 3: трифторацетат 4-{5-[(4-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (B3)
Смесь B2, NaOAc (2 экв.) и AcOH (0,16 M) нагревали при кипячении с обратным холодильником в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры и концентрировали под пониженным давлением. Неочищенный продукт очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов (колонка: Water X-Terra C18). Объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение. 1H-ЯМР (600 МГц, ДМСО-d6) δ: 12,80 (1H, м), 8,84 (2H, с), 7,38-7,28 (3H, м), 6,66 (1H, с), 4,01 (2H, с), 3,85-3,7 (2H, м), 3,55 (1H, м), 3,36-3,32 (2H, м), 3,27 (1H, м), 3,20 (1H, м), 3,16 (1H, м), 2,45-2,42 (2H, м), 2,06 (1H, м), 1,90 (1H, м), 1,11-1,07 (3H, м). MS (ES) для C19H23FN4O2 рассчитано: 358, найдено: 359 (M+H)+.
ПРИМЕР 3
6-{3-[(4-Ацетил-1,4-диазепан-1-ил)карбонил]-4-фторбензил}-4-этилпиридазин-3(2H)-он (C1)
К раствору Примера 1, A4 (1 экв.) в DCM:ДМФА (2:1. 0,5 M) добавляли DIPEA (3 экв.) с последующим добавлением AcCl (1,2 экв.). После перемешивания в течение 30 мин при комнатной температуре растворитель удаляли под пониженным давлением и неочищенное вещество повторно растворяли в EtOAc, промывали 1 M HCl, высушивали (Na2SO4) и концентрировали под пониженным давлением. Полученный сырой продукт растворяли в TΗF:Η2O (1:1) и добавляли LiOH (2 экв.), после перемешивания в течение 40 мин при комнатной температуре реакционную смесь экстрагировали EtOAc. Объединенные органические фракции промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением, что дало указанное в заголовке соединение в виде желтого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,6 (1H, с), 7,38 (1H, м), 7,28-7,17 (3H, м), 3,92 (2H, м), 3,82-3,66 (3H, м), 3,60-3,48 (3H, м), 3,43-3,30 (2H, м), 2,46 (2H, кв., J=7,3 Гц), 2,05 (1,5H, с), 1,89 (1,5H, с), 1,88-1,49 (2H, м), 1,12 (3H, т, J=7,3 Гц). MS (ES) для C21H25FN4O3 рассчитано: 400, найдено: 401 (M+H)+.
ПРИМЕР 4
1-Ацетил-4-{5-[(6-хлор-4-этилпиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан (D1)
Указанное в заголовке соединение получали, как описано в примере 3, из продукта примера 2, B3. Соединение получали в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,78 (1H, с), 7,32-7,14 (3H, м), 6,65 (1H, с), 4,01-3,99 (2H, м), 3,79-3,63 (3H, м), 3,53-3,48 (3H, м), 3,40-3,27 (2H, м), 2,48- 2,41 (2H, м), 2,04-2,02 (3H, м), 1,86-1,78 (1H, м), 1,55-1,46 (1H, м), 1,11-1,06 (3H, м). MS (ES) для C21H25FN4O3 рассчитано: 400, найдено: 401 (M+H)+.
ПРИМЕР 5
4-Этил-6-(4-фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4] триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)пиридазин-3(2H)-он (E1)
К раствору примера 1, A3 (1 экв.) в ДМФА (0,2 мл, 0,28 M) добавляли ΗBTU (1,2 экв.) и DIPEA (1 экв.). Полученный раствор перемешивали 10 мин при комнатной температуре. Затем к раствору добавляли раствор хлорида 3-(трифторметил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ия (PTC Int. Appl., WO 2005020929) (1,1 экв.) и DIPEA (1,2 экв.) в ДМФА (0,2 мл, 0,28 M). Реакционную смесь перемешивали в течение ночи при комнатной температуре. Неочищенный продукт очищали методом препаративной RP-ΗPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Фракции продукта лиофилизировали, что дало указанное в заголовке соединение в виде белого порошка. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,74 (1H, с), 7,47-7,31 (3H, м), 7,20 (1H, с), 5,11-5,09 (1,4H, м), 4,77-4,75 (0,7H, м), 4,27-4,18 (2,6H, м), 3,94 (2H, с), 3,80-3,78 (1,3H, м), 2,44 (2H, кв., J=7,3 Гц), 1,11 (3H, т, J=7,3 Гц). MS (ES) для C20H18F4N6O2 рассчитано: 450, найдено: 451 (M+H)+.
ПРИМЕР 6
Трифторацетат 4-{5-[(5-этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (F8) и трифторацетат 4-{5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (F9)
Стадия 1: 3,6-Дихлор-4-этил-5-метилпиридазин (F1)
К суспензии 3,6-дихлор-4-этилпиридазина (1 экв.), AgNO3 (0,7 экв.) и AcOH (2,8 экв.) в H2O (9,4 мл, 0,6 М) добавляли раствор концентрированной серной кислоты (6,6 экв.) в H2O (9,4 мл, 0,6 М) при 50°C, с последующим добавлением раствора пероксодисульфата аммония (5,4 экв.) в H2O (9,4 мл, 0,6 М) при 60°C в течение 20 мин. Реакционную смесь нагревали при 70-75°C в течение 30 мин. После охлаждения реакционную смесь приводили к pH 7 действием 25% раствора гидроксида аммония и экстрагировали Et2O. Экстракты промывали H2O и высушивали (Na2SO4), растворитель удаляли в высоком вакууме. Остаток очищали хроматографией на силикагеле, элюировали смесью 9:1 петролейный эфир:EtOAc, что дало желаемый продукт в виде бесцветных кристаллов. 1H-ЯМР (400 МГц, CDCl3) δ: 2,85 (2H, кв., J=7,6 Гц), 2,45 (3H, с), 1,21 (3H, т, J=7,6 Гц).
Стадия 2: 5-[(6-Хлор-5-этил-4-метилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (F2) и 5-[(6-хлор-4-этил-5-метилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (F3).
Указанные в заголовке соединения получали, как описано в примере 1, Al и A2. Соединение получали в виде смеси изомеров (соотношение 1:1), указанные изомеры было невозможно разделить хроматографией на силикагеле (элюент петролейный эфир:EtOAc, 7:3). 1H-ЯМР (300 МГц, CDCl3) δ: 7,77-7,67 (4H, м), 7,32-7,27 (2H, с), 5,76-5,72 (2H, м), 2,84 (2H, кв., J=7,5 Гц), 2,71-2,69 (2H, м), 2,44 (3H, с), 2,31 (3H, с), 1,21 (3H, т, J=7,5 Гц), 1,06 (3H, т, J=7,5 Гц). MS (ES) для C16H12ClFN4 рассчитано: 314/316, найдено: 315/317 (M+H)+.
Стадия 3: 5-[(5-Этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензойная кислота (F4) и 5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензойная кислота (F5)
Указанные в заголовке соединения получали, как описано в примере 1, A3, из смеси F2 и F3 и искомые продукты получали в виде смеси изомеров F4 и F5. MS (ES) для C15H15FN2O3 рассчитано: 290, найдено: 291 (M+H)+.
Стадия 4: трет-Бутил 4-{5-[(5-этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-карбоксилат (F6) и трет-бутил 4-{5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-карбоксилат (F7)
К раствору F4 и F5 (1 экв.) в DMA добавляли HBTU (1,2 экв.), трет-бутил 1-гомопиперазинкарбоксилат (1,4 экв.) и DIPEA (3 экв.). Реакционную смесь перемешивали 1 час при комнатной температуре. Неочищенный продукт очищали методом препаративной RP-HPLC, с применением H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов и объединенные фракции продукта лиофилизировали, что дало указанные в заголовке соединения в виде смеси изомеров с соотношением 1,6:1. MS (ES) для C25H33FN4O4 рассчитано: 472, найдено: 473 (M+H)+.
Стадия 5: трифторацетат 4-{5-[(5-этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил]-1,4-диазепан-1-ия (F8) и трифторацетат 4-{5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил-2-фторбензоил]-1,4-диазепан-1-ия (F9)
Смесь F6 и F7 растворяли в растворе TFA:CH2C12 (1:2, 2,1 мл) и полученный раствор перемешивали 1 час при комнатной температуре. Растворитель концентрировали и остаток растворяли в MeCN:H2O, замораживали и затем лиофилизировали. Соединения, обозначенные в заголовке примера, получали в виде смеси (соотношение F8:F9: 0,42/0,58). 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,70-12,67 (1H, м), 8,86 (2H, с), 7,36-7,21 (3H, м), 3,95 (2H, с), 3,90-3,55 (2H, м), 3,54-3,04 (6H, м), 2,45-2,40 (2H, м), 2,02 (3H, с), 1,99 (2H, с), 1,02-0,92 (1,7H, м, основной продукт), 0,91-081 (1,3H, м, минорный продукт). MS (ES) для C20H26FN4O2 рассчитано: 372, найдено: 373 (M+H)+.
ПРИМЕР 7
Трифторацетат 4-{2-фтор-5-[(5-изопропил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия (G3)
Стадия 1: 5-[(6-Хлор-5-изопропилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (G1)
К охлаждаемому льдом раствору 5-(цианометил)-2-фторбензонитрила (1 экв.) и 3,6-дихлор-4-изопропилпиридазина (1,3 экв.) (Ссылка: Org. Prep. + Proc. Int. 1988, 20, 117 и патент США 4628088, 1986) в THF (38 мл, 0,1 M) добавляли порциями NaH (1 экв.). Реакционную смесь перемешивали при 0°C в течение 15 мин, затем отогревали до комнатной температуры и перемешивали в течение 2 часов. Реакцию тушили насыщенным водным NaHCO3 и экстрагировали EtOAc. Объединенные органические фракции промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Неочищенный продукт очищали методом хроматографии на силикагеле, элюировали смесью петролейный эфир:EtOAc (8:2), что дало указанное в заголовке соединение. 1H-ЯМР (400 МГц, CDCl3) δ: 7,80-7,79 (2H, м), 7,49 (1H, с), 7,31-7,29 (1H, м), 5,63 (1H, с), 3,34-3,28 (1H, м), 1,36-1,29 (6H, м). MS (ES) для C16H12ClFN4 рассчитано: 314/316, найдено: 315/317 (M+H)+.
Стадия 2: 2-Фтор-5-[(5-изопропил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензойная кислота (G2)
Указанное в заголовке соединение получали, как описано в примере 1, A3. MS (ES) для C15H15FN2O3 рассчитано: 290, найдено: 291 (M+H)+.
Стадия 3: Трифторацетат 4-{2-фтор-5-[(5-изопропил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия (G3)
Указанное в заголовке соединение получали, как описано в примере 6, стадии 4+5. Указанное в заголовке соединение получали в виде желтого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,76 (1H, с), 8,74 (2H, ушир.с), 7,45-7,28 (3H, м), 7,19-7,17 (1H, м), 3,94 (2H, с), 3,86-3,73 (2H, м), 3,55-3,18 (6H, м), 3,02-3,00 (1H, м), 2,07-1,90 (2H, м), 1,15-1,12 (6H, м). MS (ES) для C20H25FN4O2 рассчитано: 372, найдено: 373 (M+H)+.
ПРИМЕР 8
Трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (H2)
Стадия 1: трет-Бутил 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-карбоксилат (H1)
К раствору из примера 14, N4 (1 экв.) в DMA (3,7 мл, 0,4 М) добавляли HBTU (1,2 экв.), трет-бутил 1-гомопиперазинкарбоксилат (1,4 экв.) и DIPEA (3 экв.). Реакционную смесь перемешивали 1 час при комнатной температуре. Реакцию тушили насыщенным водным NaHCO3 и экстрагировали CH2Cl2. Объединенные органические фракции промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Неочищенный продукт очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов и объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,69 (1H, с), 7,31-7,07 (3H, м), 4,00-3,98 (2H, м), 3,72-3,54 (3H, м), 3,39-3,35 (4H, м), 3,29-3,27 (1H, м), 2,03 (6H, ушир.с), 1,79-1,77 (1H, м), 1,50-1,48 (1H, м), 1,42 (7,7H, с), 1,31 (2,3H, с). MS (ES) для C24H31FN4O4 рассчитано: 458, найдено: 459 (M+H)+.
Стадия 2: Трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия (H2)
Указанное в заголовке соединение получали, как описано в примере 6, стадия 5, и получали в виде желтого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,73 (1H, с), 8,11 (2H, ушир.с), 7,36-7,26 (3H, м), 4,00 (2H, с), 3,85-3,54 (2H, м), 3,37-3,20 (6H, м), 2,05-2,03 (7H, м), 1,90-1,88 (1H, м). MS (ES) для C19H23FN4O2 рассчитано: 358, найдено: 359 (M+H)+.
ПРИМЕР 9
Трифторацетат 1-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,2-диметил-1-оксопропан-2-аммония (I2).
Стадия 1: трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия (I1)
К раствору промежуточного соединения примера 14, N4 (1 экв.) в ДМФА (0,97 мл, 0,4 M) добавляли HBTU (1,2 экв.) и DIPEA (5 экв.). Через 10 мин при комнатной температуре к нему добавляли трет-бутил 1-пиперазинкарбоксилат (1,2 экв.) и реакционный раствор перемешивали в течение ночи при комнатной температуре. Реакцию гасили насыщенным водным NaHCO3 и экстрагировали с CH2Cl2. Органическую фазу промывали один раз 1 н. HCl и насыщенным солевым раствором. Объединенные органические фракции промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Сырой продукт растворяли в растворе TFA:CH2C12 (1:2, 3,4 мл) и полученный раствор перемешивали 1 час при комнатной температуре. Растворитель упаривали досуха и неочищенный продукт очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов (колонка: Water X-Terra C18). Фракции продукта лиофилизировали с получением указанного в заголовке соединения в виде желтых кристаллов. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,71 (1H, с), 8,92 (2H, ушир.с), 7,32-7,30 (3H, м), 4,00 (2H, с), 3,86-3,84 (2H, м), 3,46-3,44 (2H, м), 3,25-3,23 (2H, м), 3,11-3,09 (2H, м), 2,05 (3H, с), 2,04 (3H, с). MS (ES) для C18H21FN4O2 рассчитано: 344, найдено: 345 (M+H)+.
Стадия 2: трифторацетат 1-(4-(5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,2-диметил-1-оксопропан-2-аммония (I2)
N-BOC-N,2-диметилаланин (3 экв.), HATU (3 экв.) и DIPEA (3 экв.) растворяли в ДМФА (40 мкл, 0,1 M). Через 10 мин при комнатной температуре добавляли раствор I1 и DIPEA (1,2 экв.) в ДМФА (0,1 мл, 0,3 M). Реакционный раствор перемешивали в течение ночи при комнатной температуре. Неочищенный продукт очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов (колонка: Water X-Terra C18). Продукт фракции лиофилизировали, что дало указанные в заголовке соединения в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,72 (1H, с), 8,84-8,82 (2H, м), 7,38-7,25 (3H, м), 4,00 (2H, с), 3,71 (4H, с), 3,59 (2H, ушир.с), 3,31 (2H, ушир.с), 2,06 (3H, с), 2,04 (3H, с), 1,58 (6H, с). MS (ES) для C23H30FN5O4 рассчитано: 443, найдено: 444 (M+H)+.
ПРИМЕР 10
Трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-1-азониаспиро[4,5]декана (J1)
Указанное в заголовке соединение получали, как описано в примере 9. Продукт примера 14, N4, вводили во взаимодействие с оксалатной солью трет-бутил l,8-диазаспиро[4,5]декан-1-карбоксилата. Указанное в заголовке соединение получали в виде желтого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,71 (1H, с), 8,73 (2H, ушир.с), 7,36-7,22 (3H, м), 4,15-4,11 (1H, м), 4,00 (2H, с), 3,38-3,25 (5H, м), 2,05-1,76 (14H, м). MS (ES) для C22H27FN4O2 рассчитано: 398, найдено: 399 (M+H)+.
ПРИМЕР 11
Бис(трифторацетат) 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-2-ия-3-ил)метил]-2-фторбензоил}-1- метил-8-аза-1-азониаспиро[4,5]декана (K1)
К раствору продукта примера 11, J1 (1 экв.) в MeOH (0,5 мл, 0,1 M) добавляли TEA (2,2 экв.) до pH 6-7. Затем добавляли формальдегид (10 экв., 37% в H2O), NaBH3(CN) (8 экв.) и NaOAc (2,8 экв.). Реакционный раствор перемешивали в течение ночи при комнатной температуре. Растворитель удаляли и неочищенный продукт очищали методом препаративной RP-HPLC с применением H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение. Показаны сигналы основного ротамера 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,72 (1H, ушир.с), 9,63 (1H, ушир.с), 7,36-7,24 (3H, м), 4,63-4,60 (1H, м), 4,00 (2H, с), 3,61 (1H, ушир.с), 3,49-3,42 (1H, м), 3,23-3,17 (2H, м), 2,98-2,84 (1H, м), 2,75-2,73 (2H, м), 2,58 (3H, с), 2,40-2,31 (1H, м), 2,04 (6H, с), 1,97-1,79 (4H, м), 1,63-1,60 (1H, м). MS (ES) для C23H29FN4O2 рассчитано: 412, найдено: 413 (M+H)+.
ПРИМЕР 12
Трифторацетат 4-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-N,N-диметил-2-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензоламмония (L3)
Стадия 1: 2-(Диметиламино)-5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензонитрил (L1)
Раствор продукта примера 14, N3 (1 экв.) и диметиламин (4 экв., 2 M в MeOH) в сухом ДМФА (2,7 мл, 0,1 M) запаивали в микроволновой ампуле. Реакционный раствор нагревали до 180°C и перемешивали в течение 1,5 часов. Затем раствор охлаждали до комнатной температуры и растворитель упаривали в высоком вакууме. Неочищенный продукт очищали на SCX-картридже. Указанное в заголовке соединение промывали раствором 2 M NH3 в метаноле и концентрировали под пониженным давлением. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,67 (1H, ушир.с), 7,45 (1H, с), 7,33 (1H, д, J=8,4 Гц), 7,03 (1H, д, J=8,4 Гц), 3,90 (2H, с), 2,97 (6H, с), 2,05 (3H, с), 2,03 (3H, с). MS (ES) для C16H18N4O рассчитано: 282, найдено: 283 (M+H)+.
Стадия 2: 2-(Диметиламино)-5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензойная кислота (L2)
L1 (1 экв.) суспендировали в H2O (0,4 мл, 0,7 M) и к полученной суспензии добавляли водный раствор 15 M NaOH (8 экв.) и нагревали до температуры кипения с обратным холодильником в течение 72 часов. Реакционный раствор охлаждали до комнатной температуры и подкисляли до pH 4 действием 2 M HCl. Неочищенный продукт очищали на SCX-картридже. Указанный в заголовке продукт промывали раствором 2 M аммиака в метаноле и концентрировали под пониженным давлением. MS (ES) для C16H19N3O3 рассчитано: 301, найдено: 302 (M+H)+.
Стадия 3: Трифторацетат 4-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-N,N-диметил-2-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8Н)-ил]карбонил}бензоламмония (L3)
L2 (1 экв.), TBTU (1,1 экв.) и DIPEA (1 экв.) растворяли в ДМФА (0,6 мл, 0,2 M) и раствор перемешивали 10 мин при комнатной температуре. Затем к нему добавляли раствор хлорид 3-(трифторметил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ия (PTC Int. Appl., WO 2005020929) (1,1 экв.) и DIPEA (1,2 экв.) в ДМФА (0,3 мл, 0,2 M). Реакционную смесь перемешивали в течение ночи при комнатной температуре. Неочищенный продукт очищали методом препаративной RP-HPLC с применением H2O (0,1% TFA) и MeCN (0,1 %TFA) в качестве элюентов (колонка: Water X-Terra C18). Объединенные фракции продукта лиофилизировали, что дало указанное в заголовке соединение в виде желтого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,67 (1H, ушир.с), 7,24-7,07 (3H, м), 5,07-5,05 (1H, м), 4,58 (1H, ушир.с), 4,26-4,13 (3H, м), 3,92 (2H, с), 2,75 (3H, с), 2,5 (3H, перекрывается пиком растворителя), 2,03 (6H, с). MS (ES) для C22H24F3N7O5 рассчитано: 475, найдено: 476 (M+H)+.
ПРИМЕР 13
Трифторацетат 6-(4-изопропокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия (M3)
Стадия 1: 5-[(4,5-Диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-изопропоксибензонитрил (M1)
Раствор изопропоксида натрия получали реакцией натрия (2,5 экв.) с сухим 2-пропанолом (3 мл, 0,03 M), к этому раствору добавляли раствор примера 14, N3 (1 экв.) в сухом 2-пропаноле (2,4 мл, 0,02 M). Полученный раствор нагревали до температуры кипения с обратным холодильником и перемешивали в течение 5 часов. Реакционный раствор охлаждали до комнатной температуры и растворитель упаривали в высоком вакууме. Сырой продукт растворяли в EtOAc. Органическую фазу промывали дважды водой, высушивали (Na2SO4) и растворитель упаривали досуха. MS (ES) для C17H19N3O2 рассчитано: 297, найдено: 298 (M+H)+.
Стадия 2: 5-[(4,5-Диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-изопропоксибензойная кислота (M2)
М1 (1 экв.) суспендировали в H2O (0,3 мл, 0,7 M) и к полученной суспензии добавляли 15 M водный раствор NaOH (8 экв.) и нагревали до температуры кипения с обратным холодильником в течение 48 часов. Реакционный раствор охлаждали до комнатной температуры и подкисляли до pH 4 действием 2 M HCl. Неочищенный продукт очищали на SAX-картридже. Указанный в заголовке продукт промывали раствором 2 M HCl в метаноле и растворитель концентрировали под пониженным давлением. MS (ES) для C17H20N2O4 рассчитано: 316, найдено: 317 (M+H)+.
Стадия 3: Трифторацетат 6-(4-изопропокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия (M3)
Указанное в заголовке соединение получали, как описано в примере 12, стадия 3, получали в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,70 (1H, с), 7,26-7,24 (1H, м), 7,13-7-05 (2H, м), 5,23-5,19 (0,4H, м), 4,93-4,88 (0,4H, м), 4,65-4,63 (1,6H, м), 4,54-4,25 (1,6H, м), 4,16-4,10 (2H, м), 3,93-3,87 (3H, м), 2,05-2,03 (6H, м), 1,26-1,21 (3H, м), 1,00-0,92 (3H, м). MS (ES) для C23H25F3N6O3 рассчитано: 490, найдено: 491 (M+H)+.
ПРИМЕР 14
6-(4-Фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он
Стадия 1: 5-[(6-Хлор-4,5-диметилпиридазин-3-ил)(циано)метил]-2-фторбензонитрил (N1)
Методика повторяет методику, описанную в примере 1, стадия 1, исходя из 3,6-дихлор-4,5-диметилпиридазинона (получен согласно J. Org. Chem. 1955, 20, 707-13). 1H-ЯМР (300 МГц, ДМСО-d6) δ: 8,05-7,96 (1H, м), 7,95-7,82 (1H, м), 7,70-7,61 (1H, м), 6,48 (1H, с), 2,41 (3H, с), 2,29 (3H, с). MS (ES) для C15H10ClFN4 рассчитано: 300, найдено: 301 (M+H)+.
Стадия 2: 5-[(6-Хлор-4,5-диметилпиридазин-3-ил)метил]-2-фторбензонитрил (N2)
Промежуточное соединение N1 суспендировали в смеси уксусной кислоты, концентрированной водной HCl, и воды (1:1:2, 0,07 М). Суспензию перемешивали и нагревали при кипячении с обратным холодильником в течение 75 мин. Реакционную смесь охлаждали до комнатной температуры и растворители удаляли под пониженным давлением. К остатку добавляли насыщенный водный NaHCO3 и смесь экстрагировали EtOAc. Органическую фазу сушили (Na2SO4), фильтровали и концентрировали досуха. Остаток очищали методом колоночной хроматографии на силикагеле, элюировали смесью петролейный эфир-EtOAc (10-80% EtOAc), что дало указанное в заголовке соединение в виде желтого твердого вещества. MS (ES) для C14H11ClFN3 рассчитано: 275, найдено: 276 (M+H)+.
Стадия 3: 5-[(4,5-Диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензонитрил (N3)
К раствору промежуточного соединения N2 в уксусной кислоте (0,16 M) добавляли NaOAc (2 экв.) и смесь перемешивали и нагревали до кипения с обратным холодильником в течение 1 часа. Раствор охлаждали до комнатной температуры и растворитель удаляли под пониженным давлением. Остаток суспендировали в воде и растирали в порошок до получения тонкой суспензии. Твердое вещество отфильтровывали, промывали водой, высушивали в потоке воздуха и затем в высоком вакууме. MS (ES) для C14H12FN3O рассчитано: 257, найдено: 258 (M+H)+.
Стадия 4: 5-[(4,5-Диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензойная кислота (N4)
К суспензии промежуточного соединения N3 в воде (0,35 M) добавляли NaOH (8 экв.) и полученную смесь перемешивали и нагревали до 100°C в течение 60 мин. Смесь охлаждали в ледяной бане и медленно подкисляли до pH 2-3 действием 6 н. HCl. Образующийся легкий желтый осадок отфильтровывали, высушивали в потоке воздуха и затем в высоком вакууме. MS (ES) для C14H13FN2O3 рассчитано: 276, найдено: 277 (M+H)+.
Стадия 5: 6-(4-Фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил}карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он (N5)
Промежуточное соединение N4 (1 экв.), TBTU (2 экв.) и DIPEA (1,1 экв.) растворяли в ДМФА (1,1 мл, 0,2 M) и раствор перемешивали 10 мин при комнатной температуре. Затем добавляли раствор хлорида 3-(трифторметил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-7-ия (PTC Int. Appl., WO 2005020929) (2,2 экв.) и DIPEA (1,2 экв.) в ДМФА (1,4 мл, 0,2 M). Реакционную смесь перемешивали 5 часов при комнатной температуре. Реакционную смесь разбавляли EtOAc и промывали дважды насыщенным солевым раствором. Органическую фазу сушили (Na2SO4) и концентрировали под пониженным давлением. Неочищенный продукт очищали методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Фракции продукта лиофилизировали и полученную трифторуксусную соль распределяли между EtOAc и насыщенным водным раствором NaHCO3. Органическую фазу сушили (Na2SO4) и растворитель упаривали досуха. Соединение, обозначенное в заголовке примера, получали в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,70 (1H, с), 7,42-7,31 (3H, м), 5,09 (1H, ушир.с), 4,75 (1H, ушир.с), 4,28 (1H, ушир.с), 4,16 (2H, ушир.с), 4,01 (2H, с), 3,78-3,76 (1H, м), 2,05-2,03 (6H, м). MS (ES) для C20H18F4N6O2 рассчитано: 450, найдено: 451 (M+H)+.
ПРИМЕР 15
6-(4-Фтор-3-{[4-(2-метилпролил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2H)-он
Смесь 1-(трет-бутоксикарбонил)-2-метилпролина (1 экв.), TEA (2 экв.), PyBOP (1 экв.) и 6-[4-фтор-3-(пиперазин-1-илкарбонил)бензил]-4,5-диметилпиридазин-3(2H)-она (I1) в сухом ДМФА (0,1 M) нагревали при 60°C с микроволновым облучением в течение 2 часов. Продукт выделяли методом препаративной ΗPLC. После лиофильной сушки объединенных фракций продукта остаток растворяли в 10% TFA/DCM и раствор отогревали до 45°C в течение 1 часа. Остаток, полученный после упаривания растворителя, далее очищали на SCX-картридже. Лиофильная сушка от воды/MeCN приводила к указанному в заголовке соединению в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,67 (1H, с), 7,38-7,13 (3H, м), 3,96 (2H, с), 3,8-3,5 (5H, м), 3,3 (1H под водой сигнал), 3,26-3,13 (2H, м), 2,92-2,78 (1H, м), 2,76-2,58 (1H, м), 2,34-2,15 (1H, м), 2,02 (3H, с), 2,00 (3H, с), 1,75-1,46 (3H, м), 1,26 (3H, с). MS (ES) для C24H30FN5O3 рассчитано: 455, найдено: 456 (M+H)+.
ПРИМЕР 16
Трифторацетат 6-[4-фтор-3-(4-метил-2,5-диоксоимидазолидин-1-ил)бензил]-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия
Стадия 1: трет-бутил {5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторфенил}карбамат (O1)
К смеси Примера 14, N4, в трет-BuOH:толуол (1:1, 0,171 M) добавляли дифенилфосфорилазид (2,2 экв.) и Et3N (2,2 экв.). Реакционную смесь нагревали при кипячении с обратным холодильником до исчерпания исходного вещества, затем легкокипящие продукты удаляли под пониженным давлением. Полученный остаток распределяли между DCM и насыщенным водным NaHCO3; органическую фазу отделяли, высушивали (Na2SO4) и фильтровали. Упаривание растворителя приводило к желтому маслу (O1), которое применяли как таковое на следующей стадии без очистки. MS (ES) для C18H22FN3O3 рассчитано: 347, найдено: 348 (M+H)+.
Стадия 2: трифторацетат 6-(3-{[N-(этоксикарбонил)аланил]амино}-4-фторбензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия (O2)
O1 растворяли в DCM:TFA (1:1, 0,17 M) и смесь перемешивали при комнатной температуре в течение 1 часа, затем летучие продукты удаляли в высоком вакууме. Полученное масло и DIPEA (2,35 экв.) добавляли к перемешиваемому раствору N-(этоксикарбонил)аланина (1,35 экв.), TBTU (1,35 экв.) и DIPEA (1,35 экв.) в сухом ДМФА (0,3 M). Смесь перемешивали при комнатной температуре в течение 2 дней и затем разбавляли DCM и промывали водой. Органическую фазу промывали насыщенным солевым раствором, высушивали (Na2SO4) и концентрировали под пониженным давлением. Продукт выделяли методом препаративной HPLC, используя MeCN/воду (0,1% TFA) в качестве элюентов. Объединенные фракции продукта лиофилизировали с получением указанного в заголовке соединения (О2) в виде белое пушистого порошка. MS (ES) для C19H23FN4O4 рассчитано: 390, найдено: 391 (M+H)+. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,65 (1H, с), 9,61 (1H, с), 7,76-7,65 (1H, м), 7,45-7,30 (2H, м), 7,23-7,10 (1H, м), 7,01-6,90 (1H, м), 4,27 (1H, м), 3,98 (2H, кв., J=6,9 Гц), 3,90 (2H, с), 2,03-1,96 (6H, м), 1,30-1,23 (3H, м), 1,16 (3H, т, J=6,6 Гц).
Стадия 3: трифторацетат 6-[4-фтор-3-(4-метил-2,5-диоксоимидазолидин-1-ил)бензил]-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия (О3)
К раствору О2 в ДМФА (0,1 M) добавляли DMAP (3 экв.) и смесь нагревали в микроволновой печи при 180°C в течение 2 часов. Продукт выделяли с помощью препаративной RP-HPLC, используя H2O (+0,1% TFA) и MeCN (+0,1% TFA) в качестве элюентов. Желаемые фракции лиофилизировали с получением искомого соединения. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 12,67 (1H, с), 8,52 (1H, с), 7,35-7,28 (2H, м), 7,25-7,18 (1H, м), 4,36-4,26 (1H, м), 3,97 (2H, с), 2,06-1,97 (6H, м), 1,38-1,31 (3H, м). MS (ES) для C17H18FN4O3 рассчитано: 344, найдено: 345 (M+H)+.
ПРИМЕР 17
Трифторацетат 6-(3-{[3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}-4-фторбензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия
Стадия 1: Метил N-(трет-бутоксикарбонил)-2-метилаланинат (P1)
К раствору Boc-α-метилаланина в ДМФА (0,4 M) добавляли K2CO3 (1 экв.) и MeI (1,2 экв.). Смесь перемешивали при комнатной температуре в течение 6 часов и затем разбавляли EtOAc, промывали водой и насыщенным водным NaHCO3. Органическую фазу сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением указанного в заголовке соединения в виде желтого твердого вещества. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 7,20 (1H, ушир.с), 3,58 (3H, с), 1,40-1,27 (15H, м). MS (ES) для C10H19NO4 рассчитано: 217, найдено: 240 (M+Na)+.
Стадия 2: трет-Бутил (2-гидразино-1,1-диметил-2-оксоэтил)карбамат (P2)
К раствору P1 в 2-пропаноле (0,56 M) добавляли моногидрат гидразина (10 экв.) и смесь перемешивали в течение ночи при 90°C. Летучие продукты удаляли в высоком вакууме и полученное неочищенное вещество применяли как таковое на следующей стадии. MS (ES) для C9H19N3O3 рассчитано: 217, найдено: 240 (M+Na)+.
Стадия 3: Бензил 5-(2-{2-[(трет-бутоксикарбонил)амино]-2-метилпропаноил}гидразино)-3,6-дигидропиразин-1(2H)-карбоксилат (P3)
При добавлении Me3O+BF4 - (1 экв.) к раствору бензил 3-оксопиперазин-1-карбоксилата (1 экв.) в DCM (0,85 M) реакционную смесь перемешивали в течение 48 часов. Затем добавляли P2, суспендированный в DCM, и перемешивание продолжали в течение еще 3 дней. Смесь разбавляли DCM и промывали 1 н. раствором NaOH. Органический слой сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением указанного в заголовке соединения в виде прозрачного масла, которое применяли как таковое на следующей стадии. MS (ES) для C21H31N5O5 рассчитано: 433, найдено: 434 (M+H)+.
Стадия 4: трифторацетат 7-[(бензилокси)карбонил]-3-{1-[(трет-бутоксикарбонил)амино]-1-метилэтил}-5,6,7,8- тетрагидро[1,2,4]триазоло[4,3-a]пиразин-1-ия (P4)
Раствор P3 в н-BuOH кипятили с обратным холодильником в течение 15 мин. Растворитель удаляли под пониженным давлением и полученный неочищенный продукт очищали в системе хроматографирования Biotage с градиентом при элюировании 0-15% MeOH/DCM и затем снова очищали препаративной RP-HPLC с применением H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Объединенные фракции продукта лиофилизировали с получением указанного в заголовке соединения в виде прозрачного масла. 1H-ЯМР (300 МГц, ДМСО-d6) δ: 7,55 (1H, ушир.с), 7,44-7,29 (5H, м), 5,14 (2H, ушир.с), 4,81 (2H, ушир.с), 4,08-3,97 (2H, м), 3,90-3,77 (2H, м), 1,55 (6H, ушир.с), 1,30 (9H, м). MS (ES) для C21H29N5O4 рассчитано: 415, найдено: 416 (M+H)+.
Стадия 5: Бензил 3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-карбоксилат (P5)
P4 растворяли в DCM:TFA (1:1, 0,105 M) и смесь перемешивали при комнатной температуре в течение 2 часов. Летучие продукты удаляли в высоком вакууме, остаток растворяли в MeOH (0,1 M) и затем добавляли TEA (3 экв.) до pH 7. К смеси добавляли формальдегид (37% водный раствор, 10 экв.), NaBH3(CN) (3 экв.) и AcOH (4 экв.) и смесь перемешивали при комнатной температуре в течение 2 часов. Летучие продукты упаривали и полученное неочищенное вещество очищали на SCX-картридже, элюировали желаемый продукт смесью NH3/MeOH. После упаривания растворителя прозрачное масло применяли как таковое на следующей стадии. MS (ES) для C18H25N5O2 рассчитано: 343, найдено: 344 (M+H)+.
Стадия 6: N,N-Диметил-2-(5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-a]пиразин-3-ил)пропан-2-амин (P6)
Смесь P5 (0,12 ммоль) и Pd/C (10%, 22 мг) в MeOH (0,2 M) перемешивали в атмосфере водорода в течение ночи. Катализатор отфильтровывали и растворитель удаляли под пониженным давлением для получения неочищенного масла, применяемого как таковое на следующей стадии. MS (ES) для C10H19N5 рассчитано: 209, найдено: 210 (M+H)+.
Стадия 7: трифторацетат 6-(3-{[3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-a]пиразин-7(8H)-ил]карбонил}-4-фторбензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия (P7)
К раствору из примера 14, N4, и DIPEA (1,3 экв.) в ДМФА (0,3 M) добавляли TBTU (1,3 экв.). Полученную смесь перемешивали при комнатной температуре в течение 40 минут и затем добавляли P6 (1 экв.). Перемешивание продолжали в течение 1 часа и продукт выделяли методом препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Объединенные фракции продукта лиофилизировали с получением указанного в заголовке соединения в виде белого порошка. 1H-ЯМР (400 МГц, ДМСО-d6) δ: 12,67 (1H, с), 10,12 (1H, ушир.с), 7,43-7,36 (1H, м), 7,35-7,23 (2H, м), 4,99 (1H, ушир.с), 4,66 (1H, ушир.с), 4,29 (1H, ушир.с), 3,98 (2H, с), 4,20-3,63 (3H, частично перекрывается с сигналом воды), 2,80-2,69 (6H, м), 2,04-1,97 (6H, м), 1,78-1,66 (6H, м). MS (ES) для C24H31FN7O2 рассчитано: 467, найдено: 468 (M+H)+.
ПРИМЕР 18
Трифторацетат (2R)-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилазетидиния (Q2)
Стадия 1: трет-Бутил (2R)-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилазетидин-1-карбоксилат (Q1)
Раствор (2R)-1-(трет-бутоксикарбонил)-2-метилазетидин-2-карбоновой кислоты (1,5 экв.) и HATU (1,5 экв.) в сухом ДМФА (0,1 М) перемешивали при комнатной температуре в течение 30 мин. Затем добавляли продукт Примера 14, N4 (1,0 экв.) и DIPEA (1,5 экв.). Реакционную смесь перемешивали при 40°C в течение 48 часов, затем разбавляли EtOAc, промывали последовательно насыщенным водным раствором NaHCO3, 1 н. раствором HCl и насыщенным солевым раствором. Полученный раствор сушили (Na2SO4), фильтровали и концентрировали с получением указанного в заголовке соединения, которое применяли на следующей стадии без дополнительной очистки. MS (ES) для C28H36FN5O5 рассчитано: 541, найдено: 542 (M+H)+.
Стадия 2: трифторацетат (2R)-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилазетидиния (Q2)
(Q1) растворяли в смеси DCM/TFA (9:1, 0,06 М) и перемешивали в течение 18 часов при комнатной температуре. Растворитель упаривали под пониженным давлением и неочищенный продукт очищали препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Желаемые фракции лиофилизировали с получением указанного в заголовке соединения (Q2) в виде белого твердого вещества. 1H-ЯМР (400 МГц, ДМСО-d6, 300K) δ: 12,67 (1H, с), 9,16 (1H, ушир.с), 8,91 (1H, ушир.с), 7,35-7,17 (3H, м), 4,07-3,91 (3H, м), 3,8-3,15 (9H, м), 2,92-2,73 (1H, м), 2,60-2,25 (1H, м, перекрывается с сигналом ДМСО), 2,00 (3H, с), 1,99 (3H, с), 1,77 (1,5H, с), 1,72 (1,5H, с). MS (ES) для C25H29F3N5O5 рассчитано: 441, найдено: 442 (M+H)+.
ПРИМЕР 19
Трифторацетат 6-{4-фтор-3-[(4-{[1-(изобутиламино)циклопентил]карбонил}пиперазин-1-ил}карбонил]бензил}-4,5-диметилпиридазин-3(2H)-он (R2)
Стадия 1: 6-[3-({4-[(1-аминоциклопентил)карбонил]пиперазин-1-ил}карбонил)-4-фторбензил]-4,5-диметилпиридазин-3(2H)-он (R1)
Желаемое соединение получали по следующей общей методике, приведенной в примере 18, стадия 1 и 2, используя 1-[(трет-бутоксикарбонил)амино]циклопентанкарбоновую кислоту и продукт Примера 14, N4, в качестве исходных веществ. Кроме того, на стадии 1 добавляли HOBT (1,3 экв.). Продукт получали в виде желтого твердого вещества после очистки на SCX-картридже. MS (ES+) для C24H30FN5O3 рассчитано: 455, найдено: 456 (M+H)+.
Стадия 2: трифторацетат 6-{4-фтор-3-[(4-{[1-(изобутиламино)циклопентил]карбонил}пиперазин-1-ил)карбонил]бензил}-4,5-диметилпиридазин-3(2H)-он (R2)
R1 (1,0 экв.) и 2-метилпропаналя (1,0 экв.) в сухом метаноле (0,04 М) перемешивали при комнатной температуре в течение 2 часов, NaBH3(CN) (1,0 экв.) добавляли и перемешивали при комнатной температуре в течение 1 часа. Затем добавляли воду и водную фазу экстрагировали EtOAc. Органическую фазу сушили (MgSO4), фильтровали и растворители удаляли под пониженным давлением. Неочищенный продукт очищали препаративной RP-HPLC, используя H2O (0,1% TFA) и MeCN (0,1% TFA) в качестве элюентов. Желаемые фракции лиофилизировали с получением указанного в заголовке соединения (CSF2) в виде белого твердого вещества. 1H-ЯМР (400 МГц, ДМСО-d6, 300K) δ: 12,66 (1H, с), 8,40 (2H, ушир.с), 7,35-7,16 (3H, м), 3,95 (2H, с), 3,72-3,40 (6H, м), 3,28 (2H, м), 2,68 (2H, м), 2,52 (1H, м), 2,13 (4H, м), 2,08 (3H, с), 1,98 (3H, с), 1,88 (4H, м), 0,96 (6H, д, J=6,4 Гц). MS (ES) для C28H38FN5O3 рассчитано: 511, найдено: 512 (M+H)+.
Следующие соединения получали согласно методикам, описанным в приведенных примерах.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРИДАЗИНОНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ PARP | 2008 |
|
RU2490265C2 |
| ИНГИБИТОРЫ НЕПРИЛИЗИНА | 2011 |
|
RU2622288C2 |
| ЗАМЕЩЕННЫЕ АМИНОМАСЛЯНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ НЕПРИЛИЗИНА | 2012 |
|
RU2604522C2 |
| ДИГИДРОПИРИДОФТАЛАЗИНОНОВЫЕ ИНГИБИТОРЫ ПОЛИ(АДФ-РИБОЗА)ПОЛИМЕРАЗЫ | 2009 |
|
RU2514937C2 |
| ПРОИЗВОДНОЕ ФТАЛАЗИНОНКЕТОНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2011 |
|
RU2564527C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИМИДАЗОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2686314C1 |
| КОМБИНАЦИОННОЕ ЛЕКАРСТВО | 2003 |
|
RU2328280C2 |
| ТРИЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКОЕ СОЕДИНЕНИЕ | 2016 |
|
RU2715413C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2422444C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ЦИАНОЕНОНА КАК МОДУЛЯТОРЫ KEAP1 | 2021 |
|
RU2822828C1 |
Настоящее изобретение относится к соединениям формулы (IX), в которой радикалы и символы имеют значения, определенные в формуле изобретения, и их фармацевтически приемлемым солям или таутомерам. Данные соединения являются ингибиторами поли(АDР-рибоза)полимеразы (PARP) и могут быть применены для лечения рака, воспалительных заболеваний, реперфузионных повреждений, ишемических состояний, удара, почечной недостаточности, кардиососудистых заболеваний, сосудистых заболеваний, отличных от кардиососудистых заболеваний, сахарного диабета, нейродегенеративных заболеваний, ретровирусных инфекций, повреждения сетчатки, старения кожи и индуцированного УФ-светом повреждения кожи и в качестве химио- или радиосенсибилизаторов при лечении рака. Изобретение также относится к фармацевтической композиции, их содержащей, применению этих соединений и способу лечения указанных выше заболеваний. 7 н. и 3 з.п. ф-лы, 18 пр., 1 табл.
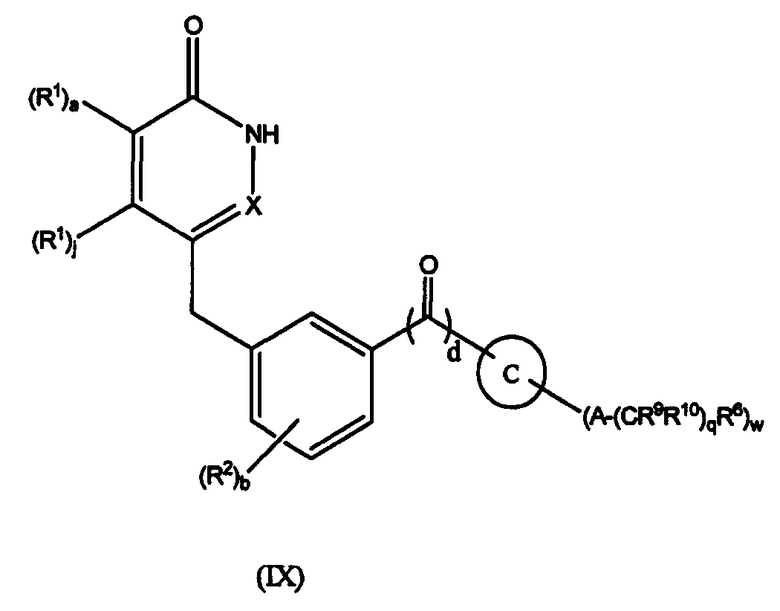
1. Соединение формулы IX:
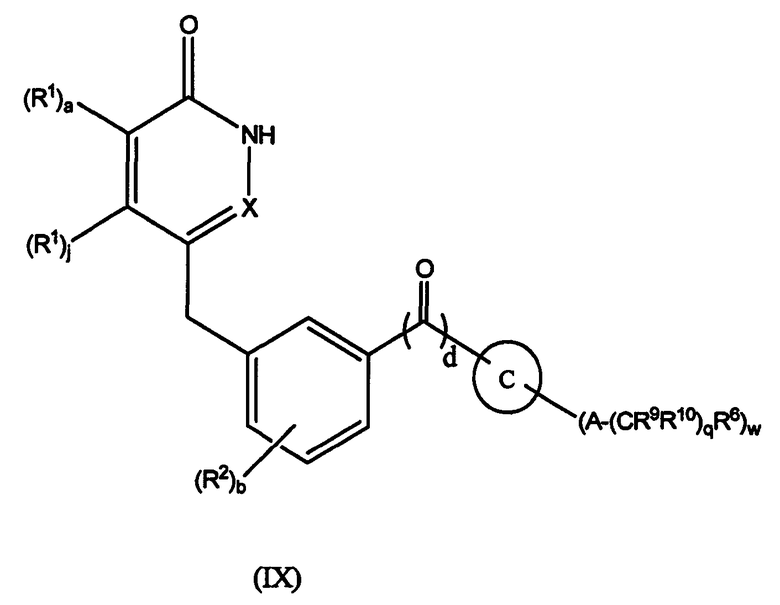
в котором сумма a и j равна 1 или 2;
b равно 0 или 1;
d равно 0 или 1;
Х представляет собой N;
R1 каждый независимо представляет собой С1-6-алкил;
R2 каждый независимо представляет собой галоген, C1-6-алкокси, NH2 или N(С1-6-алкил)2;
С представляет собой 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N, или 5- или 6-членное насыщенное гетероциклическое кольцо, содержащее один или два атома N, или 7-15-членное моноциклическое или конденсированное или спиросочлененное полициклическое насыщенное или частично насыщенное гетероциклическое кольцо, содержащее 2-4 гетероатома, независимо выбранных из N и О;
А каждый независимо представляет собой простую связь, О, С=O или NR7;
q каждый независимо равен 0, 1 или 2;
w равно 0, 1, 2 или 3;
R6 каждый независимо представляет собой оксо, С1-6-алкил, галоген-С1-6-алкил, NRaRb или цикл, который представляет собой С3-10-циклоалкил; С6-10-арил; С6-10-арилокси; 4-членное насыщенное гетероциклическое кольцо, содержащее один атом N; 5-или 6-членное насыщенное гетероциклическое кольцо, содержащее один гетероатом, выбранный из N и О; 5-членное гетероароматическое кольцо, содержащее 1 или 2 гетероатома, независимо выбранных из N, О и S, не более чем один гетероатом из которых представляет собой О или S; 6-членное гетероароматическое кольцо, содержащее 1 или 2 атома азота; или 9-10-членное бициклическое ненасыщенное или частично насыщенное гетероциклическое кольцо, содержащее 2 гетероатома, выбранных из N или О;
R7 представляет собой водород или C1-6-алкил;
R8 каждый независимо представляет собой циано, галоген, C1-6-алкил, C1-6-алкокси, галоген-С1-6-алкил, -(С=O)С1-6-алкил, NRaRb, С6-10-арил-C1-6-алкил, С6-10-арил-С1-6-алкоксикарбонил или С6-10-арил, где арильное кольцо необязательно замещено группой, независимо выбранной из галогена, C1-6-алкила или галоген-С1-6-алкила;
каждый из R9 и R10 независимо представляют собой водород, C1-6-алкил или галоген-С1-6-алкил;
каждый из Ra и Rb независимо являются выбранными из водорода, C1-6-алкила; С3-10-циклоалкил-С1-6-алкила, фенила или фенилС1-6-алкила;
или его фармацевтически приемлемая соль, или таутомер.
2. Соединение по п.1, где R2 представляет собой фтор.
3. Соединение, выбранное из группы, включающей
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
6-{3-[(4-ацетил-1,4-диазепан-1-ил)карбонил]-4-фторбензил}-4-этилпиридазин-3(2Н)-он;
1-ацетил-4-{5-[(6-хлор-4-этилпиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан;
4-этил-6-(4-фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензил)пиридазин-3(2Н)-он;
трифторацетат 4-{5-[(5-этил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4-этил-5-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{2-фтор-5-[(5-изопропил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 1-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,2-диметил-1-оксопропан-2-аммония;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-З-ил)метил]-2-фторбензоил}-8-аза-1-азониаспиро[4,5]декан;
бис(трифторацетат)8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-2-ий-3-ил)метил]-2-фторбензоил}-1-метил-8-аза-1-азониаспиро[4,5]декана;
трифторацетат 4-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-N,N-диметил-2-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензоламмония;
трифторацетат 6-(4-изопропокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
6-(4-фтор-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2Н)-он;
6-(4-фтор-3-{[4-(2-метилпролил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-[4-фтор-3-(4-метил-2,5-диоксоимидазолидин-1-ил)бензил]-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(3-{[3-[1-(диметиламино)-1-метилэтил]-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}-4-фторбензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат(2R)-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилазетидиния;
трифторацетат 6-{4-фтор-3-[(4-{[1-(изобутиламино)циклопентил]карбонил}пиперазин-1-ил)карбонил]бензил}-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ил)пиримидин-1-ия;
трифторацетат 4-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пиридиния;
трифторацетат 2-{[(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)окси]метил}пиридиния;
трифторацетат 2-{[(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-3-ил)окси]метил}пиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-5-метоксипиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-4-метоксипиридиния;
трифторацетат 4-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пирролидин-3-ил)пиридиния;
трифторацетат 1-({5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-3-ил)-N,N-диметилметанаммония;
4-этил-6-[4-фтор-3-(1'Н-спиро[1-бензофуран-3,4'-пиперидин]-1'-илкарбонил)бензил]пиридазин-3(2Н)-он;
трифторацетат 1-[2-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)этил]-1Н-пиразол-2-ия;
трифторацетат 5-хлор-2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиридиния;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-6-метоксипиридиния;
трифторацетат 3-бензил-7-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидроимидазо[1,2-а]пиразин-1-ия;
трифторацетат 2-(4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-3,6-диметилпиразин-1-ия;
трифторацетат 4-этил-6-{4-фтор-3-[(3-фенил-5,6-дигидроимидазо[1,2-а]пиразин-7(8Н)-ил)карбонил]бензил}-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-(3-метоксибензил)пиперазин-1-ия;
трифторацетат 2-(1-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)-1,2,3,4-тетрагидроизохинолиния;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
трифторацетат 4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-фенилпиперазин-1-ия;
трифторацетат 3-бензил-4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
бис(трифторацетат)4-{5-[(5-этил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-2-(пиридиний-3-илметил)пиперазин-1-ия;
6-(3-{[4-(циклопентилкарбонил)-1,4-диазепан-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2Н)-он;
6-(3-{[4-(циклопентилкарбонил)-1,4-диазепан-1-ил]карбонил}-4-фторбензил)-4-этилпиридазин-3(2Н)-он;
трифторацетат 4-{5-[(4,5-диэтил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{2-фтор-5-[(5-изопропил-4-метил-6-оксо-1,6-дигидропиридазин-3-ил)метил]бензоил}-1,4-диазепан-1-ия;
трифторацетат 4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ия;
6-{4-фтор-3-[(4-пропионилпиперазин-1-ил)карбонил]бензил}-4,5-диметилпиридазин-3(2Н)-он;
6-(3-{[4-(дифторацетил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2Н)-он;
6-(4-фтор-3-{[4-(3,3,3-трифторпропаноил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-{4-фтор-3-[(4-изобутирилпиперазин-1-ил)карбонил]бензил}-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пиридиния;
6-(4-фтор-3-{[4-(тетрагидрофуран-2-илкарбонил)пиперазин-1-ил]карбонил}бензил)-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 1-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,N,2-триметил-1-оксопропан-2-аммония;
трифторацетат 6-(4-фтор-3-{[4-(2,2,3,3,3-пентафторпропаноил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(4-фтор-3-{[4-(пирролидин-1-илкарбонил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 6-(4-фтор-3-{[4-(трифторацетил)пиперазин-1-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 1-(1-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пиперидиния;
трифторацетат 1-(1-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)пирролидиния;
трифторацетат 4-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)хиназолин-1-ия;
трифторацетат 2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиримидин-1-ия;
бис(трифторацетат)7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(3-метилфенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1,4-диия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-[4-(трифторметил)фенил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-[(4-фторфенокси)метил]-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-2-ия;
трифторацетат 3-циано-2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)пиридиния;
трифторацетат 3-(3,5-дифторфенил)-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
бис(трифторацетат) 3-[(диметиламмонио)метил]-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-2-ия;
трифторацетат (7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-3-ил)-N,N-диметилметанаммония;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил)-3-(2-фурил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(пентафторэтил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-{[4-(трифторметил)фенил]амино}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
хлорид 2-[(4-{2-фтор-5-[(6-гидрокси-4,5-диметилпиридазин-3-ил)метил]бензоил}пиперазин-1-ил)карбонил]-2-метилпирролидиния;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-фенил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 3-(1,3-бензодиоксол-5-ил)-7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(2-тиенил)-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-1-ия;
трифторацетат 3-циклопропил-6-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-4,5,6,7-тетрагидро-1Н-пиразоло[3,4-с]пиридин-2-ия;
трифторацетат 6-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(трифторметил)-4,5,6,7-тетрагидро-1Н-пиразоло[3,4-с]пиридин-2-ия;
трифторацетат 5-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-(трифторметил)-4,5,6,7-тетрагидро-1Н-пиразоло[4,3-с]пиридин-2-ия;
бис(трифторацетат) 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-3-пиридиний-3-ил-5,6,7,8-тетрагидро[1,2,4]триазоло[4,3-а]пиразин-2-ия;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-7-аза-1-азониаспиро[3,5]нонана;
трифторацетат 1-[(1-{3-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}азетидин-3-ил)метил]пирролидиния;
трифторацетат 1-(1-{3-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперидин-4-ил)-3,3-дифторазетидиния;
трифторацетат 5-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-(2,2,2-трифторэтил)-4,5,6,7-тетрагидро-1Н-[1,2,3]триазоло[4,5-с]пиридин-3-ия;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N-метилциклопентанаммония;
трифторацетат 7-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-метил-7-аза-1-азониаспиро[3,5]нонана;
трифторацетат 6-(4-метокси-3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензил)-4,5-диметил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-2-азониаспиро[4,5]декана;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-пропилпирролидиния;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-2-метил-8-аза-2-азониаспиро[4,5]декана;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пиперидиния;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-1-метилпиперидиния;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N,N-диметилциклопропанаммония;
трифторацетат 3-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-N,N-диметил-3-оксопропан-1-аммония;
трифторацетат 2-бензил-2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пирролидиния;
трифторацетат 4,5-диметил-6-(3-{[3-(трифторметил)-5,6-дигидро[1,2,4]триазоло[4,3-а]пиразин-7(8Н)-ил]карбонил}бензил)пиридазин-3(2Н)-он;
трифторацетат 6-[3-(1,8-диазаспиро[4,5]дец-8-илкарбонил)-4-фторбензил]-4-этил-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]пирролидиния;
трифторацетат 1-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-N-метилциклопропанаммония;
трифторацетат 3-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-1-метилпирролидиния;
трифторацетат 3-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-1,1,1-трифтор-N,N-диметил-3-оксопропан-2-амминия;
трифторацетат 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилпиперидиния;
бензил 2-[(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)карбонил]-2-метилпиперидин-1-карбоксилат;
4-этил-6-(4-фтор-3-{[1-(2,2,2-трифторэтил)-1,4,6,7-тетрагидро-5Н-[1,2,3]триазоло[4,5-с]пиридин-5-ил]карбонил}бензил)пиридазин-3(2Н)-он;
трифторацетат 4-этил-6-{4-фтор-3-[(1-метил-1,8-диазаспиро[4,5]дец-8-ил)карбонил]бензил}-3-оксо-2,3-дигидропиридазин-1-ия;
трифторацетат(2S)-2-[2-(4-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}пиперазин-1-ил)-2-оксоэтил]пирролидиния;
трифторацетат 8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-1-этил-8-аза-1-азониаспиро[4,5]декана;
трифторацетат 1-(циклопропилметил)-8-{5-[(4,5-диметил-6-оксо-1,6-дигидропиридазин-3-ил)метил]-2-фторбензоил}-8-аза-1-азониаспиро[4,5]декана;
6-[3-({4-[(1-анилиноциклопентил)карбонил]пиперазин-1-ил}карбонил)-4-фторбензил]-4,5-диметилпиридазин-3(2Н)-он;
6-[3-({4-[(1-аминоциклопентил)карбонил]пиперазин-1-ил}карбонил)-4-фторбензил]-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-{3-[(4-{[1-(бензиламино)циклопентил]карбонил}пиперазин-1-ил)карбонил]-4-фторбензил}-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-(3-{[4-({1-[(циклопропилметил)амино]циклопентил}карбонил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(4-фторбензил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(4-метилбензил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-[4-фтор-3-({4-[2-(1-нафтилметил)пролил]пиперазин-1-ил}карбонил)бензил]-4,5-диметилпиридазин-3(2Н)-он;
трифторацетат 6-(3-{[4-(2-этилпролил)пиперазин-1-ил]карбонил}-4-фторбензил)-4,5-диметилпиридазин-3(2Н)-он;
и их фармацевтически приемлемые соли, свободные основания и таутомеры.
4. Фармацевтическая композиция, обладающая ингибирующим действием в отношении поли(АDР-рибоза)полимеразы (PARP), включающая соединение по любому из пп.1-3, или его фармацевтически приемлемую соль, или таутомер в сочетании с фармацевтически приемлемым носителем.
5. Соединение по любому из пп.1-3, или его фармацевтически приемлемая соль, или таутомер для одновременного, раздельного или последовательного введения с противораковым средством.
6. Соединение по любому из пп.1-3, или его фармацевтически приемлемая соль, или таутомер, предназначенное для применения в терапии в качестве ингибитора PARP.
7. Применение соединения по любому из пп.1-3, или его фармацевтически приемлемой соли, или таутомера для приготовления лекарственного средства для лечения или предупреждения состояний, при которых может быть достигнуто улучшение путем ингибирования PARP.
8. Применение соединения по любому из пп.1-3, или его фармацевтически приемлемой соли, или таутомера для приготовления лекарственного средства для лечения или предупреждения рака, воспалительных заболеваний, реперфузионных повреждений, ишемических состояний, удара, почечной недостаточности, кардиососудистых заболеваний, сосудистых заболеваний, отличных от кардиососудистых заболеваний, сахарного диабета, нейродегенеративных заболеваний, ретровирусных инфекций, повреждения сетчатки, старения кожи или вызванного УФ-светом повреждения кожи.
9. Применение соединения по любому из пп.1-3, или его фармацевтически приемлемой соли, или таутомера в качестве химио- или радиосенсибилизатора при лечении рака.
10. Способ лечения или предупреждения рака, воспалительных заболеваний, реперфузионных повреждений, ишемических состояний, удара, почечной недостаточности, кардиососудистых заболеваний, сосудистых заболеваний, отличных от кардиососудистых заболеваний, сахарного диабета, нейродегенеративных заболеваний, ретровирусных инфекций, повреждения сетчатки, старения кожи или вызванного УФ-светом повреждения кожи, где способ включает введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по п.1 или композиции, включающей соединение по п.1.
| ПРОИЗВОДНЫЕ ПИРИДАЗИНОНА В КАЧЕСТВЕ АГОНИСТОВ РЕЦЕПТОРА ТИРЕОИДНОГО ГОРМОНА | 2006 |
|
RU2379295C2 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ определения истинной почеч-НОй пРОТЕиНуРии пРи зАбОлЕВАНияХ,СОпРОВОждАющиХСя гЕМАТуРиЕй | 1978 |
|
SU810218A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ ТОЧНОЙ УСТАНОВКИ В ФОРМАХ МЕТАЛЛИЧЕСКИХ ЧАСТЕЙ ПРИ ЗАЛИВКЕ ИХ В ОТЛИВАЕМЫЕ ИЗДЕЛИЯ | 1926 |
|
SU6300A1 |
| LEESON P.D | |||
| ET AL, "Selective Thyromemetics | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2013-01-20—Публикация
2007-05-25—Подача