Изобретение относится к ветеринарной вирусологии и биотехнологии и может быть использовано при изготовлении средства для специфической профилактики и диагностики инфекционной бурсальной болезни (ИББ) птиц.
ИББ птиц (болезнь Гамборо) - высококонтагиозная болезнь, характеризуется поражением фабрициевой сумки, почек, внутримышечными геморрагиями, диареей. В основном ИББ поражает В-лимфоциты фабрициевой сумки, вызывая атрофию ее лимфоидных фолликулов. Важным средством борьбы против ИББ, причиняющим экономический ущерб за счет гибели 20 - 70% птиц при остром ее течении, снижения привесов и проявления вторичных инфекций на фоне иммунодепрессивного воздействия вируса на организм птиц, является своевременная диагностика заболевания и его вакцинопрофилактика.
ИББ протекает остро с характерной клиникой заболевания и субклинически. Широкое распространение имеет субклиническая форма. При острой форме болезни на первый план выступают клинические и патологоанатомические признаки, свойственные вторичным инфекциям, что создает затруднения при постановке диагноза. Поэтому проведение лабораторных исследований имеет решающее значение при постановке диагноза и требует наличия специфических высокоактивных стандартных антигенов и сывороток. Штаммы вируса ИББ, предназначенные для производства антигена и иммунной сыворотки, должны быть свободными от контаминации и обладать высокой биологической и антигенной активностью. Технология производства антигена при ИББ предусматривает инактивацию вируса, поэтому штаммы должны быть чувствительными к воздействию инактивирующих препаратов и контролироваться на полноту инактивации. Существующие диагностикумы готовят на СПФ-цыплятах, СПФ-эмбрионах и в культуре клеток.
В зарубежной практике известен ряд штаммов вируса ИББ, используемых для изготовления антигенов и сывороток к данной инфекции - штамм "SR-1" [4], штамм "1/PY". Указанные штаммы культивируются на СПФ-цыплятах (свободных от патогенных факторов) или в культуре клеток различного происхождения [1]. Однако размножение вируса в культуре клеток вызывает снижение его антигенной активности. Полученные образцы антигена и сыворотки с использованием штаммов обладают низкой активностью и не поддаются стандартизации. Кроме того, вышеуказанные штаммы непригодны для использования в качестве вакцинных.
Известно использование высокоактивных вирулентных штаммов вируса ИББ птиц для приготовления диагностикумов.
Известен штамм "cheville", используемый для производства антигенов и сывороток для лабораторной диагностики ИББ птиц [1].
Однако указанный штамм непригоден для изготовления вакцин.
Известен также штамм "27/94" вируса ИББ птиц для получения диагностикумов. Штамм культивируется и титруется на коммерческих цыплятах 35 - 40-дневного возраста и куриных эмбрионах. Штамм вызывает характерную клиническую и патологоанатомическую картину заболевания через 48 - 72 ч c титром вируса 105,5 - 106,0 ЭИД50/мл, и активность сыворотки крови достигает в реакции нейтрализации 1:1024 и в реакции диффузионной преципитации 1:64. Вирус свободен от контаминации, специфичен и активен [1].
Недостатком данного штамма является его вирулентность, что всегда создает проблемы при соблюдении ветеринарно-санитарной безопасности.
Вакцинные штаммы непригодны в большинстве случае для изготовления диагностикумов по причине их низкой антигенной активности.
Известен штамм "52/70" вируса ИББ птиц [2].
Указанный штамм является вирулентным и пригоден для изготовления только инактивированной вакцины.
Известен вакцинный штамм "КБК" вируса ИББ птиц, репродуцируемый в перевиваемой культуре клеток почки серо-зеленой мартышки ВГМ-70 и предназначенный для изготовления вакцин [2].
Недостатками данного штамма являются его культивирование в перевиваемой культуре ткани, что всегда является потенциальной опасностью для работающего персонала ввиду онкогенности используемых клеток, а также его низкая антигенная активность.
Наиболее близким к предлагаемому изобретению по совокупности существенных признаков является штамм "ВНИВИП" вируса ИББ птиц, предназначенный для изготовления вакцины. Указанный штамм представляет собой авирулентный генетически однородный вирусный материал, легкокультивируемый в культуре клеток куриных фибробластов и биологической активностью вируса 105,5 - 106,0 ТЦД50/мл [3].
Недостаток данного штамма состоит в том, что он обладает низкой антигенной активностью.
Проблема создания эффективных средств вакцинопрофилактики ИББ в России встала очень остро с появлением целого ряда очагов заболевания в период с 1991 по 1995 гг. Применение отечественных и импортных биопрепаратов в очагах инфекции не обеспечило ожидаемого эффекта. Это объясняется тем, что их применению не предшествовало изучение антигенных свойств циркулирующих изолятов вируса, не определялись специфические антитела у птицы до и после вакцинации, а также уровень пассивного материнского иммунитета у цыплят.
Известна вакцина против ИББ птиц на основе штамма "52/70" [2].
Недостаток этой вакцины состоит в том, что штамм "52/70" является вирулентным, поэтому он пригоден для изготовления только инактивированной вакцины.
Известна также вакцина против ИББ птиц на основе штамма "КБК", адаптированного к перевиваемой культуре клеток почки серо-зеленой мартышки ВГМ-70 [2].
Недостатки данной вакцины состоят в том, что для репродукции вируса используют перевиваемую линию клеток серо-зеленой мартышки, которая еще недостаточно изучена в отношении онкогенного воздействия на занятый в производстве препарата персонал, а также не изучены последствия влияния на человеческий организм мяса птицы, иммунизированной данной вакциной.
Наиболее близкой к предлагаемому изобретению по совокупности существенных признаков является вакцина против ИББ птиц, включающая авирулентный генетически однородный вирусный материал из штамма "ВНИВИП" и стабилизатор, взятые в равном соотношении. Указанный штамм репродуцируется в культуре клеток куриных фибробластов с биологической активностью 105,5 - 106,0 ТЦД50/мл. В качестве стабилизатора используют обезжиренное молоко. Для профилактики ИББ птицу иммунизируют до 60-дневного возраста путем подачи вакцины с водой в дозе 103,0 - 104,0 ТЦД50/мл [3].
Недостаток данной вакцины состоит в том, что она обладает низкой иммуногенной активностью.
В задачу создания настоящих изобретений входило получение штамма вируса ИББ птиц, обладающих высокой биологической, иммуногенной и антигенной активностью в нативном виде и после инактивации и пригодного для производства как диагностикумов, так и живой и инактивированной вакцины, а также разработка на его основе живой и инактивированной вакцины, обладающей высокой иммуногенной активностью и безвредностью.
Технический результат от использования предлагаемых изобретений заключается в повышении специфической антигенной и иммуногенной активности и безвредности средств специфической профилактики и диагностики.
Указанный технический результат достигнут созданием группы изобретений, образующих единый изобретательский замысел. В группу включены изобретения, одно из которых предназначено для использования в другом изобретении.
Указанный технический результат достигнут созданием аттенуированного штамма "БГ" вируса ИББ птиц. Штамм "БГ" является новым, ранее не известным. Исходный вирус для получения штамма "БГ" выделен из фабрициевых сумок больных бройлеров птицефабрики "Уральская" Оренбургской области в 1993 году. Производственный штамм "БГ" получен путем многократных последовательных пассажей на 10-суточных СПФ-эмбрионах кур.
Штамм "БГ" депонирован в Государственной коллекции вирусов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ВГНКИ) 21.06.96 г. под регистрационным номером "БГ" 102 ДЕП.
По сравнению с прототипом штамм "БГ" является безвредным и обладает более высокой биологической, антигенной и иммуногенной активностью в нативном виде и после инактивации. Экспериментально подтверждена его возможность использования для приготовления живой (табл. A, 6, 7, 8, 9,), инактивированной (табл. 5) вакцины и диагностических препаратов (табл. 1, 2, 3, 4).
Штамм "БГ" вируса ИББ птиц характеризуется следующими признаками и свойствами.
Морфологические свойства.
Штамм "БГ" вируса ИББ птиц относится к семейству Birnaviridae, роду Avibirnavirus, серотипу I, обладает морфологическими признаками, характерными для возбудителя ИББ: форма вириона экосаэдрическая, размер вириона - 58 - 60 нм. Капсид - Т13, оболочка отсутствует.
Антигенные свойства.
По своим антигенным свойствам штамм "БГ" относится к сероварианту 1. Вирус стабильно нейтрализуется гомологичной антисывороткой. Вирус не проявляет гемаглютинирующей активности. При вакцинации вирус индуцирует образование специфических антител, выявляемых в РДП в разведении 1:4-1:64, в ИФА - 1: 400-1: 10000 и более, при гипериммунизации - в РДП до 1:4096 и выше, в ИФА > 1: 10000. При определении антигенного соответствия вакцинного штамма "БГ" с полевыми изолятами вируса ИББ было проведено сравнение вариабельной области VP237 полевых изолятов, выделенных в 1993 - 1996 гг. на территории РФ и странах СНГ и 7 образцов коммерческих живых вакцин. Для этого в ПЦР амплифицировали, используя специфические олигонуклеотидные праймеры и термостабильную Tag-ДНК-полимеразу, вариабельную область гена VP2, кодирующую основной конформационный этитоп. Методом прямого секвенирования определяли нуклеотидную последовательность этого наиболее важного в проявлении антигенных свойств участка генома полевых изолятов и вакцинного штамма ИББ. Установлено, что большинство полевых изолятор вируса ИББ, выделенных на птицефабриках России, антигено отличаются от импортных вакцинных штаммов фирм "Рон-Мерье" (Франция), "Интервет" (Голландия), "Солвей Дюфар" (США), "Сафит" (Израиль) на 5 - 8% и имеют структуру, близкую к вакцинному штамму "БГ".
Биотехнологические характеристики.
Штамм "БГ" проявляет высокую биологическую, иммуногенную и антигенную активность как в нативном виде, так и после инактивации, а также высокую степень гомологии (98%) по сравнению с многочисленной группой изолятов (30), выделенных на территории РФ в 1993 - 1996 гг.
Штамм "БГ" предназначен для использования в качестве сырья для приготовления живой и инактивированной вакцины и диагностических биопрепаратов. Штамм "БГ" репродуцируется в 10-суточных СПФ куриных эмбрионов при 37,7oC и влажности 55 - 64%. В течение 72 - 96 ч инкубирования вирус накапливается до 5,25 - 6,0 lg ЭИД50/0,2мл. Штамм "БГ" является стабильным и безвредным.
Хемо- и генотоксономическая характеристика.
Штамм "БГ" является РНК-содержащим вирусом с мол. мас. 2,16 • 106 Д. Нуклеиновая кислота является 2-нитевой, 2-сегментной (А и В). Вирус имеет белковую оболочку, содержащую 5 видов белков (VP1 - VP5). Липиды отсутствуют. Белковая оболочка обнаруживает следующие ферменты:
VP1 - РНК-зависимая РНК-полимераза;
VP2 и VP3 - структурные белки;
VP4 - протеаза;
VP5 - не идентифицирован.
Штамм "БГ" проявляет генетическую стабильность. Основная масса мутаций сосредоточена в VP2. Аминокислотные изменения в VP2 определяют антигенную вариабельность.
Сегмент A нуклеиновой кислоты содержит 2 частично перекрывающие открытые рамки для считывания малого VP5 и большого полипротеинового предшественника белков VP2 и VP3. Сегмент B кодирует VP1.
Физические свойства.
Масса вириона - 55 • 106Д. Коэффициент седиментации - 460S в градиенте сахарозы. Плавучая плотность 1,33 - 1,34 г/мл в градиенте CsCl.
Устойчивость к внешним факторам.
Штамм "БГ" устойчив к растворителям (эфиру, хлороформу) и детергентам, чувствителен к формальдегиду, УФ-облучению, y-облучению и высыханию.
Дополнительные признаки и свойства.
Иммуногенная активность - 100%.
Реактогенность отсутствует.
Патогенность отсутствует.
Вирулентность отсутствует.
Онкогенность отсутствует.
Контагиозность отсутствует.
Стабильность аттенуации отмечена при проведении 5 пассажей на чувствительных цыплятах.
По мнению заявителя, предлагаемый штамм соответствует условиям патентноспособности "новизна" и изобретательский уровень".
Указанный технический результат достигнут также созданием вакцины против ИББ птиц, охарактеризованной следующей совокупность признаков:
1) вакцина против ИББ птиц;
2) вируссодержащий материал из аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10-суточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2мл, в концентрации 85 - 95 мас.%;
3) стабилизатор - 5 - 15 мас.%.
В качестве стабилизатора можно использовать отдельно или в комбинации обезжиренное молоко, лактозу, желатозу, сахарозу и др.
Предлагаемое изобретение включает совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана:
1) вакцина против ИББ птиц;
2) вируссодержащий материал из аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10-суточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2, в концентрации 85 - 95 мас.%;
3) стабилизатор - 5 - 15 мас.%.
По сравнению с прототипом существенным отличительным признаком изобретения является использование в качестве вируссодержащего материала аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10 - суточных СПФ-эмбрионах кур и титром биологической активности 5,25 - 65,0 lg ЭИД50/0,2 мл.
По сравнению с прототипом вирусвакцина на основе аттенуированного штамма "БГ" обладает более высокой иммуногенной активностью, является безвредной и способна преодолеть материнские антитела против ИББ.
Проведенный заявителем анализ уровня техники, включающий поиск по патентам и научно-техническим источникам информации, и выявление источников, содержащих сведения об аналогах предлагаемого изобретения, позволил установить, что заявитель не обнаружил источник, характеризующийся признаками, тождественными (идентичными) всем существенным признакам заявленного изобретения. Определение из перечня выявленных аналогов прототипа, как наиболее близкого по совокупности признаков аналога, позволил установить совокупность существенных по отношению к усматриваемому заявителем техническому результату отличительных признаков в предлагаемой вакцине, изложенных в независимом пункте формулы изобретения.
Следовательно, заявляемое изобретение соответствует условию патентоспособности "новизна".
Для проверки соответствия предлагаемой вакцины условию патентоспособности "изобретательский уровень" проведен дополнительный поиск известных решений для выявления признаков, включенных в отличительную часть независимого пункта формулы изобретения. Результаты поиска показали, что предлагаемая вакцина не вытекает для специалиста явным образом из известного уровня техники, изложенного в соответствующем разделе описания (не выявлены решения, имеющие признаки, совпадающие с отличительными признаками предлагаемого изобретения), а также не выявлено влияние предусматриваемых существенными признаками предлагаемого изобретения преобразований для достижения технического результата. Следовательно, предлагаемая вакцина соответствует условию патентоспособности "изобретательский уровень".
Сущность предлагаемых изобретений пояснена примерами их исполнения.
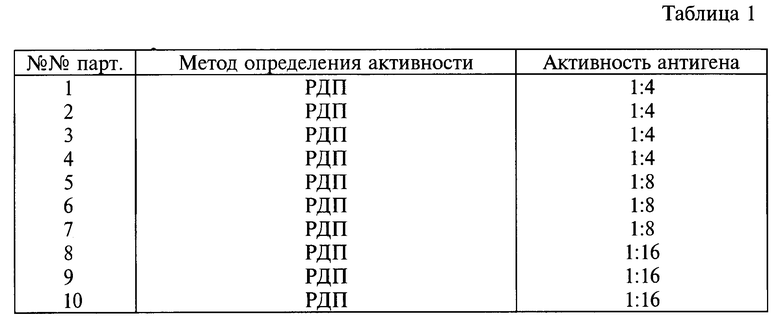
Пример 1. Приготовление диагностического антигена.
СПФ-цыплятам 14-21-дневного возраста инокулируют штамм "БГ" (интроакулярно, интраназально или орально). Через 72 цыплят убивают, берут бурсы, замораживают. Затем бурсы мелко размельчают, растирают со стерильным стеклянным песком, смешивают с фосфатным буфером 1:1, дважды промораживают, центрифугируют 1 мин при 3000 об/мин, супернатант сливают, инактивируют и используют для работы.
Результаты исследований по определению активности антигена ИББ в РДП представлены в табл. 1.
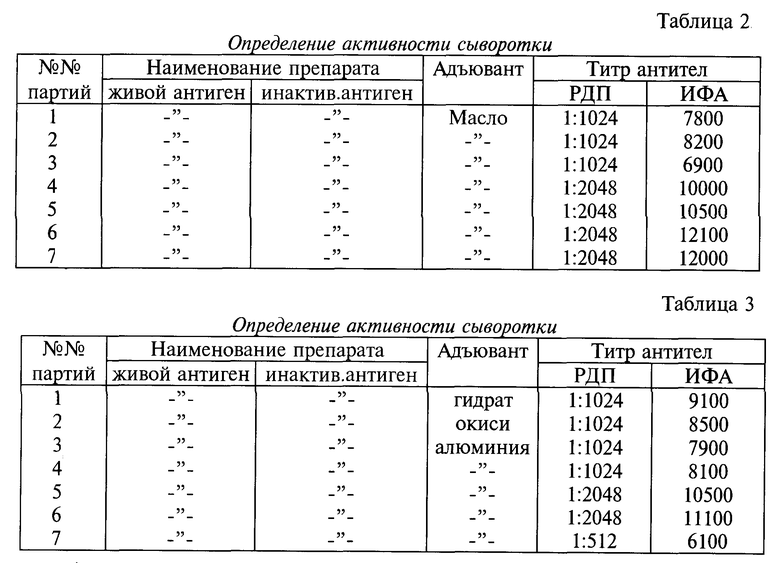
Пример 2. Приготовление диагностической сыворотки.
СПФ-цыплятам 14 - 21-дневного возраста инокулируют орально живую вакцину из штамма "БГ" вируса ИББ. Через 14 дней вводят внутримышечно инактивированный антиген, в качестве адъюванта используя масло, а через две недели цыплят обескровливают и получают генериммунную активную сыворотку и определяют ее активность в РДП и ИФА. Результаты исследований представлены в табл. 2.
Пример 3. приготовление диагностической сыворотки.
СПФ-цыплятам 14 - 21-дневного возраста вводят орально живую вакцину из штамма "БГ" вируса ИББ. Через 14 дней внутримышечно вводят инактивированный антиген, используя в качестве адъюванта гидрат окиси алюминия. Через 2 недели цыплят обескровливают, получают сыворотку и определяют ее активность в РДП и ИФА.
Результаты исследований представлены в табл. 3.
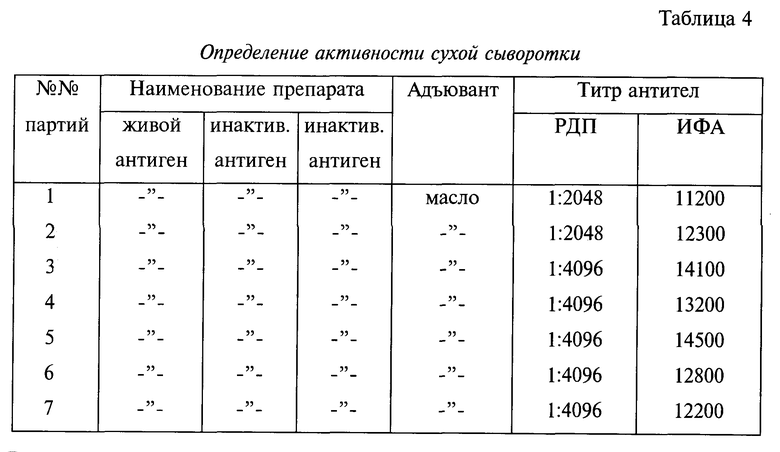
Пример 4. Приготовление диагностической сыворотки.
СПФ-цыплятам 14 - 21-дневного возраста вводят орально живую вакцину из штамма "БГ" вируса ИББ. Через 14 дней инокулируют внутримышечно инактивированный антиген, в качестве адъюванта масло, через 10 дней инактивированный антиген вводят повторно и через 7 дней цыплят обескровливают, получают сыворотку и определяют ее активность.
К исследованной сыворотке добавляют стабилизирующие добавки и ее подвергают лиофилизации. Лиофилизированную сыворотку используют для наборов ИФА и РДП. Результаты исследования полученной сыворотки представлены в табл. 4.
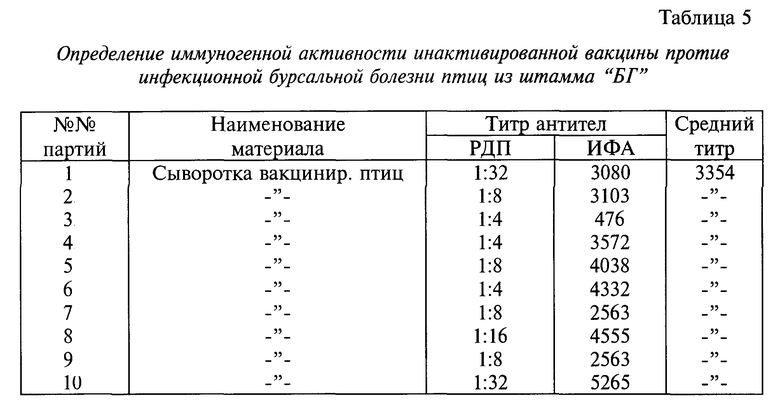
Пример 5. Приготовление и испытание инактивированной вакцины.
Инактивированную вакцину против ИББ птиц готовят из штамма "БГ" вируса, выращенного в развивающихся СПФ-эмбрионах кур. Вирус инактивируют азиридином, сорбируют на гидроокись алюминия с добавлением сапонина.
Результаты исследований по определению иммуногенной активности инактивированной вакцины из штамма "БГ" представлены в табл. 5.
Пример 6. Приготовление аттенуированной вакцины.
На первом этапе готовят матровый материал из штамма "БГ" вируса ИББ птиц. Полученную вируссодержащую жидкость используют для массового зарaжения 10-суточныx СПФ-эмбрионов кур. Вирусный материал в количестве 0,2 мл инокулируют на хориоаллантоисные оболочки (ХАО) и инкубируют при 37,7oC 48 - 120 ч. Павшие эмбрионы разделывают, замораживают при -40oC, и полученное сырье используют для приготовления вакцины. Вируссодержащий материал размораживают измельчают на коллоидной мельнице, экстрагируют при 4oC в течение 45 мин, дважды промораживают - оттаивают, добавляют фосфатный буфер pH 7,5 и центрифугируют в течение 20 мин при 3000 об/мин. Вируссодержащую надосадочную жидкость осторожно сливают в стерильных условиях, а затем добавляют стабилизатор, в качестве которого можно использовать (отдельно или в комбинации) обезжиренное молоко, лактозу, желатозу, сахарозу и др., расфасовывают во флаконы, промораживают при -60-(-80oC) и подвергают лиофилизации. Лиофилизованный материал закупоривают под вакуумом и подвергают исследованию на иммуногенность (на 14-дневных СПФ-цыплятах) и на безвредность (на 30-дневных СПФ-цыплятах).
Полученная вакцина представляет собой сухую однородную массу розово-коричневого цвета в виде цилиндрической таблетки, растворимой в воде. При растворении в воде до исходного объема она превращается в стойкую однородную суспензию розово-коричневого цвета.
Вакцину применяют в хозяйствах, где регистрируют клинические и патологоанатомические признаки проявления ИББ. Цыплят вакцинируют с 10 - 14-дневного возраста дважды с интервалом 10 - 14 дней в дозе 100 - 1000 ЭИД50/мл методом выпаивания.
Иммунитет у птиц наступает через 14 - 21-й день после второй прививки и сохраняется в течение всего восприимчивого к ИББ периода.
Полученная вакцина против ИББ птиц имеет оптимальный компонентный состав в мас.% (см. табл. A).
Полученная вакцина при титровании на 10-суточных СПФ-эмбрионах кур имеет титр 5,25 - 6,0 lg ЭИД50/0,2мл.
Пример 7. Испытание сухой аттенуированной вакцины.
Проведены испытания вакцины, содержащей, мас.%:
Вируссодержащий материал из аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10-суточных СПФ-эмбрионах кур c титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2 мл - 85
Стабилизатор - 15
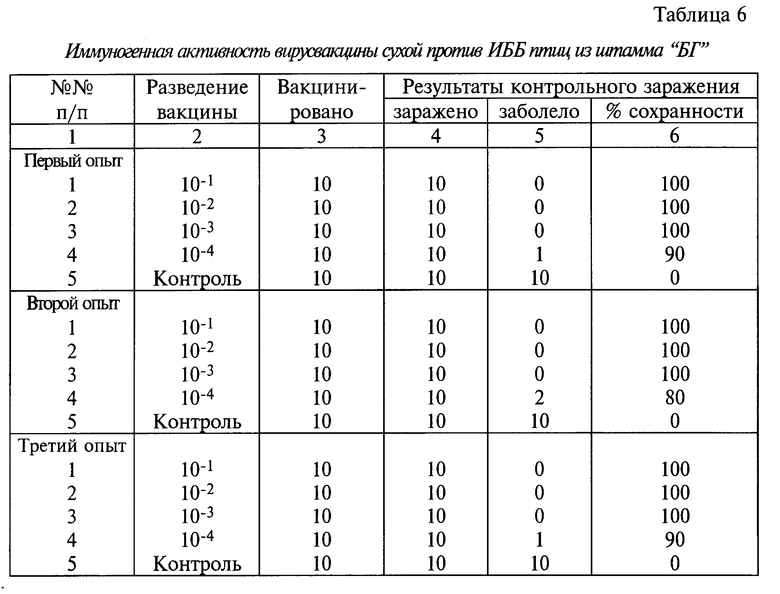
Определение иммуногенной активности вакцины проводили на цыплятах. Для этого предварительно готовили 10-крaтные разведения вакцины и каждым разведением иммунизировали по 10 цыплят путем выпаивания. Иммуногенную активность лиофилизованной вакцины оценивали по результатам контрольного заражения цыплят в опытной и контрольной группах через 14 суток после введения вакцины. Опыты проводили трехкратно. Результаты исследований приведены в табл. 6.
Данные табл. 6 свидетельствуют о том, что разведенная в 1000 раз вакцина обеспечивает 100%-ную защиту цыплят, выпаивание вакцины с водой является эффективным способом массовой вакцинации птиц.
Пример 8. Испытание сухой аттенуированной вакцины.
Проведены испытания вакцины, содержащей, мас.%:
Вируссодержащий материал из аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10-суточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2мл - 90
Стабилизатор - 10
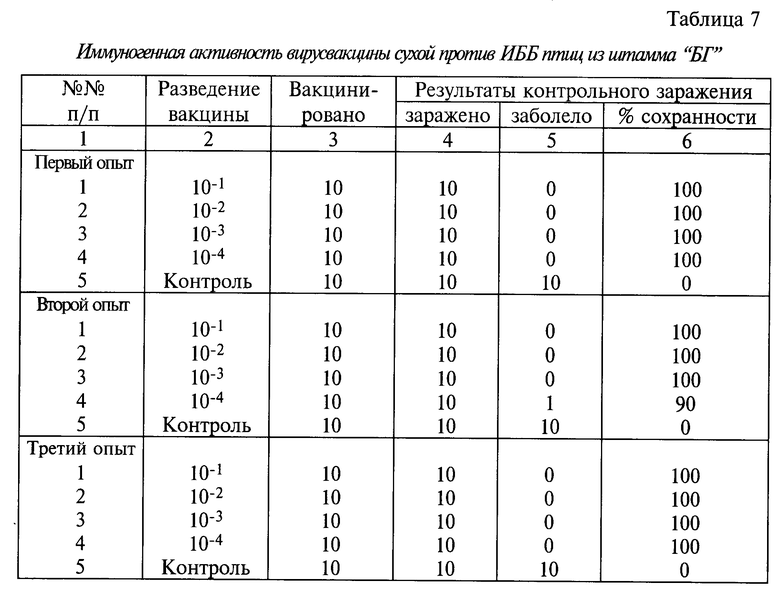
Определение иммуногенной активности проводили на цыплятах. Для этого предварительно готовили 10-кратные разведения вакцины и каждым разведением иммунизировали по 10 цыплят путем выпаивания. Иммуногенную активность лиофилизованной вакцины оценивали по результатам контрольного заражения цыплят в опытной и контрольной группах через 14 суток после введения вакцины. Опыты проводили трехкратно. Результаты исследований приведены в табл. 7.
Данные табл. 7 свидетельствуют о том, что разведенная в 1000 раз вакцина обеспечивает 100%-ную защиту цыплят, а выпаивание вакцины с водой является эффективным способом массовой вакцинации птиц.
Пример 9. Испытание сухой аттенуированной вакцины.
Проведены испытания вакцины, содержащей, мас.%:
Вирусодержащий материал из аттенуированного штамма "БГ" вируса ИББ птиц, репродуцированного на 10-суточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2мл - 95
Стабилизатор - 5
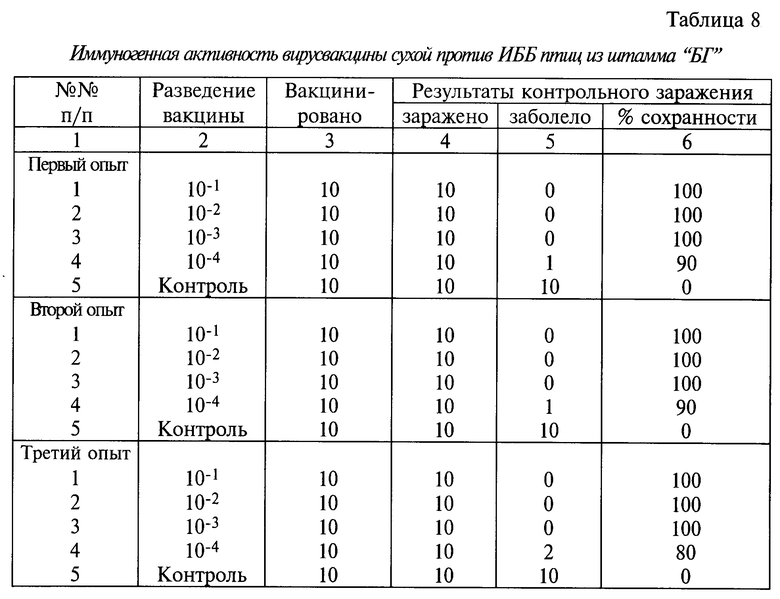
Определение иммуногенной активности проводили на цыплятах. Для этого предварительно готовили 1-кратные разведения вакцины и каждым разведением иммунизировали по 10 цыплят путем выпаивания. Иммуногенную активность лиофилизированной вакцины оценивали по результатам контрольного заражения цыплят в опытной и контрольной группах через 14 суток после введения вакцины. Опыты проводили трехкратно. Результаты исследований приведены в табл. 8.
Данные табл. 8 свидетельствуют о том, что разведенная в 1000 раз вакцина обеспечивает 100%-ную защиту цыплят, а выпаивание вакцины с водой является эффективным способом массовой вакцинации птиц.
Пример 10. Сравнительная оценка вирусвакцин против ИББ птиц.
В опытах были использованы вакцины из штамма "Тавиар" (Италия), из штамма "Д-78" (Голландия), из штамма "Гумбораль СТ" (Франция), из штамма "ВНИВИП" (Россия) и из штамма "БГ" (Россия).
Изучение эффективности указанных вакцин проводили на СПФ-цыплятах 14-дневного возраста.
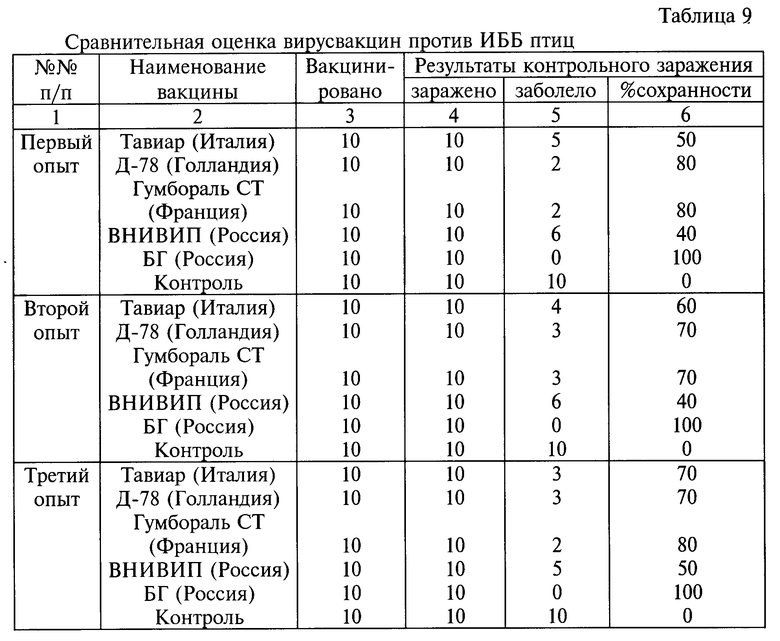
Всем цыплятам инокулировали орально по одной дозе одной из указанных выше вакцин. Оценку эффективности вакцин проводили по результатам контрольного заражения вирулентным штаммом 52/70 ИББ всех групп цыплят через 14 суток после их вакцинации. Результаты исследований приведены в табл. 9.
Данные табл. 9 свидетельствуют о том, что при контрольном заражении вакцинированных цыплят вирулентным штаммом 52/70 ИББ в дозе 104 ТЦД50/мл 100% защиту обеспечивает только вакцина, приготовленная из штамма "БГ".
Пример 11. Испытание сухой аттенуированной вакцины.
В лабораторных экспериментах и в условиях птицехозяйств Российской Федерации проведена сравнительная оценка иммуногенности различных отечественных и импортных живых вакцин против ИББ и показано, что вирусвакцина сухая против ИББ из штамма "БГ" является более надежным и эффективным биопрепаратом по сравнению с импортными вакцинами.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемых изобретений следующей совокупности условий:
- штамм "БГ" вируса ИББ птиц и вакцина против ИББ птиц, воплощающие предлагаемые изобретения, предназначены для использования в сельском хозяйстве, а именно в ветеринарной медицине и биотехнологии;
- для предлагаемых изобретений в том виде, как они охарактеризованы в независимых пунктах формулы изобретения, подтверждена возможность их осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- штамм "БГ" вируса ИББ птиц и вакцина на его основе, полученные в соответствии с предлагаемыми изобретениями, обладают высокой специфической, иммуногенной и антигенной активностью, безвредностью и ареактогенностью.
Следовательно, предлагаемая группа изобретений соответствует условию патентоспособности "промышленная применимость".
Источники информации
1. Авторское свидетельство СССР N 1761802, C 12 N 7/00, 22.11.90.
2. Патент РФ N 2054038, C 12 N 7/08, 01.06.93.
3. Авторское свидетельство СССР N 1824443, C 12 N 7/00, 19.03.91.
4. Авторское свидетельство СССР N 1668392, A 61 K 7/00, 16.09.89
5. Патент Австралии N 565768, A 61 K 39/12, 24.09.87.
6. Патент Австралии N 574190, C 12 N 15/33, 07.01.91.
7. Патент Австралии N 374885, A 61 K 39/12, 26.06.85.
8. Патент Австралии N 3825289, A 61 K 39/12, 21.07.88.
9. Патент РСТ N 85/02545, A 61 K 39/12, 20.06.85.
10. Патент РСТ N 86/00529, A 61 K 39/12, 30.01.86.
11. Патент РСТ N 91/04749, A 61 K 39/00, 18.04.91.
12. Патент РСТ N 91/04750, A 61 K 39/42, 18.04.91.
13. Патент РСТ N 91/16925, C 12 N 15/00, 14.11.91
14. Патент РСТ N 94/06475, A 61 K 39/42, 15.09.95.
15. Патент РСТ N 94/06904; A 61 K 39/12, 31.03.94.
16. Патент США N 4530831, A 61 K 39/12, 23.07.85.
17. Патент США N 5064646, A 61 K 39/12, 12.10.91.
18. Патент США N 4824668, A 61 K 35/76, 25.04.89.
19. Патент США N 5192539, A 61 K 39/12, 19.05.89.
20. Патент ЕПВ N 0352835, A 61 K 39/12, 31.01.90.
21. Патент Венгрии N 203780, C 12 N 7/00, 10.09.91.
22. Патент Венгрии N 203781, C 12 N 7/00, 30.09.91.
23. Патент ФРГ N 3604109, A 61 K 39/00, 14.08.86.
24. Патент ЧССР N 209379, A 61 K 39/12, 27.02.81
25. Патент Швейцарии N 560760, C 12 N 7/00, 09.09.71.
26. Патент Румынии N 100319, A 61 K 39/12, 29.10.90.
27. Патент Канады N 1232543, A 61 K 39/12, 09.02.88.
28. Алиев А. С. Специфическая профилактика инфекционного бурсита кур. Ветеринария. - 1991, 3, 3.
29. Гудзиев П.Х. Иммунологические свойства вакцинного штамма "СТ" и эффективность специфической профилактики бурсальной болезни птиц. - Тарту. Эстонская СХА, 1990, 21.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 1998 |
|
RU2127604C1 |
| ИНАКТИВИРОВАННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 1998 |
|
RU2127603C1 |
| ВИРУСВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 2004 |
|
RU2272649C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 2001 |
|
RU2205021C2 |
| ШТАММ "К-58" ВИРУСА ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2004 |
|
RU2268936C1 |
| ВАКЦИНА ОВАК ПРОТИВ СИНДРОМА СНИЖЕНИЯ ЯЙЦЕНОСКОСТИ-76 ПТИЦ | 1995 |
|
RU2097066C1 |
| ВИРУСВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО ЛАРИНГОТРАХЕИТА ПТИЦ | 2002 |
|
RU2214277C1 |
| ИНАКТИВИРОВАННАЯ СОРБИРОВАННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 2004 |
|
RU2283136C2 |
| ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 2004 |
|
RU2283137C2 |
| ШТАММ "О" ВИРУСА ИНФЕКЦИОННОГО ЛАРИНГОТРАХЕИТА ПТИЦ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2002 |
|
RU2207372C1 |

Изобретение предназначено для специфической профилактики и диагностики инфекционной бурсальной болезни (ИББ) птиц. Получен новый аттенуированный штамм "БГ" вируса ИББ птиц для изготовления средств специфической профилактики и диагностики. Штамм "БГ" депонирован в коллекции ВГНКИ под регистрационным номером "БГ" 102-ДЕП. Вакцина против ИББ птиц содержит вирусный материал из штамма "БГ" и стабилизатор в соотношении (маc.%) 85-95/5-15. Штамм "БГ" репродуцируется на 10-cуточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0lg ЭИД50/0,2 мл. В качестве стабилизатора используют (отдельно или в комбинации) обезжиренное молоко, лактозу, желатозу, сахарозу и др. Полученная вакцина представляет собой сухую однородную массу розово-коричневого цвета в виде цилиндрической таблетки, растворимой в воде. Цыплят вакцинируют с 10-14-дневного возраста дважды с интервалом 10 - 14 дней в дозе 100 - 1000 ЭИД50 мл методом выпаивания. Иммунитет птиц наступает через 14 - 21-й день после второй прививки и сохраняется в течение всего восприимчивого периода. Технический результат: повышение специфической, иммуногенной и антигенной активности и безвредности средств специфической профилактики и диагностики. 2 c.п. ф-лы, 10 табл.
Вируссодержащий материал из аттенуированного штамма вируса инфекционной бурсальной болезни птиц ВГНКИ N "БГ" 102-ДЕП, репродуцированного на 10-суточных СПФ-эмбрионах кур с титром биологической активности 5,25 - 6,0 lg ЭИД50/0,2 мл - 85 - 95
Стабилизатор - 5 - 15
| Способ профилактики болезни Гамборо | 1991 |
|
SU1824443A1 |
| Штамм вируса болезни Гамборо для производства вакцин | 1989 |
|
SU1668392A1 |
| Штамм вируса болезни Гамборо для получения биологических препаратов и их оценки | 1990 |
|
SU1761802A1 |
| RU 94030087 A, 10.08.96 | |||
| ШТАММ ВИРУСА ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ ПТИЦ | 1993 |
|
RU2054038C1 |
| US 5397568 A, 14.05.95 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТРИПОЛИФОСФАТА НАТРИЯ | 0 |
|
SU352835A1 |
| Устройство распределения тока | 1974 |
|
SU600723A1 |
Авторы
Даты
1999-03-20—Публикация
1997-11-24—Подача