Настоящее изобретение относится к новым эфирам бисфенилпиперазинникотиновой кислоты и их фармацевтически приемлемым солям, к способу получения таких соединений, а также новых промежуточных соединений, полезных при получении указанных соединений. Далее, настоящее изобретение относится к фармацевтически композициям, содержащим указанные соединения и к использованию указанных соединений для лечения психического расстройства.
Целью данного изобретения является предоставление соединений для терапевтического использования, особенно соединений, оказывающих терапевтическое действие на центральную нервную систему (CNS). Дополнительной целью является предоставление соединений, оказывающих действие на 5-гидрокситриптаминовые (5-HT) рецепторы млекопитающих, включая человека.
В литературе известны различные пиридил- и пиримидил производные фармакологически активные в отношении центральной нервной системы. Могут быть упомянуты некоторые характерные примеры. Азаперон, нейтролептическое лекарство серии бутирофенона, является седативным для свиней. Буспирон является анксиолитиком, анксиолитический эффект которого, как считают, проявляется через посредство 5-гидрокситриптаминовых рецепторов.
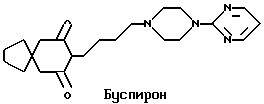
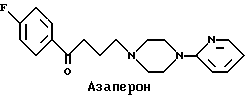
В патент США N 4937245 раскрываются соединения общей формулы I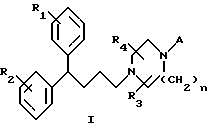
где A выбран из пиридильной или пиримидильной группы, например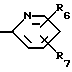
где предпочтительно R6 представляет водород и R7 представляет циано, амидный, метокси или водородный заместитель в 3-положении пиридильного кольца, полезные для лечения психических расстройств, таких как психозы, депрессия и страх.
Эфиры 3-пиридинкарбоновой кислоты (2-(4-(4,4-бис(4-фторфенил)- бутил)-1-пиперазиниловый) настоящего изобретения, как неожиданно было найдено, обладают фармакологическими свойствами, превосходящими свойствами соединений, известных в литературе.
Таким образом, настоящее изобретение обеспечивает новые соединения общей формулы II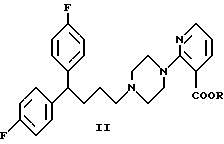
R выбран из насыщенных или ненасыщенных алкилов, насыщенных или ненасыщенных циклоалкилов, гетероциклических соединений или из: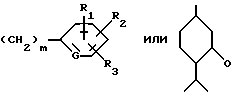
где G представляет углерод или азот;
m равно 0-10;
R1, R2 и R3 являются одинаковыми или различными и выбраны из водорода, галоида, алкила, содержащего 1-5 атомов углерода, электронодонорных групп таких как алкокси, содержащих 1-5 атомов углерода, или гидрокси, электроноакцепторных групп, выбранных из циано, нитро, трифторалкила или амида,
и их фармакологически активные соли;
и использованный в вышеуказанных определениях термин алкил включает неразветвленные или разветвленные углеводородные группы;
термин алкокси включает разветвленные или неразветвленные алкокси группы;
термин галоид включает фтор, хлор или бром.
Соединения формулы II обладает основными свойствами и, следовательно, они могут превращаться в терапевтически активные соли присоединения кислот обработкой соответствующими кислотами, например, неорганическими кислотами, такими как хлористоводородная, бромистоводородная, серная, азотная и фосфорная кислота, или органическими кислотами, такими как уксусная, пропионовая, гликолевая, молочная, малоновая, янтарная, фумаровая, винная, лимонная и памовая кислота.
И наоборот, полученная соль может быть превращена в свободное основание обработкой щелочью.
Соединения формулы II и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами, что делает их полезными для лечения психических расстройств, таких как психозы, депрессия, страх, старческое слабоумие, болезнь Альцгеймера, анорексия и нарушения, связанные со злоупотреблением каких-либо веществ.
Стресс и страх у животных также могут быть подвергнуты лечению.
Клинические исследования подтверждают 5-гидрокситриптамин (5-HT) как наиболее важный при патогенезе психических расстройств, таких как психозы, депрессия, страх и нарушения, связанные со злоупотреблением веществ (лекарств).
Текущая деятельность в значительной степени направлена на открытие новых психотропных лекарств таких как 5-HT1A агонисты, например, буспирон и ипсапирон, 5-HT2 антагонисты, например, амперозид и ритансерин, ингибиторы 5-HT поглощения (усвоения), например, флуоксетин и пароксетин.
Так как 5-HT1A и 5-HT2 рецепторы, как было найдено, взаимодействуют функционально, соединения с объединенной 5-HT1A агонистической и 5-HT2 антагонистической активностью представляли бы очень интересные лекарства для лечения пациентов, страдающих от психических расстройств.
Соединения настоящего изобретения показывают значительное сродство с 5-HT1A и 5-HT2 рецепторами и было найдено также, что они являются сильнодействующими ингибиторами повторного усвоения.
Хотя соединения общей формулы I и формулы II обладают высоким сродством с подтипами серотониновых 5-HT1A и 5-HT2 рецепторов, совершенно неожиданно было найдено, что соединения настоящего изобретения являются превосходящими с точки зрения безопасности, что делает их полезными для терапии центральной нервной системы, особенно, серотонергической системы головного мозга.
Эффективные количества любого вышеупомянутого фармакологически активного соединения формулы II может назначаться для приема человеку или животному для терапевтических целей в соответствии с обычными путям и введения и в обычных формах, таких как растворы, эмульсии, таблетки, капсулы и бляшки или пластыри в фармакологически приемлемых носителях и парентерально в форме стерильных растворов.
Препаративные формы для парентерального введения могут быть в виде водных и неводных изотонических стерильных растворов для инъекций или суспензий.
Хотя эффективными являются очень малые количества активных веществ настоящего изобретения, когда вовлекается второстепенная терапия, или в случае введения субъектам, имеющим относительно небольшой вес тела, стандартные дозы составляют обычно от 0,5 мг и выше, в зависимости от состояния, возраста и веса пациента, а также от реакции на лекарственную терапию.
Стандартная доза может быть от 0,1 до 100 мг, предпочтительно, от 1 до 10 мг. Дневные дозы должны быть предпочтительными в области от 1 до 50 мг. Точные индивидуальные дозы, а также дневные дозы будут, конечно, определяться в соответствии со стандартными медицинскими принципами, по указанию врача или ветеринара.
Соединения, имеющие общую формулу II, могут быть получены следующими способами.
Способ 1.
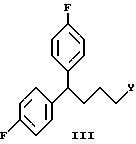
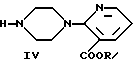
Соединение формулы (III), где Y представляет подходящую уходящую или удаляемую группу, такую как галоид, алкил- или арилсульфонат, вводится во взаимодействие с соединением формулы (IV), где R имеет значения, определенные ранее. Реакция может проводиться с использованием стандартной процедуры N-алкилирования
Способ 2.
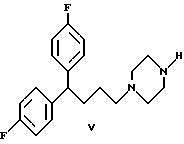
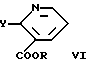
Соединение формулы V подвергается взаимодействию с соединением VI, где R имеет значения, определенные ранее, и Y представляет уходящую группу, например галоид.
Способ 2b. Способ получения промежуточного соединения (VI).
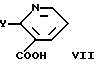
Соединения формулы (VI) получают с помощью новой процедуры в одном сосуде, где соединение формулы VII подвергается взаимодействию с соединением формулы VIII, где R имеет значения, определенные ранее, в условиях катализа кислотами Льюиса в диоксане.
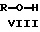
Способ 3.
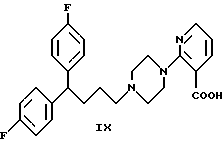
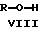
Соединение формулы IX вводится в реакцию с соединением формулы VIII, где R имеет значения, определенные ранее, при катализе соответствующей кислотой в соответствующем растворителе.
Следующие примеры предназначены для иллюстрации, но не ограничивают объем изобретения, хотя названные соединения представляют особый интерес для предназначенных целей. Эти соединения обозначены кодом, a : b, где a обозначает номер примера, где описывают получение соединения, и b относится к порядковому номеру соединения, полученного согласно этому примеру. Пример 1: 2 обозначает второе соединение, полученное согласно примеру 1.
Структуры соединений подтверждаются ИК-, ЯМР-, МС-спектрами и данными элементного анализа. Если даны температуры плавления, то они являются некорректированными.
Пример 1. 4-(4,4-бис(п-фторфенил)бутил)-1-(2-(этил-пиридин-3-карборксилат)-ил)пиперазин -гидрохлорид.
3,3 г (0,01 моля) 1-хлор-4,4-бис (п-фторфенил)бутана, 4,42 г (0,02 моля) 1-(2-(этил-пиридин-3-карбоксилат)-ил)пиперазина и 0,05 кг K1 кипятят с обратным холодильником в 30 мл толуола в течение 36 часов. После охлаждения и добавления 45 мл эфира, твердый осадок отфильтровывают. После последующего промывания несколько раз водой органический слой сушат Na2SO4. Выпаривание растворителей дает сырое основание. Это основание растворяют в эфире и добавляют HCl в этаноле для осаждения гидрохлорида. Перекристаллизация из EtOAc/EtOH дает 2,1 г (42%) указанного в названии соединения (1:1), т.пл. 156 - 157oC.
Пример 2. Гидрохлорид 2-(4-(4,4-бис(4-фторфенил)бутил)-1-пиперазинил/этилового эфира 3-пиридинакорбоновой кислоты
10,0 г (0,03 моля) 1-(4,4-бис(п-фторфенил)бутил)-пиперазина и 5,7 г (0,033 моля) 2-хлор-(этилпиридин-3-карбоксилата) кипятят с обратным холодильником в 10 мл толуола в течение 16 часов. После охлаждения до комнатной температуры реакционную смесь экстрагируют несколько раз, и органический слой сушат над сульфатом натрия. Выпаривание растворителей дает сырое основание. Основание растворяют в 11,5 мл ацетона и добавляют 57 мл 5-N HCl. Смесь оставляют на ночь при комнатной температуре, и кристаллизуется указанное в названии соединение. Выход 14,9 г (99%) указанного в названии соединения (2:1), т.пл. 156 - 157oC.
Следующие соединения были получены в основном таким же образом.
2: 2 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-изопропоксикарбонил-2-пиридил)-пиперазина, т.пл. 155 - 156oC,
2: 3 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(3-фторфенокси)карбонил-2-пиридил) -пиперазина, т.пл. 139 - 141oC,
2: 4 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-метоксикарбонил-2-пиридил)-пиперазина, т.пл. 167 - 168oC,
2: 5 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-бензилоксикарбонил-2-пиридил)-пиперазина, т.пл. 161 - 162oC,
2: 6 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-циклогесилоксикарбонил-2-пиридил) -пиперазина, т.пл. 155 - 156oC,
2: 7 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-изоамилоксикарбонил-2-пиридин)- -пиперазина, т.пл. 150 - 151oC,
2: 8 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-метоксикарбонил-2-пиридил)-пиперазина, т.пл. 115 - 116oC,
2: 9 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(1R, 2S, 5R)-ментоксикарбонил-2-2-пиридил)-пиперазина, т.пл. 102 - 103oC,
2: 10 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-2-пиридинилметоксикарбонил)-2-пиридил) -пиперазина, т.пл. 132 - 133oC,
2: 11 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-1-третамилоксикарбонил-2-пиридил) -пиперазина, т.пл. 139 - 140oC,
2: 12 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-циклооктилоксикарбонил-2-пиридил) -пиперазина, т.пл. 183 - 184oC,
2: 13 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-4-фенил-2-бутилоксикарбонил)-2-пиридил) -пиперазина, т.пл. 96 - 98oC,
2: 14 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(4-хлор-2-метилфеноксикарбонил)-2-пиридил) -пиперазина, т.пл. 155 - 156oC,
2: 15 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(4-карбоэтоксифеноксикарбонил)-2-пиридил) -пиперазина, т.пл. 182 - 183oC,
2: 16 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(2,5-дихлорбензилоксикарбонил)-2-пиридил) -пиперазина, т.пл. 131oC,
2: 17 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(4-цианофеноксикарбонил)-2-пиридил) -пиперазина, т.пл.
2: 18 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(3-нитрофеноксикарбонил)-2-пиридил) -пиперазина, т.пл.
2: 19 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(2-нитрофеноксикарбонил)-2-пиридил) -пиперазина, т.пл.
2: 20 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(2-фенилэтоксикарбонил)-2-пиридил) -пиперазина, т.пл.
2: 21 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(4-бром-3,5-диметилоксикарбонил)-2-пиридил) -пиперазина, т.пл. 107 - 108oC,
2: 22 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(3-фторбензилоксикарбонил)-2-пиридил) -пиперазина, т.пл. 160 - 161oC,
2: 23 Гидрохлорид 1-(4,4-бис(п-фторфенил)бутил)-4-(3-(4-карбамилфеноксикарбонил)2-пиридил) -пиперазина, т.пл.
Пример 2b.
Этиловый эфир 2-хлор-(3-пиридинкарбоновой)кислоты
10 г (0,0635 моля) 2-хлорникотиновой кислоты, 4,86 мл (0,067 моля) тионилхлорида и 30 мл диоксана нагревают при 70oC в течение 3 часов. Добавляют 20 мл этанола, и смесь нагревают в течение 2 часов. После охлаждения до комнатной температуры добавляют 10 мл триэтиламина, 10 мл воды и 5 мл этанола. Растворители выпаривают, и остаток экстрагируют эфиром и водой. Эфир выпаривают, и сырой продукт выделяют. Выход составляет 10,3 г (95%). Перегонка сырого продукта при 8 мм, т.кип. 122 - 123oC дает 9,4 г (90%) указанного в названии соединения (2:1) т.кип. 122 - 123oC при 8 мм рт. см.
Пример 4.
Этот пример иллюстрирует активность соединений формулы II и их терапевтически активных солей присоединения кислоты для лечения психических нарушений.
Тест 1. Сродство к 5HT2-рецепторам.
Анализ связывания, в основном, проводили, как описано Leysen и др. (Mol. Pharmacol. 21, 301 - 314, 1982), используя 3H-кетансерин в качестве лиганда (см. табл. 1).
Тест 2. Сродство к 5HT1A-рецепторам.
Анализ связывания в основном проводили, как описано Peroutka S.J. (Brain.Res. 344, 167 - 171, 1985) (см. табл. 2).
Пример 5.
Следующие композиции представлены для всех фармакологически активных соединений этого изобретения. Пример подходящей капсулированной формы препарата: - На капсулу
Активный ингредиент, в виде соли - 5 мг
Лактоза - 250 мг
Крахмал - 120 мг
Стеарат магния - 5 мг
Всего - 385 мг
В случае больших количеств активного ингредиента, количество используемой лактозы может быть уменьшено.
Пример соответствующей таблетированной формы препарата: - На таблетку
Активный ингредиент, в виде соли - 5 мг
Картофельный крахмал - 90 мг
Каллоидный кремний - 10 мг
Тальк - 20 мг
Стеарат магния - 2 мг
5%-ный водный раствор желатина - 25 мг
Всего - 152 мг
Растворы для парентерального введения путем инъекции могут быть приготовлены в водном растворе водорастворимой фармацевтически приемлемой соли присоединения кислоты активного вещества, предпочтительно в концентрации от 0,1 до около 5 вес.%. Эти растворы могут также содержать стабилизирующие агенты и/или буферные агенты.

Описываются новые соединения формулы I, где R выбран из насыщенных аллилов, циклоадкилов, или группа формулы II, где G представляет СH или азот; m = 0-4; R1, R2 и R3 являются одинаковыми или различными и выбраны из водорода, галоида, С1 - С5 - алкила, циано, нитро, -СОNН2 или его фармакологически активная соль. Новые соединения могут быть использованы для лечения расстройств центральной нервной системы. Описывается способ получения вышеуказанных соединений, фармацевтическая композиции на основе соединения формулы I и способ лечения центральной нервной системы с использованием соединения формулы I. 5 с. и 5 з.п.ф-лы, 2 табл.
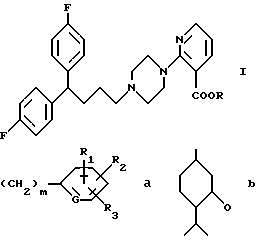
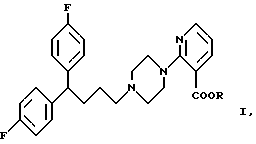
в которой R представляет насыщенный алкил, насыщенный циклоалкил или группу формулы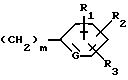
в которой G представляет СН или N;
m - целое число от 0 до 4;
R1, R2 и R3 является одинаковыми или различными и выбраны из группы, состоящей из водорода, галогена, С1 - С5-алкила, нитро, цианогруппы, CONH2,
или его фармакологически приемлемая соль.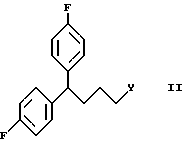
где Y представляет галоген,
подвергают взаимодействию с соединением формулы III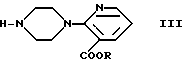
где R имеет данные в п.1 значения,
с использованием стандартных процедур N-алкилирования с последующим превращением полученного соединения, в случае необходимости, в фармакологически приемлемую соль.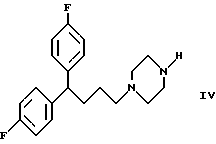
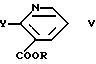
где R имеет указанные в п.1 значения;
Y представляет галоген,
с использованием стандартных процедур N-алкилирования с последующим превращением полученного соединения, в случае необходимости, в фармакологически приемлемую соль.
| ИМПУЛЬСНЫЙ ГАЗОРАЗРЯДНЫЙ ИСТОЧНИК СВЕТА | 0 |
|
SU385351A1 |
| Устройство для отделения деталей швейных изделий от пачки | 1972 |
|
SU441226A1 |
| СЦЕНИЧЕСКИЙ НАСТИЛ | 0 |
|
SU361271A1 |
| DE 3334757, 1984 | |||
| US 4839353, 1989 | |||
| US 5135931, 1992 | |||
| US 4937245, 1990 | |||
| US 4956368, 1990 | |||
| Машковский М.Д | |||
| Лекарственные средства.-М.: Медицина, 1988, ч.1, с.41-44 | |||
| Каплан Г.И | |||
| и др | |||
| Клиническая психиатрия.-М., 1988, N1, 237-238 | |||
| Карпов В.А | |||
| Терапия нервных болезней.-М.: Медицина, 1987, с.4 | |||
| Холодов Л.Е | |||
| и др | |||
| Клиническая фармакокинетика.-М.: Медицина, 1985, с.5-12, 20-22, 115-126. | |||
Авторы
Даты
1999-03-20—Публикация
1993-06-23—Подача