Изобретение относится к новым биологически активным пиридил- или пиримидилсодержащим производным пиперазина или 1,4-диазациклогептана, или их фармакологически активных кислотно-аддитивных солей, обладающих психотропным действием.
В области лечения психических расстройств существует насущная потребность в эффективных лекарственных препаратах, которые являются более эффективными и которые проявляют меньше побочных эффектов, чем лекарства, которые находят клиническое применение в настоящее время. Антипсихотропные лекарства, используемые в настоящее время, дают ряд мучительных экстрапирамидальных расстройств движения (например, острые дистонические реакции и позднюю диокинезию) и являются неудовлетворительными в отношении улучшения негативных симптомов (например, ограниченное или притупленное эмоциональное возбуждение) шизофрении. Основным недостатком антидепрессантов является то, что они не смягчают депрессию у 30-40% пациентов. Транквилизаторы или анксиолитики обычно ассоциируются со свойствами наркомании или алкоголизма.
В технике известны различные производные пиридил- и пиримидилпиперазина фармакологически активные в отношении центральной нервной системы (1-2). Могут быть упомянуты некоторые характерные примеры их представителей. Азаперон нейролептическое лекарство бутирофенонового ряда, является седативным препаратом для свиней. Анксиолитиком является буспирон. Считается, что анксиолитический эффект является промежуточным звеном или проявляется через воздействие на 5НТ-рецепторы.
F CO
CO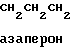 -N
-N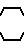 N
N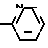
 -
- CH2-N
CH2-N N
N
Пиридил- и пиримидил-пиперазины, замещенные в 4 положении пиперазинового кольца фенилбутильной или феноксипропильной группой, как было неожиданно найдено, проявляются фармакологические свойства, превосходящие свойства соединений, известных в данной области техники.
Согласно изобретению предлагаются новые соединения, имеющие общую формулу I
F XCH2CH2CH2N
XCH2CH2CH2N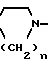 A где R1 представляет собой водород или фтор, Х является кислородом, серой или метиленом, n = 2 или 3, А - пиридильная или пиримидильная группа формул II или III:
A где R1 представляет собой водород или фтор, Х является кислородом, серой или метиленом, n = 2 или 3, А - пиридильная или пиримидильная группа формул II или III: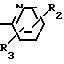 II
II  III где R2 - водород или хлор; R3 - водород, низший алкил, хлор, гидрокси, низший алкокси, нитро, трифторметил, карбамоил, N-метилкарбамоил, морфолинокарбонильная или пиперидинокарбонильная группа. Причем, когда А представляет собой пиримидильную группу, Х является кислородом или метиленом и n = 2.
III где R2 - водород или хлор; R3 - водород, низший алкил, хлор, гидрокси, низший алкокси, нитро, трифторметил, карбамоил, N-метилкарбамоил, морфолинокарбонильная или пиперидинокарбонильная группа. Причем, когда А представляет собой пиримидильную группу, Х является кислородом или метиленом и n = 2.
Соединения формулы I обладают основными свойствами, и соответственно, они могут превращаться в их терапевтически активные кислотно-аддитивные соли с помощью обработки неорганической кислотой, или органическими кислотами, такими как уксусная, пропановая, гликолевая, молочная, яблочная, щавелевая, янтарная, фумаровая, винная, лимонная и памовая кислота.
Солевая форма, наоборот, может превращаться в форму свободного основания с помощью обработки щелочью.
Соединения формулы 1 и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами, что делает их полезными для лечения психических расстройств, таких как психозы, депрессия и чувства тревоги и беспокойства. С их помощью можно также лечить стрессы и беспокойство у животных. Соединения по изобретению проявляют психотропные свойства. Например, они обнаруживают сродство с 5-НТ2 и Д2связующим участкам в головном мозге. В испытаниях на поведение на моделях данные соединения проявляют конечностный профиль действия, т.е. они обнаруживают сильный эффект в испытаниях на исследовательское или эксплоративное поведение, например, в испытании на феномен лестницы.
Соединения с объединенным 5-НТ2/Д2 средством, например, клозапин, оказывают антипсихотический эффект с низкой степенью экстрапирамидальных побочных эффектов; Кроме того, было найдено, что соединения со средством к 5-НТ2 связующим участком воздействуют на депрессивные болезни, а также на состояния беспокойства.
Для терапевтических целей эффективные количества любого из описываемых, фармакологически активных соединений формулы l могут назначаться для приема согласно обычным способам назначения и в обычных формах, таких как оральные способы назначения в виде растворов, эмульсий, суспензий, пилюль, таблеток и капсул, в фармацевтически приемлемых носителях, и парэнтерально, в форме стерильных растворов. Для парэнтерального способа назначения активного вещества носителем эксципиента может быть стерильная парэнтерально приемлемая жидкость, например вода, или парэнтерально приемлемое масло, например, арахиновое масло.
Хотя эффективными являются очень небольшие количества активных материалов изобретения, когда речь идет о незначительном или второстепенном лечении или в случаях назначения субъектам с относительно низким весом тела, дозированные единицы обычно составляют от 2 мг и выше, и предпочтительно 10,25 или 50 мг или даже выше, в зависимости от состояния подвергаемого лечению, возраста и веса пациентов, а также от ответной реакции на принимаемое лекарство.
Стандартная доза может составлять 0,1-100 мг, предпочтительно 10-50 мг. Дневная или суточная доза предварительно колеблется от 10 до 200 мг. Точные индивидуальные дозировки, а также суточные дозы, конечно определяются в соответствии со стандартными медицинскими принципами по указанию врача или ветеринара.
Соединения формулы I могут быть получены с помощью обычных способов.
Способ 1.
F XCH2CH2CH2-Y+NH
XCH2CH2CH2-Y+NH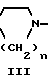 A __→ I
A __→ I
Соединение формулы II, в которой R1 и Х имеют значения, указанные ранее, представляет собой подходящую удаляемую группу, такую как галоген и алкил - или арилсульфонат, подвергается взаимодействию с соединением формулы III, в которой А и n имеют значения, определенные выше. Реакции могут осуществляться с использованием стандартных приемов N-алкилирования.
Способ 2.
F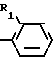 XCH2CH2CH2N
XCH2CH2CH2N +Z
+Z  или Z-
или Z-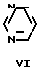
Соединение формулы IV, в котором R1, Х и n имеют значения, определенные ранее, подвергают взаимодействию с соединением формулы V или VI, где R2 и R3 имеют значения, определенные выше, и Z представляет собой удаляемую группу, например, галоген.
Изобретение иллюстрируют следующие примеры, в которых полученные соединения обозначены кодовыми номерами, а : b, где а означает номер примера, в котором описывается получение соединения, о котором идет речь, и b относится к порядковому номеру соединения, о котором идет речь, получаемого согласно данному примеру. Так, соединение 1:2 означает второе соединение, полученное согласно примеру 1.
Структуры соединений подтверждаются с помощью анализа ЯМР, масс-спектров и элементного анализа. Когда даются точки плавления, они являются нескорректированными.
П р и м е р 1. 4[4-(п-Фторфенил)бутил]-1-(2-пиридил)пиперизин-фумарат.
6,0 г (0,0323 моля) 4-(п-фторфенил)бутилхлорида, 5,3 г (0,0323 моля) пиридилпиперазина, 5,2 г карбоната натрия и 0,1 г йода нагревают вместе с 25 мл ксилола при 150оС (температура масляной бани) течение 20 ч.
После охлаждения реакционной смеси до приблизительно 100оС, добавляют 50 мл толуола и смесь фильтруют. К фильтрату добавляют 25 мл простого эфира. Органический раствор промывают три раза 25 миллилитрами воды, и наконец один раз 25-мл-ми насыщенного раствора хлористого натрия.
Упаривание растворителей дает неочищенное основание, которое кристаллизуют с использованием циклогексана. Точка плавления полученного свободного основания составляет 57-58оС.
Свободное основание затем растворяют в смеси этанол/простой эфир, и с помощью избытка фумаровой кислоты в этаноле осаждался фумарат.
Перекристаллизация из этанола давала 4,8 г целевого соединения (1:1) т. пл. 160-161оС.
П р и м е р 2. Дихлоргидрат 4-[4-(п-фторфенил)бутил]-1-[2-(3-карбамоилпиридил)]пи- перазина.
5,9 г (0,025 моля) 1-[4-(п-фторфенил)бутил]пиперазина, 3,9 г (0,025 моля) амида 2-хлорникотиновой кислоты и 3,1 г карбоната натрия нагревают с обратным холодильником вместе с 20 мл толуола в течение 20 ч.
После охлаждения получают твердую смесь, которую растворяют в этилацетате и воде. Толуол/этилацетатную фазу отделяют, а затем промывают водой и раствором хлористого натрия, а затем сушат сульфатом натрия.
Выпаривание растворителей дает неочищенное свободное основание, которое перекристаллизовывают из толуола. Полученное свободное основание плавилось при 135-136оС.
5 г свободного основания растворяют в этаноле, и избытком соляной кислоты в этаноле осаждают дихлоргидрат. Перекристаллизация дает 3,0 г целевого соединения (2:1), т.пл. 210-213оС.
При использовании в основном той же процедуры получают следующие соединения (выделенные и очищенные с помощью мгновенной хроматографии в виде чистого основания или в виде соответствующих солей) из соответствующих исходных материалов.
2:2 4[3-(п-Фторфенокси)пропил]-1-[6-хлор-2-пиридил]пиперазин-
хлоргидрат, т.пл. 185-186оС
2:3 Полугидрат хлоргидрата 4-[3-(п-фторфенокси)пропил]-
1- [2-пиримидил]пиперазина, т.пл. 208-210оС
2:4 Дихлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[2-пири-
дил] пиперазина, т.пл. 233-235оС.
2:5 Дихлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[3-карбамоил-
2-пиридил]пиперазина, т.пл. 240-242оС.
2:6 Хлоргидрат 4-[4-(п-фторфенил)бутил]-1-[2-пиримидил] пи-
перазина, т.пл, 197-198оС.
2:7 Фумарат 4-[4-(п-фторфенил)бутил-1-[2-пиридил] пипера-
зина, т.пл. 160-161оС.
2:8 Хлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[3-нитро-2-
пиридил]-пиперазина, т.пл. 182-183оС.
2:9 Хлоргидрат 4-[4-(п-фторфенил)бутил]-1-[6-хлор-2-пири-
дил] пиперазина, т.пл. 150-151оС.
2:10 Фумарат 4-[3-(п-фторфенокси)пропил]-1-[6-метокси-2- пири-
дил]-пиперазина, т.пл. 185-186оС
2:11 Оксалат 4-[3-(п-фторфенокси)пропил]-1-[3-карбамил-2- пири-
дил]-[1,4-диазациклогептана], т.пл. 148-150оС /основание,
т.пл, 140-141оС
2:12 Полуизопропанол-полугидрат дихлоргидрата 4-[4-(п-фтор-
фенил)-бутил]-1-[3-этокси-2-пиридил]пиперазина, т.пл. 168-169оС
2:13 Фумарат 4-[4-(п-фторфенил)бутил]-1-[6-метил-2-пири-
дил]пиперазина, т.пл.172-173оС
2:14 Дихлоргидрат 4-[3-(3,4-дифторфенокси)пропил]-1- [6-метил-
2-пиридил]пиперазина, разл. 230оС
2:15 1,5 хлоргидрат 4-[3-(3,4-дифторфенокси)пропил]-1- [3-(N-ме-
тилкарбамоил)-2-пиридил]пиперазина, т.пл. 211-213оС
2:16 Дихлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[3-гидрокси-
2-пиридил]пиперазина, т.пл. 240оС (основание т.пл. 105оС).
2:17 Хлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[3-трифторметил-
6-хлор2-пиридил]пиперазина, т.пл.190оС.
2:18 Дихлоргидрат 4-[3-(п-фторфенокси)пропил]-1-[3-карбамоил-2-
пиридил]пиперазина, т.пл. 205оС
2:19 Дихлоргидрат 4-[3-(п-фтортиофенокси)пропил]-1-[2-пири-
дил] пиперазина, т.пл. 150оС
2:20 4-[3-(п-Фторфенокси)пропил]-1-[5-морфолинокабонил-2- пири-
дил]пиперазин
2:21 4-[4-(п-фторфенил)бутил]-1-[3-пиперидинокарбонил- 2-пири-
дил]пиперазин.
П р и м е р 3. Средство к 5-НТ2 рецепторам.
Анализ связывания осуществляется в основном, как описано авторами Leysen et al (Mot Parmacol 21, 301-14, 1982) с использованием 3Н-кетансерина в качестве лиганда.
Результаты испытаний приведены в таблице.
Соединение-аналог по структуре формулы
F- X-(CH2)3 N
X-(CH2)3 N N-
N- Y где Х СНОН, Y = F не обладает значительным сродством к рецепторам 5 НТ2.
Y где Х СНОН, Y = F не обладает значительным сродством к рецепторам 5 НТ2.
Как показывает опыт длительной работы изобретателей с соединениями сходной структуры, у них нет оснований предполагать возникновение каких-либо серьезных проблем, связанных с токсикологией, и в испытанных дозах, эффективных в фармакологическом отношении, соединения не обнаружили каких-либо признаков токсичности.
П о и м е р 4. Следующие препаративные формы являются характерными представителями для всех фармакологически активных соединений данного изобретения. Пример подходящей капсульной препаративной формы:
На капсулу, мг
Активный ингредиент в виде соли 10 Лактоза 250 Крахмал 120 Стеарат магния 5 Всего 385
В случае большего количества активных ингредиентов количество лактозы может быть снижено.
Пример подходящей препаративной формы в виде таблеток
На капсулу, мг
Активный ингредиент в виде соли 10 Картофельный крахмал 90 Коллоидная двуокись кремния 10 Тальк 20 Стеарат магния 2 5% водный раствор желатина 25 Всего 157
Растворы для парэнтерального применения с помощью инъекции могут приготавливаться в водном растворе растворимой в воде фармацевтически приемлемой соли активного вещества предпочтительно в концентрации примерно от 0,5% до 5% по массе. Эти растворы могут также содержать стабилизирующие агенты и/или буферирующие агенты и могут удобно предоставляться в различных дозированных ампулах.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭФИРЫ БИС-ФЕНИЛПИПЕРАЗИННИКОТИНОВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ РАССТРОЙСТВ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 1993 |
|
RU2127732C1 |
| ПРИМЕНЕНИЕ БИСФЕНИЛАЛКИЛПИПЕРАЗИНОВ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, ВЫЗВАННЫХ ЗЛОУПОТРЕБЛЕНИЕМ ВЕЩЕСТВАМИ, И СПОСОБ ЛЕЧЕНИЯ | 1993 |
|
RU2126254C1 |
| Способ получения пиперазинилалкил-3(2Н)-пиридазинонов или их фармацевтически приемлемых солей | 1989 |
|
SU1823874A3 |
| Способ получения производных пиперидиндиона-2,6 или их солей | 1983 |
|
SU1333237A3 |
| N(ГЕТЕРО)-АРИЛ-N(ГЕТЕРО)-ТЕТРАЛИН-АЛКИЛ-ПИПЕРАЗИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2115651C1 |
| Способ получения производных 3-фенил-2-пропенамина в виде геометрических изомеров или их смесей, а также фармакологически приемлемых солей | 1986 |
|
SU1402251A3 |
| Способ получения производных @ -карболина или их фармацевтически приемлемых солей | 1986 |
|
SU1442074A3 |
| Способ получения производных 5-/4-диарилметил/-1-пиперазинилалкилбензимидазола или их солей | 1978 |
|
SU986297A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗАМИДОЭТИЛ-ПИПЕРАЗИНА | 1972 |
|
SU336873A1 |
| Способ получения производных бензимидазола или их солей | 1975 |
|
SU602118A3 |


Использование: для лечения психических расстройств. Продукты: пиридил- и пиримидилсодержащие производные пиперазина или 1,4-диазациклогептана общей формулы 1  , где R1 - водород или фтор; X - кислород, сера или метилен; n = 2 или 3; А - 2-пиридильная группа C5H2NR2R3 или 2-пиримидильная группа C4H3N2, причем, когда А представляет собой 2-пиримидильную группу, X является кислородом или метиленом и n = 2, R2 - водород, или хлор; R3 - водород, низший алкил, хлор, гидрокси, низший алкокси, нитро, трифторметил, карбамоил, N - метилкарбамоил, морфолинокарбонильная или пиперидинокарбонильная группа или их фармакологически активные кислотно-аддитивные соли. Реагент 1: соединение общей формулы
, где R1 - водород или фтор; X - кислород, сера или метилен; n = 2 или 3; А - 2-пиридильная группа C5H2NR2R3 или 2-пиримидильная группа C4H3N2, причем, когда А представляет собой 2-пиримидильную группу, X является кислородом или метиленом и n = 2, R2 - водород, или хлор; R3 - водород, низший алкил, хлор, гидрокси, низший алкокси, нитро, трифторметил, карбамоил, N - метилкарбамоил, морфолинокарбонильная или пиперидинокарбонильная группа или их фармакологически активные кислотно-аддитивные соли. Реагент 1: соединение общей формулы 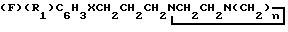 , в которой R1, X и n имеют указанные значения, Реагент 2: 2X-C5H2NR2R3 или 2-Z-C4H3N2, где R2 и R3 имеют указанные значения, Z - галоид. Условия: нагревание в присутствии основания. 1 табл.
, в которой R1, X и n имеют указанные значения, Реагент 2: 2X-C5H2NR2R3 или 2-Z-C4H3N2, где R2 и R3 имеют указанные значения, Z - галоид. Условия: нагревание в присутствии основания. 1 табл.
Пиридил- или пиримидилсодержащие производные пиперазина или 1,4-диазациклогептана общей формулы
F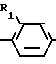 XCH2CH2CH2N
XCH2CH2CH2N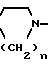 A
A
где R1 - водород или фтор;
X - кислород, сера или метилен;
n = 2 или 3;
A - пиридильная или пиримидильная группа формулы или
или 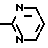
где R2 - водород или хлор;
R3 - водород, низший алкил, хлор, гидрокси, низший алкокси, нитро, трифторметил, карбамоил, N-метилкарбамоил, морфолинокарбонильная или пиперидинокарбонильная группа, причем когда A - пиримидильная группа, то X - кислород или метилен, и n = 2,
или их фармакологически активные кислотно-аддитивные соли, обладающие психотропным действием.
| РЕВОЛЬВЕР ДВОЙНОГО ДЕЙСТВИЯ С ПОСЛЕДУЮЩИМ АВТОМАТИЧЕСКИМ ВЗВОДОМ | 1999 |
|
RU2155925C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1994-10-15—Публикация
1989-09-27—Подача